1.1物质及其反应的分类 课件(共40张ppt)人教版(2019)必修第一册
文档属性
| 名称 | 1.1物质及其反应的分类 课件(共40张ppt)人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-10 00:00:00 | ||
图片预览




文档简介
(共40张PPT)
第一节 物质及其反应的分类
第一章 物质的分类及计量
一门中心的、实用的、创造性的科学。
化学的价值
食
衣
住
行
让生活更美好
一、高中化学简介
化学的价值
青蒿素提取
口罩、防护服
信息材料
一、高中化学简介
化学的价值
航天材料
一、高中化学简介
磷酸铁锂电池
三元锂电池
马斯克1亿美金
设立碳捕获大赛
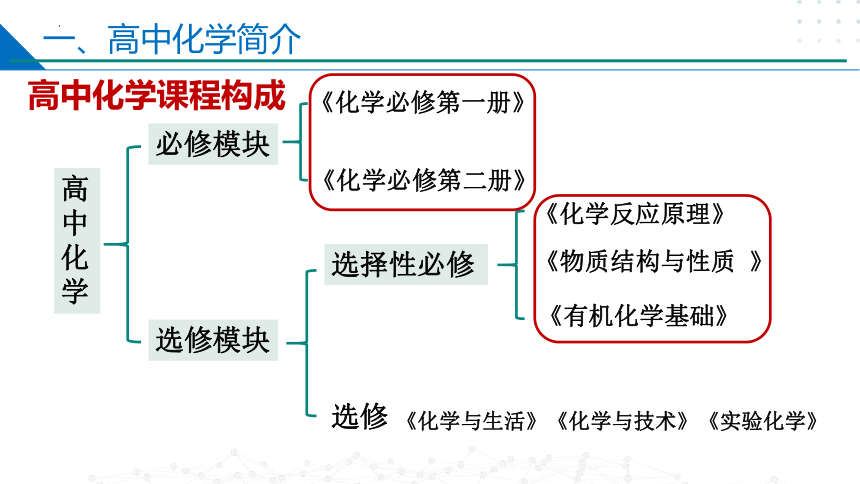
高中化学课程构成
高中化学
必修模块
选修模块
《化学必修第一册》
《化学必修第二册》
《化学反应原理》
《有机化学基础》
《物质结构与性质 》
选择性必修
选修
《化学与生活》《化学与技术》《实验化学》
一、高中化学简介
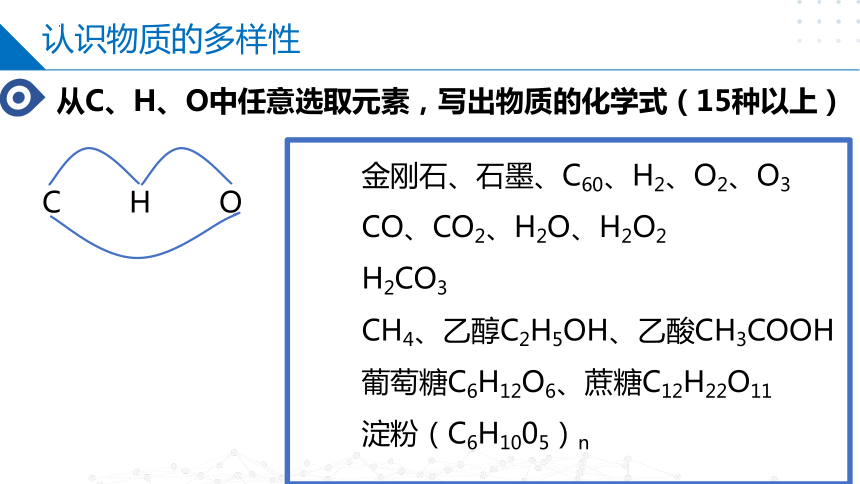
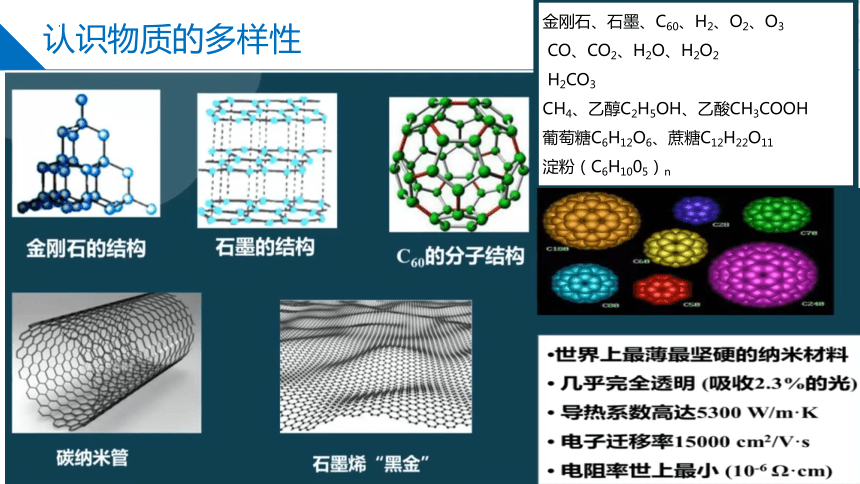
认识物质的多样性
从C、H、O中任意选取元素,写出物质的化学式(15种以上)
金刚石、石墨、C60、H2、O2、O3
CO、CO2、H2O、H2O2
H2CO3
CH4、乙醇C2H5OH、乙酸CH3COOH
葡萄糖C6H12O6、蔗糖C12H22O11
淀粉(C6H1005)n
C H O
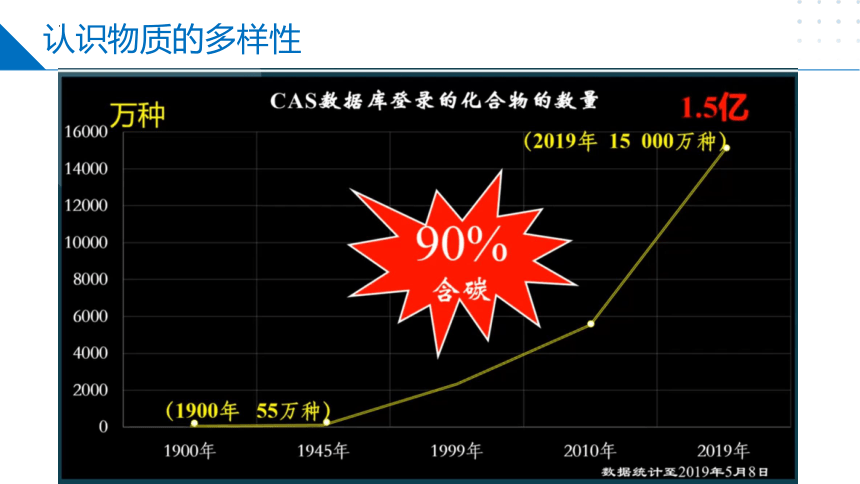
认识物质的多样性
认识物质的多样性
金刚石、石墨、C60、H2、O2、O3
CO、CO2、H2O、H2O2
H2CO3
CH4、乙醇C2H5OH、乙酸CH3COOH
葡萄糖C6H12O6、蔗糖C12H22O11
淀粉(C6H1005)n
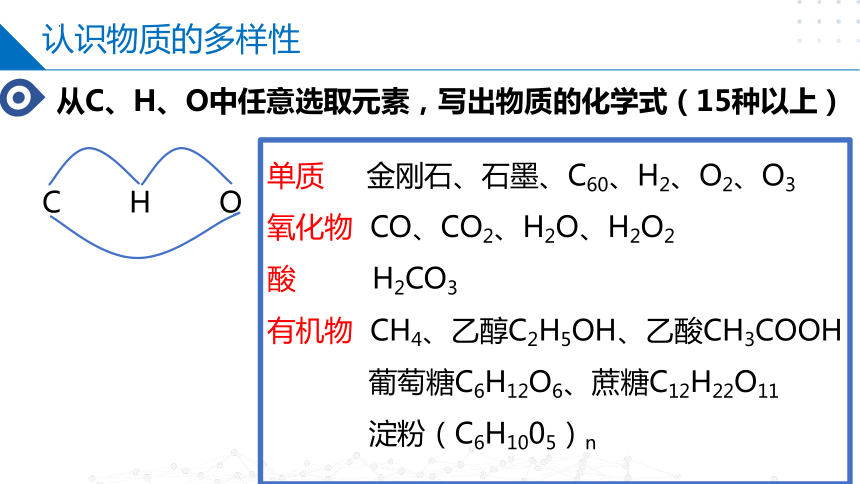
认识物质的多样性
从C、H、O中任意选取元素,写出物质的化学式(15种以上)
单质 金刚石、石墨、C60、H2、O2、O3
氧化物 CO、CO2、H2O、H2O2
酸 H2CO3
有机物 CH4、乙醇C2H5OH、乙酸CH3COOH
葡萄糖C6H12O6、蔗糖C12H22O11
淀粉(C6H1005)n
C H O
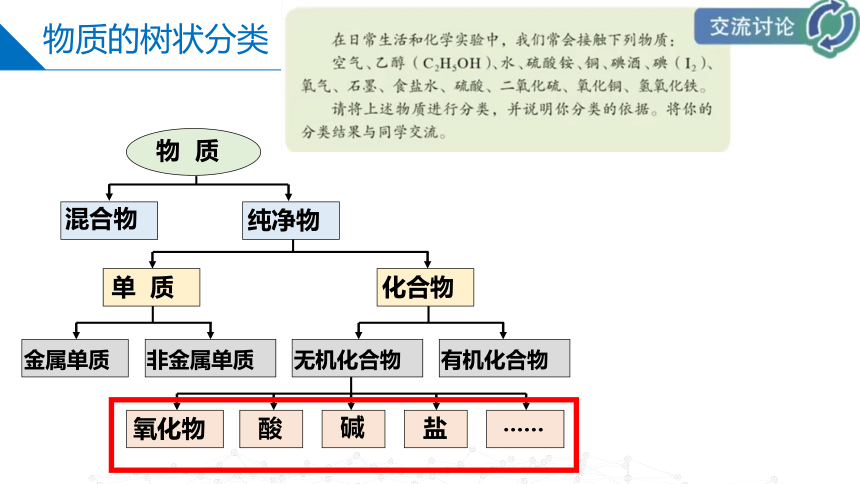
物质的树状分类
物 质
混合物
纯净物
单 质
化合物
氧化物
金属单质
非金属单质
无机化合物
有机化合物
酸
碱
盐
……
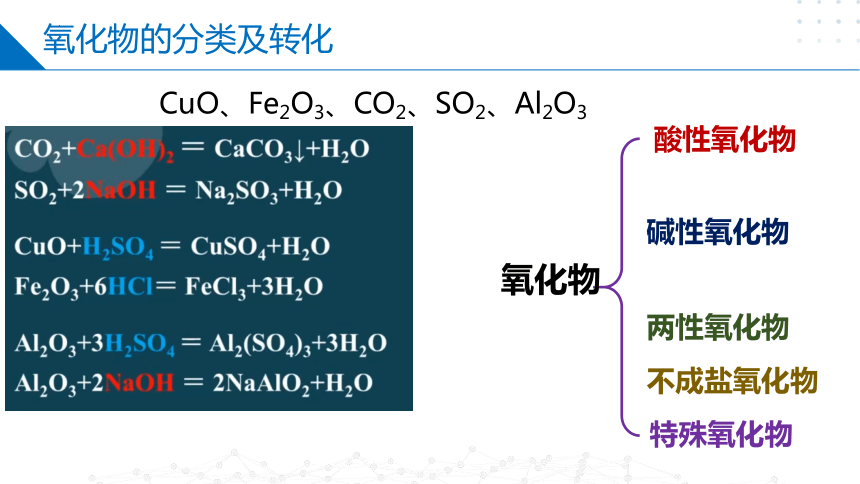
氧化物的分类及转化
CuO、Fe2O3、CO2、SO2、Al2O3
碱性氧化物
氧化物
两性氧化物
不成盐氧化物
特殊氧化物
酸性氧化物
氧化物的分类及转化
酸性氧化物
碱性氧化物
与碱反应生成盐和水的氧化物
与酸反应生成盐和水的氧化物
氧化物
CaO、Na2O等
CO2、SO2等
两性氧化物
不成盐氧化物
特殊氧化物
Al2O3
NO、CO、NO2等
Na2O2、H2O2等
氧化物的分类及转化
S →SO2 SO3 →H2SO4
氧化物的分类及转化
氧化物的分类及转化
CaCO3 → CaO → CaSO3
氧化物的分类及转化
非金属氧化物不全是酸性氧化物,如CO、NO不是酸性氧化物。
酸性氧化物也不全是非金属氧化物,如Mn2O7对应的水化物是HMnO4,Mn2O7是酸性氧化物,但不是非金属氧化物。
金属氧化物不全是碱性氧化物,碱性氧化物一定是金属氧化物
碱性氧化物
金属氧化物
酸性氧化物
非金属氧化物
一定
不一定
不一定
不一定
氧化物的分类及转化
!
注意
酸和碱的分类及转化
酸:电离时生成的阳离子全部是H+的化合物
碱:电离时生成的阴离子全部是OH-的化合物
H2SO4、HNO3、H2CO3
HCl、H2S
酸
从是否含氧分
无氧酸
含氧酸
……
酸的分类
按照酸是否容易分解分为稳定性酸H2SO4和不稳定酸H2CO3
强酸和弱酸
按照酸的沸点高低分为难挥发酸H2SO4和易挥发酸HNO3
从电离产生的H+数目分
二元酸
三元酸
一元酸
HNO3、HCl
H2SO4 H2CO3
H3PO4
酸和碱的分类及转化
酸和碱的分类及转化
酸:电离时生成的阳离子全部是H+的化合物
碱:电离时生成的阴离子全部是OH-的化合物
酸和碱的分类及转化
碱的分类
从电离产生的OH-数目分
二元碱
……
一元碱
NaOH、KOH、Ba(OH)2、NH3·H2O
Cu(OH)2、Mg(OH)2、Fe(OH) 3
NaOH、KOH、 NH3·H2O
Ba(OH)2、 Ca(OH)2
碱
从是否溶于水分
难溶碱
可溶碱
还可以将碱分为
强碱
弱碱
酸和碱的分类及转化
[问题解决1]电解MgCl2的方法获得Mg,有多少反应可以生成MgCl2?
Mg+Cl2MgCl2
Mg+2HClMgCl2+H2↑
MgO+2HClMgCl2+H2O
Mg(OH)2+2HClMgCl2+2H2O
MgCO3+2HClMgCl2+H2O+CO2↑
MgCO3 MgO → MgCl2 → Mg
酸和碱的分类及转化
[问题解决2]海水中有大量的MgCl2,如何利用海水提取MgCl2?(2.1×1015t)
Ca(OH)2+MgCl2CaCl2+Mg(OH)2
Mg(OH)2+2HClMgCl2+2H2O
酸和碱的分类及转化
酸和碱可以发生中和反应生成盐和水,写出下列中和反应的方程式HCl+NaOHNaCl+H2OHNO3+NH3·H2ONH4NO3+H2O
H2SO4+2NaOHNa2SO4+2H2O2HCl+Mg(OH)2MgCl2+2H2OH2SO4+ NaOH NaHSO4+H2OHCl+Mg(OH)2 Mg(OH)Cl+H2O
五、盐的分类及转化
(1)盐:在水溶液中电离产生金属阳离子(或)和酸根离子的化合物。
(2)正盐:在水溶液中电离只产生一种阳离子和一种阴离子的盐。
(3)酸式盐:在水溶液中电离还能产生H+的盐。
(4)碱式盐:在水溶液中电离还能产生OH-的盐。
(5)复盐:在水溶液中电离产生两种或两种以上金属阳离子(或)的盐,如KAl(SO4)2。
盐的理解
二、物质的分类
盐的分类
盐
从是否溶于水分
按盐的组成分
无氧酸盐
正盐
酸式盐
碱式盐
Na2CO3 、K2SO4
NaHSO4 、KHCO3
Cu2(OH)2CO3 、 Mg(OH) Cl
按酸根是否含氧分
含氧酸盐
可溶盐
难溶盐
NaCl、AgNO3、CuSO4
CaCO3、BaSO4、ZnS
KNO3、KMnO4、FeSO4
NaCl、ZnS、CaCl2
……
六、从元素和化合价的角度认识物质的分类
硫元素常见的化合态有-2、+4、+6,请写出含硫元素的纯净物的化学式
随堂练习
1.物质的分类如下图所示:
由图判断,下列说法中不正确的是( )
A.甲图所示的分类方法属于树状分类法
B.乙图所示的分类方法属于交叉分类法
C.碱性氧化物一定是金属氧化物
D.非金属氧化物一定是酸性氧化物
D
随堂练习
2.下列有关物质的分类正确的是( )
C
选项 物质 分类
A 雾霾、水银、冰水混合物 混合物
B Ba(OH)2、烧碱、生石灰 碱
C 氯化钠、CaCO3、无水硫酸铜 盐
D CO、CO2、Mn2O7 酸性氧化物
有机物和无机物能相互转化吗?
人类首次将无机化合物转化为有机化合物
1828年,德国化学家维勒通过蒸发氰酸铵(NH4CNO,一种无机化合物,可由氯化铵和氰酸银反应制得)水溶液得到了尿素[CO(NH2)2]。
尿素的合成揭开了人工合成有机化合物的序幕。
尿素的分子结构模型
六、从元素和化合价的角度认识物质的分类
反应通式 反应类型 实例(化学方程式)
A + B = C
C = A + B
AB + C = A + CB
AB + CD = AD + CB
化合反应
分解反应
置换反应
复分解反应
Fe2O3+3CO =2Fe + 3CO2属于什么反应?
六、从元素和化合价的角度认识物质的分类
化学反应
氧化还原反应
非氧化还原反应
有元素化合价发生变化的反应
元素化合价不发生变化的反应
四大基本反应类型和氧化还原反应的关系如何
六、从元素和化合价的角度认识物质的分类
分解反应
是
化合反应
反应类型
反应实例
是否氧化
还原反应
① 3Fe+2O2 Fe3O4
点燃
②CaO+H2O Ca(OH)2
③ Na2O2+SO2 Na2SO4
④ 2KClO3 2KCl+3O2↑
MnO2
△
⑤ CaCO3 CaO+CO2↑
高温
⑥2FeSO4 Fe2O3+SO2↑+SO3↑
△
⑦2CuO+C 2Cu+CO2↑
△
⑧2NaOH+H2SO4=Na2SO4+2H2O
化合反应
化合反应
分解反应
分解反应
复分解反应
置换反应
非
是
是
非
是
是
非
六、从元素和化合价的角度认识物质的分类
氧化还原反应与四种基本反应类型之间的关系
随堂练习
BC
随堂练习
B
谢谢观看
THANKS
第一节 物质及其反应的分类
第一章 物质的分类及计量
一门中心的、实用的、创造性的科学。
化学的价值
食
衣
住
行
让生活更美好
一、高中化学简介
化学的价值
青蒿素提取
口罩、防护服
信息材料
一、高中化学简介
化学的价值
航天材料
一、高中化学简介
磷酸铁锂电池
三元锂电池
马斯克1亿美金
设立碳捕获大赛
高中化学课程构成
高中化学
必修模块
选修模块
《化学必修第一册》
《化学必修第二册》
《化学反应原理》
《有机化学基础》
《物质结构与性质 》
选择性必修
选修
《化学与生活》《化学与技术》《实验化学》
一、高中化学简介
认识物质的多样性
从C、H、O中任意选取元素,写出物质的化学式(15种以上)
金刚石、石墨、C60、H2、O2、O3
CO、CO2、H2O、H2O2
H2CO3
CH4、乙醇C2H5OH、乙酸CH3COOH
葡萄糖C6H12O6、蔗糖C12H22O11
淀粉(C6H1005)n
C H O
认识物质的多样性
认识物质的多样性
金刚石、石墨、C60、H2、O2、O3
CO、CO2、H2O、H2O2
H2CO3
CH4、乙醇C2H5OH、乙酸CH3COOH
葡萄糖C6H12O6、蔗糖C12H22O11
淀粉(C6H1005)n
认识物质的多样性
从C、H、O中任意选取元素,写出物质的化学式(15种以上)
单质 金刚石、石墨、C60、H2、O2、O3
氧化物 CO、CO2、H2O、H2O2
酸 H2CO3
有机物 CH4、乙醇C2H5OH、乙酸CH3COOH
葡萄糖C6H12O6、蔗糖C12H22O11
淀粉(C6H1005)n
C H O
物质的树状分类
物 质
混合物
纯净物
单 质
化合物
氧化物
金属单质
非金属单质
无机化合物
有机化合物
酸
碱
盐
……
氧化物的分类及转化
CuO、Fe2O3、CO2、SO2、Al2O3
碱性氧化物
氧化物
两性氧化物
不成盐氧化物
特殊氧化物
酸性氧化物
氧化物的分类及转化
酸性氧化物
碱性氧化物
与碱反应生成盐和水的氧化物
与酸反应生成盐和水的氧化物
氧化物
CaO、Na2O等
CO2、SO2等
两性氧化物
不成盐氧化物
特殊氧化物
Al2O3
NO、CO、NO2等
Na2O2、H2O2等
氧化物的分类及转化
S →SO2 SO3 →H2SO4
氧化物的分类及转化
氧化物的分类及转化
CaCO3 → CaO → CaSO3
氧化物的分类及转化
非金属氧化物不全是酸性氧化物,如CO、NO不是酸性氧化物。
酸性氧化物也不全是非金属氧化物,如Mn2O7对应的水化物是HMnO4,Mn2O7是酸性氧化物,但不是非金属氧化物。
金属氧化物不全是碱性氧化物,碱性氧化物一定是金属氧化物
碱性氧化物
金属氧化物
酸性氧化物
非金属氧化物
一定
不一定
不一定
不一定
氧化物的分类及转化
!
注意
酸和碱的分类及转化
酸:电离时生成的阳离子全部是H+的化合物
碱:电离时生成的阴离子全部是OH-的化合物
H2SO4、HNO3、H2CO3
HCl、H2S
酸
从是否含氧分
无氧酸
含氧酸
……
酸的分类
按照酸是否容易分解分为稳定性酸H2SO4和不稳定酸H2CO3
强酸和弱酸
按照酸的沸点高低分为难挥发酸H2SO4和易挥发酸HNO3
从电离产生的H+数目分
二元酸
三元酸
一元酸
HNO3、HCl
H2SO4 H2CO3
H3PO4
酸和碱的分类及转化
酸和碱的分类及转化
酸:电离时生成的阳离子全部是H+的化合物
碱:电离时生成的阴离子全部是OH-的化合物
酸和碱的分类及转化
碱的分类
从电离产生的OH-数目分
二元碱
……
一元碱
NaOH、KOH、Ba(OH)2、NH3·H2O
Cu(OH)2、Mg(OH)2、Fe(OH) 3
NaOH、KOH、 NH3·H2O
Ba(OH)2、 Ca(OH)2
碱
从是否溶于水分
难溶碱
可溶碱
还可以将碱分为
强碱
弱碱
酸和碱的分类及转化
[问题解决1]电解MgCl2的方法获得Mg,有多少反应可以生成MgCl2?
Mg+Cl2MgCl2
Mg+2HClMgCl2+H2↑
MgO+2HClMgCl2+H2O
Mg(OH)2+2HClMgCl2+2H2O
MgCO3+2HClMgCl2+H2O+CO2↑
MgCO3 MgO → MgCl2 → Mg
酸和碱的分类及转化
[问题解决2]海水中有大量的MgCl2,如何利用海水提取MgCl2?(2.1×1015t)
Ca(OH)2+MgCl2CaCl2+Mg(OH)2
Mg(OH)2+2HClMgCl2+2H2O
酸和碱的分类及转化
酸和碱可以发生中和反应生成盐和水,写出下列中和反应的方程式HCl+NaOHNaCl+H2OHNO3+NH3·H2ONH4NO3+H2O
H2SO4+2NaOHNa2SO4+2H2O2HCl+Mg(OH)2MgCl2+2H2OH2SO4+ NaOH NaHSO4+H2OHCl+Mg(OH)2 Mg(OH)Cl+H2O
五、盐的分类及转化
(1)盐:在水溶液中电离产生金属阳离子(或)和酸根离子的化合物。
(2)正盐:在水溶液中电离只产生一种阳离子和一种阴离子的盐。
(3)酸式盐:在水溶液中电离还能产生H+的盐。
(4)碱式盐:在水溶液中电离还能产生OH-的盐。
(5)复盐:在水溶液中电离产生两种或两种以上金属阳离子(或)的盐,如KAl(SO4)2。
盐的理解
二、物质的分类
盐的分类
盐
从是否溶于水分
按盐的组成分
无氧酸盐
正盐
酸式盐
碱式盐
Na2CO3 、K2SO4
NaHSO4 、KHCO3
Cu2(OH)2CO3 、 Mg(OH) Cl
按酸根是否含氧分
含氧酸盐
可溶盐
难溶盐
NaCl、AgNO3、CuSO4
CaCO3、BaSO4、ZnS
KNO3、KMnO4、FeSO4
NaCl、ZnS、CaCl2
……
六、从元素和化合价的角度认识物质的分类
硫元素常见的化合态有-2、+4、+6,请写出含硫元素的纯净物的化学式
随堂练习
1.物质的分类如下图所示:
由图判断,下列说法中不正确的是( )
A.甲图所示的分类方法属于树状分类法
B.乙图所示的分类方法属于交叉分类法
C.碱性氧化物一定是金属氧化物
D.非金属氧化物一定是酸性氧化物
D
随堂练习
2.下列有关物质的分类正确的是( )
C
选项 物质 分类
A 雾霾、水银、冰水混合物 混合物
B Ba(OH)2、烧碱、生石灰 碱
C 氯化钠、CaCO3、无水硫酸铜 盐
D CO、CO2、Mn2O7 酸性氧化物
有机物和无机物能相互转化吗?
人类首次将无机化合物转化为有机化合物
1828年,德国化学家维勒通过蒸发氰酸铵(NH4CNO,一种无机化合物,可由氯化铵和氰酸银反应制得)水溶液得到了尿素[CO(NH2)2]。
尿素的合成揭开了人工合成有机化合物的序幕。
尿素的分子结构模型
六、从元素和化合价的角度认识物质的分类
反应通式 反应类型 实例(化学方程式)
A + B = C
C = A + B
AB + C = A + CB
AB + CD = AD + CB
化合反应
分解反应
置换反应
复分解反应
Fe2O3+3CO =2Fe + 3CO2属于什么反应?
六、从元素和化合价的角度认识物质的分类
化学反应
氧化还原反应
非氧化还原反应
有元素化合价发生变化的反应
元素化合价不发生变化的反应
四大基本反应类型和氧化还原反应的关系如何
六、从元素和化合价的角度认识物质的分类
分解反应
是
化合反应
反应类型
反应实例
是否氧化
还原反应
① 3Fe+2O2 Fe3O4
点燃
②CaO+H2O Ca(OH)2
③ Na2O2+SO2 Na2SO4
④ 2KClO3 2KCl+3O2↑
MnO2
△
⑤ CaCO3 CaO+CO2↑
高温
⑥2FeSO4 Fe2O3+SO2↑+SO3↑
△
⑦2CuO+C 2Cu+CO2↑
△
⑧2NaOH+H2SO4=Na2SO4+2H2O
化合反应
化合反应
分解反应
分解反应
复分解反应
置换反应
非
是
是
非
是
是
非
六、从元素和化合价的角度认识物质的分类
氧化还原反应与四种基本反应类型之间的关系
随堂练习
BC
随堂练习
B
谢谢观看
THANKS
