【核心素养目标】人教版(2019)高一化学必修第一册 2.2 氯及其化合物(第3课时 氯气的实验室制法)(共20张PPT)
文档属性
| 名称 | 【核心素养目标】人教版(2019)高一化学必修第一册 2.2 氯及其化合物(第3课时 氯气的实验室制法)(共20张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 10.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-09-18 10:46:47 | ||
图片预览






文档简介
(共20张PPT)
第二节 氯及其化合物
第3课时 氯气的实验室制法
人教版必修第一册
榆次一中 李金虎
学习目标
1.掌握氯气的实验室制法。
2.总结实验室制备气体的思路
学习目标
1.根据Cl2的性质,掌握Cl2的实验室制法(发生、除杂、收集和尾气处理),培养学生的“科学探究与创新意识”的核心素养。
2.形成实验室制备气体的实验模型,培养学生的“证据推理与模型认知”的核心素养。
素养目标
情境引入
18世纪70年代,舍勒将软锰矿与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体,他发现这种气体的水溶液对纸张、蔬菜等具有永久性的漂白作用以及能与金属化合物发生化学反应。
但在燃素说的大环境下,他认为这种气体是一种化合物,是由氧和另外一种未知的基所组成的,所以舍勒称它为“氧化盐酸”。
瑞典化学家舍勒
教学过程
英国化学家戴维
英国化学家戴维却持有不同的观点,他想尽了一切办法也不能从氧化盐酸中把氧夺取出来,均告失败。他怀疑氧化盐酸中根本就没有氧存在。
1810年,戴维以无可辩驳的事实证明了所谓的氧化盐酸不是一种化合物,而是一种化学元素的单质,他将这种元素命名为“Chlorine”,它的希腊文原意是“绿色”,中文译名为氯。
教学过程
氯气的实验室制法
1.实验原理
利用强氧化剂氧化浓盐酸中的Cl-生成Cl2,该反应中MnO2为氧化剂,浓盐酸为还原剂,并且该实验还体现了浓盐酸的酸性。
教学过程
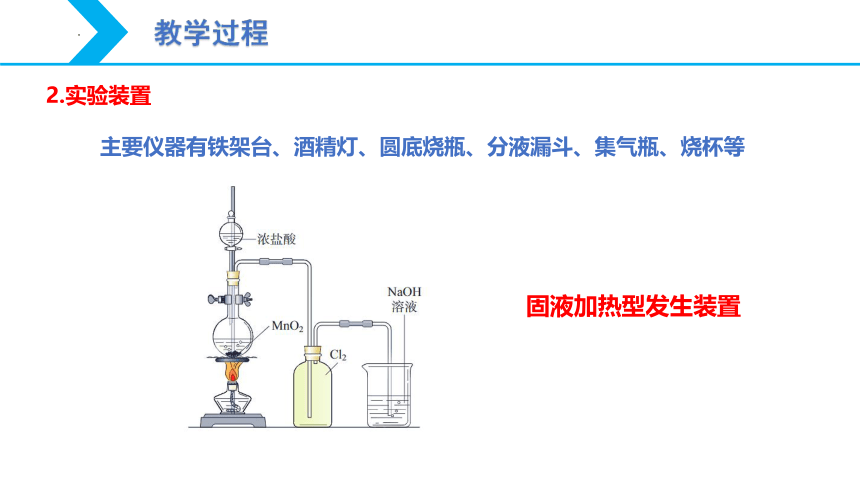
2.实验装置
主要仪器有铁架台、酒精灯、圆底烧瓶、分液漏斗、集气瓶、烧杯等
固液加热型发生装置
教学过程
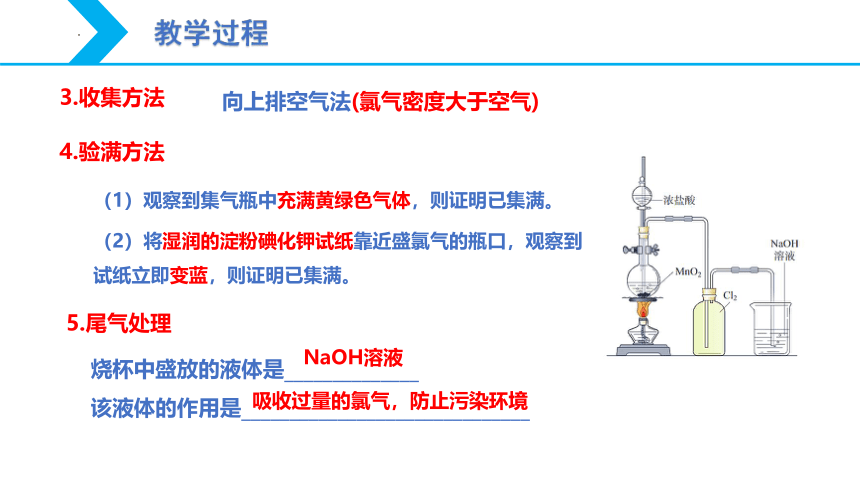
烧杯中盛放的液体是______________
该液体的作用是______________________________
向上排空气法(氯气密度大于空气)
NaOH溶液
(1)观察到集气瓶中充满黄绿色气体,则证明已集满。
吸收过量的氯气,防止污染环境
3.收集方法
4.验满方法
(2)将湿润的淀粉碘化钾试纸靠近盛氯气的瓶口,观察到试纸立即变蓝,则证明已集满。
5.尾气处理
教学过程
教学过程
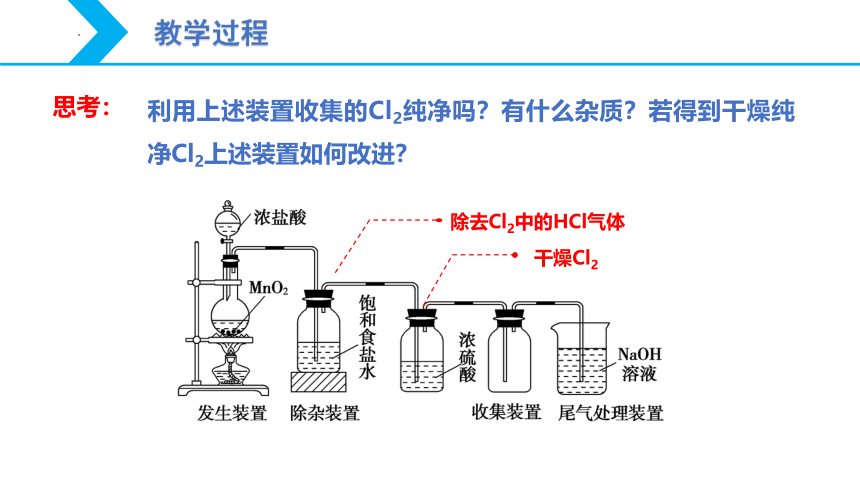
利用上述装置收集的Cl2纯净吗?有什么杂质?若得到干燥纯净Cl2上述装置如何改进?
思考:
除去Cl2中的HCl气体
干燥Cl2
教学过程
一套完整的制气装置包括:发生装置→净化装置→收集或性质验证装置→尾气处理装置。
选择各部分装置时应注意:
(1)依据反应物的状态和反应条件,选择气体发生装置;
(2)依据气体及所含杂质的性质,选择除杂装置;
(3)依据气体的密度、气体在水中的溶解性以及是否与水、空气反应,选择收集装置;
(4)依据气体的性质,选择尾气处理装置。
【模型构建】
制取气体装置模型
教学过程
装置的基本类型
固体+固体 气体
固体+液体 气体
固体+液体 气体
(1)依据反应物的状态和反应条件,选择气体发生装置;
教学过程
(2)依据气体及所含杂质的性质,选择除杂装置;
净化原则
装置Ⅰ(洗气瓶):盛液体除杂试剂,气流方向是长管进,短管出。
不减少被净化气体的量;不引入新杂质;操作简便,易于分离。
净化装置
装置Ⅱ(干燥管):盛固体除杂试剂,气流方向是粗口进,细口出。
教学过程
(3)依据气体的密度、气体在水中的溶解性以及是否与水、空气反应,选择收集装置;
方法选择
排水法:适用于难溶于水且不与水反应的气体,如O2、H2等
向上排空气法:气体不与空气反应,且密度比空气大,如O2、CO2、Cl2等
向下排空气法:气体不与空气反应,且密度比空气小,如H2等
教学过程
(4)依据气体的性质,选择尾气处理装置
②点燃法:如CO、H2、CH4等易燃性气体可用此法,必须先验纯,再点燃
①吸收法:如Cl2、SO2、HCl、H2S、NH3等可用碱液吸收
典例1.
1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名―氯气)。实验室制取Cl2时,下列装置能达到相应实验目的的是( )
课堂练习
答案 D
典例2.
某研究性学习小组的同学利用MnO2、浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法正确的是( )
A.按气体流动的先后顺序,装置连接顺序依次为dacbe
B.按气体流动的先后顺序,装置连接顺序依次为dabae
C.装置e的主要用途是制备NaClO
D.在实验中使用到装置c且有色布条褪色,则说明湿润的氯气有漂白性
课堂练习
【答案】B
典例3.
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图所示。
回答下列问题:
(1)连接上述仪器的正确顺序(填各接口处的字母): 接 ; 接 ; 接 ; 接 。
(2)装置中,饱和食盐水的作用是 ;NaOH溶液的作用是 。
(3)化学实验中常用湿润的淀粉 KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到 ,反应的化学方程式为 。
(4)写出下列反应的离子方程式: 。
①气体发生装置中进行的反应: 。
②NaOH溶液中发生的反应: 。
课堂练习
课堂练习
【答案】
(1) E接C;D接A;B接H;G接F 。
(2) 除去氯气中的HCl杂质 吸收过量的氯气
(3) 试纸变蓝 2KI+Cl2=2KCl+I2
(4) ①
② 2OH-+Cl2=Cl-+ClO-+H2O。
课堂小结
感 谢 倾 听
第二节 氯及其化合物
第3课时 氯气的实验室制法
人教版必修第一册
榆次一中 李金虎
学习目标
1.掌握氯气的实验室制法。
2.总结实验室制备气体的思路
学习目标
1.根据Cl2的性质,掌握Cl2的实验室制法(发生、除杂、收集和尾气处理),培养学生的“科学探究与创新意识”的核心素养。
2.形成实验室制备气体的实验模型,培养学生的“证据推理与模型认知”的核心素养。
素养目标
情境引入
18世纪70年代,舍勒将软锰矿与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体,他发现这种气体的水溶液对纸张、蔬菜等具有永久性的漂白作用以及能与金属化合物发生化学反应。
但在燃素说的大环境下,他认为这种气体是一种化合物,是由氧和另外一种未知的基所组成的,所以舍勒称它为“氧化盐酸”。
瑞典化学家舍勒
教学过程
英国化学家戴维
英国化学家戴维却持有不同的观点,他想尽了一切办法也不能从氧化盐酸中把氧夺取出来,均告失败。他怀疑氧化盐酸中根本就没有氧存在。
1810年,戴维以无可辩驳的事实证明了所谓的氧化盐酸不是一种化合物,而是一种化学元素的单质,他将这种元素命名为“Chlorine”,它的希腊文原意是“绿色”,中文译名为氯。
教学过程
氯气的实验室制法
1.实验原理
利用强氧化剂氧化浓盐酸中的Cl-生成Cl2,该反应中MnO2为氧化剂,浓盐酸为还原剂,并且该实验还体现了浓盐酸的酸性。
教学过程
2.实验装置
主要仪器有铁架台、酒精灯、圆底烧瓶、分液漏斗、集气瓶、烧杯等
固液加热型发生装置
教学过程
烧杯中盛放的液体是______________
该液体的作用是______________________________
向上排空气法(氯气密度大于空气)
NaOH溶液
(1)观察到集气瓶中充满黄绿色气体,则证明已集满。
吸收过量的氯气,防止污染环境
3.收集方法
4.验满方法
(2)将湿润的淀粉碘化钾试纸靠近盛氯气的瓶口,观察到试纸立即变蓝,则证明已集满。
5.尾气处理
教学过程
教学过程
利用上述装置收集的Cl2纯净吗?有什么杂质?若得到干燥纯净Cl2上述装置如何改进?
思考:
除去Cl2中的HCl气体
干燥Cl2
教学过程
一套完整的制气装置包括:发生装置→净化装置→收集或性质验证装置→尾气处理装置。
选择各部分装置时应注意:
(1)依据反应物的状态和反应条件,选择气体发生装置;
(2)依据气体及所含杂质的性质,选择除杂装置;
(3)依据气体的密度、气体在水中的溶解性以及是否与水、空气反应,选择收集装置;
(4)依据气体的性质,选择尾气处理装置。
【模型构建】
制取气体装置模型
教学过程
装置的基本类型
固体+固体 气体
固体+液体 气体
固体+液体 气体
(1)依据反应物的状态和反应条件,选择气体发生装置;
教学过程
(2)依据气体及所含杂质的性质,选择除杂装置;
净化原则
装置Ⅰ(洗气瓶):盛液体除杂试剂,气流方向是长管进,短管出。
不减少被净化气体的量;不引入新杂质;操作简便,易于分离。
净化装置
装置Ⅱ(干燥管):盛固体除杂试剂,气流方向是粗口进,细口出。
教学过程
(3)依据气体的密度、气体在水中的溶解性以及是否与水、空气反应,选择收集装置;
方法选择
排水法:适用于难溶于水且不与水反应的气体,如O2、H2等
向上排空气法:气体不与空气反应,且密度比空气大,如O2、CO2、Cl2等
向下排空气法:气体不与空气反应,且密度比空气小,如H2等
教学过程
(4)依据气体的性质,选择尾气处理装置
②点燃法:如CO、H2、CH4等易燃性气体可用此法,必须先验纯,再点燃
①吸收法:如Cl2、SO2、HCl、H2S、NH3等可用碱液吸收
典例1.
1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名―氯气)。实验室制取Cl2时,下列装置能达到相应实验目的的是( )
课堂练习
答案 D
典例2.
某研究性学习小组的同学利用MnO2、浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法正确的是( )
A.按气体流动的先后顺序,装置连接顺序依次为dacbe
B.按气体流动的先后顺序,装置连接顺序依次为dabae
C.装置e的主要用途是制备NaClO
D.在实验中使用到装置c且有色布条褪色,则说明湿润的氯气有漂白性
课堂练习
【答案】B
典例3.
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图所示。
回答下列问题:
(1)连接上述仪器的正确顺序(填各接口处的字母): 接 ; 接 ; 接 ; 接 。
(2)装置中,饱和食盐水的作用是 ;NaOH溶液的作用是 。
(3)化学实验中常用湿润的淀粉 KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到 ,反应的化学方程式为 。
(4)写出下列反应的离子方程式: 。
①气体发生装置中进行的反应: 。
②NaOH溶液中发生的反应: 。
课堂练习
课堂练习
【答案】
(1) E接C;D接A;B接H;G接F 。
(2) 除去氯气中的HCl杂质 吸收过量的氯气
(3) 试纸变蓝 2KI+Cl2=2KCl+I2
(4) ①
② 2OH-+Cl2=Cl-+ClO-+H2O。
课堂小结
感 谢 倾 听
