【核心素养目标】人教版(2019)高一化学必修第一册 3.2 金属材料(第2课时 铝合金)
文档属性
| 名称 | 【核心素养目标】人教版(2019)高一化学必修第一册 3.2 金属材料(第2课时 铝合金) |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-09-18 00:00:00 | ||
图片预览







文档简介
(共23张PPT)
第二节 金属材料
第2课时 铝及其化合物性质
人教版必修第一册
榆次一中 李金虎
学习目标
1. 了解铝和氧化铝的性质。
2. 了解铝合金的用途。
学习目标
1. 通过实验探究铝和氧化铝的性质,认识两性氧化物的性质。培养学生“变化观念与科学探究”的核心素养。
2. 通过认识铝合金的用途,培养学生“科学态度与社会责任”的核心素养。
素养目标
情境引入
铝的化学性质比较活泼,为什么铝制品不容易生锈?
在常温下铝能与空气中的氧气发生反应,表面生成一层致密的氧化铝薄膜。人们日常用的铝制品通常都是由铝合金制造的,其表面总是覆盖着致密的氧化铝薄膜,这层膜起着保护内部金属的作用。
教学过程
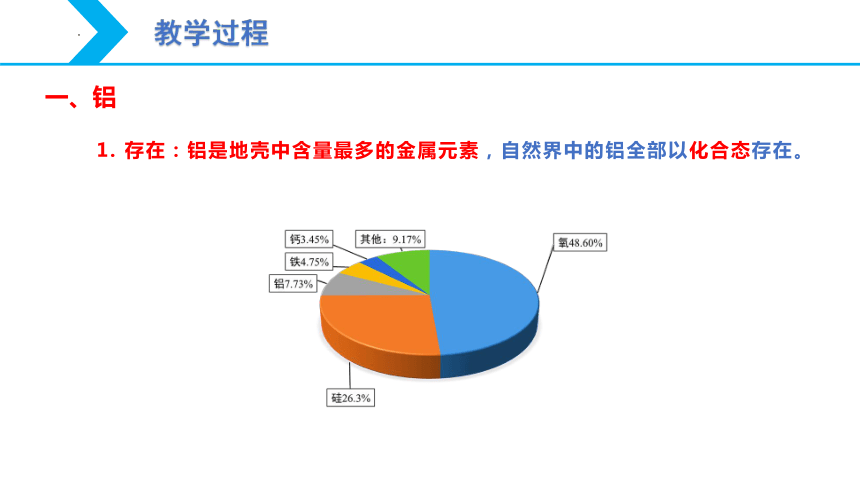
1. 存在:铝是地壳中含量最多的金属元素,自然界中的铝全部以化合态存在。
一、铝
教学过程
4. 用途:① 纯铝用作导线;②铝合金用于制造汽车、飞机、生活用品等。
一、铝
2.结构:铝的原子结构示意图为
3. 物理性质:银白色有金属光泽的固体,有良好的延展性、导电性和传热性等,密度较小,质地柔软。
教学过程
纯铝的硬度和强度较小,不适合制造机器零件等。向铝中加入少量的合金元素,如Cu、Mg、Si、Mn、Zn及稀土元素等,可制成铝合金。铝合金是目前用途广泛的合金之一。例如,硬铝(一种铝合金) 中含Cu 4%、Mg 0.5%、Mn 0.5%、Si 0.7%,它的密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
硬铝常用于制造飞机的外壳
教学过程
5.化学性质:
(1)铝与氧气的反应
① 常温:铝与空气中的氧气反应,表面生成一层致密的氧化铝薄膜,对内部金属起着保护作用,化学方程式为
② 点燃:铝在氧气中点燃,放出大量的热和耀眼的白光,化学方程式为
4Al+3O2===2Al2O3
4Al+3O2===2Al2O3
点燃
教学过程
(2)铝与(非氧化性)酸的反应
2Al+6HCl=2AlCl3+3H2↑
2Al+6H+=2Al3++3H2↑
思考:铝制餐具为何不宜用来蒸煮或长时间存放酸性或碱性食品?
(3)铝与碱的反应
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
2Al+2OH-+6H2O= 2[Al(OH)4]-+3H2↑
教学过程
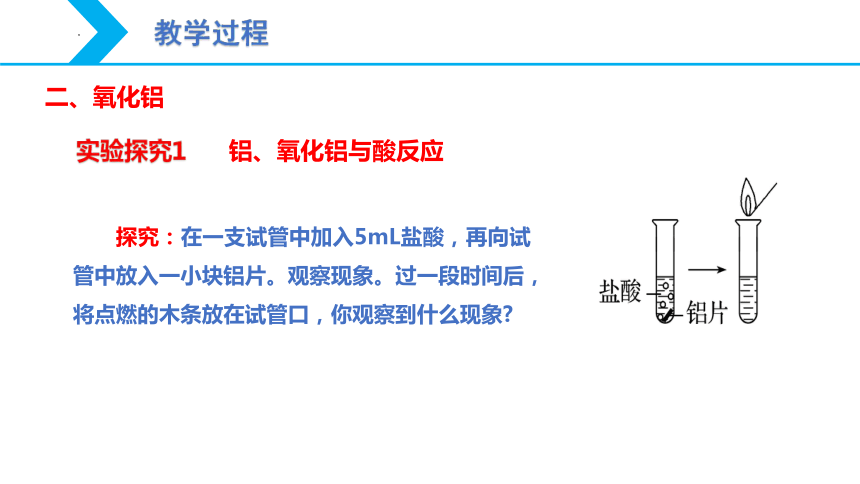
实验探究1
探究:在一支试管中加入5mL盐酸,再向试管中放入一小块铝片。观察现象。过一段时间后,将点燃的木条放在试管口,你观察到什么现象
二、氧化铝
铝、氧化铝与酸反应
教学过程
【实验现象】
开始不太明显,铝片逐渐溶解,有气泡冒出,将点燃的木条放在试管口爆鸣声。
1. 铝、氧化铝的性质——与酸反应
Al2O3+6HCl = 2AlCl3+3H2O、2Al+6HCl = 2AlCl3+3H2↑
Al2O3+6H+ = 2Al3++3H2O、2Al+6H+ = 2Al3++3H2↑
教学过程
探究:在两支试管中分别加入少量的NaOH溶液,然后向其中一支试管中放入一小块铝片,向另一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。过一段时间后,将点燃的木条分别放在两支试管口。你观察到什么现象
二、氧化铝
实验探究2
铝、氧化铝与碱的反应
教学过程
教学过程
(3)铝与碱的反应
【实验现象】
试管①中一开始无气泡产生,一段时间后,铝片逐渐溶解,有无色气泡冒出,试管②中铝片溶解,立即产生无色气泡,将点燃的木条放在试管口,都有爆鸣声。
Al2O3+2NaOH+3H2O=2Na[Al(OH)4]、2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
Al2O3+2OH-+3H2O=2[Al(OH)4]-、2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
教学过程
两性氧化物:
既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,如Al2O3。
两性氢氧化物:
既能与酸反应生成盐和水,又能与碱反应生成盐和水的氢氧化物,如Al(OH)3。
Al(OH)3溶于盐酸:
Al(OH)3溶于NaOH溶液:
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+NaOH=Na[Al(OH)4]
在医疗上有一种药叫胃舒平,你知道它的主要成分和作用吗?
说明书:
【成分】本品为复方制剂,
每片含主要成份氢氧化铝
0.45g
【性状】本品为白色片
【适应症】用于缓解胃酸过多
引起的胃痛
教学过程
教学过程
归纳总结——Al3+、Al(OH)3、AlO2-的转化
Al3+ + 3OH- === Al(OH)3↓
Al3+ + 4OH- === AlO2- + 2H2O
AlO2- + 4H+ === Al3+ + 2H2O
Al(OH)3 + OH- === AlO2- + 2H2O
H+ + AlO2- + H2O === Al(OH)3↓
Al(OH)3 + 3H+ === Al3+ + 3H2O
典例1.
取等质量的铝粉两份,分别放入足量的浓氢氧化钠溶液和盐酸溶液中,充分反应后,两者放出氢气的体积( )
A.1:1 B.1:3
C.1:2 D.2:1
课堂练习
【答案】A
典例2.
用氧化铝为原料来制取氢氧化铝的最好的方法是( )
A.将氧化铝粉末溶于水
B.将氧化铝粉 末溶于盐酸,再滴加氢氧化钠溶液
C.将氧化铝粉末溶于盐酸中,再滴加氨水
D.将氧化铝粉末溶于氢氧化铝溶液中,再滴加盐酸
课堂练习
【答案】C
典例3.
用铁、铝的混合物进行如下实验:
课堂练习
(1)操作X的名称是________。
(2)气体A是________。
(3)A与Cl2混合光照可能发生爆炸,生成________(填化学式),A在该反应中作为__________(填“氧化剂”或“还原剂”)。
(4)溶液B中阴离子除OH-外还有________,溶液D中存在的金属离子为________。
过滤
H2
HCl
还原剂
AlO2-
Fe2+
课堂小结
课堂小结
课后小任务
家庭的厨卫管道内常因留有油脂、毛发、菜渣、纸棉纤维等而造成堵塞,此时可以用一种固体管道疏通剂疏通。这种固体管道疏通剂的主要成分有NaOH和铝粉,请解释其疏通原理。
工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对毛发等淤积物的腐蚀,同时产生氢气增加管道内的气压,利于疏通。
感 谢 倾 听
第二节 金属材料
第2课时 铝及其化合物性质
人教版必修第一册
榆次一中 李金虎
学习目标
1. 了解铝和氧化铝的性质。
2. 了解铝合金的用途。
学习目标
1. 通过实验探究铝和氧化铝的性质,认识两性氧化物的性质。培养学生“变化观念与科学探究”的核心素养。
2. 通过认识铝合金的用途,培养学生“科学态度与社会责任”的核心素养。
素养目标
情境引入
铝的化学性质比较活泼,为什么铝制品不容易生锈?
在常温下铝能与空气中的氧气发生反应,表面生成一层致密的氧化铝薄膜。人们日常用的铝制品通常都是由铝合金制造的,其表面总是覆盖着致密的氧化铝薄膜,这层膜起着保护内部金属的作用。
教学过程
1. 存在:铝是地壳中含量最多的金属元素,自然界中的铝全部以化合态存在。
一、铝
教学过程
4. 用途:① 纯铝用作导线;②铝合金用于制造汽车、飞机、生活用品等。
一、铝
2.结构:铝的原子结构示意图为
3. 物理性质:银白色有金属光泽的固体,有良好的延展性、导电性和传热性等,密度较小,质地柔软。
教学过程
纯铝的硬度和强度较小,不适合制造机器零件等。向铝中加入少量的合金元素,如Cu、Mg、Si、Mn、Zn及稀土元素等,可制成铝合金。铝合金是目前用途广泛的合金之一。例如,硬铝(一种铝合金) 中含Cu 4%、Mg 0.5%、Mn 0.5%、Si 0.7%,它的密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
硬铝常用于制造飞机的外壳
教学过程
5.化学性质:
(1)铝与氧气的反应
① 常温:铝与空气中的氧气反应,表面生成一层致密的氧化铝薄膜,对内部金属起着保护作用,化学方程式为
② 点燃:铝在氧气中点燃,放出大量的热和耀眼的白光,化学方程式为
4Al+3O2===2Al2O3
4Al+3O2===2Al2O3
点燃
教学过程
(2)铝与(非氧化性)酸的反应
2Al+6HCl=2AlCl3+3H2↑
2Al+6H+=2Al3++3H2↑
思考:铝制餐具为何不宜用来蒸煮或长时间存放酸性或碱性食品?
(3)铝与碱的反应
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
2Al+2OH-+6H2O= 2[Al(OH)4]-+3H2↑
教学过程
实验探究1
探究:在一支试管中加入5mL盐酸,再向试管中放入一小块铝片。观察现象。过一段时间后,将点燃的木条放在试管口,你观察到什么现象
二、氧化铝
铝、氧化铝与酸反应
教学过程
【实验现象】
开始不太明显,铝片逐渐溶解,有气泡冒出,将点燃的木条放在试管口爆鸣声。
1. 铝、氧化铝的性质——与酸反应
Al2O3+6HCl = 2AlCl3+3H2O、2Al+6HCl = 2AlCl3+3H2↑
Al2O3+6H+ = 2Al3++3H2O、2Al+6H+ = 2Al3++3H2↑
教学过程
探究:在两支试管中分别加入少量的NaOH溶液,然后向其中一支试管中放入一小块铝片,向另一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。过一段时间后,将点燃的木条分别放在两支试管口。你观察到什么现象
二、氧化铝
实验探究2
铝、氧化铝与碱的反应
教学过程
教学过程
(3)铝与碱的反应
【实验现象】
试管①中一开始无气泡产生,一段时间后,铝片逐渐溶解,有无色气泡冒出,试管②中铝片溶解,立即产生无色气泡,将点燃的木条放在试管口,都有爆鸣声。
Al2O3+2NaOH+3H2O=2Na[Al(OH)4]、2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
Al2O3+2OH-+3H2O=2[Al(OH)4]-、2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
教学过程
两性氧化物:
既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,如Al2O3。
两性氢氧化物:
既能与酸反应生成盐和水,又能与碱反应生成盐和水的氢氧化物,如Al(OH)3。
Al(OH)3溶于盐酸:
Al(OH)3溶于NaOH溶液:
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+NaOH=Na[Al(OH)4]
在医疗上有一种药叫胃舒平,你知道它的主要成分和作用吗?
说明书:
【成分】本品为复方制剂,
每片含主要成份氢氧化铝
0.45g
【性状】本品为白色片
【适应症】用于缓解胃酸过多
引起的胃痛
教学过程
教学过程
归纳总结——Al3+、Al(OH)3、AlO2-的转化
Al3+ + 3OH- === Al(OH)3↓
Al3+ + 4OH- === AlO2- + 2H2O
AlO2- + 4H+ === Al3+ + 2H2O
Al(OH)3 + OH- === AlO2- + 2H2O
H+ + AlO2- + H2O === Al(OH)3↓
Al(OH)3 + 3H+ === Al3+ + 3H2O
典例1.
取等质量的铝粉两份,分别放入足量的浓氢氧化钠溶液和盐酸溶液中,充分反应后,两者放出氢气的体积( )
A.1:1 B.1:3
C.1:2 D.2:1
课堂练习
【答案】A
典例2.
用氧化铝为原料来制取氢氧化铝的最好的方法是( )
A.将氧化铝粉末溶于水
B.将氧化铝粉 末溶于盐酸,再滴加氢氧化钠溶液
C.将氧化铝粉末溶于盐酸中,再滴加氨水
D.将氧化铝粉末溶于氢氧化铝溶液中,再滴加盐酸
课堂练习
【答案】C
典例3.
用铁、铝的混合物进行如下实验:
课堂练习
(1)操作X的名称是________。
(2)气体A是________。
(3)A与Cl2混合光照可能发生爆炸,生成________(填化学式),A在该反应中作为__________(填“氧化剂”或“还原剂”)。
(4)溶液B中阴离子除OH-外还有________,溶液D中存在的金属离子为________。
过滤
H2
HCl
还原剂
AlO2-
Fe2+
课堂小结
课堂小结
课后小任务
家庭的厨卫管道内常因留有油脂、毛发、菜渣、纸棉纤维等而造成堵塞,此时可以用一种固体管道疏通剂疏通。这种固体管道疏通剂的主要成分有NaOH和铝粉,请解释其疏通原理。
工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对毛发等淤积物的腐蚀,同时产生氢气增加管道内的气压,利于疏通。
感 谢 倾 听
