3.4 配合物与超分子 (第2课时 超分子)(共23张PPT)-【核心素养目标】2023-2024学年高二化学同步精品课件(人教版2019选择性必修2)
文档属性
| 名称 | 3.4 配合物与超分子 (第2课时 超分子)(共23张PPT)-【核心素养目标】2023-2024学年高二化学同步精品课件(人教版2019选择性必修2) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-09-18 00:00:00 | ||
图片预览



文档简介
(共23张PPT)
第二节 配合物与超分子
第2课时 超分子
人教版选择性必修2
榆次一中 李金虎
学习目标
1.了解超分子的结构特点和性质。
2. 了解超分子与分子的区别、超分子的简单应用。
学习目标
1.通过学习和理解超分子内容,充分发挥超分子的学科价值意义,开拓学生科学视野,培养学生学习兴趣,培养学生的科学态度与社会价值的学科素养。
2. 通过研究超分子的结构与用途,进一步培养学生宏观辨识与微观探析的学科素养,强化结构决定性质的化学学科核心思想。
素养目标
情境引入
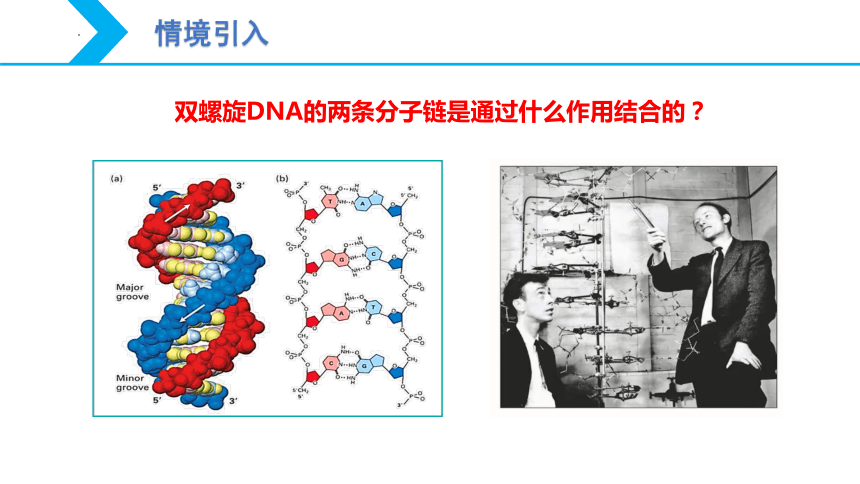
双螺旋DNA的两条分子链是通过什么作用结合的?
教学过程
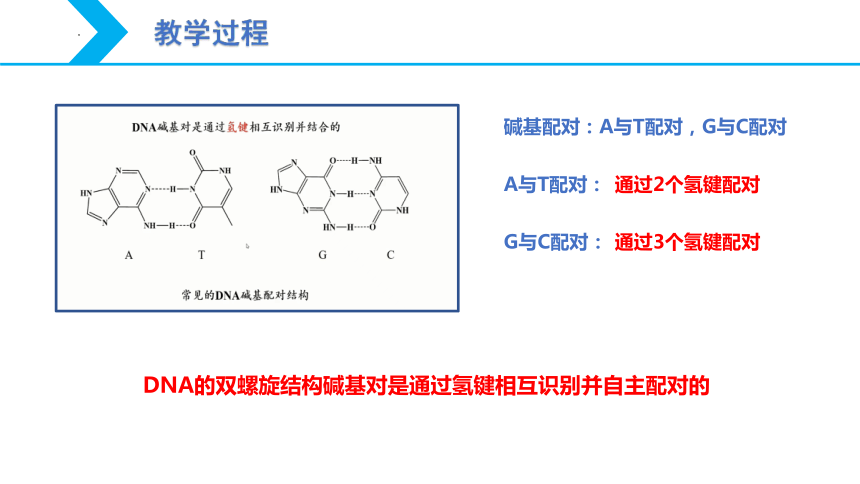
碱基配对:A与T配对,G与C配对
A与T配对:
G与C配对:
通过2个氢键配对
通过3个氢键配对
DNA的双螺旋结构碱基对是通过氢键相互识别并自主配对的
教学过程
氢键是最强的分子间相互作用,很多分子可以通过氢键相互结合,形成具有固定组成的一个分子簇,这就是所谓的超分子。
超分子化学是化学学科的前沿课题之一,超分子在生命科学、材料科学、纳米技术等领域有着广泛的应用,超分子化学涉及到许多新的概念和方法,如分子识别、分子组装、超分子器件等,
教学过程
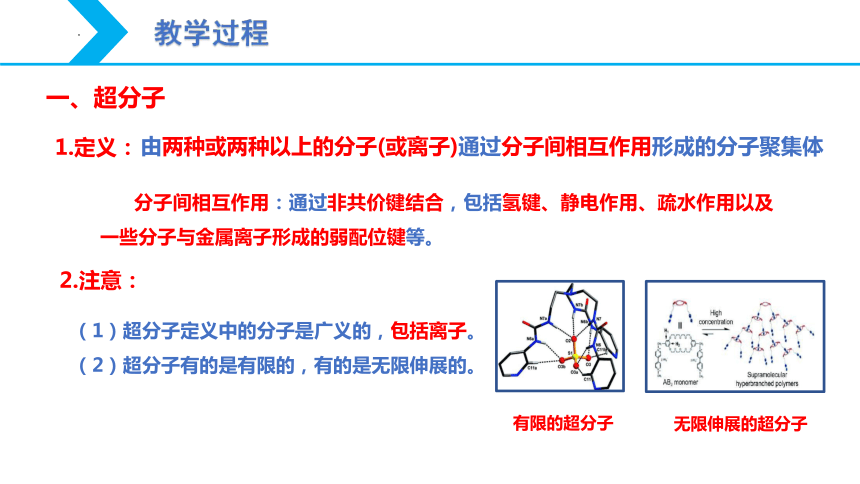
由两种或两种以上的分子(或离子)通过分子间相互作用形成的分子聚集体
一、超分子
1.定义:
分子间相互作用:通过非共价键结合,包括氢键、静电作用、疏水作用以及一些分子与金属离子形成的弱配位键等。
2.注意:
(1)超分子定义中的分子是广义的,包括离子。
(2)超分子有的是有限的,有的是无限伸展的。
有限的超分子
无限伸展的超分子
教学过程
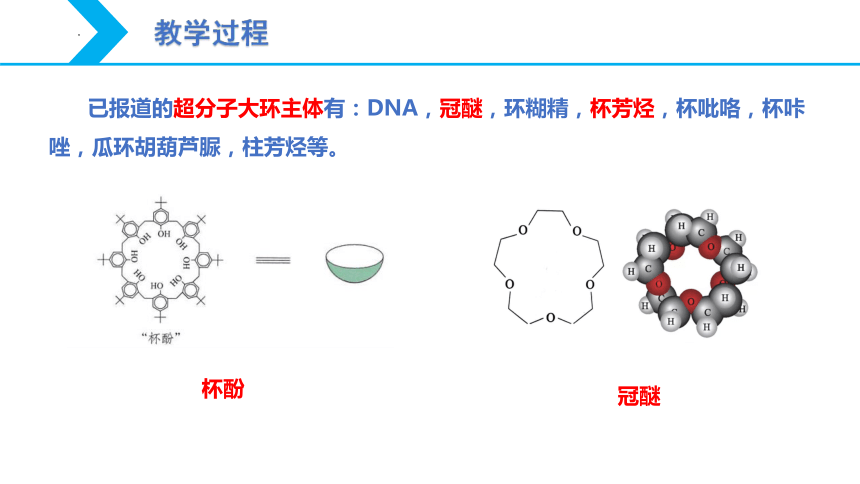
已报道的超分子大环主体有:DNA,冠醚,环糊精,杯芳烃,杯吡咯,杯咔唑,瓜环胡葫芦脲,柱芳烃等。
冠醚
杯酚
教学过程
二、超分子的重要特征及其应用
1.分子识别
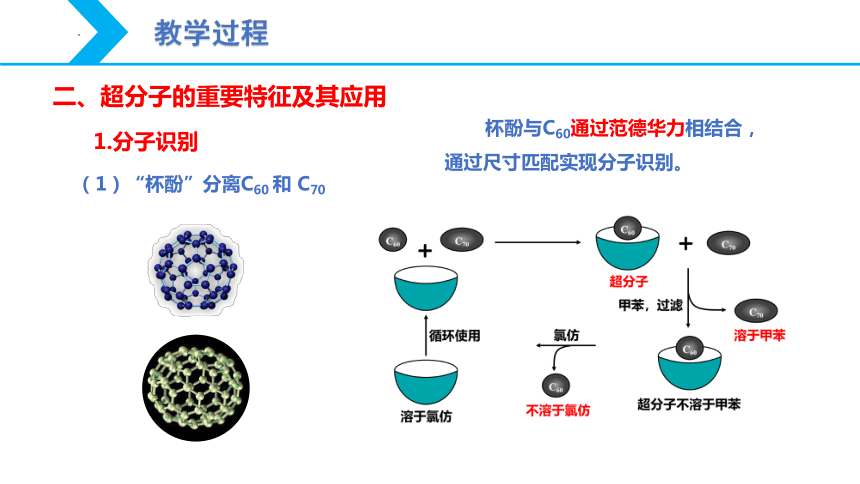
(1)“杯酚”分离C60 和 C70
杯酚与C60通过范德华力相结合,通过尺寸匹配实现分子识别。
教学过程
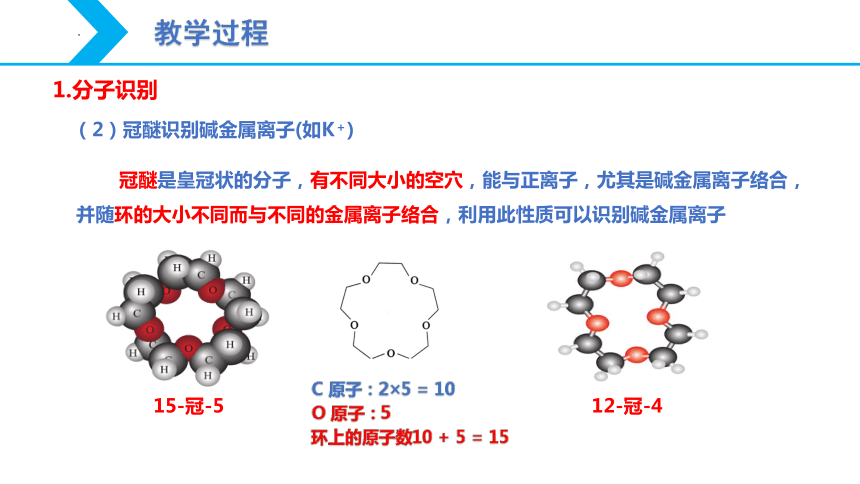
冠醚是皇冠状的分子,有不同大小的空穴,能与正离子,尤其是碱金属离子络合,并随环的大小不同而与不同的金属离子络合,利用此性质可以识别碱金属离子
1.分子识别
(2)冠醚识别碱金属离子(如K+)
12-冠-4
15-冠-5
C 原子:2×5 = 10
O 原子:5
环上的原子数10 + 5 = 15
教学过程
冠醚,是分子中含有多个-氧-亚甲基-结构单元的大环多醚。冠醚的空穴结构对离子有选择作用,不同冠醚的空腔尺寸不同,与不同的阳离子相匹配(配位作用),从而实现选择性结合(识别不同大小的碱金属离子),在有机反应中可作催化剂。
冠醚环的大小与金属离子匹配,才能识别
教学过程
思考1:冠醚通过什么作用力吸引金属阳离子?
冠醚中含有若干个氧原子,带有较多孤电子对,容易通过静电作用与碱金属离子相互吸引(弱配位键)。
思考2:冠醚为什么能定向识别金属离子?
不同的冠醚空腔尺寸不同,与不同阳离子相匹配时,若阳离子直径太大,无法装入空腔,若阳离子直径太小,作用力不充分,形成的超分子不稳定。
教学过程
思考3:KMnO4水溶液对烯烃氧化效果差,在烯烃中加入冠醚时,氧化能力变强,原因是什么呢?
冠醚通过与K+结合而将高锰酸根也带入烯烃中;而冠醚不与高锰酸根结合,使游离的高锰酸根反应活性很高,从而快速发生反应。
教学过程
二、超分子的重要特征及其应用
2.分子自组装
第二章 第三节的“科学·技术·社会”栏表面活性与细胞和细胞器的双分子膜
超分子组装的过程称为分子自组装,是使超分子产生高度有序的过程。
教学过程
超分子有序体
表面活性剂
从分子结构上说,也可以叫“两亲分子”,分子的一端有极性,称为亲水基团,分子的另一端没有或者几乎没有极性,称为疏水基团。
教学过程
这些分子之所以称为表面活性剂,是由于它们会分散在水的液体表面形成一层疏水基团朝向空气的单分子层,又称单分子膜,从而大大降低水的表面张力。高浓度时,剩余的表面活性剂在溶液中形成胶束。
烷基磺酸根离子
胶束
表面活性剂在水的表面形成单分子层
表面活性剂在水中会形成亲水基团向外、疏水基团向内的胶束。由于油渍等污垢是疏水的,会被包裹在胶束内腔,这就是肥皂和洗涤剂的去污原理。
教学过程
细胞膜两侧为水溶液,水是极性分子,而构成膜的两性分子的头基是极性基团,而尾基是非极性基团。头基为亲水基团,头部会朝向水溶液一侧,从而实现自组装。
细胞和细胞器的双分子膜
自组装过程是使超分子产生高度有序的过程
细胞质
疏水端
亲水端
亲水端
教学过程
2020年,我国博士后王振元:潜心创新,成功开发出超分子生物催化技术,打破了国外巨头在化妆品高端原料市场的垄断地位。
通过对超分子研究,人们可以模拟生物系统,复制出一些新材料,如:新催化剂、新药物、分子器件、生物传感器等功能材料。
下列关于超分子的说法不正确的是( )
A.C70属于超分子
B.超分子有的是有限的,有的是无限伸展的
C.C60与“杯酚”可通过分子间作用力形成超分子
D.超分子具有“分子识别”“自组装”两大重要特征
典例1.
【答案】A
课堂练习
典例2.
课堂练习
冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并随着环的大小不同而与不同金属离子作用。
(1)Li+的体积与X的空腔大小相近,恰好能进入X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图)。
①基态锂离子核外能量最高的电子所处电子层符号为 ________。
②W中Li+与孤电子对之间的作用属于________(填字母)。
A.离子键 B.共价键 C.配位键 D.氢键 E.以上都不是
(2)冠醚Y能与K+形成稳定结构,但不能与Li+形成稳定结构。理由是________________。
教学过程
(3)烯烃难溶于水,被KMnO4水溶液氧化的效果较差。若烯烃中溶入冠醚Z,氧化效果明显提升。
①水分子中键角________(填“>”“<”或“=”)109°28′。
②已知:冠醚Z与KMnO4可以发生如图所示的变化。
加入冠醚Z后,烯烃的氧化效果明显提升的原因是 。
教学过程
14.答案 (1)①K ②C
(2)Li+半径比Y的空腔小很多,不易与空腔内O原子的孤电子对作用形成稳定结构
(3)①< ②冠醚Z可溶于烯烃,加入冠醚之中的K+因静电作用将MnO4-带入烯烃中,增大反应物的接触面积,提高了氧化效果
解析:
(1)①基态锂离子核外只有1s能级上有电子,为K层上的电子,所以其电子层符号为K。Li+提空空轨道、O原子提供孤电子对,二者形成配位键。②冠醚Y空腔较大,Li+半径较小,导致该离子不易与氧原子的孤电子对形成配位键,所以得不到稳定结构。(3)①水分子中氧原子的价电子对数是4,根据价层电子对互斥模型判断水分子价层电子对空间结构为四面体。由于水分子中O原子含有2个孤电子对,孤电子对之间的排斥力较强,导致水分子中键角小于109°28′。②根据相似相溶原理知,冠醚Z可溶于烯烃,加入冠醚Z中的K+因静电作用将MnO4-带入烯烃中增,应物的接触面积,提高了氧化效果。
课堂小结
感 谢 倾 听
第二节 配合物与超分子
第2课时 超分子
人教版选择性必修2
榆次一中 李金虎
学习目标
1.了解超分子的结构特点和性质。
2. 了解超分子与分子的区别、超分子的简单应用。
学习目标
1.通过学习和理解超分子内容,充分发挥超分子的学科价值意义,开拓学生科学视野,培养学生学习兴趣,培养学生的科学态度与社会价值的学科素养。
2. 通过研究超分子的结构与用途,进一步培养学生宏观辨识与微观探析的学科素养,强化结构决定性质的化学学科核心思想。
素养目标
情境引入
双螺旋DNA的两条分子链是通过什么作用结合的?
教学过程
碱基配对:A与T配对,G与C配对
A与T配对:
G与C配对:
通过2个氢键配对
通过3个氢键配对
DNA的双螺旋结构碱基对是通过氢键相互识别并自主配对的
教学过程
氢键是最强的分子间相互作用,很多分子可以通过氢键相互结合,形成具有固定组成的一个分子簇,这就是所谓的超分子。
超分子化学是化学学科的前沿课题之一,超分子在生命科学、材料科学、纳米技术等领域有着广泛的应用,超分子化学涉及到许多新的概念和方法,如分子识别、分子组装、超分子器件等,
教学过程
由两种或两种以上的分子(或离子)通过分子间相互作用形成的分子聚集体
一、超分子
1.定义:
分子间相互作用:通过非共价键结合,包括氢键、静电作用、疏水作用以及一些分子与金属离子形成的弱配位键等。
2.注意:
(1)超分子定义中的分子是广义的,包括离子。
(2)超分子有的是有限的,有的是无限伸展的。
有限的超分子
无限伸展的超分子
教学过程
已报道的超分子大环主体有:DNA,冠醚,环糊精,杯芳烃,杯吡咯,杯咔唑,瓜环胡葫芦脲,柱芳烃等。
冠醚
杯酚
教学过程
二、超分子的重要特征及其应用
1.分子识别
(1)“杯酚”分离C60 和 C70
杯酚与C60通过范德华力相结合,通过尺寸匹配实现分子识别。
教学过程
冠醚是皇冠状的分子,有不同大小的空穴,能与正离子,尤其是碱金属离子络合,并随环的大小不同而与不同的金属离子络合,利用此性质可以识别碱金属离子
1.分子识别
(2)冠醚识别碱金属离子(如K+)
12-冠-4
15-冠-5
C 原子:2×5 = 10
O 原子:5
环上的原子数10 + 5 = 15
教学过程
冠醚,是分子中含有多个-氧-亚甲基-结构单元的大环多醚。冠醚的空穴结构对离子有选择作用,不同冠醚的空腔尺寸不同,与不同的阳离子相匹配(配位作用),从而实现选择性结合(识别不同大小的碱金属离子),在有机反应中可作催化剂。
冠醚环的大小与金属离子匹配,才能识别
教学过程
思考1:冠醚通过什么作用力吸引金属阳离子?
冠醚中含有若干个氧原子,带有较多孤电子对,容易通过静电作用与碱金属离子相互吸引(弱配位键)。
思考2:冠醚为什么能定向识别金属离子?
不同的冠醚空腔尺寸不同,与不同阳离子相匹配时,若阳离子直径太大,无法装入空腔,若阳离子直径太小,作用力不充分,形成的超分子不稳定。
教学过程
思考3:KMnO4水溶液对烯烃氧化效果差,在烯烃中加入冠醚时,氧化能力变强,原因是什么呢?
冠醚通过与K+结合而将高锰酸根也带入烯烃中;而冠醚不与高锰酸根结合,使游离的高锰酸根反应活性很高,从而快速发生反应。
教学过程
二、超分子的重要特征及其应用
2.分子自组装
第二章 第三节的“科学·技术·社会”栏表面活性与细胞和细胞器的双分子膜
超分子组装的过程称为分子自组装,是使超分子产生高度有序的过程。
教学过程
超分子有序体
表面活性剂
从分子结构上说,也可以叫“两亲分子”,分子的一端有极性,称为亲水基团,分子的另一端没有或者几乎没有极性,称为疏水基团。
教学过程
这些分子之所以称为表面活性剂,是由于它们会分散在水的液体表面形成一层疏水基团朝向空气的单分子层,又称单分子膜,从而大大降低水的表面张力。高浓度时,剩余的表面活性剂在溶液中形成胶束。
烷基磺酸根离子
胶束
表面活性剂在水的表面形成单分子层
表面活性剂在水中会形成亲水基团向外、疏水基团向内的胶束。由于油渍等污垢是疏水的,会被包裹在胶束内腔,这就是肥皂和洗涤剂的去污原理。
教学过程
细胞膜两侧为水溶液,水是极性分子,而构成膜的两性分子的头基是极性基团,而尾基是非极性基团。头基为亲水基团,头部会朝向水溶液一侧,从而实现自组装。
细胞和细胞器的双分子膜
自组装过程是使超分子产生高度有序的过程
细胞质
疏水端
亲水端
亲水端
教学过程
2020年,我国博士后王振元:潜心创新,成功开发出超分子生物催化技术,打破了国外巨头在化妆品高端原料市场的垄断地位。
通过对超分子研究,人们可以模拟生物系统,复制出一些新材料,如:新催化剂、新药物、分子器件、生物传感器等功能材料。
下列关于超分子的说法不正确的是( )
A.C70属于超分子
B.超分子有的是有限的,有的是无限伸展的
C.C60与“杯酚”可通过分子间作用力形成超分子
D.超分子具有“分子识别”“自组装”两大重要特征
典例1.
【答案】A
课堂练习
典例2.
课堂练习
冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并随着环的大小不同而与不同金属离子作用。
(1)Li+的体积与X的空腔大小相近,恰好能进入X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图)。
①基态锂离子核外能量最高的电子所处电子层符号为 ________。
②W中Li+与孤电子对之间的作用属于________(填字母)。
A.离子键 B.共价键 C.配位键 D.氢键 E.以上都不是
(2)冠醚Y能与K+形成稳定结构,但不能与Li+形成稳定结构。理由是________________。
教学过程
(3)烯烃难溶于水,被KMnO4水溶液氧化的效果较差。若烯烃中溶入冠醚Z,氧化效果明显提升。
①水分子中键角________(填“>”“<”或“=”)109°28′。
②已知:冠醚Z与KMnO4可以发生如图所示的变化。
加入冠醚Z后,烯烃的氧化效果明显提升的原因是 。
教学过程
14.答案 (1)①K ②C
(2)Li+半径比Y的空腔小很多,不易与空腔内O原子的孤电子对作用形成稳定结构
(3)①< ②冠醚Z可溶于烯烃,加入冠醚之中的K+因静电作用将MnO4-带入烯烃中,增大反应物的接触面积,提高了氧化效果
解析:
(1)①基态锂离子核外只有1s能级上有电子,为K层上的电子,所以其电子层符号为K。Li+提空空轨道、O原子提供孤电子对,二者形成配位键。②冠醚Y空腔较大,Li+半径较小,导致该离子不易与氧原子的孤电子对形成配位键,所以得不到稳定结构。(3)①水分子中氧原子的价电子对数是4,根据价层电子对互斥模型判断水分子价层电子对空间结构为四面体。由于水分子中O原子含有2个孤电子对,孤电子对之间的排斥力较强,导致水分子中键角小于109°28′。②根据相似相溶原理知,冠醚Z可溶于烯烃,加入冠醚Z中的K+因静电作用将MnO4-带入烯烃中增,应物的接触面积,提高了氧化效果。
课堂小结
感 谢 倾 听
