第1节金属材料
图片预览








文档简介
(共29张PPT)
香港 中银大厦
这些建筑物所用的各种物品都是由什么材料制成的 你知道它是由哪些元素组成的吗
几十万种材料;由100多种元素中的几十种进行不同的排列组合而形成的。
金属材料(合金)
无机非金属材料(水泥.玻璃.陶瓷)
有机合成材料 (合成纤维.塑料.橡胶)
常见
材料
新材料
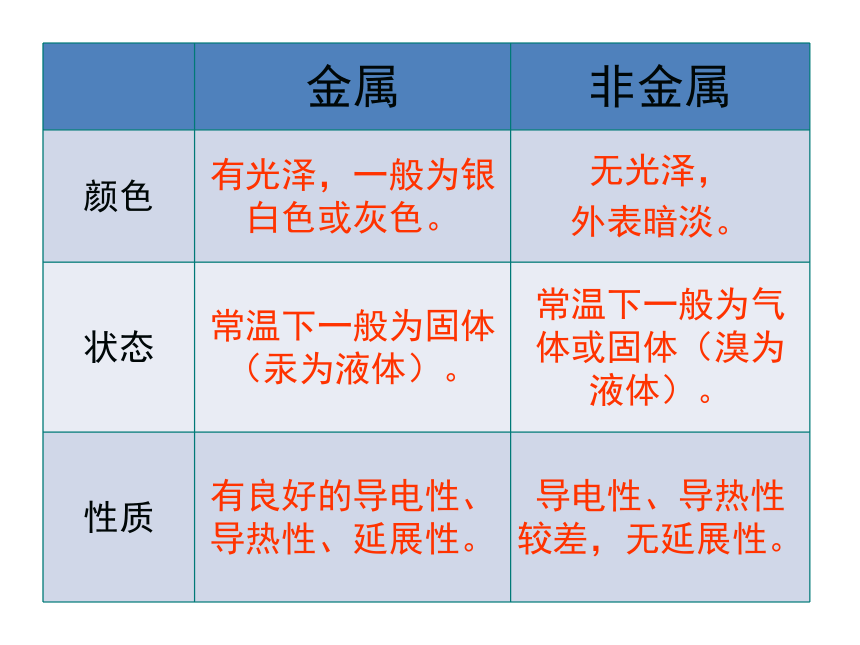
金属 非金属
颜色 有光泽,一般为银白色或灰色。 无光泽,
外表暗淡。
状态 常温下一般为固体(汞为液体)。 常温下一般为气体或固体(溴为液体)。
性质 有良好的导电性、导热性、延展性。 导电性、导热性较差,无延展性。
讨论::在日常生活中哪些地方用到金属?
生活用品,房屋建筑,交通工具,农业生产
铂
水银
铝
铁
镁
钠
思考
现有一种单质,要分辨它是金属还是非金属,你可以用到哪些方法?
1、放在光照下,根据颜色可分辨
可锻性:指金属材料在压力加工时,能改变形状而不产生裂纹的性能。它包括在热态或冷态下能够进行锤锻,轧制,拉伸,挤压等加工。
延展性指的是可以被拉得很长,很薄,但不会断开。可锻性只得是可以被反复捶打。
2、手拿单质在火边烤,根据导热性可分辨
3、用硬物重击单质,可根据可锻性来分辨
4、用力拉单质,可根据延展性来分辨
5、做导电性实验,可根据导电性来分辨……
常见金属的性质:
①有光泽
②比较硬
③有延展性
④有导电性
⑤导热性
⑥具有一定的熔点和沸点等。
有光泽
比较硬
有延展
有导电性
导热性
铁磁性
物 理 特 性 用 途
铁锅、铝茶壶等
铝丝、铜丝等做导线。
做装饰品
做钻头、机器、建筑材料等
拉铁丝、打锄头、做铝箔等
永久磁铁等。
想一想、连一连
1.银是最佳的导热体,为什么银不宜用来 制造煮食器皿?试说出2 种原因。
2.为什么装食品的罐头一般用镀锡的铁制造,而不用纯锡制造?
①银是重金属,易发生重金属中毒
②银年产量低,价格太贵 ③银太软,易变形
④……
因为锡较软,能用小刀切削,且锡的价格比较贵,而机械强度比铁差。镀锡的铁使铁不会被腐蚀(锡的化学性质相对较稳定),而且锡无毒。
合金
18K金
我们可以发现,日常生活中有许多物品是由金属材料制成的。但大多数的金属材料实际上是合金,你知道这是为什么吗
二、常见金属材料
1.合金:把一种金属跟其他一种或几种金属(或非金属)一起熔合而成的,就成为合金。
2.钢:是最常见、应用最广的一种合金材料。
成分:
机械性能好:
用途:
一种由铁和碳等元素组成的合金。
质坚硬、有弹性和延展性。
制作车身、刀具、量具、模具。
注意:1.合金一定有金属特征
2.合金不是单质,也不是化合物,
是一种特殊的混合物
3.合金=金属+金属(或非金属)
4.合金中至少含一种金属.
5.铁的合金——钢和生铁。
(根本区别在于含碳量不同)
6. 使金属材料变成很小很小(纳米级)的粒
子,就会形成纳米粒子。这时,金属的性
质就会发生变化,甚至与原来的性质完全不
同。
铁的合金 生 铁 钢
含碳量
机械性能
加工方法
用途
2%-4.3%
0.03%-2%
硬而脆,无韧性
坚硬,韧性大,弹性好
可铸而不可锻
可铸可锻可压延
含碳量越高,越硬越脆;含碳量越低,韧性越好,越柔软(一般来说,钢的机械性能比生铁好)
制铁锅等
一般用于制造机械、交通工具。
1)合金的导电性较弱。
2)合金的熔点较低。
3)合金强度或硬度较高。
讨论:
1、你觉得合金的性质与纯金属相比有哪些改变呢?哪一类应用更广泛?
合金由于在导电、导热、硬度、延展性等方面具有良好的性质而得到了广泛的应用。
合金往往比金属具有更好的性能。
一些特定成分的合金(如镍钛合金),在外力作用下会发生变形,当把外力去掉后,在一定的温度条件下,能恢复原来的形状。这种合金具有百万次以上的回复功能,人们形象地称之为“记忆合金”。记忆合金在航空、军事、工业、农业、医疗等领域有着重要的用途,从而使得金属的应用又向前跨进了一步。例如,在做牙齿矫形时,人们就是利用记忆合金在一定温度下做成矫形弓丝,矫形弓丝为了恢复原来的形状,便对牙齿施力,于是牙齿在记忆合金的作用下变得整齐好看。而用记忆合金制作的眼镜架,如图所示,则具有良好的弹性、强度和抗拉性能。
记忆合金的用途:
牙齿的矫正
制作航天材料
钛合金的密度约为4.5g/cm3,强度可与钢材相比,抗腐蚀性能好,具有多次锻打加工的性能好等优点,是较为理想的航天工程材料.例如美国的B-1轰炸机的机体结构材料中,钛合金约占21%,主要用于制造机身、机翼、蒙皮和承力构件.随着技术发展,钛合金进入普通百姓家庭,钛合金的眼镜架显得高贵典雅.飞机上用钛合金代替钢材利用了哪些物理性质?
航空航天器在与大气摩擦时,会产生大量的热,使自身温度大幅升高,为保证安全,采用耐高温的钛合金,同时在保证安全、能够完成设计任务的前提下,要尽可能地减轻质量.从减轻质量的要求考虑,由公式m=ρV知,在航空器体积一定的情况下,要减轻质量,只能选择密度较小的材料,因为钛和钛的合金密度小、可塑性好、易于加工,所以可用于制造航天飞机
三、金属的污染与回收利用
1、日常生活废弃的金属垃圾;
2、大量工业废弃的金属垃圾;
3、工厂排出含重金属的污水。
污染来源
金属污染危害
1.浪费大量资源
2.铝等金属在自然界不会自行分解,积累在土壤中,破坏土壤结构。
3.含铅、镉等有毒金属被腐蚀后,导致土壤和地下水源重金属污染。
4.大量使用含铅汽油和废弃的电池都可引起土壤重金属污染。
防治金属污染方法
1.垃圾进行分类回收
2.分类回收各种废弃的金属材料。
3.使用无铅汽油。
4.废旧电池不能任意丢弃。
5.工业废水和废渣不能任意排放和堆放。
1.生铁和稀盐酸溶液充分反应后,总会有残
渣产生,残渣的成分是( )
A.铁 B.氯化铁 C.氯化亚铁 D.碳和一些杂质
2.下列物质中属于合金的是( )
A.三氧化二铁 B.不锈钢
C.铁粉和铜粉混合 D.铁矿石
铝合金
铅锑合金
钢铁
窗材料
保险丝
合金轮胎架等
3.连线题:
4.下列各项比较中,正确的是( )
A.含碳量:生铁>钢 B.含铁量:Fe2O3 > FeO
C.地壳中元素含量:Al<Fe D.韧性:生铁>钢
A
D
B
5.铁是人类生活、生产实际中应用很广的一种金属材料。有关铁的叙述正确的是( )
A.铁能置换出酸中的氢气
B.铁是一种晶体,熔化时温度逐渐升高
C.使用铁锅比使用铝锅更有利于人的健康
D.铁是电的良导体,因为铁是由铁原子直接构成的
C
6.某学生做了如下实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球悬浮于液面;将几枚小铁钉投入烧杯中,到不再有气泡逸出(溶液的体积变化忽略不计),和开始相比,小球的位 置将( )
A.上浮 B.不变 C.下沉 D.沉至杯底
A
7.氯化铁是一种良好的净水剂,化学上可以用多种方法来制取,请写出四种用铁及铁的化合物通过一步化学反应制取氯化铁的四个化学方程式: (注:碳酸铁不要作反应物)
2Fe+3Cl2△2FeCl3
Fe2O3+6HCl=2FeCl3+3H2O
Fe(OH)3+3HCl=FeCl3+3H2O
Fe2(SO4)3+BaCl2=BaSO4↓ +2FeCl3
8.广东佛山是有色金属之乡,其中铝合金材料的产量约占全国的一半;铝合金材料属于_______(选填“纯净物”“混合物”或“单质”),铝是活泼金属,生活中的铝锅却有较强的抗腐蚀性,原因是__________________(用化学方程式表示)如果将铝片投入到稀硫酸中,片刻之后才有气泡产生,请用化学方程式表示这一过程:
混合物
4Al+3O2==2Al2O3
2Al+3H2SO4===Al2(SO4)3+3H2
Al2O3+3H2SO4===Al2(SO4)3+3H2O
9.巳知+3价铁盐跟铁粉在溶液中能发生化合反应,生成亚铁盐,现往生锈的铁粉中加入稀盐酸,过一会儿有气泡产生,反应后铁粉剩余,最终得到一种浅绿色的溶液;写出整个实验过程中所发生的化学方程式。
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
2FeCl3+Fe=3FeCl2
11、研究表明,一节含汞、镉、铅等金属的电池所造成的污染能使600吨水无法饮用,相当于一个人一生的饮水量.为了避免水资源受到污染,防止废旧电池的危害,作为一名中学生,你应该怎样做?
不乱扔废旧电池;废旧电池回收,集中处理.
10.废旧电池易造成有毒金属污染,控制废旧电池危害的根本措施是( )
A.禁止销售电池
B.禁止生产和销售危害性大的电池
C.鼓励把危害性大的电池扔到垃圾箱中
D.把危害性大的电池进行粉碎后,再扔到垃圾箱中
B
钠单质很软,可以用小刀切割.切开外皮后,可以看到钠具有银白色 的金属光泽.钠是热和电的良导体.钠的密度是0.97g/cm3,比水的密度小,钠的熔点是97.81℃,沸点是882.9℃.钠在空气中点燃时,迅速熔化为一个闪亮的小球,发出黄色火焰,生成过氧化钠,钠极易与水反应.根据上述文字描述中,描述的物理性质的有
_____________________________________,化学性质的有 _________________________.
.
质软、银白色、有金属光泽、导电导热、密度小、熔沸点低
易与氧气反应、易与水反应
香港 中银大厦
这些建筑物所用的各种物品都是由什么材料制成的 你知道它是由哪些元素组成的吗
几十万种材料;由100多种元素中的几十种进行不同的排列组合而形成的。
金属材料(合金)
无机非金属材料(水泥.玻璃.陶瓷)
有机合成材料 (合成纤维.塑料.橡胶)
常见
材料
新材料
金属 非金属
颜色 有光泽,一般为银白色或灰色。 无光泽,
外表暗淡。
状态 常温下一般为固体(汞为液体)。 常温下一般为气体或固体(溴为液体)。
性质 有良好的导电性、导热性、延展性。 导电性、导热性较差,无延展性。
讨论::在日常生活中哪些地方用到金属?
生活用品,房屋建筑,交通工具,农业生产
铂
水银
铝
铁
镁
钠
思考
现有一种单质,要分辨它是金属还是非金属,你可以用到哪些方法?
1、放在光照下,根据颜色可分辨
可锻性:指金属材料在压力加工时,能改变形状而不产生裂纹的性能。它包括在热态或冷态下能够进行锤锻,轧制,拉伸,挤压等加工。
延展性指的是可以被拉得很长,很薄,但不会断开。可锻性只得是可以被反复捶打。
2、手拿单质在火边烤,根据导热性可分辨
3、用硬物重击单质,可根据可锻性来分辨
4、用力拉单质,可根据延展性来分辨
5、做导电性实验,可根据导电性来分辨……
常见金属的性质:
①有光泽
②比较硬
③有延展性
④有导电性
⑤导热性
⑥具有一定的熔点和沸点等。
有光泽
比较硬
有延展
有导电性
导热性
铁磁性
物 理 特 性 用 途
铁锅、铝茶壶等
铝丝、铜丝等做导线。
做装饰品
做钻头、机器、建筑材料等
拉铁丝、打锄头、做铝箔等
永久磁铁等。
想一想、连一连
1.银是最佳的导热体,为什么银不宜用来 制造煮食器皿?试说出2 种原因。
2.为什么装食品的罐头一般用镀锡的铁制造,而不用纯锡制造?
①银是重金属,易发生重金属中毒
②银年产量低,价格太贵 ③银太软,易变形
④……
因为锡较软,能用小刀切削,且锡的价格比较贵,而机械强度比铁差。镀锡的铁使铁不会被腐蚀(锡的化学性质相对较稳定),而且锡无毒。
合金
18K金
我们可以发现,日常生活中有许多物品是由金属材料制成的。但大多数的金属材料实际上是合金,你知道这是为什么吗
二、常见金属材料
1.合金:把一种金属跟其他一种或几种金属(或非金属)一起熔合而成的,就成为合金。
2.钢:是最常见、应用最广的一种合金材料。
成分:
机械性能好:
用途:
一种由铁和碳等元素组成的合金。
质坚硬、有弹性和延展性。
制作车身、刀具、量具、模具。
注意:1.合金一定有金属特征
2.合金不是单质,也不是化合物,
是一种特殊的混合物
3.合金=金属+金属(或非金属)
4.合金中至少含一种金属.
5.铁的合金——钢和生铁。
(根本区别在于含碳量不同)
6. 使金属材料变成很小很小(纳米级)的粒
子,就会形成纳米粒子。这时,金属的性
质就会发生变化,甚至与原来的性质完全不
同。
铁的合金 生 铁 钢
含碳量
机械性能
加工方法
用途
2%-4.3%
0.03%-2%
硬而脆,无韧性
坚硬,韧性大,弹性好
可铸而不可锻
可铸可锻可压延
含碳量越高,越硬越脆;含碳量越低,韧性越好,越柔软(一般来说,钢的机械性能比生铁好)
制铁锅等
一般用于制造机械、交通工具。
1)合金的导电性较弱。
2)合金的熔点较低。
3)合金强度或硬度较高。
讨论:
1、你觉得合金的性质与纯金属相比有哪些改变呢?哪一类应用更广泛?
合金由于在导电、导热、硬度、延展性等方面具有良好的性质而得到了广泛的应用。
合金往往比金属具有更好的性能。
一些特定成分的合金(如镍钛合金),在外力作用下会发生变形,当把外力去掉后,在一定的温度条件下,能恢复原来的形状。这种合金具有百万次以上的回复功能,人们形象地称之为“记忆合金”。记忆合金在航空、军事、工业、农业、医疗等领域有着重要的用途,从而使得金属的应用又向前跨进了一步。例如,在做牙齿矫形时,人们就是利用记忆合金在一定温度下做成矫形弓丝,矫形弓丝为了恢复原来的形状,便对牙齿施力,于是牙齿在记忆合金的作用下变得整齐好看。而用记忆合金制作的眼镜架,如图所示,则具有良好的弹性、强度和抗拉性能。
记忆合金的用途:
牙齿的矫正
制作航天材料
钛合金的密度约为4.5g/cm3,强度可与钢材相比,抗腐蚀性能好,具有多次锻打加工的性能好等优点,是较为理想的航天工程材料.例如美国的B-1轰炸机的机体结构材料中,钛合金约占21%,主要用于制造机身、机翼、蒙皮和承力构件.随着技术发展,钛合金进入普通百姓家庭,钛合金的眼镜架显得高贵典雅.飞机上用钛合金代替钢材利用了哪些物理性质?
航空航天器在与大气摩擦时,会产生大量的热,使自身温度大幅升高,为保证安全,采用耐高温的钛合金,同时在保证安全、能够完成设计任务的前提下,要尽可能地减轻质量.从减轻质量的要求考虑,由公式m=ρV知,在航空器体积一定的情况下,要减轻质量,只能选择密度较小的材料,因为钛和钛的合金密度小、可塑性好、易于加工,所以可用于制造航天飞机
三、金属的污染与回收利用
1、日常生活废弃的金属垃圾;
2、大量工业废弃的金属垃圾;
3、工厂排出含重金属的污水。
污染来源
金属污染危害
1.浪费大量资源
2.铝等金属在自然界不会自行分解,积累在土壤中,破坏土壤结构。
3.含铅、镉等有毒金属被腐蚀后,导致土壤和地下水源重金属污染。
4.大量使用含铅汽油和废弃的电池都可引起土壤重金属污染。
防治金属污染方法
1.垃圾进行分类回收
2.分类回收各种废弃的金属材料。
3.使用无铅汽油。
4.废旧电池不能任意丢弃。
5.工业废水和废渣不能任意排放和堆放。
1.生铁和稀盐酸溶液充分反应后,总会有残
渣产生,残渣的成分是( )
A.铁 B.氯化铁 C.氯化亚铁 D.碳和一些杂质
2.下列物质中属于合金的是( )
A.三氧化二铁 B.不锈钢
C.铁粉和铜粉混合 D.铁矿石
铝合金
铅锑合金
钢铁
窗材料
保险丝
合金轮胎架等
3.连线题:
4.下列各项比较中,正确的是( )
A.含碳量:生铁>钢 B.含铁量:Fe2O3 > FeO
C.地壳中元素含量:Al<Fe D.韧性:生铁>钢
A
D
B
5.铁是人类生活、生产实际中应用很广的一种金属材料。有关铁的叙述正确的是( )
A.铁能置换出酸中的氢气
B.铁是一种晶体,熔化时温度逐渐升高
C.使用铁锅比使用铝锅更有利于人的健康
D.铁是电的良导体,因为铁是由铁原子直接构成的
C
6.某学生做了如下实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球悬浮于液面;将几枚小铁钉投入烧杯中,到不再有气泡逸出(溶液的体积变化忽略不计),和开始相比,小球的位 置将( )
A.上浮 B.不变 C.下沉 D.沉至杯底
A
7.氯化铁是一种良好的净水剂,化学上可以用多种方法来制取,请写出四种用铁及铁的化合物通过一步化学反应制取氯化铁的四个化学方程式: (注:碳酸铁不要作反应物)
2Fe+3Cl2△2FeCl3
Fe2O3+6HCl=2FeCl3+3H2O
Fe(OH)3+3HCl=FeCl3+3H2O
Fe2(SO4)3+BaCl2=BaSO4↓ +2FeCl3
8.广东佛山是有色金属之乡,其中铝合金材料的产量约占全国的一半;铝合金材料属于_______(选填“纯净物”“混合物”或“单质”),铝是活泼金属,生活中的铝锅却有较强的抗腐蚀性,原因是__________________(用化学方程式表示)如果将铝片投入到稀硫酸中,片刻之后才有气泡产生,请用化学方程式表示这一过程:
混合物
4Al+3O2==2Al2O3
2Al+3H2SO4===Al2(SO4)3+3H2
Al2O3+3H2SO4===Al2(SO4)3+3H2O
9.巳知+3价铁盐跟铁粉在溶液中能发生化合反应,生成亚铁盐,现往生锈的铁粉中加入稀盐酸,过一会儿有气泡产生,反应后铁粉剩余,最终得到一种浅绿色的溶液;写出整个实验过程中所发生的化学方程式。
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
2FeCl3+Fe=3FeCl2
11、研究表明,一节含汞、镉、铅等金属的电池所造成的污染能使600吨水无法饮用,相当于一个人一生的饮水量.为了避免水资源受到污染,防止废旧电池的危害,作为一名中学生,你应该怎样做?
不乱扔废旧电池;废旧电池回收,集中处理.
10.废旧电池易造成有毒金属污染,控制废旧电池危害的根本措施是( )
A.禁止销售电池
B.禁止生产和销售危害性大的电池
C.鼓励把危害性大的电池扔到垃圾箱中
D.把危害性大的电池进行粉碎后,再扔到垃圾箱中
B
钠单质很软,可以用小刀切割.切开外皮后,可以看到钠具有银白色 的金属光泽.钠是热和电的良导体.钠的密度是0.97g/cm3,比水的密度小,钠的熔点是97.81℃,沸点是882.9℃.钠在空气中点燃时,迅速熔化为一个闪亮的小球,发出黄色火焰,生成过氧化钠,钠极易与水反应.根据上述文字描述中,描述的物理性质的有
_____________________________________,化学性质的有 _________________________.
.
质软、银白色、有金属光泽、导电导热、密度小、熔沸点低
易与氧气反应、易与水反应
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
