共价键高一上化学人教版(2019)必修第一册(共26张PPT)
文档属性
| 名称 | 共价键高一上化学人教版(2019)必修第一册(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-24 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
第四章 第三节化学键
第二课时 共价键
新课引入
为什么2个氢原子结合成氢分子,2个氯原子结合成氯 分子,而不是3个、4个呢 为什么1个氢原子和1个氯原子 结合成氯化氢分子,而不是以其他的个数比相结合呢
Cl 的形成过程
((
通过共用电子对: Cl 17
原子最外层电子数目
一般能达到稳定结构
Cl原子们,你们
愿意各自拿出1个
电子共用吗
00
电子
电子
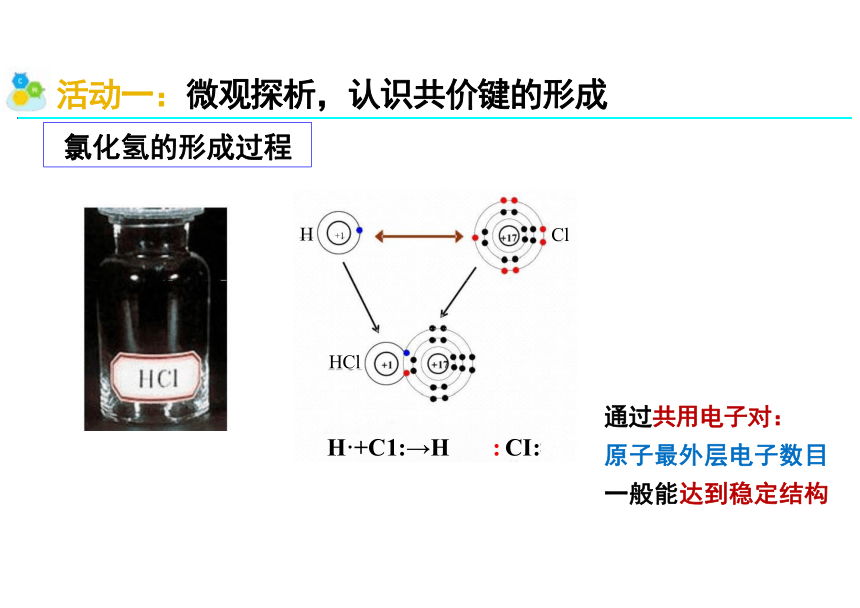
活动一:微观探析,认识共价键的形成
愿意
Cl
共用电子对
H +1 Cl
HCl
H·+C1:→H : CI:
通过共用电子对:
原子最外层电子数目
一般能达到稳定结构
活动一:微观探析,认识共价键的形成
氯化氢的形成过程
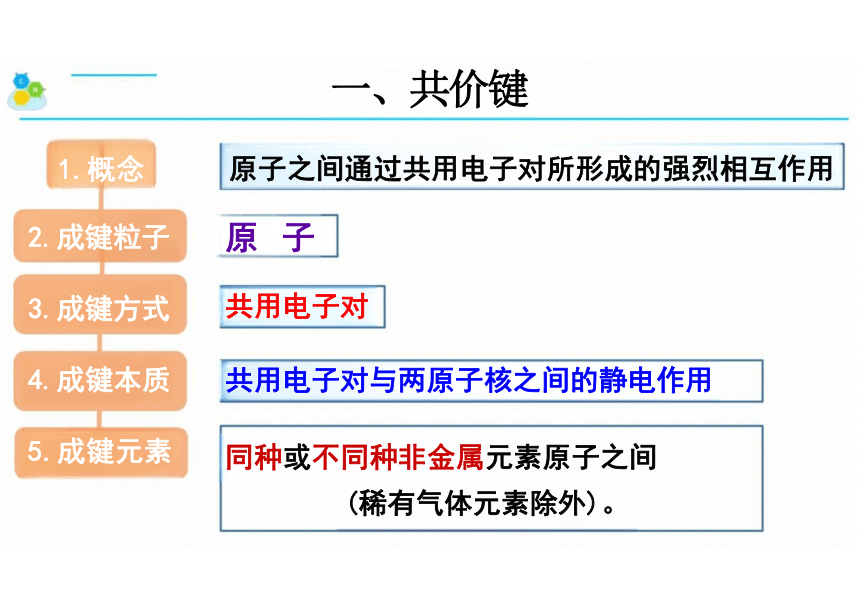
一、共价键
原子之间通过共用电子对所形成的强烈相互作用
原 子
共用电子对
共用电子对与两原子核之间的静电作用
同种或不同种非金属元素原子之间
(稀有气体元素除外)。
1.概念
2.成键粒子 3.成键方式 4.成键本质 5.成键元素
共价化合物类别:
①非金属氢化物如H C、H O 等;
②非金属氧化物如CO 、SO 等;
③酸如H SO 、HNO 等;
④大多数有机化合物如甲烷、酒精等。
二、共价键化合物
定 义 :以 共用电子对形成分子的化合物,叫共价化合物。 如:HCl、CO 、NH 等
非金属氧化物(H O、CO、CO )
非金属氢化物(HCl、 酸 )
大多数有机化合物(CH 等 )
注意:
稀有气体单质中 不存在共价键
某些离子化合物(即原子团) (NaOH、NH Cl )
6.共价键的存在
非金属单质(H 、O )
1、下列哪些物质是共价化合物
①CH ②CO ③HNO ④C H OH ⑤NaCl
2、判断正误
(1)共价键与离子键的成键微粒是一样的( )
(2)非金属元素只能形成共价键( )
(3)单质分子中一定含共价键( )
(4)只由非金属元素组成的化合物一定是共价化合物( )
课堂练习
(1)两个“一定”
①共价化合物中一定只含有 共价键;
②共价化合物中一定 不含离子键。
(2)两个“不一定”
①含共价键的物质不一定是共价化合物,也可能是单质,如O 、 N 、H 、Cl 等 ;
②含共价键的化合物不一定是共价化合物,也可能是离子化合物,
如NaOH中含有0—H共价键,Na O 中含有0—0共价键, NH Cl中含有N—H共价键,但它们都是离子化合物。
共价键的两个“一定”和两个“不一定”
电子对偏向Cl
共用电子对偏向吸引电子 能力强的原子,成键的原 子呈正电性或负电性。
电子对不偏移
共用电子对不偏向任 何一个原子,两个原 子均不显电性。
【思考】Cl 和HCl都靠共价键形成的分子,其共价键是否相同呢
成键元素相同A-A 型 成键元素不同A-B 型
7.共价键的分类
非极性共价键一
极性共价键
分子
电子式
N
:N::N:
CO
:xC:
H O
H: ×H
CH
H
H:CH
H
NH
h
书写要求: ①每个原子均应达到稳定的结构 ②不加中括号[],不标正负电荷数 与离子化合 物书写的区别
③原子最外层电子数距8电子稳定结构差几个
电子,就提供几个电子,并在此原子周围形成 几对共用电子对(即几个共价键)
三、共价分子结构的表示方法
1. 电子式
H:H
::C::
L 。N。●I
H
N
H O
HCl
H
CO
NH
H: :H
H :C1:
练习、书写下列物质的电子式
:N::N:
H·N 1
2.结构式
化学上,常用“—”表示一对共用电子,非共用电子省略不标。 H
规律:共用的电子对数=8-最外层电子数(H 除外)
分别用“一、=、=”表示一对、二对和三对共用电子对
HONOH
H
H —N—H
:Nθ ) N:
N = N
分子 电子式 结构式 分子结构模型
N :N::N: N 三 N
直
线
CO O=C=0
型
H O H× ×H
V形
CH 正四面体
NH HxNxH H 三角锥形
几种常见的以共价键形成的分子及其结构
*H 的 形 成 : H · 十 ·H →H:H
*HCl分子的形成:H·+·Cl:→H:C:
H
*氨分子的形成:3H ·十 ·N: →H:N:
H
*二氧化碳分子的形成: ·C ·+2 ·0 ·→0::C::0 注意事项:①因没有发生电子的得失,不能画弯箭号
②没有形成离子,不加中括号[],不标正负电荷数
3、用电子式表示原子形成共价键的形成过程表示
:i+ :i:j
2 H·十 · H: :H
碘
硫化氢
过氧化氢
练习 用电子式表示下列共价分子的形成过程
定
义 物质中相邻的原子之间强烈的相互作用叫做化学键
原子的价电子间的转移 形成
类别 原子的价电子间的共用
四、构成物质微粒间的相互作用
一般的化学物质主要由离子键或共价键结合而成。
极性键
非极性键
离子键
共价键
1.化学键
化学键
2. 从化学键的角度认识化学反应的本质
H 和Cl 反应生成HCl可用如下过程表示:
化学反应的过程7本质上就是旧化学键断裂和新化学键形成。
断裂H—H
断 裂C1—C1
形成H—Cl
2H:Cl:
H:H
:C1:Ci
2H ·
2: C
3 .知识拓展
(1)分子间作用力
①分子之间存在一种把分子聚集在一起的作用力,叫做分子间作用力,最初 又称范德华力。范德华力比化学键弱得多。
②由分子构成的物质,其熔、沸点等物理性质主要由分子间作用力大小决定。
一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力
越大,分子的熔、沸点越高。如:F(2)氢键
①氢键不是化学键,通常把氢键看作是 一种较强的分子间作用力。氢键比化学 键弱 ,比范德华力强。
②分子间形成的氢键会使物质的熔、沸 点升 高,水分子间的氢键可使其密度在 固态时小于液态时的密度。
氢键
化学键
水分子
H O
化学键 分子间作用力
氢键
概念 物质中相邻的原子之 间强烈的相互作用 分子间存在着将分子 聚集在一起的作用力
N、O、F这些氢化物分子间 的相互作用
存在 范围 相邻原子之间 分子间
HF、H O、NH 等分子间
强弱 较强 很弱
比化学键弱,比分子间作用 力强
对物质 性质的 影响 主要影响化学性质 只影响物理性质 随相对分子质量的增 大,熔点、沸点升高
使得物质的熔点、沸点升高, 在水中的溶解度增大
化学键、分子间作用力与氢键的比较
判断正误
(1)NaOH 中含有离子键和极性共价键( √ )
(2)氢键是化学键的一种(× )
(3)稀有气体中不存在化学键(√ )
(4)水分子稳定,是因为水分子间存在氢键(× )
练习1
下列变化中,既有旧化学键断裂又有新化学键形成过程的是( B )
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
练习2
非极性共价键
极性共价键
氢键及分子 间作用力
离子键
共价键
熔沸点 硬度 溶解性
原子间
价电子 的得失
原子间 价电子 的共用
不偏移
偏移
学习小结
共用
电子对
决定
反映
物理性质
化学键
1.下列表述正确的是( B )
A.H O 的电子式:H+[:0:0:]H
B.Cl原子的结构示意图:
C.氮气的结构式::N=N:
D.CO 的分子结构模型:O0O
自我测试
2.在下列物质中:
A.氩 B.NaOH C.甲烷(CH )D. 氯化钡 E.氮气 F.NH G.CCl H.H O
(1)只含离子键的物质是 D (填字母,下同)。
(2)既有离子键又有共价键的物质是 B 0
(3)只含极性键的物质是_CFG 。
(4)含非极性键的物质是_EH 。
(5)NaOH溶于水时,断开的化学键的类型为 离子键。
自我测试
第四章 第三节化学键
第二课时 共价键
新课引入
为什么2个氢原子结合成氢分子,2个氯原子结合成氯 分子,而不是3个、4个呢 为什么1个氢原子和1个氯原子 结合成氯化氢分子,而不是以其他的个数比相结合呢
Cl 的形成过程
((
通过共用电子对: Cl 17
原子最外层电子数目
一般能达到稳定结构
Cl原子们,你们
愿意各自拿出1个
电子共用吗
00
电子
电子
活动一:微观探析,认识共价键的形成
愿意
Cl
共用电子对
H +1 Cl
HCl
H·+C1:→H : CI:
通过共用电子对:
原子最外层电子数目
一般能达到稳定结构
活动一:微观探析,认识共价键的形成
氯化氢的形成过程
一、共价键
原子之间通过共用电子对所形成的强烈相互作用
原 子
共用电子对
共用电子对与两原子核之间的静电作用
同种或不同种非金属元素原子之间
(稀有气体元素除外)。
1.概念
2.成键粒子 3.成键方式 4.成键本质 5.成键元素
共价化合物类别:
①非金属氢化物如H C、H O 等;
②非金属氧化物如CO 、SO 等;
③酸如H SO 、HNO 等;
④大多数有机化合物如甲烷、酒精等。
二、共价键化合物
定 义 :以 共用电子对形成分子的化合物,叫共价化合物。 如:HCl、CO 、NH 等
非金属氧化物(H O、CO、CO )
非金属氢化物(HCl、 酸 )
大多数有机化合物(CH 等 )
注意:
稀有气体单质中 不存在共价键
某些离子化合物(即原子团) (NaOH、NH Cl )
6.共价键的存在
非金属单质(H 、O )
1、下列哪些物质是共价化合物
①CH ②CO ③HNO ④C H OH ⑤NaCl
2、判断正误
(1)共价键与离子键的成键微粒是一样的( )
(2)非金属元素只能形成共价键( )
(3)单质分子中一定含共价键( )
(4)只由非金属元素组成的化合物一定是共价化合物( )
课堂练习
(1)两个“一定”
①共价化合物中一定只含有 共价键;
②共价化合物中一定 不含离子键。
(2)两个“不一定”
①含共价键的物质不一定是共价化合物,也可能是单质,如O 、 N 、H 、Cl 等 ;
②含共价键的化合物不一定是共价化合物,也可能是离子化合物,
如NaOH中含有0—H共价键,Na O 中含有0—0共价键, NH Cl中含有N—H共价键,但它们都是离子化合物。
共价键的两个“一定”和两个“不一定”
电子对偏向Cl
共用电子对偏向吸引电子 能力强的原子,成键的原 子呈正电性或负电性。
电子对不偏移
共用电子对不偏向任 何一个原子,两个原 子均不显电性。
【思考】Cl 和HCl都靠共价键形成的分子,其共价键是否相同呢
成键元素相同A-A 型 成键元素不同A-B 型
7.共价键的分类
非极性共价键一
极性共价键
分子
电子式
N
:N::N:
CO
:xC:
H O
H: ×H
CH
H
H:CH
H
NH
h
书写要求: ①每个原子均应达到稳定的结构 ②不加中括号[],不标正负电荷数 与离子化合 物书写的区别
③原子最外层电子数距8电子稳定结构差几个
电子,就提供几个电子,并在此原子周围形成 几对共用电子对(即几个共价键)
三、共价分子结构的表示方法
1. 电子式
H:H
::C::
L 。N。●I
H
N
H O
HCl
H
CO
NH
H: :H
H :C1:
练习、书写下列物质的电子式
:N::N:
H·N 1
2.结构式
化学上,常用“—”表示一对共用电子,非共用电子省略不标。 H
规律:共用的电子对数=8-最外层电子数(H 除外)
分别用“一、=、=”表示一对、二对和三对共用电子对
HONOH
H
H —N—H
:Nθ ) N:
N = N
分子 电子式 结构式 分子结构模型
N :N::N: N 三 N
直
线
CO O=C=0
型
H O H× ×H
V形
CH 正四面体
NH HxNxH H 三角锥形
几种常见的以共价键形成的分子及其结构
*H 的 形 成 : H · 十 ·H →H:H
*HCl分子的形成:H·+·Cl:→H:C:
H
*氨分子的形成:3H ·十 ·N: →H:N:
H
*二氧化碳分子的形成: ·C ·+2 ·0 ·→0::C::0 注意事项:①因没有发生电子的得失,不能画弯箭号
②没有形成离子,不加中括号[],不标正负电荷数
3、用电子式表示原子形成共价键的形成过程表示
:i+ :i:j
2 H·十 · H: :H
碘
硫化氢
过氧化氢
练习 用电子式表示下列共价分子的形成过程
定
义 物质中相邻的原子之间强烈的相互作用叫做化学键
原子的价电子间的转移 形成
类别 原子的价电子间的共用
四、构成物质微粒间的相互作用
一般的化学物质主要由离子键或共价键结合而成。
极性键
非极性键
离子键
共价键
1.化学键
化学键
2. 从化学键的角度认识化学反应的本质
H 和Cl 反应生成HCl可用如下过程表示:
化学反应的过程7本质上就是旧化学键断裂和新化学键形成。
断裂H—H
断 裂C1—C1
形成H—Cl
2H:Cl:
H:H
:C1:Ci
2H ·
2: C
3 .知识拓展
(1)分子间作用力
①分子之间存在一种把分子聚集在一起的作用力,叫做分子间作用力,最初 又称范德华力。范德华力比化学键弱得多。
②由分子构成的物质,其熔、沸点等物理性质主要由分子间作用力大小决定。
一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力
越大,分子的熔、沸点越高。如:F
①氢键不是化学键,通常把氢键看作是 一种较强的分子间作用力。氢键比化学 键弱 ,比范德华力强。
②分子间形成的氢键会使物质的熔、沸 点升 高,水分子间的氢键可使其密度在 固态时小于液态时的密度。
氢键
化学键
水分子
H O
化学键 分子间作用力
氢键
概念 物质中相邻的原子之 间强烈的相互作用 分子间存在着将分子 聚集在一起的作用力
N、O、F这些氢化物分子间 的相互作用
存在 范围 相邻原子之间 分子间
HF、H O、NH 等分子间
强弱 较强 很弱
比化学键弱,比分子间作用 力强
对物质 性质的 影响 主要影响化学性质 只影响物理性质 随相对分子质量的增 大,熔点、沸点升高
使得物质的熔点、沸点升高, 在水中的溶解度增大
化学键、分子间作用力与氢键的比较
判断正误
(1)NaOH 中含有离子键和极性共价键( √ )
(2)氢键是化学键的一种(× )
(3)稀有气体中不存在化学键(√ )
(4)水分子稳定,是因为水分子间存在氢键(× )
练习1
下列变化中,既有旧化学键断裂又有新化学键形成过程的是( B )
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
练习2
非极性共价键
极性共价键
氢键及分子 间作用力
离子键
共价键
熔沸点 硬度 溶解性
原子间
价电子 的得失
原子间 价电子 的共用
不偏移
偏移
学习小结
共用
电子对
决定
反映
物理性质
化学键
1.下列表述正确的是( B )
A.H O 的电子式:H+[:0:0:]H
B.Cl原子的结构示意图:
C.氮气的结构式::N=N:
D.CO 的分子结构模型:O0O
自我测试
2.在下列物质中:
A.氩 B.NaOH C.甲烷(CH )D. 氯化钡 E.氮气 F.NH G.CCl H.H O
(1)只含离子键的物质是 D (填字母,下同)。
(2)既有离子键又有共价键的物质是 B 0
(3)只含极性键的物质是_CFG 。
(4)含非极性键的物质是_EH 。
(5)NaOH溶于水时,断开的化学键的类型为 离子键。
自我测试
