4.1.2元素周期表 同位素 课件 高中化学人教版(2019)必修第一册(共20张PPT)
文档属性
| 名称 | 4.1.2元素周期表 同位素 课件 高中化学人教版(2019)必修第一册(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-24 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
第一节
原子结构与元素周期表
第2课时
元素周期表
1869年,门捷列夫依据相对原子质量,制出元素周期表, 并发现元素周期律,对未知元素留空位
德米特里 ·伊万诺维奇 ·门捷列夫
I I 】 M V M M W
X
Li7.01 B 11 C11.97 Al 27.3 Si 28 Ti 48 Zr 89.7 In 113.4 Sn 117.8
T1202.7 Pb 206.4
N14.01 P 30.9 V 51.2 As 74.9 Nb 93.7 Sb 122.1 Ta 182.2
Bi207.5
015.96 S 31.98 Cr 52.4 Se 78.0 Mo 95.6 Te 128 W 183.5
F19.1 CI 35.38 Mn 54.8 Fe 55.9 Co &.Ni 58.6 Br 79.75 Ru 103.5 Rh 104.1 Pd 106.2 I126.5 Os 198.6 Ir 196.7 Pt 196.7
Na 22.99 K 39.04 Cu 63.3 Rb 85.2 Ag 107.66 Cs 132.7 Au 196.2
Be 9.3 Mg 23.9 Ca 39.9 Zn 64.9 Sr 87.0 Cd 111.6 Ba 136.8 Hg 199.8
日.N日
1870年,迈尔划分相似元素,形成过渡元素
迈 尔 的 元 素 周 期 表 (1869)
70 Yb
镱
173.0
71 Lu
镥
17496
化 学 元 素 周 期 表 ⅡA ⅢA IVA VA VIA VIIA 00
2 He
氦
4.0026
3E 锂 6.941 11Na 钠 229898 4 Be 铍 90122 12 Mg 镁 24305 ⅢIB VB VB VIB VIIB VⅢ IB ⅢB 081 碳 2011 7N 氮 14007 8.0 氧 6099 9 18993
10 Ne
氖
20.17
13AL 铝 26.982 14Si 硅 28085 5F 磷 20904 65 硫 3206 17dl 氩 453
18Ar
氩
39.94
19k 钾 39.098 20 Ca 钙 40.03 21 Sc 钪 44.956 22Ti 钛 47.9 23V 钒 50.9415 24 Cr 铬 51.996 25 Mn 锰 54938 26 Fe 铁 55.84 27 Co 钴 58.9332 28 Ni 镍 58.69 29 Cu 铜 63,54 30 Zn 锌 65.38 31Ga 镓 6902 32 Ge 锗 72.59 23As 砷 74921 34Se 硒 739 35Bn 溴 09904
36 Kr
氪
83.8
37Rb 85.467 38Sr 锶 87.62 39Y 钇 88.906 40 Zr 锆 91,22 41 Nb 铌 92.9064 42 Mo 钼 95.94 43 To 锝 99 44RU 钌 101.07 45 Rh 铑 102.906 46 Pd 钯 106.42 47 Ag 银 107.868 48 Cd 镉 112.41 49In 铟 114.82 50.Sn 锡 1186 511Sb 锑 1217 52 Te 碲 1276 531 碘 6903
54Xe
氙
1313
5s Cs 铯 132.905 87Er 钫 (223) 56.Ba 钡 13733 88镭Ra 226,03 57-71 La-Lu 镧系 89-103 Ac-Lr 锏系 72 Hf 铪 178.4 104 Rf 鳙 (261) 73Ta 钽 180.947 105 Db 壮 (262) 74W 钨 183.8 106 Sg 馆 (266) 75 Re 铼 186.207 76.0s 锇 190.2 77 Ir 铱 192.2 78 Pt 铂 195.08 79 Au 金 196.967 80 Hg 汞 2005 81 铊 2043 82Pb 铅 2072 83 B 铋 20898 84 Po 钋 (209) 85 砹 (201
86 Rn
氡
(222)
107 Bh 铍 (264) 108Hs (269) 109 Mt 绥 (268) 110 Ds 键 (271) 111 Rg 输 (272) 112 Uub (285) 113 Uut (284 114 Uuq (289) 115 Uup (288) 116 Uuh (292) 117 Uus
118
Uuo
询 系 57 La 镧 138.905 58 Ce 铈 140.12 59 Pr 镨 140.91 60 Nd 钕 144.2 61 Pm 钷 147 62 Sm 钐 150.4 63 Eu 铕 151.96 64 Gd 钆 157.25 65 Tb 铽 158.93 66 Dy 镝 162.5 67 Ho 钬 164.93 68 Er 铒 167.2 69 Tm 铥 168.934
89 Ac 的 (227) 90 Th 钍 232.03 91 Pa 镁 231.03 92U 铀 238.02 93 Np 锋 237.04 94 Pu 钚 (244) 95 Am 错 (243) 96 Cm 铜 (247) 97 Bk 镨 (247) 98 Cf 镧 (251) 99 Es 铱 (254 100 Fm 锁 (257) 101 Md 们 (258)
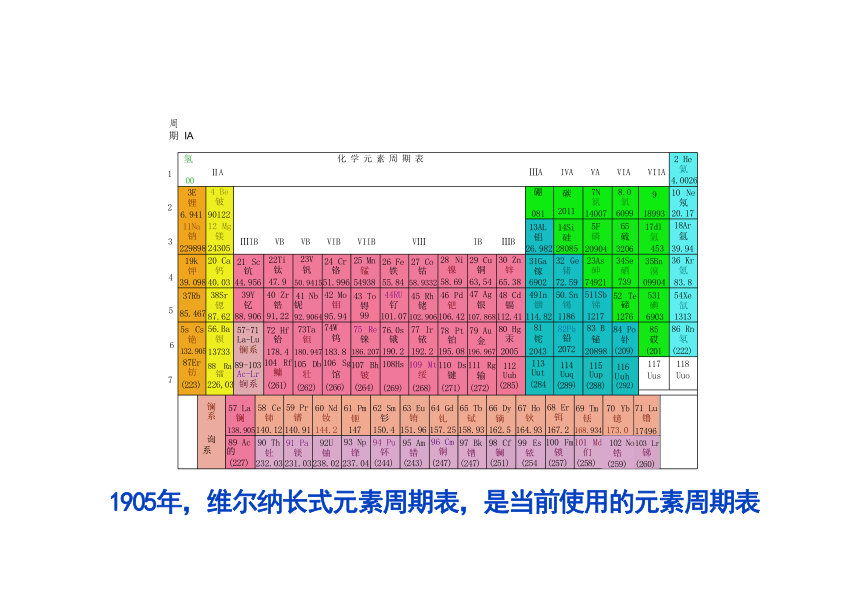
1905年,维尔纳长式元素周期表,是当前使用的元素周期表
1
2
3
4
5
6
7
103 Lr
锑
(260)
102 No
锆
(259)
周
期 IA
镧系
氢
硼
Periodic Table of the Elements A 3A 14 VA 4A 15 5A 16 /A 5A 17 VILA
2
He
40
Be Mg 3 3 1B 38 48VB 5 VB 58 6 /1B 6B 7 VIIB 78 9 /Ill 10 11 1B 2B 5 B 10.811 C 12011 N 14007 0 15.999 F 18998
10
Ne
20.180
13 AI 26982 14 Si 2B.086 15 P 30974 16 S 32066 17 CI 35453
18
Ar
39948
20 Ca 10.078 21 Sc 44956 22 Ti 47.88 23 V 50.042 24 Cr 51.906 25 Mn 549 26 Fe 55933 27 Co 58.903 28 Ni 29 Cu 834 30 Zn 65.39 31 Ga 00732 32 Ge 72.61 33 As 74922 34 Se 7809 35 Br 79.904
36
Kr
8480
Sr 76 39 906 Z 22 41 Nb 06 42 Mo h 05.9 3 Tc 93.907 4 Ru 101.0 45 Rh 102.9 46 Pd 106.42 47 Ag 10786 48 Cd 1124u 49 In 114.818 50 Sn 11871 51 Sb 121.760 52 Te 1276 53 126904
54
Xe
13129
32.90 Ba 37.32 7. 2 Hf 178.49 73 80948 74 75 6 68.207 76 O 9 77 92 78 08 79 80 Hg 200.59 81 TI 204383 82 Pb 2072 83 Bi 203980 84 Po 203992 85 At 209987
86
Rn
222018
Ra 39.103 04 Rf 05 ) 06 107 Bh 108 109 Cr Ju 14 F t JuS
Juo
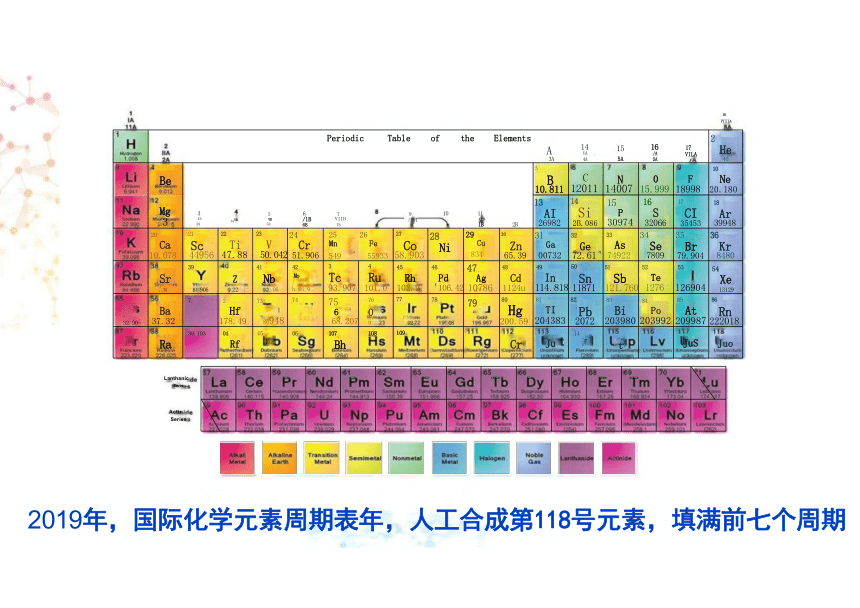
2019年,国际化学元素周期表年,人工合成第118号元素,填满前七个周期
Lanthanic
Serie
Actir
Series
18
VIIIA
I IⅡ Ⅲ IV V VI VII VIII
【回顾初中】
质子数=原子序数=核外电子数=核电荷数
电子层数=周期数,最外层电子数相同排一纵列
【展示】 由相对原子质量改为原子的质子数(核外电子数或核电荷数),形成现行的元素周期表
每一个横行叫作一个周 期,每一个纵行叫作一个族(VI 族包含三个纵列)
B C N 0
13 14 15 16 17
Al Si P S CI
31 32 33 34 35
Zn Ga Ge As Se Br
48 49 60 51 62 53
105 106 107 108 109 110 111 112
Db Sg Bh Hs Mt Ds Rg Cn
58 59 60 61 62 63 64 65
Ce Pr Nd Pm Sm Eu Gd Tb
Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te Xe
72 73 74 75 76 77 78 79 80 81 82 83 B4 85
周 期 族
元素周期表有7个横行,18个纵列
22 2 25 26 27 28
Sc T V Gr Mn Fe Co Ni Cu
39 40 41 42 43 44 45 46 47
113 114 115 116 117 Uut F Uup LV Uus
f6 67 68 69 70
Dy Ho Er Tm Yb
01 95 96
Pu Am Cm Bk
7个
10s
16个
Ba Hf Ta W Re Os Ir Pt Au Hg T Pb Bi Po At Rn
【看图识记】
la Mg
Ca
8
ie
Ne
An Kr
2
3
5
6
7
101 10 Md No
9B
CF Es
01
Pa U
u
LU
93 Np
104
Rf
Th
Fm
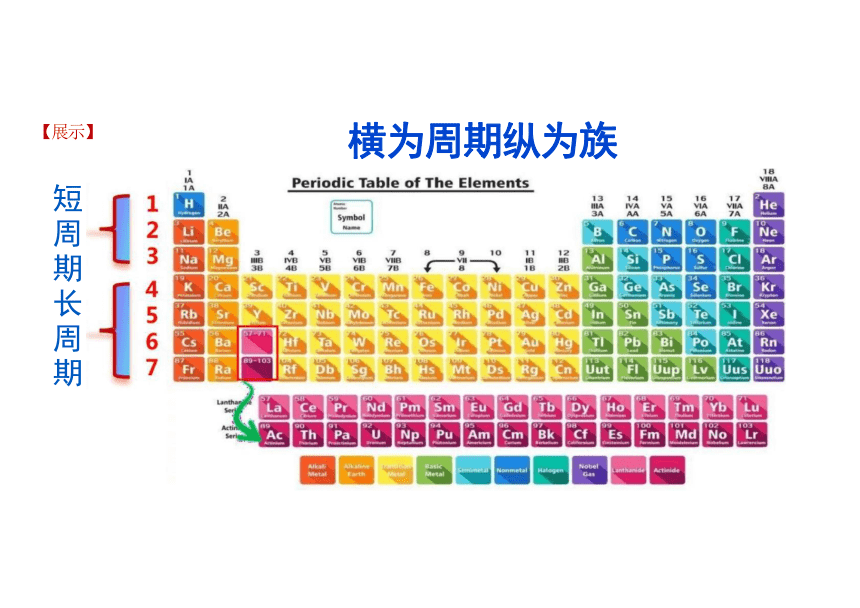
【展示】 横为周期纵为族
短周期长周期
周期数 起~终 元素种数
电子层数
短 1 H~ He 2
1
周 2 Li~ Ne 8
2
期 3 Na~Ar 8
3
4 K~Kr 18
4
长周 5 Rb~Xe 18
5
期 6 Cs~Rn 32
6
7 Fr~Og 32
7
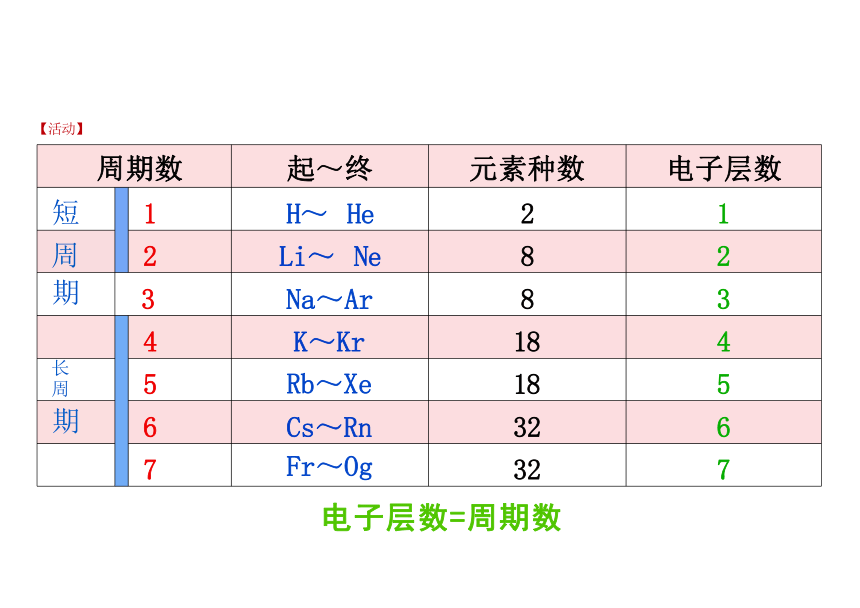
电子层数=周期数
【活动】
横为周期纵为族
B族:副族ble of 7 VⅢ族
短周期长周期
A族:主族
【展示】
0族
【活动】
IA ( 除H外)称为碱金属元素:
锂(Li)、 钠 (Na)、 钾 (K)、 铷 (Rb)、 铯 (Cs)、 钫 (Fr)
ⅡA 称为碱土金属元素:
铍 (Be)、 镁 (Mg)、 钙 (Ca)、 锶 (Sr)、 钡 (Ba)、 镭 (Ra)
ⅢA称为硼族元素:
硼 (B)、 铝 (Al)、 镓 (Ga)、 铟 (In)、 铊(Tl)、
称 (Nh)
IVA称为碳族元素:
碳(C)、 硅 (Si)、 锗(Ge)、 锡 (Sn)、 铅 (Pb)、
鈇 (FI)
【活动】
VA 称为氮族元素:
氮(N)、 磷 (P)、 砷 (As)、 锑 (Sb)、 铋 (Bi)、 馍 (Mc)
VIA称为氧族元素:
氧(O)、 硫 (S)、 硒 (Se)、 碲 (Te)、 钋 (Po)、 垃 (Lv)
VIA称为卤族元素:
氟 (F)、 氯 (Cl)、 溴 (Br)、 碘 (I)、 砹 (At)
副族和第VⅢ族均为金属元素;又称过渡金属元素:
Sc、Ti、V、Cr、Mn、Fe、Co、Ni、Y、Zr、Nb、Mo、Tc、Ru、Rh、 Pd、La、Hf、Ta、'W、Re、Os、′Ir、Pt
0 IA 填 空
0
1 1 氢
2
氦
ⅡA 钾 硅 硫钙 ⅢA IVA VA VA VIA
2 3 锂 4 铍 5 硼 6 碳 7 氮 8 氧 9 氟
10
氖
3 11 12 13 14 15 16 17
18
ⅢB IVB VB VIB VIB VⅢ p 1 IⅡB
4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35
36
5 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53
54
6 55 56 57-71 72 73 74 75 76 77 78 79 80 81 82 83 84 85
86
7 87 88 89-103 104 105 106 107 108 109 110 111
【活动】
氢 H 原子结构示意图1~20号
氦 H e
锂 L i 铍 B e 硼 B 碳 C 氮N 氧 0 氟 F
氖 N e
钠 N a 镁 M g 铝 A l 硅 S i 磷 P 硫 S 氯 C l
氩 A r
钾 K 钙 C a
估测元素的相对原子质量
【活动】
族 周期 元素 符号 -K 19 钾 ·39.098 原子序数 固态 液态 气态 人造元素 元素名称
I A
0
H 1 氢 1.0079
He 2
氦
4.0026
lIA 原子量- IIIA IVA VA VIA MIA
Li 3 锂 6.941 Be 4 铍 9.0122 B 5 硼 10.811 C 6 碳 12.011 N 7 氮 14.007 0 8 氧 15.999 F 9 氟 18.998
Ne 10
氖 20.17
三 Na 1 钠 22.9898 Mg 12 镁 24.305 Al 13 铝 26.982 Si 14 硅 28.085 P 15 磷 30.974 S 16 硫 32.06 CI 17 氯 35.453
Ar 18 氯
39.94
IIIB IVB VB VIB MIB V IB ⅡB
四 K 19 钾 39.098 Ca 20 钙 40.08 Sc 2 钪 44.956 Ti 22 钛 47.9 v 23 钒 50.915 Cr 24 铬 51.996 Mn 25 锰 54.938 Fe 26 铁 55.84 Co 27 钴 58.933 Ni 28 镍 58.69 Cu 29 铜 63.54 Zn 30 锌 65.38 Gr 3 镓 69.72 Ge 32 锗 72.5 As 33 砷 74.922 Se 34 硒 78.9 Br 35 溴 79.904
Kr 36
氮
83.8
五 Rb 37 85.467 Sr 38 锶 87.62 Y 39 钇 88.906 Zr 40 锆 91.22 Nb 41 铌 92.906 Mo 42 钼 95.94 Te 43 锝 99 Ru 44 钌 101.07 Rh 45 铑 102.91 Pd 46 钯 106.42 Ag 47 银 107.87 Cd 48 镉 112.41 In 49 铟 114.82 Sn 50 锡 118.6 Sb 51 锑 121.7 Te 52 碲 127.6 1 53 碘 126.91
Xe 54
氙 131.3
六 Cs 55 铯 132.91 Ba 56 钡 137.33 57-71 镧系 La-Lu Hf 72 铪 178.4 Ta 73 钽 180.95 |w 74 钨 183.8 Re 75 铼 186.21 Os 76 锇 190.2 Ir 77 铱 192.2 Pt 78 铂 195.08 Au 79 金 196.97 Hg 80 汞 200.5 T1 81 铊 204.3 Pb 82 铅 207.2 Bi 83 铋 208.98 Po 84 钋 209 At 85 砹 201
Rn 86
氢
222
七 Fr 87 钫 223 Ra 88 镭 226.03 39—103 钢系 Ac-Lr 104 Rf 261 105 Db 262 106 Sg 263 107 Bh 262 108 Hs 265 109 Mt 266 110 Uun 269 111 Uuu 272 112 Uub 277 113 Uut — 114 Uuq
相对原子质量考虑该元素的同位素在自然界的丰度,经计算得到平均值。
同种元素原子的质子数相同,中子数可
具有一定数目质子和中子数的一种原子,叫做核素。
某元素有多种核素,它们互为同位素。
【展示】
氢-1:符号H ,普通氢
氢-2:符号D或2H ,重 氢
氢-3:符号T ,超重氢
【展示】 自然界中氢以气(piē)(1H) 、 氘 (dāo)(2H) 、 氘 (chuān)(3H) 三种同
位素形式存在。
水:H O, 相对分子质量为18
重水:D O ,相对分子质量为20
超重水:T O, 相对分子质量为22
重水在自然界含量稀少,自然界却几乎不含超重水,超重水不能从自然界获得
【展示】
【辨析】 同素异形体:是指由同样的单一化学元素组成,因排列方式不同,而具有不同性质的单质。
磷的两种同素异形体,红磷和白 磷 碳的同素异形体:金刚石、石墨
氧的同素异形体:氧气、臭氧
同素异形体
单质
1. 化学家为社会发展做出了巨大贡献,下列研究成果与化学家对应正确的是(
①提出化学元素的概念——卢瑟福…… 波义耳在1661年,提出化学元素的概念,标志着近代化学的诞生
拉瓦锡
②提出氧化学说——波义耳
③提出原子论——道尔顿
④提出分子学说——阿伏加德罗
⑤发现元素周期律——门捷列夫
A.①②③ B.②③④ C.③④⑤ D.①③⑤
【作业】
2. 下列叙述不正确的是( D )A. 同主族两相邻元素的原子序数之差 可能为2、8、18、32B. 同族元素的最外层电子数一定相同C.23592U 中的 中子数为143D. 元素周期表有7个周期,7个主族,8个副族,0族
3. 下列说法中正确的是( B )
A. 元素周期表中第15个纵列为VIA族
B .74 W 的中子数为107
C.16o 和 O 互为同素异形体
D .3 Cl 和 Cl 互为同位素
4. 按要求填空。
(1)已知A原子,其核外电子数为17,则A是_ (填元素符号)。
(2)已知B原 子 ,L层上的电子数为K层的3倍,则其原子结构示意图是_
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离
子结构示意图
碳
第一节
原子结构与元素周期表
第2课时
元素周期表
1869年,门捷列夫依据相对原子质量,制出元素周期表, 并发现元素周期律,对未知元素留空位
德米特里 ·伊万诺维奇 ·门捷列夫
I I 】 M V M M W
X
Li7.01 B 11 C11.97 Al 27.3 Si 28 Ti 48 Zr 89.7 In 113.4 Sn 117.8
T1202.7 Pb 206.4
N14.01 P 30.9 V 51.2 As 74.9 Nb 93.7 Sb 122.1 Ta 182.2
Bi207.5
015.96 S 31.98 Cr 52.4 Se 78.0 Mo 95.6 Te 128 W 183.5
F19.1 CI 35.38 Mn 54.8 Fe 55.9 Co &.Ni 58.6 Br 79.75 Ru 103.5 Rh 104.1 Pd 106.2 I126.5 Os 198.6 Ir 196.7 Pt 196.7
Na 22.99 K 39.04 Cu 63.3 Rb 85.2 Ag 107.66 Cs 132.7 Au 196.2
Be 9.3 Mg 23.9 Ca 39.9 Zn 64.9 Sr 87.0 Cd 111.6 Ba 136.8 Hg 199.8
日.N日
1870年,迈尔划分相似元素,形成过渡元素
迈 尔 的 元 素 周 期 表 (1869)
70 Yb
镱
173.0
71 Lu
镥
17496
化 学 元 素 周 期 表 ⅡA ⅢA IVA VA VIA VIIA 00
2 He
氦
4.0026
3E 锂 6.941 11Na 钠 229898 4 Be 铍 90122 12 Mg 镁 24305 ⅢIB VB VB VIB VIIB VⅢ IB ⅢB 081 碳 2011 7N 氮 14007 8.0 氧 6099 9 18993
10 Ne
氖
20.17
13AL 铝 26.982 14Si 硅 28085 5F 磷 20904 65 硫 3206 17dl 氩 453
18Ar
氩
39.94
19k 钾 39.098 20 Ca 钙 40.03 21 Sc 钪 44.956 22Ti 钛 47.9 23V 钒 50.9415 24 Cr 铬 51.996 25 Mn 锰 54938 26 Fe 铁 55.84 27 Co 钴 58.9332 28 Ni 镍 58.69 29 Cu 铜 63,54 30 Zn 锌 65.38 31Ga 镓 6902 32 Ge 锗 72.59 23As 砷 74921 34Se 硒 739 35Bn 溴 09904
36 Kr
氪
83.8
37Rb 85.467 38Sr 锶 87.62 39Y 钇 88.906 40 Zr 锆 91,22 41 Nb 铌 92.9064 42 Mo 钼 95.94 43 To 锝 99 44RU 钌 101.07 45 Rh 铑 102.906 46 Pd 钯 106.42 47 Ag 银 107.868 48 Cd 镉 112.41 49In 铟 114.82 50.Sn 锡 1186 511Sb 锑 1217 52 Te 碲 1276 531 碘 6903
54Xe
氙
1313
5s Cs 铯 132.905 87Er 钫 (223) 56.Ba 钡 13733 88镭Ra 226,03 57-71 La-Lu 镧系 89-103 Ac-Lr 锏系 72 Hf 铪 178.4 104 Rf 鳙 (261) 73Ta 钽 180.947 105 Db 壮 (262) 74W 钨 183.8 106 Sg 馆 (266) 75 Re 铼 186.207 76.0s 锇 190.2 77 Ir 铱 192.2 78 Pt 铂 195.08 79 Au 金 196.967 80 Hg 汞 2005 81 铊 2043 82Pb 铅 2072 83 B 铋 20898 84 Po 钋 (209) 85 砹 (201
86 Rn
氡
(222)
107 Bh 铍 (264) 108Hs (269) 109 Mt 绥 (268) 110 Ds 键 (271) 111 Rg 输 (272) 112 Uub (285) 113 Uut (284 114 Uuq (289) 115 Uup (288) 116 Uuh (292) 117 Uus
118
Uuo
询 系 57 La 镧 138.905 58 Ce 铈 140.12 59 Pr 镨 140.91 60 Nd 钕 144.2 61 Pm 钷 147 62 Sm 钐 150.4 63 Eu 铕 151.96 64 Gd 钆 157.25 65 Tb 铽 158.93 66 Dy 镝 162.5 67 Ho 钬 164.93 68 Er 铒 167.2 69 Tm 铥 168.934
89 Ac 的 (227) 90 Th 钍 232.03 91 Pa 镁 231.03 92U 铀 238.02 93 Np 锋 237.04 94 Pu 钚 (244) 95 Am 错 (243) 96 Cm 铜 (247) 97 Bk 镨 (247) 98 Cf 镧 (251) 99 Es 铱 (254 100 Fm 锁 (257) 101 Md 们 (258)
1905年,维尔纳长式元素周期表,是当前使用的元素周期表
1
2
3
4
5
6
7
103 Lr
锑
(260)
102 No
锆
(259)
周
期 IA
镧系
氢
硼
Periodic Table of the Elements A 3A 14 VA 4A 15 5A 16 /A 5A 17 VILA
2
He
40
Be Mg 3 3 1B 38 48VB 5 VB 58 6 /1B 6B 7 VIIB 78 9 /Ill 10 11 1B 2B 5 B 10.811 C 12011 N 14007 0 15.999 F 18998
10
Ne
20.180
13 AI 26982 14 Si 2B.086 15 P 30974 16 S 32066 17 CI 35453
18
Ar
39948
20 Ca 10.078 21 Sc 44956 22 Ti 47.88 23 V 50.042 24 Cr 51.906 25 Mn 549 26 Fe 55933 27 Co 58.903 28 Ni 29 Cu 834 30 Zn 65.39 31 Ga 00732 32 Ge 72.61 33 As 74922 34 Se 7809 35 Br 79.904
36
Kr
8480
Sr 76 39 906 Z 22 41 Nb 06 42 Mo h 05.9 3 Tc 93.907 4 Ru 101.0 45 Rh 102.9 46 Pd 106.42 47 Ag 10786 48 Cd 1124u 49 In 114.818 50 Sn 11871 51 Sb 121.760 52 Te 1276 53 126904
54
Xe
13129
32.90 Ba 37.32 7. 2 Hf 178.49 73 80948 74 75 6 68.207 76 O 9 77 92 78 08 79 80 Hg 200.59 81 TI 204383 82 Pb 2072 83 Bi 203980 84 Po 203992 85 At 209987
86
Rn
222018
Ra 39.103 04 Rf 05 ) 06 107 Bh 108 109 Cr Ju 14 F t JuS
Juo
2019年,国际化学元素周期表年,人工合成第118号元素,填满前七个周期
Lanthanic
Serie
Actir
Series
18
VIIIA
I IⅡ Ⅲ IV V VI VII VIII
【回顾初中】
质子数=原子序数=核外电子数=核电荷数
电子层数=周期数,最外层电子数相同排一纵列
【展示】 由相对原子质量改为原子的质子数(核外电子数或核电荷数),形成现行的元素周期表
每一个横行叫作一个周 期,每一个纵行叫作一个族(VI 族包含三个纵列)
B C N 0
13 14 15 16 17
Al Si P S CI
31 32 33 34 35
Zn Ga Ge As Se Br
48 49 60 51 62 53
105 106 107 108 109 110 111 112
Db Sg Bh Hs Mt Ds Rg Cn
58 59 60 61 62 63 64 65
Ce Pr Nd Pm Sm Eu Gd Tb
Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te Xe
72 73 74 75 76 77 78 79 80 81 82 83 B4 85
周 期 族
元素周期表有7个横行,18个纵列
22 2 25 26 27 28
Sc T V Gr Mn Fe Co Ni Cu
39 40 41 42 43 44 45 46 47
113 114 115 116 117 Uut F Uup LV Uus
f6 67 68 69 70
Dy Ho Er Tm Yb
01 95 96
Pu Am Cm Bk
7个
10s
16个
Ba Hf Ta W Re Os Ir Pt Au Hg T Pb Bi Po At Rn
【看图识记】
la Mg
Ca
8
ie
Ne
An Kr
2
3
5
6
7
101 10 Md No
9B
CF Es
01
Pa U
u
LU
93 Np
104
Rf
Th
Fm
【展示】 横为周期纵为族
短周期长周期
周期数 起~终 元素种数
电子层数
短 1 H~ He 2
1
周 2 Li~ Ne 8
2
期 3 Na~Ar 8
3
4 K~Kr 18
4
长周 5 Rb~Xe 18
5
期 6 Cs~Rn 32
6
7 Fr~Og 32
7
电子层数=周期数
【活动】
横为周期纵为族
B族:副族ble of 7 VⅢ族
短周期长周期
A族:主族
【展示】
0族
【活动】
IA ( 除H外)称为碱金属元素:
锂(Li)、 钠 (Na)、 钾 (K)、 铷 (Rb)、 铯 (Cs)、 钫 (Fr)
ⅡA 称为碱土金属元素:
铍 (Be)、 镁 (Mg)、 钙 (Ca)、 锶 (Sr)、 钡 (Ba)、 镭 (Ra)
ⅢA称为硼族元素:
硼 (B)、 铝 (Al)、 镓 (Ga)、 铟 (In)、 铊(Tl)、
称 (Nh)
IVA称为碳族元素:
碳(C)、 硅 (Si)、 锗(Ge)、 锡 (Sn)、 铅 (Pb)、
鈇 (FI)
【活动】
VA 称为氮族元素:
氮(N)、 磷 (P)、 砷 (As)、 锑 (Sb)、 铋 (Bi)、 馍 (Mc)
VIA称为氧族元素:
氧(O)、 硫 (S)、 硒 (Se)、 碲 (Te)、 钋 (Po)、 垃 (Lv)
VIA称为卤族元素:
氟 (F)、 氯 (Cl)、 溴 (Br)、 碘 (I)、 砹 (At)
副族和第VⅢ族均为金属元素;又称过渡金属元素:
Sc、Ti、V、Cr、Mn、Fe、Co、Ni、Y、Zr、Nb、Mo、Tc、Ru、Rh、 Pd、La、Hf、Ta、'W、Re、Os、′Ir、Pt
0 IA 填 空
0
1 1 氢
2
氦
ⅡA 钾 硅 硫钙 ⅢA IVA VA VA VIA
2 3 锂 4 铍 5 硼 6 碳 7 氮 8 氧 9 氟
10
氖
3 11 12 13 14 15 16 17
18
ⅢB IVB VB VIB VIB VⅢ p 1 IⅡB
4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35
36
5 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53
54
6 55 56 57-71 72 73 74 75 76 77 78 79 80 81 82 83 84 85
86
7 87 88 89-103 104 105 106 107 108 109 110 111
【活动】
氢 H 原子结构示意图1~20号
氦 H e
锂 L i 铍 B e 硼 B 碳 C 氮N 氧 0 氟 F
氖 N e
钠 N a 镁 M g 铝 A l 硅 S i 磷 P 硫 S 氯 C l
氩 A r
钾 K 钙 C a
估测元素的相对原子质量
【活动】
族 周期 元素 符号 -K 19 钾 ·39.098 原子序数 固态 液态 气态 人造元素 元素名称
I A
0
H 1 氢 1.0079
He 2
氦
4.0026
lIA 原子量- IIIA IVA VA VIA MIA
Li 3 锂 6.941 Be 4 铍 9.0122 B 5 硼 10.811 C 6 碳 12.011 N 7 氮 14.007 0 8 氧 15.999 F 9 氟 18.998
Ne 10
氖 20.17
三 Na 1 钠 22.9898 Mg 12 镁 24.305 Al 13 铝 26.982 Si 14 硅 28.085 P 15 磷 30.974 S 16 硫 32.06 CI 17 氯 35.453
Ar 18 氯
39.94
IIIB IVB VB VIB MIB V IB ⅡB
四 K 19 钾 39.098 Ca 20 钙 40.08 Sc 2 钪 44.956 Ti 22 钛 47.9 v 23 钒 50.915 Cr 24 铬 51.996 Mn 25 锰 54.938 Fe 26 铁 55.84 Co 27 钴 58.933 Ni 28 镍 58.69 Cu 29 铜 63.54 Zn 30 锌 65.38 Gr 3 镓 69.72 Ge 32 锗 72.5 As 33 砷 74.922 Se 34 硒 78.9 Br 35 溴 79.904
Kr 36
氮
83.8
五 Rb 37 85.467 Sr 38 锶 87.62 Y 39 钇 88.906 Zr 40 锆 91.22 Nb 41 铌 92.906 Mo 42 钼 95.94 Te 43 锝 99 Ru 44 钌 101.07 Rh 45 铑 102.91 Pd 46 钯 106.42 Ag 47 银 107.87 Cd 48 镉 112.41 In 49 铟 114.82 Sn 50 锡 118.6 Sb 51 锑 121.7 Te 52 碲 127.6 1 53 碘 126.91
Xe 54
氙 131.3
六 Cs 55 铯 132.91 Ba 56 钡 137.33 57-71 镧系 La-Lu Hf 72 铪 178.4 Ta 73 钽 180.95 |w 74 钨 183.8 Re 75 铼 186.21 Os 76 锇 190.2 Ir 77 铱 192.2 Pt 78 铂 195.08 Au 79 金 196.97 Hg 80 汞 200.5 T1 81 铊 204.3 Pb 82 铅 207.2 Bi 83 铋 208.98 Po 84 钋 209 At 85 砹 201
Rn 86
氢
222
七 Fr 87 钫 223 Ra 88 镭 226.03 39—103 钢系 Ac-Lr 104 Rf 261 105 Db 262 106 Sg 263 107 Bh 262 108 Hs 265 109 Mt 266 110 Uun 269 111 Uuu 272 112 Uub 277 113 Uut — 114 Uuq
相对原子质量考虑该元素的同位素在自然界的丰度,经计算得到平均值。
同种元素原子的质子数相同,中子数可
具有一定数目质子和中子数的一种原子,叫做核素。
某元素有多种核素,它们互为同位素。
【展示】
氢-1:符号H ,普通氢
氢-2:符号D或2H ,重 氢
氢-3:符号T ,超重氢
【展示】 自然界中氢以气(piē)(1H) 、 氘 (dāo)(2H) 、 氘 (chuān)(3H) 三种同
位素形式存在。
水:H O, 相对分子质量为18
重水:D O ,相对分子质量为20
超重水:T O, 相对分子质量为22
重水在自然界含量稀少,自然界却几乎不含超重水,超重水不能从自然界获得
【展示】
【辨析】 同素异形体:是指由同样的单一化学元素组成,因排列方式不同,而具有不同性质的单质。
磷的两种同素异形体,红磷和白 磷 碳的同素异形体:金刚石、石墨
氧的同素异形体:氧气、臭氧
同素异形体
单质
1. 化学家为社会发展做出了巨大贡献,下列研究成果与化学家对应正确的是(
①提出化学元素的概念——卢瑟福…… 波义耳在1661年,提出化学元素的概念,标志着近代化学的诞生
拉瓦锡
②提出氧化学说——波义耳
③提出原子论——道尔顿
④提出分子学说——阿伏加德罗
⑤发现元素周期律——门捷列夫
A.①②③ B.②③④ C.③④⑤ D.①③⑤
【作业】
2. 下列叙述不正确的是( D )A. 同主族两相邻元素的原子序数之差 可能为2、8、18、32B. 同族元素的最外层电子数一定相同C.23592U 中的 中子数为143D. 元素周期表有7个周期,7个主族,8个副族,0族
3. 下列说法中正确的是( B )
A. 元素周期表中第15个纵列为VIA族
B .74 W 的中子数为107
C.16o 和 O 互为同素异形体
D .3 Cl 和 Cl 互为同位素
4. 按要求填空。
(1)已知A原子,其核外电子数为17,则A是_ (填元素符号)。
(2)已知B原 子 ,L层上的电子数为K层的3倍,则其原子结构示意图是_
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离
子结构示意图
碳
