6.2.1化学反应的速率 (教学课件)- 高中化学人教版(2019)必修第二册(共19张PPT)
文档属性
| 名称 | 6.2.1化学反应的速率 (教学课件)- 高中化学人教版(2019)必修第二册(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 611.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-25 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
第六章化学反应与能量
第二节化学反应的速率与限度 第1课时化学反应的速率
爆炸:瞬间完成
牛奶变质
图6-15 快告奶变质花数天完成
你了解这些化学反应的快慢吗
生锈——数月或数年
溶洞形成:数万年
化学反应速率
一 、化学反应速率
1、定义:化学反应速率是用来衡量化学反应进行快慢的物理 量。
通常用单位时间内反应物浓度的减少量或生成物浓 度的增加量 (均取正值)来表示。
单位时间物质浓度的改变
化学反应速率:
化学反应速率
一、化学反应速率
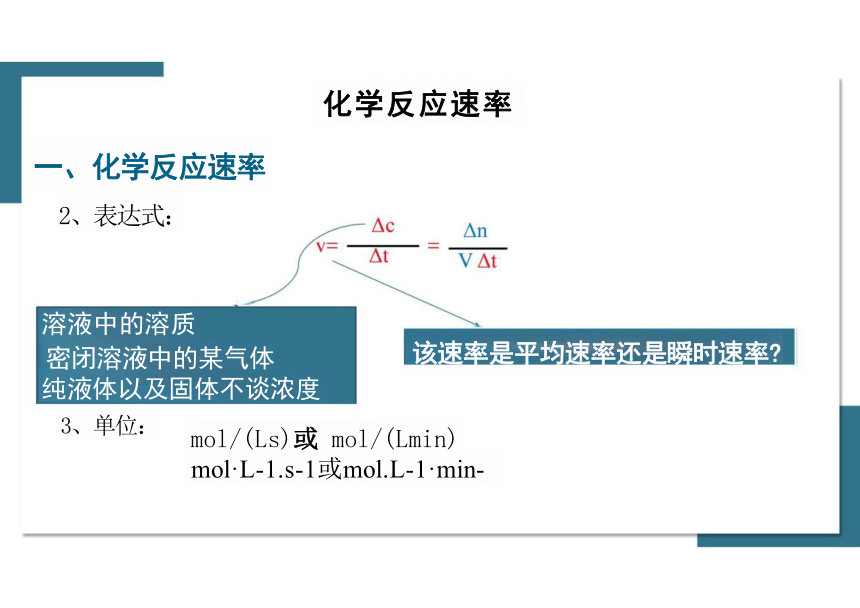
2、表达式:
溶液中的溶质
密闭溶液中的某气体 该速率是平均速率还是瞬时速率
纯液体以及固体不谈浓度
mol/(Ls)或 mol/(Lmin)
mol·L-1.s-1或mol.L-1·min-
3、单位:
1.在某化学反应中,某一反应物B的初始浓度为6moL/L ,经过5min后 ,B 的浓度变成了2moL/L, 则在这5min内 B的化学反应速率v(B) 为 0.8moL·L-1·min-1 0
思考
2 . 一 定温度下,在容积为2L的密闭容器中加入2 mol N2和6 mol H ,在10min时N2剩余1.8mol, 求 v(N ),v
(H ),v(NH )
解:N + 3 H 一 2 NH
起始量(mol) 2 6 0
变化量(mol)
10min 末 (mol)
思考
0.2
1.8
0.4
0.4
0.6
5.4
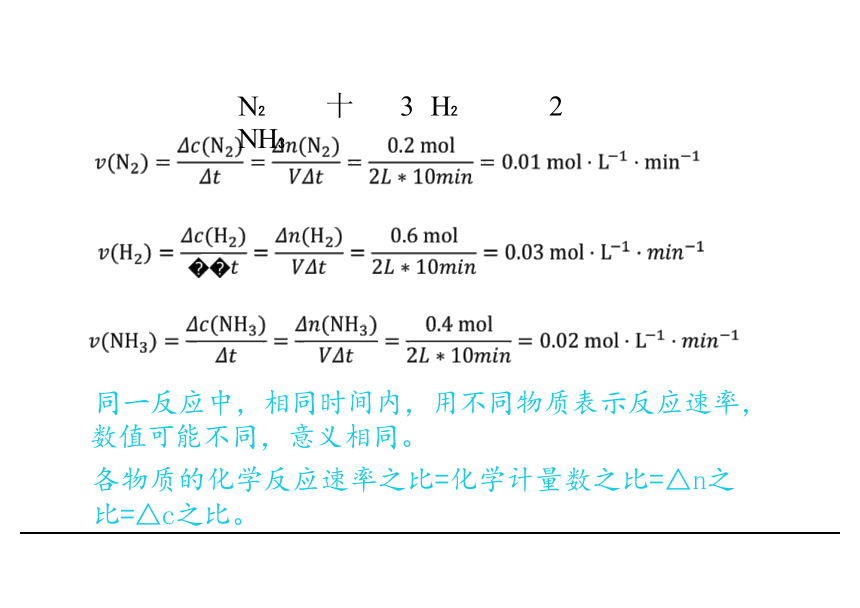
同一反应中,相同时间内,用不同物质表示反应速率, 数值可能不同,意义相同。
各物质的化学反应速率之比=化学计量数之比=△n之 比=△c之比。
N 十 3 H 2 NH
可逆反应4NH (g)+50 (g) 4NO(g)+6H O(g) 在5L 的 密闭容器中进行,2s后 ,NO 的物质的量增加了0.4 mol, 分 别用四种物质表示该化学反应的平均速率。
在m A+n B—pC的反应中,m 、n 、p为各物质的计量
数。现测得C每分钟增加a mol/L,B每分钟减少1.5a
mol/L,A 每分钟减少0.5a mol/L, 则m:n:p 为 ( C )
A.2:3:2 B.2:3:3
C.1:3:2 D.3:1:2
课本55页10题
已知反应4CO+2NO 催化剂N +4CO 在不同条件下的化学反应速率如
下:
①v(CO)=1.5 mol·L-1·min-1
②v(NO =0.01 mol·L-1·s-1
③v(N )=0.4 mol·L-1·min-1
④v(CO )=1.1 mol·L-1·min-1
请比较上述4种情况反应的快慢:③①②④(由大到小的顺序)。
比较反应的快慢,应取同一参照物且单位要一致。
练习册
在相同条件下,等质量(金属颗粒大小相同)的下列金
属与等量1mol/L盐酸反应时,速率最快的是()
A镁 B 铝 C 钠 D 铁 E 石墨
1.内在因素:物质本身的结构与性质。(主要因素)
二 、影响化学反应速率的因素
思考
实验 操作 2 mL5%H O 溶液(滴有两滴FeCl 溶液) 冷水 热水 (5℃) 常温 40℃) ① ②
实验 现象 ①产生气泡速率 最慢 ②产生气泡速 率较快
③产生气泡速率 最快
实验 结论 对于反应2H O 催化剂2H O+O 个来说,温度升 高,H O 的分解速率 加快
二 、影响化学反应速率的因素
2.外界因素(1)温度
实验操作 FeCl 溶液
FeCl
溶液
4%H O 溶液12%H O 溶液
实验现象 装有12%H O 溶液的试管中先产生气泡
实验结论 增大反应物浓度能使H O 分解速率 加快
(2)反应物浓度 设计实验说明反应物浓度对化学反应速率的影响
思考
实验现象 ①有少量气泡出现 ②能产生大量气泡
实验结论 FeCl 可以使H O 分解的速率加快
(3)催化剂
实验操作
FeCl 溶液
H O 溶液
H O 溶液
①
②
催化剂是现代化学中关键而神奇的物质 之一。据统计,有80%以上的化工生产过程 (如氨、硫酸、硝酸的合成,乙烯、丙烯、 苯乙烯的聚合,煤、石油、天然气的综合利 用,等等)使用了催化剂,目的是增大反应 速率,提高生产效率。在资源利用、能源开 发、医药制造、环境保护等领域,催化剂有 着广泛的应用。催化剂十分神奇,它能极大 地提高化学反应速率(可使反应速率增大几 个到十几个数量级),而自身的组成、化学 性质和质量在反应前后不发生变化;它和一 些反应体系的关系就像钥匙与锁的关系,具 有一定的选择性。
生物体内几乎所有的化学反应(如淀 粉、脂肪、蛋白质的水解,DNA的复制等) 都是由生物体内存在的特殊催化剂——酶所 催化的。酶比一般的催化剂具有更高的选择 性和催化效率,而且是在正常体温的条件
下发生作用,反应条件温和。受酶的启示, 科学家开辟了设计和合成催化剂的新途径, 正在研制具有生物酶某些特性的化学酶,以 期实现“仿酶催化”。催化剂的神奇面纱至 今尚未完全揭开,对催化剂的研究是当代化学 一个极具魅力和应用前景的重要课题。
科 学 ·技术 · 社会 神奇的催化剂
图6-17 氨氧化法制硝酸使用的网状
铂-钯-铑合金催化剂
(4)压强对化学反应速率的影响
对于气体来说,在相同温度下,压强越 大,一定质量气体的体积越小,单位体
积内气体的分子数越多(如图6-16)。增 大 压强(减小容器容积)相当于增大反应物的 浓 度 ,化学反应速率增大;减小压强(增大 容器容积)相当于减小反应物的浓度,化
学反应速率减小。
图6-16 压强增大,气体浓度增大
反应物的表面积
光波,电磁波,超声波,溶剂等
你还知道哪些因素会影响反应速率
思考
已知反应(C(s)+CO (g)=2CO(g)) 在某密闭容器中进行,现采取下列措
施,其中能够使该反应速率加快的是( C )
①增大压强②增加C的量③恒容条件下充入CO ④恒容条件下充入 N ⑤ 恒压条件下充入N
A.①④ B.②③⑤ C.①③ D.①②④
①该反应为有气体参加的反应,增大压强,反应速率加快,符合
题意;②C 为固体,增加其用量,不影响化学反应速率,不符合题意;③ 恒容条件下充入CO , 反应物浓度增大,反应速率加快,符合题意;④恒 容条件下充入N , 各反应物的浓度不变,反应速率不变,不符合题意;⑤ 恒压条件下充入N , 各反应物的浓度减小,反应速率减慢,不符合题意。
第六章化学反应与能量
第二节化学反应的速率与限度 第1课时化学反应的速率
爆炸:瞬间完成
牛奶变质
图6-15 快告奶变质花数天完成
你了解这些化学反应的快慢吗
生锈——数月或数年
溶洞形成:数万年
化学反应速率
一 、化学反应速率
1、定义:化学反应速率是用来衡量化学反应进行快慢的物理 量。
通常用单位时间内反应物浓度的减少量或生成物浓 度的增加量 (均取正值)来表示。
单位时间物质浓度的改变
化学反应速率:
化学反应速率
一、化学反应速率
2、表达式:
溶液中的溶质
密闭溶液中的某气体 该速率是平均速率还是瞬时速率
纯液体以及固体不谈浓度
mol/(Ls)或 mol/(Lmin)
mol·L-1.s-1或mol.L-1·min-
3、单位:
1.在某化学反应中,某一反应物B的初始浓度为6moL/L ,经过5min后 ,B 的浓度变成了2moL/L, 则在这5min内 B的化学反应速率v(B) 为 0.8moL·L-1·min-1 0
思考
2 . 一 定温度下,在容积为2L的密闭容器中加入2 mol N2和6 mol H ,在10min时N2剩余1.8mol, 求 v(N ),v
(H ),v(NH )
解:N + 3 H 一 2 NH
起始量(mol) 2 6 0
变化量(mol)
10min 末 (mol)
思考
0.2
1.8
0.4
0.4
0.6
5.4
同一反应中,相同时间内,用不同物质表示反应速率, 数值可能不同,意义相同。
各物质的化学反应速率之比=化学计量数之比=△n之 比=△c之比。
N 十 3 H 2 NH
可逆反应4NH (g)+50 (g) 4NO(g)+6H O(g) 在5L 的 密闭容器中进行,2s后 ,NO 的物质的量增加了0.4 mol, 分 别用四种物质表示该化学反应的平均速率。
在m A+n B—pC的反应中,m 、n 、p为各物质的计量
数。现测得C每分钟增加a mol/L,B每分钟减少1.5a
mol/L,A 每分钟减少0.5a mol/L, 则m:n:p 为 ( C )
A.2:3:2 B.2:3:3
C.1:3:2 D.3:1:2
课本55页10题
已知反应4CO+2NO 催化剂N +4CO 在不同条件下的化学反应速率如
下:
①v(CO)=1.5 mol·L-1·min-1
②v(NO =0.01 mol·L-1·s-1
③v(N )=0.4 mol·L-1·min-1
④v(CO )=1.1 mol·L-1·min-1
请比较上述4种情况反应的快慢:③①②④(由大到小的顺序)。
比较反应的快慢,应取同一参照物且单位要一致。
练习册
在相同条件下,等质量(金属颗粒大小相同)的下列金
属与等量1mol/L盐酸反应时,速率最快的是()
A镁 B 铝 C 钠 D 铁 E 石墨
1.内在因素:物质本身的结构与性质。(主要因素)
二 、影响化学反应速率的因素
思考
实验 操作 2 mL5%H O 溶液(滴有两滴FeCl 溶液) 冷水 热水 (5℃) 常温 40℃) ① ②
实验 现象 ①产生气泡速率 最慢 ②产生气泡速 率较快
③产生气泡速率 最快
实验 结论 对于反应2H O 催化剂2H O+O 个来说,温度升 高,H O 的分解速率 加快
二 、影响化学反应速率的因素
2.外界因素(1)温度
实验操作 FeCl 溶液
FeCl
溶液
4%H O 溶液12%H O 溶液
实验现象 装有12%H O 溶液的试管中先产生气泡
实验结论 增大反应物浓度能使H O 分解速率 加快
(2)反应物浓度 设计实验说明反应物浓度对化学反应速率的影响
思考
实验现象 ①有少量气泡出现 ②能产生大量气泡
实验结论 FeCl 可以使H O 分解的速率加快
(3)催化剂
实验操作
FeCl 溶液
H O 溶液
H O 溶液
①
②
催化剂是现代化学中关键而神奇的物质 之一。据统计,有80%以上的化工生产过程 (如氨、硫酸、硝酸的合成,乙烯、丙烯、 苯乙烯的聚合,煤、石油、天然气的综合利 用,等等)使用了催化剂,目的是增大反应 速率,提高生产效率。在资源利用、能源开 发、医药制造、环境保护等领域,催化剂有 着广泛的应用。催化剂十分神奇,它能极大 地提高化学反应速率(可使反应速率增大几 个到十几个数量级),而自身的组成、化学 性质和质量在反应前后不发生变化;它和一 些反应体系的关系就像钥匙与锁的关系,具 有一定的选择性。
生物体内几乎所有的化学反应(如淀 粉、脂肪、蛋白质的水解,DNA的复制等) 都是由生物体内存在的特殊催化剂——酶所 催化的。酶比一般的催化剂具有更高的选择 性和催化效率,而且是在正常体温的条件
下发生作用,反应条件温和。受酶的启示, 科学家开辟了设计和合成催化剂的新途径, 正在研制具有生物酶某些特性的化学酶,以 期实现“仿酶催化”。催化剂的神奇面纱至 今尚未完全揭开,对催化剂的研究是当代化学 一个极具魅力和应用前景的重要课题。
科 学 ·技术 · 社会 神奇的催化剂
图6-17 氨氧化法制硝酸使用的网状
铂-钯-铑合金催化剂
(4)压强对化学反应速率的影响
对于气体来说,在相同温度下,压强越 大,一定质量气体的体积越小,单位体
积内气体的分子数越多(如图6-16)。增 大 压强(减小容器容积)相当于增大反应物的 浓 度 ,化学反应速率增大;减小压强(增大 容器容积)相当于减小反应物的浓度,化
学反应速率减小。
图6-16 压强增大,气体浓度增大
反应物的表面积
光波,电磁波,超声波,溶剂等
你还知道哪些因素会影响反应速率
思考
已知反应(C(s)+CO (g)=2CO(g)) 在某密闭容器中进行,现采取下列措
施,其中能够使该反应速率加快的是( C )
①增大压强②增加C的量③恒容条件下充入CO ④恒容条件下充入 N ⑤ 恒压条件下充入N
A.①④ B.②③⑤ C.①③ D.①②④
①该反应为有气体参加的反应,增大压强,反应速率加快,符合
题意;②C 为固体,增加其用量,不影响化学反应速率,不符合题意;③ 恒容条件下充入CO , 反应物浓度增大,反应速率加快,符合题意;④恒 容条件下充入N , 各反应物的浓度不变,反应速率不变,不符合题意;⑤ 恒压条件下充入N , 各反应物的浓度减小,反应速率减慢,不符合题意。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
