糖类(教学课件) 高中化学人教版(2019)必修 第二册(共25张PPT)
文档属性
| 名称 | 糖类(教学课件) 高中化学人教版(2019)必修 第二册(共25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-25 00:00:00 | ||
图片预览







文档简介
(共25张PPT)
第四节
有机营养物质
第 一 课时
糖类
第七章有机化合物
5%
脂肪、油、糖类
20%
肉、鱼、奶、蛋类
35%
水果、蔬菜类
40%
面食、谷物
传统美食
蔬菜水果
吃出健康
糖类
蛋白质 油脂
维生素
无机盐
水
思考:我们在生活中接触到的营养物质主要有哪一些
人体基本 营养物质
食物中营 养物质
【学习任务一】糖类的组成与分类
1.组成
糖类是绿色植物光合作用的产物,也是人类 最重要的能量来源。人们最初发现的这一类
化合物的化学组成大多符合Cn(H O)m的通式
(但不全是),因此糖类也被称为碳水化合
物。
1.糖类组成:糖类是由C、H、O 三种元素组成的一类有机化合物,
其组成大多可以用通式C,(H O)m 表示,过去曾称其为碳水化合物
糖 类 = “碳水化合物”
2.糖的分类:糖类可以根据其能否水解以及水解产物的多少不同, 划分为单糖、二糖、多糖。
多糖通常没有甜味,有甜味的不一定是糖类,例如木糖醇
糖类 有甜味
糖类
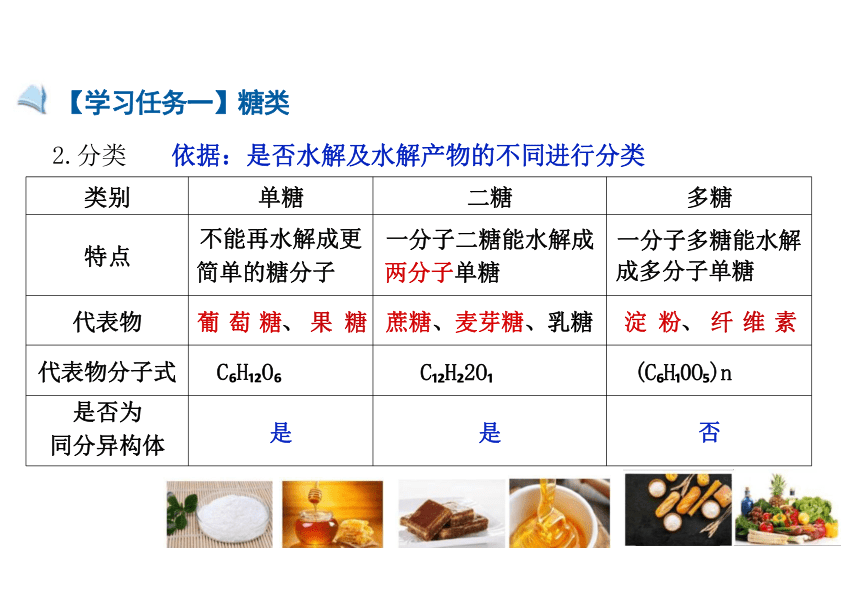
类别 单糖 二糖
多糖
特点 不能再水解成更 简单的糖分子 一分子二糖能水解成 两分子单糖
一分子多糖能水解 成多分子单糖
代表物 葡 萄 糖、 果 糖 蔗糖、麦芽糖、乳糖
淀 粉、 纤 维 素
代表物分子式 C H O C H 2O
(C H 0O )n
是否为 同分异构体 是 是
否
【学习任务一】糖类
2.分类 依据:是否水解及水解产物的不同进行分类
葡萄糖 蔗糖 淀粉
麦芽糖 纤维素 果糖
结 构 简 式 :CH OH—CHOH—CHOH—CHOH—CHOH—CHO
或CH OH(CHOH) CHO
官能团:羟基、醛基
2.物理性质
葡萄糖是一种有有甜味 的 无色 晶 体 ,能 溶于水。
【学习任务二】葡萄糖
请同学们阅读课本84页内容,归纳葡萄糖的物理性质和化学性质。
分子式:
1.结构
C H 2O
根据实验7-7,回答以下问题: (1)Cu(OH) 要现用现配;(2)配制Cu(OHD 时NaOH 溶液要过量。
1.葡萄糖与新制Cu(OH) 反应的实验操作中,有哪些注意事项
2.如何配制银氨溶液 向硝酸银溶液中逐滴加入稀氨水,直到最初产生的沉淀恰好溶解为止。
3.葡萄糖的两个实验中,它们的加热方式是否完全相同 操 作I 加热煮沸;操作Ⅱ水浴加热
4 .葡萄糖的两个实验中可分别观察到什么现象 体现了葡萄糖的什么性质
操作I产生砖红色沉淀 Cu O, 操作Ⅱ试管内壁形成光亮的银镜。氢氧化铜被还原成Cu O,Agt→Ag, -CHO 被氧化成-COOH, 葡萄糖表现还原性。
【学习任务二】葡萄糖
3.葡萄糖的化学性质
(1)葡萄糖+新制Cu(OH) →砖红色沉淀(Cu O) 检验葡萄糖 (医疗上尿糖的检验)
砖红色沉淀
(Cu O)
5滴
5%的CuSO 溶液
0
2 mL
10%的葡萄糖溶液
0
2 mL 10%的NaOH溶液
(2)葡萄糖+银氨溶液 → 银镜( Ag)
检验葡萄糖
至产生的沉淀
恰好溶解为止
1 mL 10%
葡萄糖溶液
0
2%的AgNO
溶 液 1 mL
得到银氨溶液 用途:用于检验醛基、工业上用 Ag(NH ) OH 于制镜工业、热水瓶胆镀银等。
【学习任务二】葡萄糖
2%
氨水
银镜
热水
0
【学习任务三】蔗糖
1.组成
蔗糖分子式为 C 2H 2O 1 ,与麦芽糖、乳糖互为 同分异构体。
【学习任务三】蔗糖
2.化学性质
催化剂
蔗糖水解:C H O +H O — → C H O +C H O
蔗糖 葡萄糖 果糖
【实验7-8】
(1)回忆生物课中学习的检验淀粉的方
头或土豆上,观察现象。
(2)在试管中加入0.5 2m
待溶液冷却后向其中加) 将
少 量 新 制 的Cu(OH) , 力加 释
【学习任务四】淀粉
1.组成
通式为 (C H Os)n ,属于天然高分子化合物。
实验操作 稀硫酸 淀粉 溶液 NaOH 溶液 5min后 热水
新制的
Cu(OH)
实验现象 最终有 砖红色沉淀 生成 实验结论 淀粉水解生成的 葡萄糖 ,与新制的Cu(OH) 共 热 生 成 氧化亚铜。 淀粉水解的化 学反应方程式 催化剂 (C H 0O )n+nH O 淀 粉 ( 或 纤 维 素 )
C H 2O
葡萄糖
【学习任务四】淀粉 关键!!!
情况 现象A 现象B
结论
① 溶液呈蓝色 未产生银镜
未水解
② 溶液呈蓝色 出现银镜
部分水解
③ 溶液不变蓝色 出现银镜
完全水解
淀粉水解程度的判断检验
现象A
淀 粉 稀H SO 水 解
溶液 溶液
中和液(呈碱性)
实验现象及结论
碘水
NaOH
银氨溶液
△
现象B
【学习任务四】淀粉
2.化学性质
a.特征反应:淀粉遇单质碘变蓝。
b.淀粉水解反应:
催化剂
(C H 0O )n+nH O nC H 2O 淀粉(或纤维素) 葡萄糖
用于工业生产葡萄糖
缓慢氧化,释放能量
C H O +60 -酶6CO +6H O
(2)人体内,无纤维素酶,无法吸收和利用,但纤维素 能刺激肠道蠕动促进消化 和 排泄 0
【学习任务五】糖类的应用
1.人体应用
(1)淀粉为人体提供能量
【学习任务五】糖类的应用
2.工业应用
以富含 淀粉的农作物为原料酿酒,以富含纤维素的植物秸秆为原料 生产燃料乙醇。
酶
淀粉或纤维素葡萄糖 一 乙醇
【学习评价】
1. 糖类是人类最重要的能量来源,下列关于糖类的说法中,正确的是 A. 糖类都可以水解 C
B.糖类是具有甜味的物质
C.糖类都含有C 、H 、O元素
D.淀粉和纤维素互为同分异构体
2.能证明淀粉已经完全水解的试剂是 B
A. 碘化钾溶液 B. 碘水
C. 银氨溶液 D. 酚酞溶液
【学习评价】
3.葡萄糖(C H O )是一种重要的营养物质,下列关于葡萄糖的说法正确 的是 A
A.葡萄糖是一种单糖
B. 葡萄糖分子中有6个碳原子、6个水分子
C.常温下,葡萄糖可与新制的氢氧化铜悬浊液反应
D.1 mol葡萄糖完全燃烧需要9 mol氧气
蔗糖
双糖
NaOH 麦芽糖
溶液 中和液(呈碱性)
水解程度的实验
淀粉 水解液
C H 2O
具有醇的
)H 性质
CHO 具有还原性
不含醛基,水解
生成葡萄糖和果糖
含有醛基,水解
生成葡萄糖
结构 CH -(CHOH)4— CHO 葡萄糖 简式 OH
单糖
.H、O 组成元素
碘水 银氨溶液
现象A 现象B
分子式
官能团
纤维素
淀粉
最简式 CH O
20%硫酸
果糖
多糖
糖 类
第四节
有机营养物质
第 一 课时
糖类
第七章有机化合物
5%
脂肪、油、糖类
20%
肉、鱼、奶、蛋类
35%
水果、蔬菜类
40%
面食、谷物
传统美食
蔬菜水果
吃出健康
糖类
蛋白质 油脂
维生素
无机盐
水
思考:我们在生活中接触到的营养物质主要有哪一些
人体基本 营养物质
食物中营 养物质
【学习任务一】糖类的组成与分类
1.组成
糖类是绿色植物光合作用的产物,也是人类 最重要的能量来源。人们最初发现的这一类
化合物的化学组成大多符合Cn(H O)m的通式
(但不全是),因此糖类也被称为碳水化合
物。
1.糖类组成:糖类是由C、H、O 三种元素组成的一类有机化合物,
其组成大多可以用通式C,(H O)m 表示,过去曾称其为碳水化合物
糖 类 = “碳水化合物”
2.糖的分类:糖类可以根据其能否水解以及水解产物的多少不同, 划分为单糖、二糖、多糖。
多糖通常没有甜味,有甜味的不一定是糖类,例如木糖醇
糖类 有甜味
糖类
类别 单糖 二糖
多糖
特点 不能再水解成更 简单的糖分子 一分子二糖能水解成 两分子单糖
一分子多糖能水解 成多分子单糖
代表物 葡 萄 糖、 果 糖 蔗糖、麦芽糖、乳糖
淀 粉、 纤 维 素
代表物分子式 C H O C H 2O
(C H 0O )n
是否为 同分异构体 是 是
否
【学习任务一】糖类
2.分类 依据:是否水解及水解产物的不同进行分类
葡萄糖 蔗糖 淀粉
麦芽糖 纤维素 果糖
结 构 简 式 :CH OH—CHOH—CHOH—CHOH—CHOH—CHO
或CH OH(CHOH) CHO
官能团:羟基、醛基
2.物理性质
葡萄糖是一种有有甜味 的 无色 晶 体 ,能 溶于水。
【学习任务二】葡萄糖
请同学们阅读课本84页内容,归纳葡萄糖的物理性质和化学性质。
分子式:
1.结构
C H 2O
根据实验7-7,回答以下问题: (1)Cu(OH) 要现用现配;(2)配制Cu(OHD 时NaOH 溶液要过量。
1.葡萄糖与新制Cu(OH) 反应的实验操作中,有哪些注意事项
2.如何配制银氨溶液 向硝酸银溶液中逐滴加入稀氨水,直到最初产生的沉淀恰好溶解为止。
3.葡萄糖的两个实验中,它们的加热方式是否完全相同 操 作I 加热煮沸;操作Ⅱ水浴加热
4 .葡萄糖的两个实验中可分别观察到什么现象 体现了葡萄糖的什么性质
操作I产生砖红色沉淀 Cu O, 操作Ⅱ试管内壁形成光亮的银镜。氢氧化铜被还原成Cu O,Agt→Ag, -CHO 被氧化成-COOH, 葡萄糖表现还原性。
【学习任务二】葡萄糖
3.葡萄糖的化学性质
(1)葡萄糖+新制Cu(OH) →砖红色沉淀(Cu O) 检验葡萄糖 (医疗上尿糖的检验)
砖红色沉淀
(Cu O)
5滴
5%的CuSO 溶液
0
2 mL
10%的葡萄糖溶液
0
2 mL 10%的NaOH溶液
(2)葡萄糖+银氨溶液 → 银镜( Ag)
检验葡萄糖
至产生的沉淀
恰好溶解为止
1 mL 10%
葡萄糖溶液
0
2%的AgNO
溶 液 1 mL
得到银氨溶液 用途:用于检验醛基、工业上用 Ag(NH ) OH 于制镜工业、热水瓶胆镀银等。
【学习任务二】葡萄糖
2%
氨水
银镜
热水
0
【学习任务三】蔗糖
1.组成
蔗糖分子式为 C 2H 2O 1 ,与麦芽糖、乳糖互为 同分异构体。
【学习任务三】蔗糖
2.化学性质
催化剂
蔗糖水解:C H O +H O — → C H O +C H O
蔗糖 葡萄糖 果糖
【实验7-8】
(1)回忆生物课中学习的检验淀粉的方
头或土豆上,观察现象。
(2)在试管中加入0.5 2m
待溶液冷却后向其中加) 将
少 量 新 制 的Cu(OH) , 力加 释
【学习任务四】淀粉
1.组成
通式为 (C H Os)n ,属于天然高分子化合物。
实验操作 稀硫酸 淀粉 溶液 NaOH 溶液 5min后 热水
新制的
Cu(OH)
实验现象 最终有 砖红色沉淀 生成 实验结论 淀粉水解生成的 葡萄糖 ,与新制的Cu(OH) 共 热 生 成 氧化亚铜。 淀粉水解的化 学反应方程式 催化剂 (C H 0O )n+nH O 淀 粉 ( 或 纤 维 素 )
C H 2O
葡萄糖
【学习任务四】淀粉 关键!!!
情况 现象A 现象B
结论
① 溶液呈蓝色 未产生银镜
未水解
② 溶液呈蓝色 出现银镜
部分水解
③ 溶液不变蓝色 出现银镜
完全水解
淀粉水解程度的判断检验
现象A
淀 粉 稀H SO 水 解
溶液 溶液
中和液(呈碱性)
实验现象及结论
碘水
NaOH
银氨溶液
△
现象B
【学习任务四】淀粉
2.化学性质
a.特征反应:淀粉遇单质碘变蓝。
b.淀粉水解反应:
催化剂
(C H 0O )n+nH O nC H 2O 淀粉(或纤维素) 葡萄糖
用于工业生产葡萄糖
缓慢氧化,释放能量
C H O +60 -酶6CO +6H O
(2)人体内,无纤维素酶,无法吸收和利用,但纤维素 能刺激肠道蠕动促进消化 和 排泄 0
【学习任务五】糖类的应用
1.人体应用
(1)淀粉为人体提供能量
【学习任务五】糖类的应用
2.工业应用
以富含 淀粉的农作物为原料酿酒,以富含纤维素的植物秸秆为原料 生产燃料乙醇。
酶
淀粉或纤维素葡萄糖 一 乙醇
【学习评价】
1. 糖类是人类最重要的能量来源,下列关于糖类的说法中,正确的是 A. 糖类都可以水解 C
B.糖类是具有甜味的物质
C.糖类都含有C 、H 、O元素
D.淀粉和纤维素互为同分异构体
2.能证明淀粉已经完全水解的试剂是 B
A. 碘化钾溶液 B. 碘水
C. 银氨溶液 D. 酚酞溶液
【学习评价】
3.葡萄糖(C H O )是一种重要的营养物质,下列关于葡萄糖的说法正确 的是 A
A.葡萄糖是一种单糖
B. 葡萄糖分子中有6个碳原子、6个水分子
C.常温下,葡萄糖可与新制的氢氧化铜悬浊液反应
D.1 mol葡萄糖完全燃烧需要9 mol氧气
蔗糖
双糖
NaOH 麦芽糖
溶液 中和液(呈碱性)
水解程度的实验
淀粉 水解液
C H 2O
具有醇的
)H 性质
CHO 具有还原性
不含醛基,水解
生成葡萄糖和果糖
含有醛基,水解
生成葡萄糖
结构 CH -(CHOH)4— CHO 葡萄糖 简式 OH
单糖
.H、O 组成元素
碘水 银氨溶液
现象A 现象B
分子式
官能团
纤维素
淀粉
最简式 CH O
20%硫酸
果糖
多糖
糖 类
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
