乙醇 高中化学人教版(2019)必修 第二册(共17张PPT)
文档属性
| 名称 | 乙醇 高中化学人教版(2019)必修 第二册(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-25 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
生活中两种常见的有机物
--乙醇
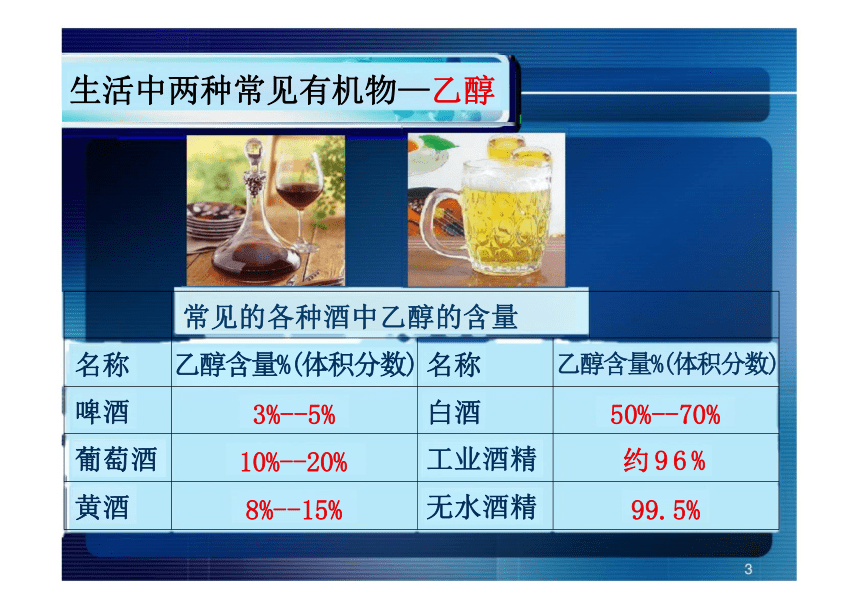
常见的各种酒中乙醇的含量
名称 乙醇含量%(体积分数) 名称 乙醇含量%(体积分数) 啤酒 3%--5% 白酒 50%--70% 葡萄酒 10%--20% 工业酒精 约96% 黄酒 8%--15% 无水酒精 99.5%
生活中两种常见有机物—乙醇
西藏风情画藏泉青积酒
原青
【雪域典藏】 稞
香型:青稞浓香型酒精度:52%vol 净含量:500ml
颜 色 无色透明
气 味 ,特殊香味
状 态。液体
挥发件。易挥发 度。比水小
溶 解 性跟水以任意比互溶
能够溶解多种无机物和有机物
一、乙醇的物理性质
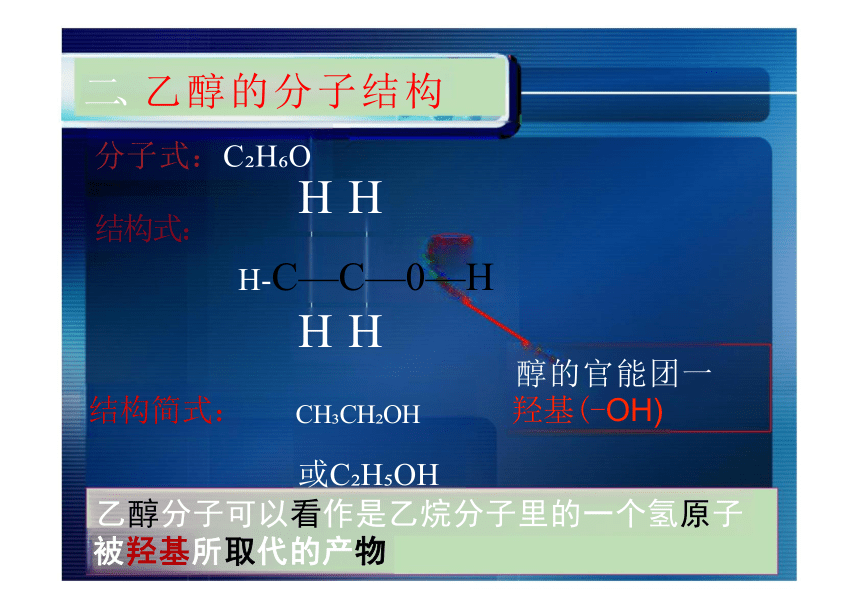
二、乙醇的分子结构
分子式:C H O
结构式:
H-C—C—0—H
H H
醇的官能团一
结构简式: CH CH OH 羟基(-OH)
或C H OH
乙醇分子可以看作是乙烷分子里的一个氢原子
被羟基所取代的产物
H H
思 考
1、-OH 与OH 二有何区别
(1).一OH 是中性官能团,不能独立存在, 可电离出H+ 或不电离。
(2).OH- 是带一个单位负电荷,可自由 移动的离子,呈碱性。
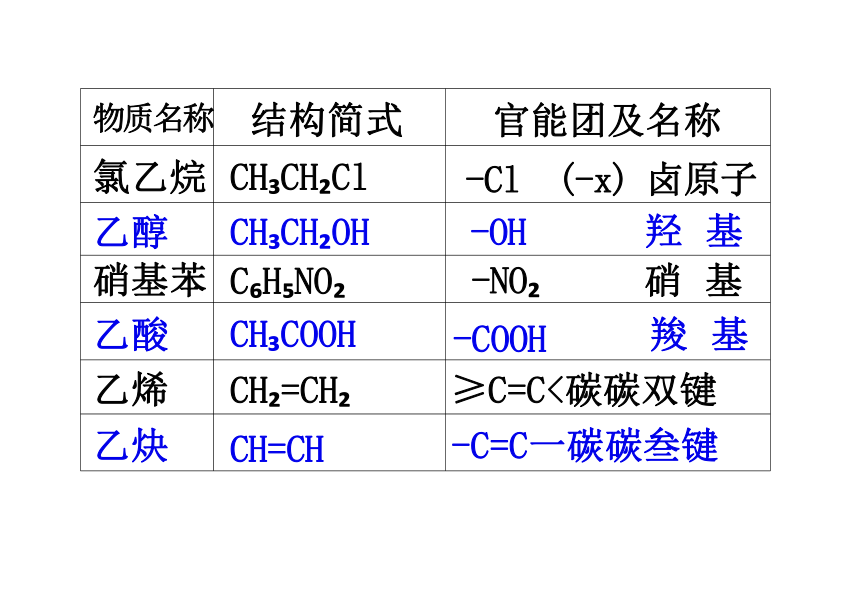
物质名称 结构简式
官能团及名称
氯乙烷 CH CH Cl
-Cl (-x) 卤原子
乙醇 CH CH OH
-OH 羟 基
硝基苯 C H NO
-NO 硝 基
乙酸 CH COOH
-COOH 羧 基
乙烯 CH =CH
≥C=C<碳碳双键
乙炔 CH=CH
-C=C一碳碳叁键
C CH CH
D CH CH OH
G CH COOH
下列几种物质是否属于烃的衍生物
如果是烃的衍生物,请指出它们的官能团。
练习
IB
F。
A H
H
H
E
NO
H
三、乙醇的化学性质
1、乙醇的氧化反应
①乙醇的燃烧
C H OH+30, 点燃、2CO +3H O
现象:乙醇在空气中燃烧,火焰呈 淡蓝色,同时放出大量的热。
因此:实验室里也常用它作为燃料。
实验探究一
·在试管中加入3~4ml乙 醇,将铜丝在酒精灯外 焰上灼烧至红热,迅速 插入乙醇中。反复几次, 观察铜丝颜色变化,闻 试管中气味变化。
观察并思考:
铜丝灼烧后是什么颜色,趁热插入乙醇后呢
铜丝先后发生了什么反应 乙醇呢
味 铜丝作催化剂
总反应方程式:
乙醛
[思考]铜丝在此实验中起什么作用
②乙醇的催化氧化
铜丝
2CuO
→CH CHO +Cu+H O
Cu/A0
人 20H GHO+2H O
2Cu+O
C H OH+CuO
2GHGHOH 率
变黑
变红
产生刺
激性气
△
去H 氧化规律:去掉—OH 上的H
和—OH 所在的碳原子上H
应力程
③被酸性KMnO 、K Cr O 溶液氧化
K Cr O — →Cr (SO4)3
驾驶员正在接受酒精检查
小结
一、乙醇的物理性质
二、乙醇的结构
三、乙醇的化学性质
1、乙醇的氧化反应
①燃 烧
②催化氧化
2@HCHLO,aOH0+2H,0
断 键 H- C- C-
H H
B: ① ③
1、发生催化氧化反应时在何处 H H
H
15
Thank You!
官 能 团:决 定 有 机 化 合
物 的 化 学 特 性 的 原 子 或 原子团叫做官能团。
烃 的 衍 生 物: 由 烃 演 变 而来的非烃类有机物。
生活中两种常见的有机物
--乙醇
常见的各种酒中乙醇的含量
名称 乙醇含量%(体积分数) 名称 乙醇含量%(体积分数) 啤酒 3%--5% 白酒 50%--70% 葡萄酒 10%--20% 工业酒精 约96% 黄酒 8%--15% 无水酒精 99.5%
生活中两种常见有机物—乙醇
西藏风情画藏泉青积酒
原青
【雪域典藏】 稞
香型:青稞浓香型酒精度:52%vol 净含量:500ml
颜 色 无色透明
气 味 ,特殊香味
状 态。液体
挥发件。易挥发 度。比水小
溶 解 性跟水以任意比互溶
能够溶解多种无机物和有机物
一、乙醇的物理性质
二、乙醇的分子结构
分子式:C H O
结构式:
H-C—C—0—H
H H
醇的官能团一
结构简式: CH CH OH 羟基(-OH)
或C H OH
乙醇分子可以看作是乙烷分子里的一个氢原子
被羟基所取代的产物
H H
思 考
1、-OH 与OH 二有何区别
(1).一OH 是中性官能团,不能独立存在, 可电离出H+ 或不电离。
(2).OH- 是带一个单位负电荷,可自由 移动的离子,呈碱性。
物质名称 结构简式
官能团及名称
氯乙烷 CH CH Cl
-Cl (-x) 卤原子
乙醇 CH CH OH
-OH 羟 基
硝基苯 C H NO
-NO 硝 基
乙酸 CH COOH
-COOH 羧 基
乙烯 CH =CH
≥C=C<碳碳双键
乙炔 CH=CH
-C=C一碳碳叁键
C CH CH
D CH CH OH
G CH COOH
下列几种物质是否属于烃的衍生物
如果是烃的衍生物,请指出它们的官能团。
练习
IB
F。
A H
H
H
E
NO
H
三、乙醇的化学性质
1、乙醇的氧化反应
①乙醇的燃烧
C H OH+30, 点燃、2CO +3H O
现象:乙醇在空气中燃烧,火焰呈 淡蓝色,同时放出大量的热。
因此:实验室里也常用它作为燃料。
实验探究一
·在试管中加入3~4ml乙 醇,将铜丝在酒精灯外 焰上灼烧至红热,迅速 插入乙醇中。反复几次, 观察铜丝颜色变化,闻 试管中气味变化。
观察并思考:
铜丝灼烧后是什么颜色,趁热插入乙醇后呢
铜丝先后发生了什么反应 乙醇呢
味 铜丝作催化剂
总反应方程式:
乙醛
[思考]铜丝在此实验中起什么作用
②乙醇的催化氧化
铜丝
2CuO
→CH CHO +Cu+H O
Cu/A0
人 20H GHO+2H O
2Cu+O
C H OH+CuO
2GHGHOH 率
变黑
变红
产生刺
激性气
△
去H 氧化规律:去掉—OH 上的H
和—OH 所在的碳原子上H
应力程
③被酸性KMnO 、K Cr O 溶液氧化
K Cr O — →Cr (SO4)3
驾驶员正在接受酒精检查
小结
一、乙醇的物理性质
二、乙醇的结构
三、乙醇的化学性质
1、乙醇的氧化反应
①燃 烧
②催化氧化
2@HCHLO,aOH0+2H,0
断 键 H- C- C-
H H
B: ① ③
1、发生催化氧化反应时在何处 H H
H
15
Thank You!
官 能 团:决 定 有 机 化 合
物 的 化 学 特 性 的 原 子 或 原子团叫做官能团。
烃 的 衍 生 物: 由 烃 演 变 而来的非烃类有机物。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
