6.2.1 化学反应的速率与限度 课时1(教学课件)- 高中化学人教版(2019)必修第二册(共16张PPT)
文档属性
| 名称 | 6.2.1 化学反应的速率与限度 课时1(教学课件)- 高中化学人教版(2019)必修第二册(共16张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 552.9KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-25 00:00:00 | ||
图片预览






文档简介
(共16张PPT)
第六章化学反应与能量
第二节化学反应的速率与限度
课时1化学反应的速率
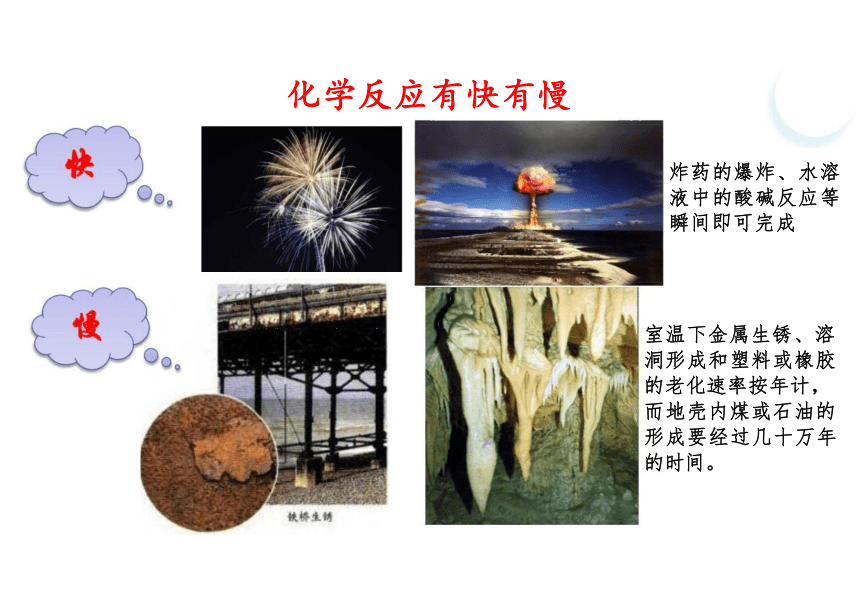
炸药的爆炸、水溶 液中的酸碱反应等 瞬间即可完成
室温下金属生锈、溶 洞形成和塑料或橡胶 的老化速率按年计, 而地壳内煤或石油的 形成要经过几十万年 的时间。
化学反应有快有慢
通常用 单位时间 内反应物浓度的减小或生成物浓度的
增大 来表示 (取正值)。(p43)
△c(A)
v(A)
t
单位: mol/(L·min)
mol/(L·s)
mol-L-1·min-1
molL-1.s-1
一 、化学反应的速率
在2SO +O 化剂、2 SO 反应中:如果2min内SO 的
浓度由6 mol/L 下降为2 mol/L, 那么,
用SO 浓度变化来表示的化学反应速率为 2 mol/(L·min)
课 堂 练习
起始浓度(mol/L) 1 3
浓度变化量(mol/L) 0.4 1.2
2s后浓度(mol/L) 0.6
反应速率 v(N )v(H )
mol/(L·s) 0.2 0.6
1 :3
已知在2L的密闭容器中合成氨反应如下:
N +3n,准化術2NH
0
0.8
v(NH ) 0.4
2
课 堂 练 习
注意
(1)同一反应可用不同物质来表示v,
速率之比等于方程式的化学计量数之比
(2)v 需指明具体物质
一、化学反应的速率
2 、反 应A(g)+3B(g)=2C(g) 在2L密闭容器中反应,0.5min内C的 物质的量增加了0.6mol, 有关反应速率正确的是( A )
A 、v(A)=0.3mol/(L·min) B 、v(C)=0.12mol/(L·min)
C 、v(B)=v(A)/3 D 、v(A)=0.6mol/(L·min)
1 、在 一 定条件下,mA+nB=pC 的反应中,各物质的化学反应
速率为v(A)=amol/(L · s),v(B)=0.5amol/(L · s),v(C)=amol/(L · s), 则该反应的化学方程式为: 2A+B=2C
课 堂练 习
3. 在2A+B=3C+4D 反应中,下列各表示该反应的速度
最快的是 ( B ) 全部用物质B表示
A.v(A)=0.4mol/(L·min) 0.2
B.v(B)=0.4mol/(L·min)
C.v(C)=0.9mol/(L·min) 0.3
D.v(D)=1.2mol/(L·min) 0.3
▲比较反应的快慢,应取同一参照物!
课 堂练 习
冷 却 器
氨 合 成 塔
能否控制化学反应速率呢
有害的——越慢越好!
有利的——越快越好!
氮氢混合气
压练机
缩机
铂
影响化学反应速率的因素
(1)内因:反应物本身的性质
(反应物越活泼,反应速率越快)
(2) 外因:温度、反应物浓度、压强、催化剂、固体表面积...
一 、化学反应的速率
(2)外因:p45
①温度:T 个,v个
②反应物浓度:C反个,v 个(适用于气体和溶液)
③压强:P个,c反 ,v (适用于气体)
如:2SO (g)+0 (g)÷2SO (g)
气体体积缩小 气体浓度增大)反应速率增大
增大压强:
气体体积不变
气体浓度不变 反应速率不变
影响化学反应速率的因素
(2)外因:
④ 催 化 剂 :v 个
自学P 神奇的催化剂
催化剂能极大地改变反应速率,而自身的组成、化学性质 和质量在反应前后不发生变化,具有一定的选择性。
⑤ 固体表面积: S 个,v 个
影响化学反应速率的因素
[小结]影响化学反应速率的因素:
(1)内因(决定性因素):反应物本身的性质
(2)外因(外界条件):在其它条件相同时——
①使用(正)催化剂,可以加快 化学反应速率
②温度越高,化学反应速率越快 。
③反 应物浓度越大,化学反应速率_越 快。
④反应物之间接触面积越大,化学反应速率越快 。
⑤其它条件:压 强、反应物状态等。
下列调控反应速率的措施或实验中,分别利用或体现了哪些影响反应速率的因素
(1) 向炉膛内鼓风,用煤粉代替煤块可以使炉火更旺 增大反应物的接触面积 大O 浓 度
( 2 ) 把食物存放在冰箱里、在糕点包装内放置除氧剂可以延长食品保质期。
度 2 浓度
(3)做化学实验时,为加速反应的进行,通常将块状或颗粒状的固体药品研细并 混匀,或者将固体试剂溶于水配成溶液后再进行实验。 增大反应物的接触面积
(4)铁在空气中和在纯氧中反应的剧烈程度明显不同。
增大O 浓度
【思考与讨论】p45
【思考与讨论】
1.Ba(OH) ·8H O和NH C1一起放入烧杯中,为什么要用玻璃棒
快速搅拌 增大反应物的接触面积
2.实验室制取氢气时,是用粗锌好(有杂质)还是用纯锌好
构成原电池
课 堂小 结 化学反应速率
mol/(L·min) mol/(L·s)
2.特点 参加反应的各物质的化学反应速率之比等于化学计量数之比 3.影响因素
内因:反应物本身的性质
外因:温度、反应物浓度、压强、催化剂、固体表面积 . .
1.定义式
第六章化学反应与能量
第二节化学反应的速率与限度
课时1化学反应的速率
炸药的爆炸、水溶 液中的酸碱反应等 瞬间即可完成
室温下金属生锈、溶 洞形成和塑料或橡胶 的老化速率按年计, 而地壳内煤或石油的 形成要经过几十万年 的时间。
化学反应有快有慢
通常用 单位时间 内反应物浓度的减小或生成物浓度的
增大 来表示 (取正值)。(p43)
△c(A)
v(A)
t
单位: mol/(L·min)
mol/(L·s)
mol-L-1·min-1
molL-1.s-1
一 、化学反应的速率
在2SO +O 化剂、2 SO 反应中:如果2min内SO 的
浓度由6 mol/L 下降为2 mol/L, 那么,
用SO 浓度变化来表示的化学反应速率为 2 mol/(L·min)
课 堂 练习
起始浓度(mol/L) 1 3
浓度变化量(mol/L) 0.4 1.2
2s后浓度(mol/L) 0.6
反应速率 v(N )v(H )
mol/(L·s) 0.2 0.6
1 :3
已知在2L的密闭容器中合成氨反应如下:
N +3n,准化術2NH
0
0.8
v(NH ) 0.4
2
课 堂 练 习
注意
(1)同一反应可用不同物质来表示v,
速率之比等于方程式的化学计量数之比
(2)v 需指明具体物质
一、化学反应的速率
2 、反 应A(g)+3B(g)=2C(g) 在2L密闭容器中反应,0.5min内C的 物质的量增加了0.6mol, 有关反应速率正确的是( A )
A 、v(A)=0.3mol/(L·min) B 、v(C)=0.12mol/(L·min)
C 、v(B)=v(A)/3 D 、v(A)=0.6mol/(L·min)
1 、在 一 定条件下,mA+nB=pC 的反应中,各物质的化学反应
速率为v(A)=amol/(L · s),v(B)=0.5amol/(L · s),v(C)=amol/(L · s), 则该反应的化学方程式为: 2A+B=2C
课 堂练 习
3. 在2A+B=3C+4D 反应中,下列各表示该反应的速度
最快的是 ( B ) 全部用物质B表示
A.v(A)=0.4mol/(L·min) 0.2
B.v(B)=0.4mol/(L·min)
C.v(C)=0.9mol/(L·min) 0.3
D.v(D)=1.2mol/(L·min) 0.3
▲比较反应的快慢,应取同一参照物!
课 堂练 习
冷 却 器
氨 合 成 塔
能否控制化学反应速率呢
有害的——越慢越好!
有利的——越快越好!
氮氢混合气
压练机
缩机
铂
影响化学反应速率的因素
(1)内因:反应物本身的性质
(反应物越活泼,反应速率越快)
(2) 外因:温度、反应物浓度、压强、催化剂、固体表面积...
一 、化学反应的速率
(2)外因:p45
①温度:T 个,v个
②反应物浓度:C反个,v 个(适用于气体和溶液)
③压强:P个,c反 ,v (适用于气体)
如:2SO (g)+0 (g)÷2SO (g)
气体体积缩小 气体浓度增大)反应速率增大
增大压强:
气体体积不变
气体浓度不变 反应速率不变
影响化学反应速率的因素
(2)外因:
④ 催 化 剂 :v 个
自学P 神奇的催化剂
催化剂能极大地改变反应速率,而自身的组成、化学性质 和质量在反应前后不发生变化,具有一定的选择性。
⑤ 固体表面积: S 个,v 个
影响化学反应速率的因素
[小结]影响化学反应速率的因素:
(1)内因(决定性因素):反应物本身的性质
(2)外因(外界条件):在其它条件相同时——
①使用(正)催化剂,可以加快 化学反应速率
②温度越高,化学反应速率越快 。
③反 应物浓度越大,化学反应速率_越 快。
④反应物之间接触面积越大,化学反应速率越快 。
⑤其它条件:压 强、反应物状态等。
下列调控反应速率的措施或实验中,分别利用或体现了哪些影响反应速率的因素
(1) 向炉膛内鼓风,用煤粉代替煤块可以使炉火更旺 增大反应物的接触面积 大O 浓 度
( 2 ) 把食物存放在冰箱里、在糕点包装内放置除氧剂可以延长食品保质期。
度 2 浓度
(3)做化学实验时,为加速反应的进行,通常将块状或颗粒状的固体药品研细并 混匀,或者将固体试剂溶于水配成溶液后再进行实验。 增大反应物的接触面积
(4)铁在空气中和在纯氧中反应的剧烈程度明显不同。
增大O 浓度
【思考与讨论】p45
【思考与讨论】
1.Ba(OH) ·8H O和NH C1一起放入烧杯中,为什么要用玻璃棒
快速搅拌 增大反应物的接触面积
2.实验室制取氢气时,是用粗锌好(有杂质)还是用纯锌好
构成原电池
课 堂小 结 化学反应速率
mol/(L·min) mol/(L·s)
2.特点 参加反应的各物质的化学反应速率之比等于化学计量数之比 3.影响因素
内因:反应物本身的性质
外因:温度、反应物浓度、压强、催化剂、固体表面积 . .
1.定义式
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
