6.1.2化学反应与电能 (教学课件)- 高中化学人教版(2019)必修第二册(共21张PPT)
文档属性
| 名称 | 6.1.2化学反应与电能 (教学课件)- 高中化学人教版(2019)必修第二册(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-25 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
第六章化学反应与能量
第一节 化学反应与能量变化 第2课时化学反应与电能
【学习目标与核心素养】
学习目标
1.通过实验探究认识化学能与电能之间转化的实质。
2.理解原电池的概念及工作原理和构成条件。
3. 能正确书写简单化学电源的电极反应式。
核心素养
1.科学探究:认识构成原电池的条件及其原理,判断原电池的正负极。 2.创新意识:利用原电池原理能设计原电池。
3.宏观辨识与微观探析:会分析物质化学变化中的能量变化与物质微观结
构的关系。
电力改变了我们的生活那么,电是怎么来的呢
核电3%
7图6-52015年我国电力生产量构成图
火电74%
水电19%
发电
电
其他1% 风电3%
电的来源
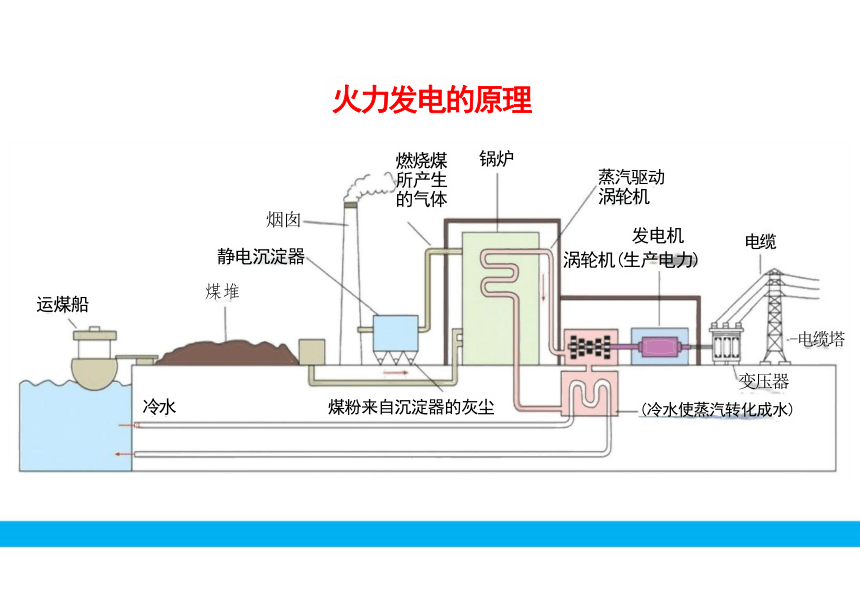
燃烧煤 所产生 的气体
烟囱
静电沉淀器
煤堆
-电缆塔
变压器
(冷水使蒸汽转化成水)
运煤船
冷水
在
蒸汽驱动
涡轮机
发电机
涡轮机(生产电力)
火力发电的原理
煤粉来自沉淀器的灰尘
锅炉
电缆
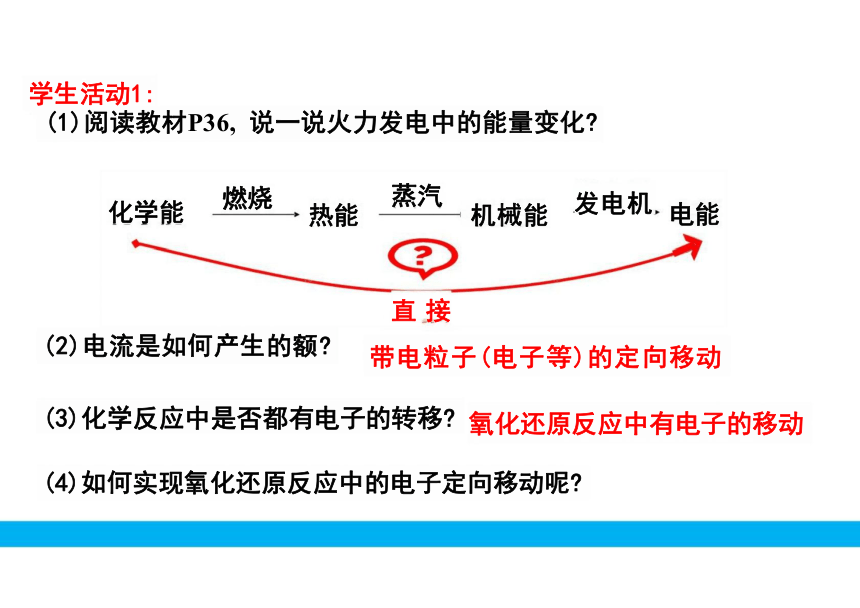
(3)化学反应中是否都有电子的转移 氧化还原反应中有电子的移动
(4)如何实现氧化还原反应中的电子定向移动呢
学生活动1:
(1)阅读教材P36, 说一说火力发电中的能量变化
直 接
带电粒子(电子等)的定向移动
(2)电流是如何产生的额
发电机
机械能
化学能
电能
蒸汽
燃烧
热能
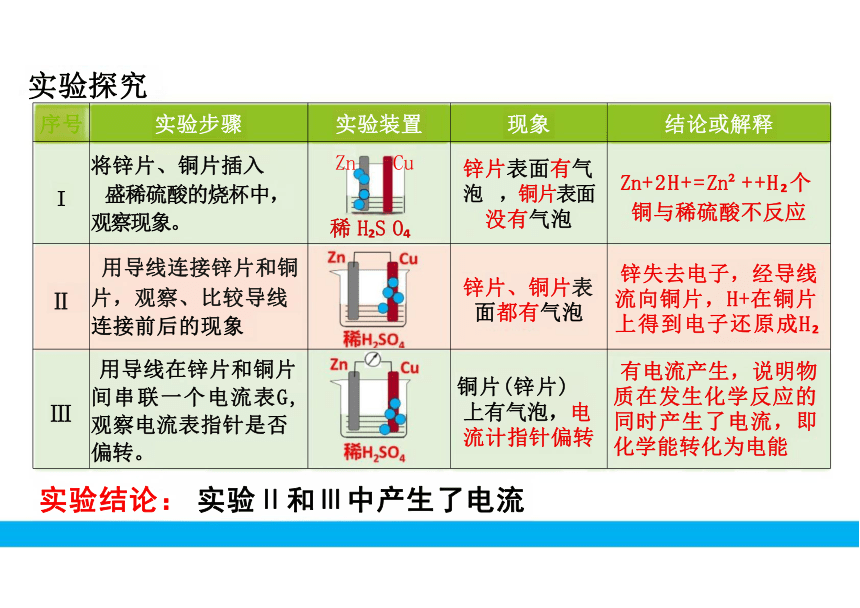
实验探究
【实验6-3】
(1)将锌片和铜片插入盛有稀硫酸的烧杯中,观察现象。
(2)用导线连接锌片和铜片,观察、比较导线连接前后的现象。
(3)如图所示,用导线在锌片和铜片之间串联一个电流表,观察电流表的
指针是否偏转。
序号 实验步骤 实验装置 现象
结论或解释
I 将锌片、铜片插入 盛稀硫酸的烧杯中, 观察现象。 Zn Cu 稀 H S O 锌片表面有气 泡 ,铜片表面 没有气泡
Zn+2H+=Zn ++H 个 铜与稀硫酸不反应
Ⅱ 用导线连接锌片和铜 片,观察、比较导线 连接前后的现象 锌片、铜片表 面都有气泡
锌失去电子,经导线 流向铜片,H+在铜片 上得到电子还原成H
Ⅲ 用导线在锌片和铜片 间串联一个电流表G, 观察电流表指针是否 偏转。 铜片(锌片) 上有气泡,电 流计指针偏转
有电流产生,说明物 质在发生化学反应的 同时产生了电流,即 化学能转化为电能
实验结论: 实验Ⅱ和Ⅲ中产生了电流
实验探究
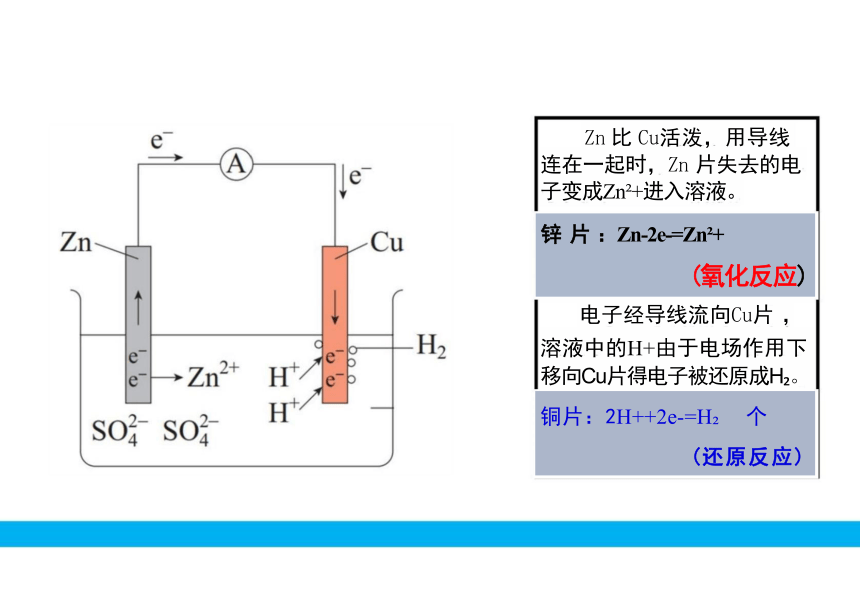
电子经导线流向Cu片 ,
溶液中的H+由于电场作用下 移向Cu片得电子被还原成H 。
铜片:2H++2e-=H 个
(还原反应)
锌 片 :Zn-2e-=Zn +
(氧化反应)
Zn 比 Cu活泼,用导线 连在一起时,Zn 片失去的电 子变成Zn +进入溶液。
一、原电池
1.定义:将化学能直接转变成电能的装置,称为原电池
2.本质:氧化反应和还原反应分别在两个不同的区域进行,使电子发 生定向移动,从而产生了电流。
3.正负极:
负 极 : 电子流出(或电流流进)的一极
正 极 : 电子流进(或电流流出)的一极
电极材料 原电池正负极 电极反应式
发生的反应
Zn片 负极 Zn-2e-=Zn2+
氧化反应
Cu片 正极 2H++2e-=H 个
还原反应
电极总离子反应 Zn+2H+=Zn ++H 个(两个电极反应之和) 小结:
负极 正极 失去电子的一极 得到电子的一极 氧化反应 还原反应
活性强
活性弱
锌 -A-
s話
_
4.电极反应:
e- 铜
外电路: 负极 今 正 极 正极 负极
内电路: 阳离子向正极移动 阴离子向负极移动
这样整个电路构成了闭合回路,带电粒子的定向移动产生电流
电极反应类型:
氧化反应
电极反应式:
Zn-2e-=Zn 2+
原电池总反应式:
电极反应类型:还原反应
电极反应式:
2H++2e-=H
5.工作原理:
电极名称:负 极
e-
铜
电极名称:正极
Zn+2H+==Zn ++H 个
H
H+
SO2-Ht
e-
锌
A-
SO2-
①自发的氧化还原反应均可构成原电池
②具有活动性不同的两个电极(金属与金属或金属与能导电的非金属);
③溶液:两电极均插入电解质溶液中;
④导线:两极用导线相连,形成闭合回路。
电解质溶液的作用:传 导离子、参与电极反应
学生活动2:根据原电池的工作原理,讨论形成原电池的条件有哪些
构成条件:
稀疏酸 稀硫酸 稀硫酸
⑤
C.①②③④
课堂练习:下列装置能形成原电池的是( )
CuSO溶 液
②
稀硫酸
③
稀硫酸
①
稀盐酸 ⑦
D.①②③⑥⑦
酒精 ⑥
B.①②⑤⑥
学生活动4: 阅读优化设计P44方法突破,并完成【例 题 1】、【 变 式设
问】、【针对训练1】
较不活泼金属或 能导电的非金属
还原反应
电子流入
电极增重或 有气体产生
阳离子移向
较活泼金属
氧化反应
电子流出
不断溶解 质量减小
阴离子移向
电极材料
反应类型
电子流向
电极现象
离子移向
Zn Cu
H SO
电解质溶液
e-沿导线传递,有电流产生
A
学生活动3:如何判断原电池正负极
阳离子移向
不断溶解
正极
负极
【课堂练习】1.右图是Zn 和Cu形成的原电池,某实验兴趣小组做完实验
后,记录如下:
①Zn 为 正 极 ,Cu 为负极
②H+ 向负极移动
③电子流动方向,从Zn 经外电路流向Cu④Cu 极_
⑤若有1mol 电子流过导线,则产生0.5 molH ⑥ 正极的电极反应式为 Zn -2e-==Zn +。
B
描述合理的是( )
B.③④⑤ D.②③④
H SO
CuSO (aq)
负 极(Zn ):Zn -2e=Zn +. 正极(Cu):Cu ++2e-=Cu.
总反应式:Zn +Cu += Zn +Cu.
H SO (aq)
负极(Fe ):Fe -2e-=Fe +.
正极(Ag):2H++2e-=H 个.
总反应式:Fe+2H+=Fe ++H 个
【课堂练习】2.请在图上标出电子的流动方向和电流方向,并判断正负
极,写出电极反应式和总反应式。
学生活动5:阅读优化设计P45-46方法突破,并完成【例题2】【针对训练2】
1.加快反应速率
实验室制H 时,由于锌太纯,反应一般较慢,可加入少量CuSO 以加快反应速率或使用粗锌。
2.比较金属活动性的强弱
一般负极金属活泼性大于正极金属
3.用于金属的防护
原理:使被保护的金属制品作原电池的正极而得到保护。
实例:用导线将铁阀门与锌片相连以保护铁制阀门
4.原电池的设计
(1)找:找一个能够自发进行的氧化还原反应,只有自发进行的氧化还 原反应才能被设计成原电池。
(2)拆:将氧化还原反应拆分为氧化反应和还原反应两个半反应,分别 作为负极和正极的电极反应。
还原剂一ne-= 氧化产物(负极电极反应)
氧化剂十ne-= 还原产物(正极电极反应)
(3)定:根据氧化还原反应中的还原剂和氧化剂确定原电池的负极和电 解质溶液,正极一般选择比负极活泼性差的金属或能导电的非金属。
(4)画:连接电路,形成闭合回路,画出原电池示意图。
A B C
D
正极 Zn Cu Cu
Fe
负极 Cu Zn Zn
Zn
电解质溶液 CuCl H SO CuSO
HCI
于此装置的下列叙述中,不正确的是(D
A.N上有气体放出
B.M为负极,N 为正极
C.稀硫酸中S0 2-移向M极
D.导线中有电流通过,电流方向是由M到N
【课堂练习】3.一个电池反应的离子方程式是 Zn+Cu +==Zn ++Cu,该反 应的的原电池正确组合是( C )
4.如图所示的装置,M为活动性顺序位于氢之前的金属,N为石墨棒,关
稀硫酸
)
5.如图所示,电流计指针发生偏转,同时A极质量减少,B 极上有气
泡产生,C 为电解质溶液,下列说法错误的是( C )
A.B极为原电池的正极
B.A、B、C可能分别为Zn、Cu、稀盐酸
C.C中阳离子向A极移动
D.A极发生氧化反应
6.某原电池2Fe ++Fe==3Fe +不能实现该反应的原电池是( D )
A.正极Cu,负极Fe,电解质溶液FeCl
B.正极C,负极Fe,电解质溶液Fe(NO )
C.正极Pt,负极Fe,电解质溶液Fe (SO )
D.正极Ag,负极Fe,电解质溶液CuSO
第六章化学反应与能量
第一节 化学反应与能量变化 第2课时化学反应与电能
【学习目标与核心素养】
学习目标
1.通过实验探究认识化学能与电能之间转化的实质。
2.理解原电池的概念及工作原理和构成条件。
3. 能正确书写简单化学电源的电极反应式。
核心素养
1.科学探究:认识构成原电池的条件及其原理,判断原电池的正负极。 2.创新意识:利用原电池原理能设计原电池。
3.宏观辨识与微观探析:会分析物质化学变化中的能量变化与物质微观结
构的关系。
电力改变了我们的生活那么,电是怎么来的呢
核电3%
7图6-52015年我国电力生产量构成图
火电74%
水电19%
发电
电
其他1% 风电3%
电的来源
燃烧煤 所产生 的气体
烟囱
静电沉淀器
煤堆
-电缆塔
变压器
(冷水使蒸汽转化成水)
运煤船
冷水
在
蒸汽驱动
涡轮机
发电机
涡轮机(生产电力)
火力发电的原理
煤粉来自沉淀器的灰尘
锅炉
电缆
(3)化学反应中是否都有电子的转移 氧化还原反应中有电子的移动
(4)如何实现氧化还原反应中的电子定向移动呢
学生活动1:
(1)阅读教材P36, 说一说火力发电中的能量变化
直 接
带电粒子(电子等)的定向移动
(2)电流是如何产生的额
发电机
机械能
化学能
电能
蒸汽
燃烧
热能
实验探究
【实验6-3】
(1)将锌片和铜片插入盛有稀硫酸的烧杯中,观察现象。
(2)用导线连接锌片和铜片,观察、比较导线连接前后的现象。
(3)如图所示,用导线在锌片和铜片之间串联一个电流表,观察电流表的
指针是否偏转。
序号 实验步骤 实验装置 现象
结论或解释
I 将锌片、铜片插入 盛稀硫酸的烧杯中, 观察现象。 Zn Cu 稀 H S O 锌片表面有气 泡 ,铜片表面 没有气泡
Zn+2H+=Zn ++H 个 铜与稀硫酸不反应
Ⅱ 用导线连接锌片和铜 片,观察、比较导线 连接前后的现象 锌片、铜片表 面都有气泡
锌失去电子,经导线 流向铜片,H+在铜片 上得到电子还原成H
Ⅲ 用导线在锌片和铜片 间串联一个电流表G, 观察电流表指针是否 偏转。 铜片(锌片) 上有气泡,电 流计指针偏转
有电流产生,说明物 质在发生化学反应的 同时产生了电流,即 化学能转化为电能
实验结论: 实验Ⅱ和Ⅲ中产生了电流
实验探究
电子经导线流向Cu片 ,
溶液中的H+由于电场作用下 移向Cu片得电子被还原成H 。
铜片:2H++2e-=H 个
(还原反应)
锌 片 :Zn-2e-=Zn +
(氧化反应)
Zn 比 Cu活泼,用导线 连在一起时,Zn 片失去的电 子变成Zn +进入溶液。
一、原电池
1.定义:将化学能直接转变成电能的装置,称为原电池
2.本质:氧化反应和还原反应分别在两个不同的区域进行,使电子发 生定向移动,从而产生了电流。
3.正负极:
负 极 : 电子流出(或电流流进)的一极
正 极 : 电子流进(或电流流出)的一极
电极材料 原电池正负极 电极反应式
发生的反应
Zn片 负极 Zn-2e-=Zn2+
氧化反应
Cu片 正极 2H++2e-=H 个
还原反应
电极总离子反应 Zn+2H+=Zn ++H 个(两个电极反应之和) 小结:
负极 正极 失去电子的一极 得到电子的一极 氧化反应 还原反应
活性强
活性弱
锌 -A-
s話
_
4.电极反应:
e- 铜
外电路: 负极 今 正 极 正极 负极
内电路: 阳离子向正极移动 阴离子向负极移动
这样整个电路构成了闭合回路,带电粒子的定向移动产生电流
电极反应类型:
氧化反应
电极反应式:
Zn-2e-=Zn 2+
原电池总反应式:
电极反应类型:还原反应
电极反应式:
2H++2e-=H
5.工作原理:
电极名称:负 极
e-
铜
电极名称:正极
Zn+2H+==Zn ++H 个
H
H+
SO2-Ht
e-
锌
A-
SO2-
①自发的氧化还原反应均可构成原电池
②具有活动性不同的两个电极(金属与金属或金属与能导电的非金属);
③溶液:两电极均插入电解质溶液中;
④导线:两极用导线相连,形成闭合回路。
电解质溶液的作用:传 导离子、参与电极反应
学生活动2:根据原电池的工作原理,讨论形成原电池的条件有哪些
构成条件:
稀疏酸 稀硫酸 稀硫酸
⑤
C.①②③④
课堂练习:下列装置能形成原电池的是( )
CuSO溶 液
②
稀硫酸
③
稀硫酸
①
稀盐酸 ⑦
D.①②③⑥⑦
酒精 ⑥
B.①②⑤⑥
学生活动4: 阅读优化设计P44方法突破,并完成【例 题 1】、【 变 式设
问】、【针对训练1】
较不活泼金属或 能导电的非金属
还原反应
电子流入
电极增重或 有气体产生
阳离子移向
较活泼金属
氧化反应
电子流出
不断溶解 质量减小
阴离子移向
电极材料
反应类型
电子流向
电极现象
离子移向
Zn Cu
H SO
电解质溶液
e-沿导线传递,有电流产生
A
学生活动3:如何判断原电池正负极
阳离子移向
不断溶解
正极
负极
【课堂练习】1.右图是Zn 和Cu形成的原电池,某实验兴趣小组做完实验
后,记录如下:
①Zn 为 正 极 ,Cu 为负极
②H+ 向负极移动
③电子流动方向,从Zn 经外电路流向Cu④Cu 极_
⑤若有1mol 电子流过导线,则产生0.5 molH ⑥ 正极的电极反应式为 Zn -2e-==Zn +。
B
描述合理的是( )
B.③④⑤ D.②③④
H SO
CuSO (aq)
负 极(Zn ):Zn -2e=Zn +. 正极(Cu):Cu ++2e-=Cu.
总反应式:Zn +Cu += Zn +Cu.
H SO (aq)
负极(Fe ):Fe -2e-=Fe +.
正极(Ag):2H++2e-=H 个.
总反应式:Fe+2H+=Fe ++H 个
【课堂练习】2.请在图上标出电子的流动方向和电流方向,并判断正负
极,写出电极反应式和总反应式。
学生活动5:阅读优化设计P45-46方法突破,并完成【例题2】【针对训练2】
1.加快反应速率
实验室制H 时,由于锌太纯,反应一般较慢,可加入少量CuSO 以加快反应速率或使用粗锌。
2.比较金属活动性的强弱
一般负极金属活泼性大于正极金属
3.用于金属的防护
原理:使被保护的金属制品作原电池的正极而得到保护。
实例:用导线将铁阀门与锌片相连以保护铁制阀门
4.原电池的设计
(1)找:找一个能够自发进行的氧化还原反应,只有自发进行的氧化还 原反应才能被设计成原电池。
(2)拆:将氧化还原反应拆分为氧化反应和还原反应两个半反应,分别 作为负极和正极的电极反应。
还原剂一ne-= 氧化产物(负极电极反应)
氧化剂十ne-= 还原产物(正极电极反应)
(3)定:根据氧化还原反应中的还原剂和氧化剂确定原电池的负极和电 解质溶液,正极一般选择比负极活泼性差的金属或能导电的非金属。
(4)画:连接电路,形成闭合回路,画出原电池示意图。
A B C
D
正极 Zn Cu Cu
Fe
负极 Cu Zn Zn
Zn
电解质溶液 CuCl H SO CuSO
HCI
于此装置的下列叙述中,不正确的是(D
A.N上有气体放出
B.M为负极,N 为正极
C.稀硫酸中S0 2-移向M极
D.导线中有电流通过,电流方向是由M到N
【课堂练习】3.一个电池反应的离子方程式是 Zn+Cu +==Zn ++Cu,该反 应的的原电池正确组合是( C )
4.如图所示的装置,M为活动性顺序位于氢之前的金属,N为石墨棒,关
稀硫酸
)
5.如图所示,电流计指针发生偏转,同时A极质量减少,B 极上有气
泡产生,C 为电解质溶液,下列说法错误的是( C )
A.B极为原电池的正极
B.A、B、C可能分别为Zn、Cu、稀盐酸
C.C中阳离子向A极移动
D.A极发生氧化反应
6.某原电池2Fe ++Fe==3Fe +不能实现该反应的原电池是( D )
A.正极Cu,负极Fe,电解质溶液FeCl
B.正极C,负极Fe,电解质溶液Fe(NO )
C.正极Pt,负极Fe,电解质溶液Fe (SO )
D.正极Ag,负极Fe,电解质溶液CuSO
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
