烯烃(教学课件)-高中化学人教版(2019)选择性必修三(共45张PPT)
文档属性
| 名称 | 烯烃(教学课件)-高中化学人教版(2019)选择性必修三(共45张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-25 00:00:00 | ||
图片预览







文档简介
(共45张PPT)
第二章第二节
烯烃、炔烃
一、烷烃的结构和性质
二、烷烃的命名
第二章第二节
第一课时 烯烃
一、烯烃的结构
二、烯烃的命名
三、烯烃的性质
>它能使溴的四氯化碳溶液褪色;
>它的产量可以用来衡量一个国家石油化学工业的发展水平;
>1 mol该物质完全燃烧生成2 mol CO 和2 mol H O,它的实验式是CH 。
它能用排水法收集;
猜猜它是谁
>它能使酸性高锰酸钾溶液褪色;
乙烯的球棍模型 乙烯的空间填充模型
新课导入
66
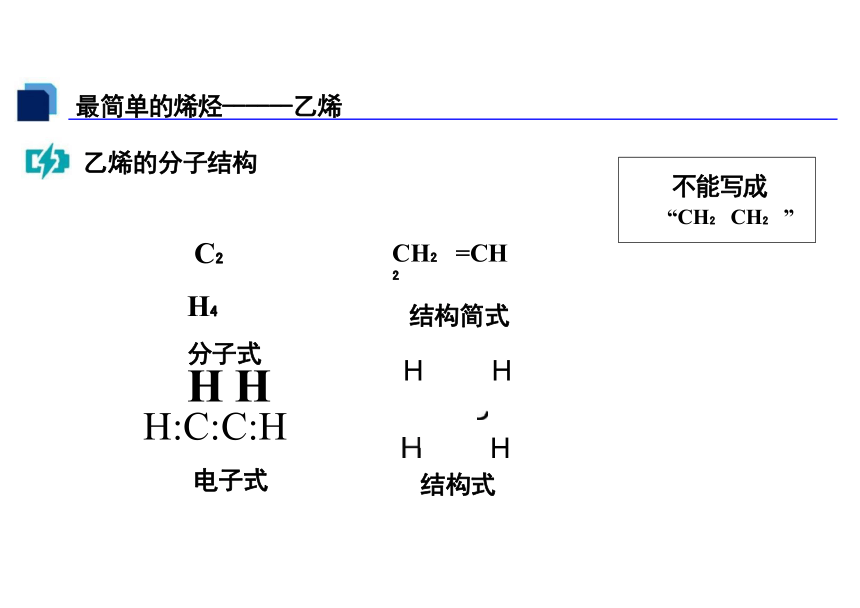
最简单的烯烃------乙烯
乙烯的分子结构
C H 分子式
H H
H:C:C:H
电子式
不能写成
“CH CH ”
H H
H
结构式
CH =CH
结构简式
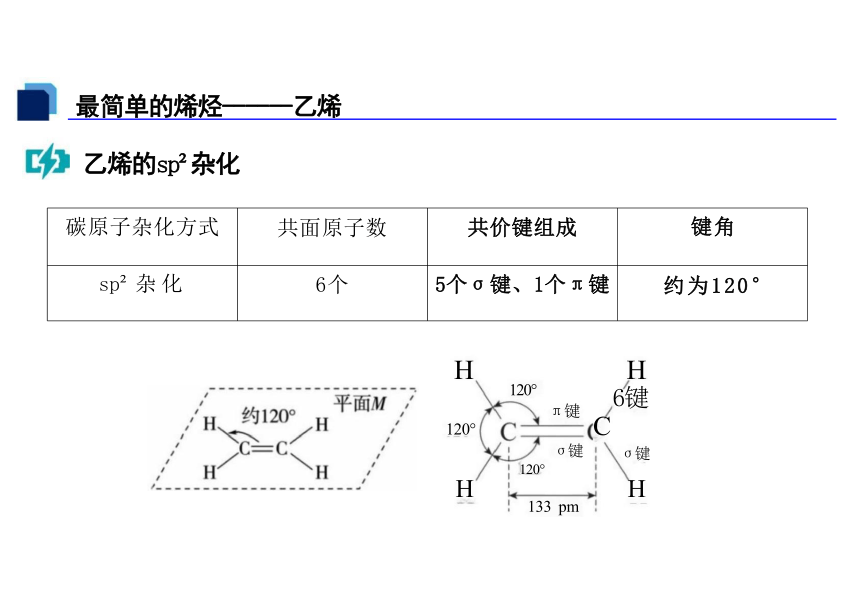
碳原子杂化方式 共面原子数 共价键组成
键角
sp 杂化 6个 5个σ键、1个π键
约为120°
最简单的烯烃------乙烯
乙烯的sp 杂化
H H
120° π键 6键 120° C
σ键 σ键
120°
H H
133 pm
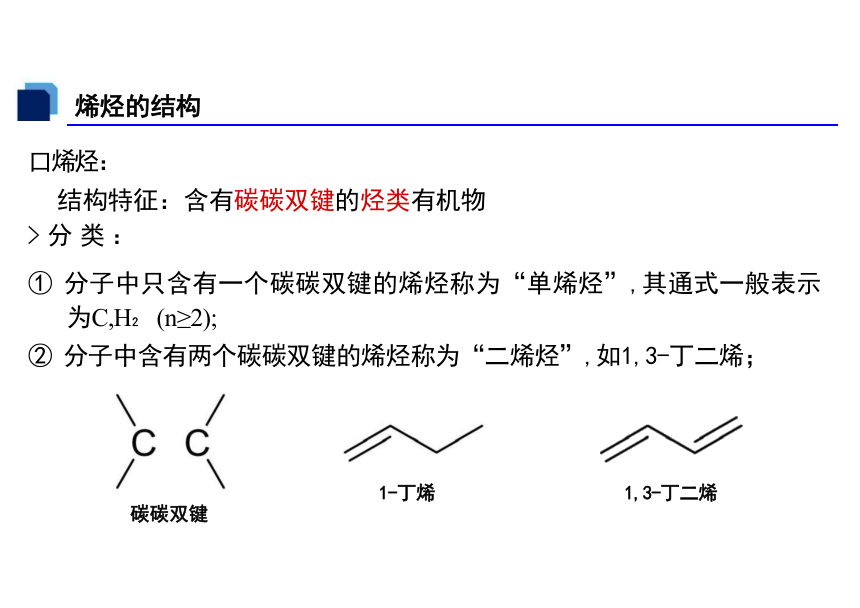
口烯烃:
结构特征:含有碳碳双键的烃类有机物
> 分 类 :
① 分子中只含有一个碳碳双键的烯烃称为“单烯烃”,其通式一般表示 为C,H (n≥2);
② 分子中含有两个碳碳双键的烯烃称为“二烯烃”,如1,3-丁二烯;
烯烃的结构
1-丁烯 1,3-丁二烯
碳碳双键
口讨论二:烯烃一定符合C H n通式吗 通式满足C,H n一定是烯烃吗 请写
出满足单烯烃结构特征,但通式不为C,H n的烯烃;
口讨论一:你是如何辨识陌生有机物是否为烯烃
烃类中含有“碳碳双键”,一根是σ键,一根是π键
环烯烃的通式 不符合C,H
环烷烃的通式
也是C,H2n
烯烃的结构
1,3-环己二烯
蒽
萘
菲
芘
烯烃的结构
口讨论三:判断丙烯(CH -CH=CH ) 分子中碳原子的杂化方式,分子中所有原 子都在同一平面上吗
口讨论四:右图结构中最少多少个原子共面 最多呢
双键碳原子均采取sp 杂化,至少6个原子共面, 最多8个原子共面!
碳原子杂化方式:sp 和sp 杂化;由于存在sp 杂化 的碳原子,所有原子不可能在同一平面上!
H
C
H C
CH 3
C
H
H
C
H
H
H
H H
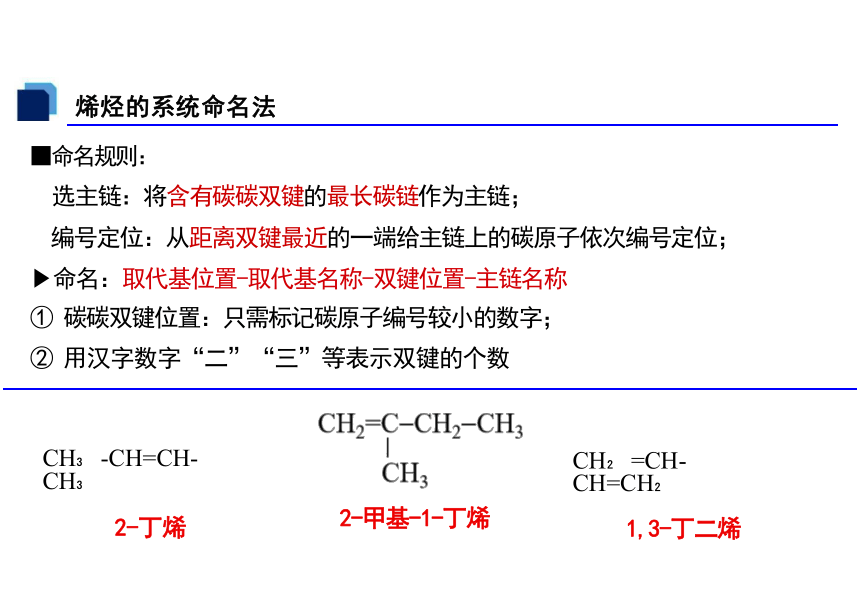
■命名规则:
选主链:将含有碳碳双键的最长碳链作为主链;
编号定位:从距离双键最近的一端给主链上的碳原子依次编号定位;
命名:取代基位置-取代基名称-双键位置-主链名称
① 碳碳双键位置:只需标记碳原子编号较小的数字;
② 用汉字数字“二”“三”等表示双键的个数
CH =CH-CH=CH
1,3-丁二烯
CH -CH=CH-CH
2-丁烯
烯烃的系统命名法
2-甲基-1-丁烯
烷烃与烯烃选主链的差异:
■烷烃:选定分子中最长的碳链作为主链;
■烯烃:将含有双键的最长碳原子作为主链;
3-甲基戊烷 2-乙基-1-丁烯
烯烃的系统命名法
烷烃与烯烃编号定位的差异:
■烷烃:从距离取代基最近的一端给主链上的碳原子编号定位;;
■烯烃:距离碳碳双键最近的一端开始编号;
2-甲基丁烷 3-甲基-1-丁烯
烯烃的系统命名法
【注意一】编号定位时,如果两端离碳碳双键的距离相同,则从离取代基较近 的一端开始编号;
【注意二】用阿拉伯数字表明碳碳双键的位置,用汉字数字表示碳碳双键的数
目(只有1个碳碳双键时不需要注明);
烯烃的系统命名法
2,4-二甲基-2,4-己二烯
2-甲基-3-己烯
【例2】判断下列命名是否正确
(1)2-丙烯;(2)2-乙基丙烯;(3)2-乙基-1-丁烯
1-丙烯 2-甲基-1-丁烯
【例1】用系统命名法给下列烯烃命名:
CH -CH=C-CH -(
CH
CH
烯烃的系统命名法
3-乙基-2-己烯
CH
2
名称 结构简式 沸点
相对密度
乙烯 CH =CH -103.7
0.566
丙烯 CH =CHCH -47.4
0.5193
1-丁烯 CH =CHCH CH -6.3
0.5951
1-戊烯 CH =CH(CH ) CH 30
0.6405
1-己烯 CH =CH(CH ) CH 63.3
0.6731
1-庚烯 CH =CH(CH ) CH 93.6
0.6970
口讨论五:结合单烯烃的结构简式及沸点、相对密度数据,并类比烷烃的物理
性质,分析烯烃的物理性质具有哪些递变性规律
烯烃的物理性质
溶解性:都难溶于水,可溶于苯等有机溶剂;
密度:随碳原子个数递增而增大,但都小于水;
沸点:随碳原子个数递增而增大,常温下碳数≤4的烯烃为气 态;
>甲烷为无色无味的气体,而乙烯是一种无色、稍有气味的气体!
烯烃的物理性质
口讨论五:结合单烯烃的结构简式及沸点、相对密度数据,并类比烷烃的物理 性质,分析烯烃的物理性质具有哪些递变性规律
相同点
差异性
烯烃的物理性质
天然的水果催熟剂:乙烯
乙烯广泛存在于植物的各种组织、器官中,是由蛋氨酸在供养充足的条件 下转化而成的。乙烯可以促进RNA 和蛋白质的合成,在高等植物体内,并使 细胞膜的透性增加,加速呼吸作用。 长途运输水果,为什么会在水果旁边喷 有高锰酸钾的硅藻土
乙烯是水果的催熟剂,乙烯与高锰酸钾发生氧 化还原反应,则利用KMnO 溶液除去乙烯,可 使水果缓慢成熟,以赢得长途运输时间!
乙烯催熟剂
不可食用
Ethylene ripener
Don'teat.
乙烯催熟剂 不可食用
Ethylene rpener
Don'teat
化学键
键能/(kJ ·mol- )
C-C
347.7
C=C
615
碳碳双键的π键键能小 于σ键,属于反应活性 部位!
烯烃的化学性质
结构
口易氧化
口能加成 口能加聚
120°
π键
σ键 120°
133 pm
性质
H
120°
H
H o键
σ键 H
决定
■氧化反应:
单烯烃在氧气中完全燃烧的通式:
烯烃可使酸性高锰酸钾溶液褪色,该反应常用于烯烃的检验!
烯烃的化学性质
乙烯与酸性高锰酸钾溶液的反应
酸性
KMnO 溶液
通入
乙烯
烯烃被氧化的部分 CH = RCH=
氧化产物 CO 、H O O R C OH
O
R1 C R 2
烯烃的化学性质
烯烃与酸性KMnO 溶液的反应规律
用酸性高锰酸钾溶液氧化碳碳双键可以缩短碳链!
【例3】烯烃被KMnO 氧化:已知某些烯烃被酸性高锰酸钾溶液氧化可生 成羧酸和酮,例如:
分子式为C H 0的某烯烃被酸性高锰酸钾溶液氧化后,生成正丁酸 (CH CH CH COOH) 和3-己酮(CH CH COCH CH CH )。 推测该烯烃的结 构简式。
烯烃的化学性质
烯烃的化学性质
■加成反应:
烯烃与溴水、溴的四氯化碳溶液反应属于无条件加成;与卤化氢、水、
氢气的加成属于有条件加成!
>与水:
>与卤素单质:CH =CH +Br — →BrCH CH Br
66
常用于烯烃的检验!
口讨论六:写出丙烯与下列物质反应的化学方程式,并说明反应中官能团和
化学键的变化。(提示:丙烯与HC1、丙烯与水的反应都可能有两种产物。)
OH
正丙醇
Br
Br
Cl
2-氯丙烷
CI
1-氯丙烷
烯烃的化学性质
secondary
Bi
mainly
secondary
H O cat./heat 异丙醇
1,2-二溴丙烷
cat./heat
mainly
+ HCI
OH
反马氏规则:在光照或过氧化物存在下,氢原子主要加在连
有较少氢原子的双键碳原子上。 δ
CH - CH— CH
甲基的推电子作用示意图
CH -8H=δH,+H-&—→CH - H-CH
2-氯丙烷
C
Cl
不对称烯烃与含氢化合物(HX、H O 等)发生加成反应时,氢
原子主要加到连有较多氢原子的双键碳原子上。
烯烃的化学性质
马氏规则
马尔科夫尼科夫 (1837年-1904年)
烯烃的化学性质
■ 加成聚合(加聚)反应:
加聚反应是获得高分子材料的重要途径之一,人们日常生活中经常接触到的 聚乙烯、聚氯乙烯、聚苯乙烯、ABS 工程塑料、顺丁橡胶等材料,以及一些重 要新型材料如导电高聚物等都是通过加聚反应得到的。
聚乙烯塑料
合成橡胶
■ 加成聚合(加聚)反应:
催化剂
nCH =CH
单体
烯烃的化学性质
聚合度
[CH —
聚乙烯
链节
CH
1
2 n
口讨论七:含有碳碳双键官能团的有机物在一定条件下能发生类似乙烯的加
聚反应。请根据乙烯发生的加聚反应,分别写出氯乙烯、丙烯、异丁烯发 生加聚反应的化学方程式。
烯烃的化学性质
异丁烯 聚异丁烯(PIB)
氯乙烯 聚氯乙烯(PVC)
丙烯 聚 内 烯(PP)
【例4】反应类型的判断:以下反应属于哪一类反应 加成反应
R cat. S
R SH 十 R R
*取代反应: 在一定条件下,烯烃分子中饱和碳原子上的C-H 键可 发生断裂,与卤素单质发生取代反应。
l2 十 HCI
烯烃的化学性质
500-600°C CI
口讨论九:要除去乙烷中的乙烯,应选择何种试剂
酸性高锰酸钾溶液 浓溴水
氢气 稀溴水
溴的四氯化碳溶液
口讨论八:如何鉴别乙烷和乙烯
酸性高锰酸钾溶液、溴水或溴的四氯化碳溶液!
氧化褪色
加成褪色
烯烃的化学性质
烯烃的化学性质
口讨论八:如何鉴别乙烷和乙烯
酸性高锰酸钾溶液、溴水或溴的四氯化碳溶液!
口讨论九:要除去乙烷中的乙烯,应选择何种试剂
酸性高锰酸钾溶液(引入CO ) 浓溴水(挥发出Br ) 氢气(无法保证用量) >稀溴水
溴的四氯化碳溶液(会溶解乙烷)
氧化褪色
加成褪色
—→
乙烷
(乙烯)
→
乙烷
口产生原因:形成双键的两个碳原子不能绕键轴旋转,导致与它们相连的原子
或原子团的空间排列方式不同,产生异构现象;
口存在条件:
①有阻碍碳碳键旋转的双键;
②碳碳双键两端连接的原子或原子团不同;
【例5】判断以下有机物是否互为同分异构体 ① Br H CI H ② Br CI Br C C CI H Br H H H H
H
CI
二者为同一种物质 二者互为顺反异构体
烯烃的立体异构
1-丁烯
立体异构
H
顺-2-丁烯
H
CH 反-2-丁烯
口讨论十:丁烯有几种链状的同分异构体
烯烃的立体异构
构造异构
H C
H
2-甲基丙烯
2-丁烯
CH
H
H
口顺式结构:相同的原子或原子团位于双键的同一侧;
口反式结构:相同的原子或原子团位于双键的两侧;
口二者联系:化学性质基本相同,物理性质有一定的差异;
H3 CH 3 H C
H
结构 顺-2-丁烯
反-2-丁烯
熔点/(℃) -138.9
-105.5
沸点/(℃) 3.7
0.9
密度/(g ·cm-3) 0.621
0.604
烯烃的立体异构
H
CH3
【 例 5 】顺反异构的判断:以下物质是否存在顺反异构
①CH CH CH ;× ②CH =CH ; ×
③CH =CH-CH ; × ④CH -CH=CH-CH √
【 例 6 】烯烃的同分异构:有机物A分子式为C H10,与丙烯互为同系物, 则有机物A的结构有多少种(含顺反异构) 6种
烯烃的立体异构
第二章第二节 第二课时二烯烃
一、二烯烃加成
二、二烯烃加聚
三、二烯烃成环
烯烃被氧化的部分 CH = RCH=
氧化产物 CO 、H O O R C OH
O
R R2
烯烃的氧化
烯烃与酸性KMnO 溶液的反应规律
【例1】已知某种烯烃经臭氧氧化后,在Zn存在下水解,可得到醛和酮。 现有分子式为C H 4的某烯烃,它与H 加成后生成2,3-二甲基戊烷,它经 臭氧氧化后,在锌存在下水解得到乙醛和一种酮,据此推知该烯烃的结 构简式为( C )
A. B. )
烯烃的氧化
3,4-二溴-1-丁烯
1,2,3,4-四溴丁烷
口讨论一:1,3-丁二烯(CH =CH-CH=CH )与Br 的加成产物可能有几种
1,4-加成
全加成
二烯烃的加成
1,2-加成
【例2】如下有机物与等物质的量的溴发生加成反应,其加成产物中二溴
代物有( D )种(考虑顺反异构) A.1 种 B.2 种 C.3 种 D.4 种
二烯烃的加成
口讨论二:1,4-戊二烯(CH =CH-CH -CH=CH ) 与Br 的加成产物可能有几种
1,2-加成
二烯烃的加成
全加成
二烯烃的加成
口讨论三:一分子该物质与两分子溴发生加成反应的产物(不考虑顺反异构), 理论上最多有多少种
共四种:
①②③④;①②⑤⑥;
③④⑤⑥;①④⑤⑥;
【例3】某烃的结构如下图所示,则该烃与Br2加成时(物质的量之比为1:
1)所得产物有( C )种(不考虑立体异构)。
A.3 种
B.4 种
C.5 种
D.6 种
二烯烃的加成
二烯烃加聚时,断π键,成新键(双变单,单变双)!
口若加聚产物中出现了双键,则单体可能有共轭二烯烃或炔烃:
口若加聚产物中都是单键,则单体都是单烯烃(或卤代单烯烃):
二烯烃的加聚
两端半键反着放,双变单,单变双,超过四键就分家!
口讨论四:根据下列聚合物的结构,写出相应单体的结构!
二烯烃的加聚
CH
口第尔斯- 阿尔德反应(Diels-Alder reaction,D-A反应):
共轭二烯烃(含有两个碳碳双键,且两个双键被一个单键隔开的烯烃)与含碳 碳双键(或碳碳三键)的化合物在一定条件下反应,得到环加成产物,构建了 环状碳骨架;
反应规律:双键或三键加成1,4位上的碳原子,同时拆开π键
一定条件
一定条件
二烯烃的成环
十
十
口讨论五:根据第尔斯-阿尔德反应规律,写出下列反应的产物。
一定条件
一定条件
二烯烃的成环
一定条件 H COOC
COOCH
十
第二章第二节
烯烃、炔烃
一、烷烃的结构和性质
二、烷烃的命名
第二章第二节
第一课时 烯烃
一、烯烃的结构
二、烯烃的命名
三、烯烃的性质
>它能使溴的四氯化碳溶液褪色;
>它的产量可以用来衡量一个国家石油化学工业的发展水平;
>1 mol该物质完全燃烧生成2 mol CO 和2 mol H O,它的实验式是CH 。
它能用排水法收集;
猜猜它是谁
>它能使酸性高锰酸钾溶液褪色;
乙烯的球棍模型 乙烯的空间填充模型
新课导入
66
最简单的烯烃------乙烯
乙烯的分子结构
C H 分子式
H H
H:C:C:H
电子式
不能写成
“CH CH ”
H H
H
结构式
CH =CH
结构简式
碳原子杂化方式 共面原子数 共价键组成
键角
sp 杂化 6个 5个σ键、1个π键
约为120°
最简单的烯烃------乙烯
乙烯的sp 杂化
H H
120° π键 6键 120° C
σ键 σ键
120°
H H
133 pm
口烯烃:
结构特征:含有碳碳双键的烃类有机物
> 分 类 :
① 分子中只含有一个碳碳双键的烯烃称为“单烯烃”,其通式一般表示 为C,H (n≥2);
② 分子中含有两个碳碳双键的烯烃称为“二烯烃”,如1,3-丁二烯;
烯烃的结构
1-丁烯 1,3-丁二烯
碳碳双键
口讨论二:烯烃一定符合C H n通式吗 通式满足C,H n一定是烯烃吗 请写
出满足单烯烃结构特征,但通式不为C,H n的烯烃;
口讨论一:你是如何辨识陌生有机物是否为烯烃
烃类中含有“碳碳双键”,一根是σ键,一根是π键
环烯烃的通式 不符合C,H
环烷烃的通式
也是C,H2n
烯烃的结构
1,3-环己二烯
蒽
萘
菲
芘
烯烃的结构
口讨论三:判断丙烯(CH -CH=CH ) 分子中碳原子的杂化方式,分子中所有原 子都在同一平面上吗
口讨论四:右图结构中最少多少个原子共面 最多呢
双键碳原子均采取sp 杂化,至少6个原子共面, 最多8个原子共面!
碳原子杂化方式:sp 和sp 杂化;由于存在sp 杂化 的碳原子,所有原子不可能在同一平面上!
H
C
H C
CH 3
C
H
H
C
H
H
H
H H
■命名规则:
选主链:将含有碳碳双键的最长碳链作为主链;
编号定位:从距离双键最近的一端给主链上的碳原子依次编号定位;
命名:取代基位置-取代基名称-双键位置-主链名称
① 碳碳双键位置:只需标记碳原子编号较小的数字;
② 用汉字数字“二”“三”等表示双键的个数
CH =CH-CH=CH
1,3-丁二烯
CH -CH=CH-CH
2-丁烯
烯烃的系统命名法
2-甲基-1-丁烯
烷烃与烯烃选主链的差异:
■烷烃:选定分子中最长的碳链作为主链;
■烯烃:将含有双键的最长碳原子作为主链;
3-甲基戊烷 2-乙基-1-丁烯
烯烃的系统命名法
烷烃与烯烃编号定位的差异:
■烷烃:从距离取代基最近的一端给主链上的碳原子编号定位;;
■烯烃:距离碳碳双键最近的一端开始编号;
2-甲基丁烷 3-甲基-1-丁烯
烯烃的系统命名法
【注意一】编号定位时,如果两端离碳碳双键的距离相同,则从离取代基较近 的一端开始编号;
【注意二】用阿拉伯数字表明碳碳双键的位置,用汉字数字表示碳碳双键的数
目(只有1个碳碳双键时不需要注明);
烯烃的系统命名法
2,4-二甲基-2,4-己二烯
2-甲基-3-己烯
【例2】判断下列命名是否正确
(1)2-丙烯;(2)2-乙基丙烯;(3)2-乙基-1-丁烯
1-丙烯 2-甲基-1-丁烯
【例1】用系统命名法给下列烯烃命名:
CH -CH=C-CH -(
CH
CH
烯烃的系统命名法
3-乙基-2-己烯
CH
2
名称 结构简式 沸点
相对密度
乙烯 CH =CH -103.7
0.566
丙烯 CH =CHCH -47.4
0.5193
1-丁烯 CH =CHCH CH -6.3
0.5951
1-戊烯 CH =CH(CH ) CH 30
0.6405
1-己烯 CH =CH(CH ) CH 63.3
0.6731
1-庚烯 CH =CH(CH ) CH 93.6
0.6970
口讨论五:结合单烯烃的结构简式及沸点、相对密度数据,并类比烷烃的物理
性质,分析烯烃的物理性质具有哪些递变性规律
烯烃的物理性质
溶解性:都难溶于水,可溶于苯等有机溶剂;
密度:随碳原子个数递增而增大,但都小于水;
沸点:随碳原子个数递增而增大,常温下碳数≤4的烯烃为气 态;
>甲烷为无色无味的气体,而乙烯是一种无色、稍有气味的气体!
烯烃的物理性质
口讨论五:结合单烯烃的结构简式及沸点、相对密度数据,并类比烷烃的物理 性质,分析烯烃的物理性质具有哪些递变性规律
相同点
差异性
烯烃的物理性质
天然的水果催熟剂:乙烯
乙烯广泛存在于植物的各种组织、器官中,是由蛋氨酸在供养充足的条件 下转化而成的。乙烯可以促进RNA 和蛋白质的合成,在高等植物体内,并使 细胞膜的透性增加,加速呼吸作用。 长途运输水果,为什么会在水果旁边喷 有高锰酸钾的硅藻土
乙烯是水果的催熟剂,乙烯与高锰酸钾发生氧 化还原反应,则利用KMnO 溶液除去乙烯,可 使水果缓慢成熟,以赢得长途运输时间!
乙烯催熟剂
不可食用
Ethylene ripener
Don'teat.
乙烯催熟剂 不可食用
Ethylene rpener
Don'teat
化学键
键能/(kJ ·mol- )
C-C
347.7
C=C
615
碳碳双键的π键键能小 于σ键,属于反应活性 部位!
烯烃的化学性质
结构
口易氧化
口能加成 口能加聚
120°
π键
σ键 120°
133 pm
性质
H
120°
H
H o键
σ键 H
决定
■氧化反应:
单烯烃在氧气中完全燃烧的通式:
烯烃可使酸性高锰酸钾溶液褪色,该反应常用于烯烃的检验!
烯烃的化学性质
乙烯与酸性高锰酸钾溶液的反应
酸性
KMnO 溶液
通入
乙烯
烯烃被氧化的部分 CH = RCH=
氧化产物 CO 、H O O R C OH
O
R1 C R 2
烯烃的化学性质
烯烃与酸性KMnO 溶液的反应规律
用酸性高锰酸钾溶液氧化碳碳双键可以缩短碳链!
【例3】烯烃被KMnO 氧化:已知某些烯烃被酸性高锰酸钾溶液氧化可生 成羧酸和酮,例如:
分子式为C H 0的某烯烃被酸性高锰酸钾溶液氧化后,生成正丁酸 (CH CH CH COOH) 和3-己酮(CH CH COCH CH CH )。 推测该烯烃的结 构简式。
烯烃的化学性质
烯烃的化学性质
■加成反应:
烯烃与溴水、溴的四氯化碳溶液反应属于无条件加成;与卤化氢、水、
氢气的加成属于有条件加成!
>与水:
>与卤素单质:CH =CH +Br — →BrCH CH Br
66
常用于烯烃的检验!
口讨论六:写出丙烯与下列物质反应的化学方程式,并说明反应中官能团和
化学键的变化。(提示:丙烯与HC1、丙烯与水的反应都可能有两种产物。)
OH
正丙醇
Br
Br
Cl
2-氯丙烷
CI
1-氯丙烷
烯烃的化学性质
secondary
Bi
mainly
secondary
H O cat./heat 异丙醇
1,2-二溴丙烷
cat./heat
mainly
+ HCI
OH
反马氏规则:在光照或过氧化物存在下,氢原子主要加在连
有较少氢原子的双键碳原子上。 δ
CH - CH— CH
甲基的推电子作用示意图
CH -8H=δH,+H-&—→CH - H-CH
2-氯丙烷
C
Cl
不对称烯烃与含氢化合物(HX、H O 等)发生加成反应时,氢
原子主要加到连有较多氢原子的双键碳原子上。
烯烃的化学性质
马氏规则
马尔科夫尼科夫 (1837年-1904年)
烯烃的化学性质
■ 加成聚合(加聚)反应:
加聚反应是获得高分子材料的重要途径之一,人们日常生活中经常接触到的 聚乙烯、聚氯乙烯、聚苯乙烯、ABS 工程塑料、顺丁橡胶等材料,以及一些重 要新型材料如导电高聚物等都是通过加聚反应得到的。
聚乙烯塑料
合成橡胶
■ 加成聚合(加聚)反应:
催化剂
nCH =CH
单体
烯烃的化学性质
聚合度
[CH —
聚乙烯
链节
CH
1
2 n
口讨论七:含有碳碳双键官能团的有机物在一定条件下能发生类似乙烯的加
聚反应。请根据乙烯发生的加聚反应,分别写出氯乙烯、丙烯、异丁烯发 生加聚反应的化学方程式。
烯烃的化学性质
异丁烯 聚异丁烯(PIB)
氯乙烯 聚氯乙烯(PVC)
丙烯 聚 内 烯(PP)
【例4】反应类型的判断:以下反应属于哪一类反应 加成反应
R cat. S
R SH 十 R R
*取代反应: 在一定条件下,烯烃分子中饱和碳原子上的C-H 键可 发生断裂,与卤素单质发生取代反应。
l2 十 HCI
烯烃的化学性质
500-600°C CI
口讨论九:要除去乙烷中的乙烯,应选择何种试剂
酸性高锰酸钾溶液 浓溴水
氢气 稀溴水
溴的四氯化碳溶液
口讨论八:如何鉴别乙烷和乙烯
酸性高锰酸钾溶液、溴水或溴的四氯化碳溶液!
氧化褪色
加成褪色
烯烃的化学性质
烯烃的化学性质
口讨论八:如何鉴别乙烷和乙烯
酸性高锰酸钾溶液、溴水或溴的四氯化碳溶液!
口讨论九:要除去乙烷中的乙烯,应选择何种试剂
酸性高锰酸钾溶液(引入CO ) 浓溴水(挥发出Br ) 氢气(无法保证用量) >稀溴水
溴的四氯化碳溶液(会溶解乙烷)
氧化褪色
加成褪色
—→
乙烷
(乙烯)
→
乙烷
口产生原因:形成双键的两个碳原子不能绕键轴旋转,导致与它们相连的原子
或原子团的空间排列方式不同,产生异构现象;
口存在条件:
①有阻碍碳碳键旋转的双键;
②碳碳双键两端连接的原子或原子团不同;
【例5】判断以下有机物是否互为同分异构体 ① Br H CI H ② Br CI Br C C CI H Br H H H H
H
CI
二者为同一种物质 二者互为顺反异构体
烯烃的立体异构
1-丁烯
立体异构
H
顺-2-丁烯
H
CH 反-2-丁烯
口讨论十:丁烯有几种链状的同分异构体
烯烃的立体异构
构造异构
H C
H
2-甲基丙烯
2-丁烯
CH
H
H
口顺式结构:相同的原子或原子团位于双键的同一侧;
口反式结构:相同的原子或原子团位于双键的两侧;
口二者联系:化学性质基本相同,物理性质有一定的差异;
H3 CH 3 H C
H
结构 顺-2-丁烯
反-2-丁烯
熔点/(℃) -138.9
-105.5
沸点/(℃) 3.7
0.9
密度/(g ·cm-3) 0.621
0.604
烯烃的立体异构
H
CH3
【 例 5 】顺反异构的判断:以下物质是否存在顺反异构
①CH CH CH ;× ②CH =CH ; ×
③CH =CH-CH ; × ④CH -CH=CH-CH √
【 例 6 】烯烃的同分异构:有机物A分子式为C H10,与丙烯互为同系物, 则有机物A的结构有多少种(含顺反异构) 6种
烯烃的立体异构
第二章第二节 第二课时二烯烃
一、二烯烃加成
二、二烯烃加聚
三、二烯烃成环
烯烃被氧化的部分 CH = RCH=
氧化产物 CO 、H O O R C OH
O
R R2
烯烃的氧化
烯烃与酸性KMnO 溶液的反应规律
【例1】已知某种烯烃经臭氧氧化后,在Zn存在下水解,可得到醛和酮。 现有分子式为C H 4的某烯烃,它与H 加成后生成2,3-二甲基戊烷,它经 臭氧氧化后,在锌存在下水解得到乙醛和一种酮,据此推知该烯烃的结 构简式为( C )
A. B. )
烯烃的氧化
3,4-二溴-1-丁烯
1,2,3,4-四溴丁烷
口讨论一:1,3-丁二烯(CH =CH-CH=CH )与Br 的加成产物可能有几种
1,4-加成
全加成
二烯烃的加成
1,2-加成
【例2】如下有机物与等物质的量的溴发生加成反应,其加成产物中二溴
代物有( D )种(考虑顺反异构) A.1 种 B.2 种 C.3 种 D.4 种
二烯烃的加成
口讨论二:1,4-戊二烯(CH =CH-CH -CH=CH ) 与Br 的加成产物可能有几种
1,2-加成
二烯烃的加成
全加成
二烯烃的加成
口讨论三:一分子该物质与两分子溴发生加成反应的产物(不考虑顺反异构), 理论上最多有多少种
共四种:
①②③④;①②⑤⑥;
③④⑤⑥;①④⑤⑥;
【例3】某烃的结构如下图所示,则该烃与Br2加成时(物质的量之比为1:
1)所得产物有( C )种(不考虑立体异构)。
A.3 种
B.4 种
C.5 种
D.6 种
二烯烃的加成
二烯烃加聚时,断π键,成新键(双变单,单变双)!
口若加聚产物中出现了双键,则单体可能有共轭二烯烃或炔烃:
口若加聚产物中都是单键,则单体都是单烯烃(或卤代单烯烃):
二烯烃的加聚
两端半键反着放,双变单,单变双,超过四键就分家!
口讨论四:根据下列聚合物的结构,写出相应单体的结构!
二烯烃的加聚
CH
口第尔斯- 阿尔德反应(Diels-Alder reaction,D-A反应):
共轭二烯烃(含有两个碳碳双键,且两个双键被一个单键隔开的烯烃)与含碳 碳双键(或碳碳三键)的化合物在一定条件下反应,得到环加成产物,构建了 环状碳骨架;
反应规律:双键或三键加成1,4位上的碳原子,同时拆开π键
一定条件
一定条件
二烯烃的成环
十
十
口讨论五:根据第尔斯-阿尔德反应规律,写出下列反应的产物。
一定条件
一定条件
二烯烃的成环
一定条件 H COOC
COOCH
十
