糖类 (教学课件) 高中化学人教版(2019)选修三(共48张PPT)
文档属性
| 名称 | 糖类 (教学课件) 高中化学人教版(2019)选修三(共48张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-28 00:00:00 | ||
图片预览








文档简介
(共48张PPT)
第四章生物大分子
第一节 糖类
课时一糖类的组成和性质
01.从糖类的官能团微观探析糖类的结构
特点,了解糖类的分类,理解糖类的化学
性质,掌握糖类的特殊性
02.了解糖类在人体供能、储能等方面的 作用,了解糖类的摄入和代谢与人体健康
之间的关系,科学合理地搭配饮食。
学习
目标
们生活中的面粉,看到的棉花、小草、树皮中也含有大量的糖, 那么这些糖的成分一样吗 它们又有什么样的区别
说起糖,大家恐怕都不会陌生,其实除了我们吃的这些糖,我
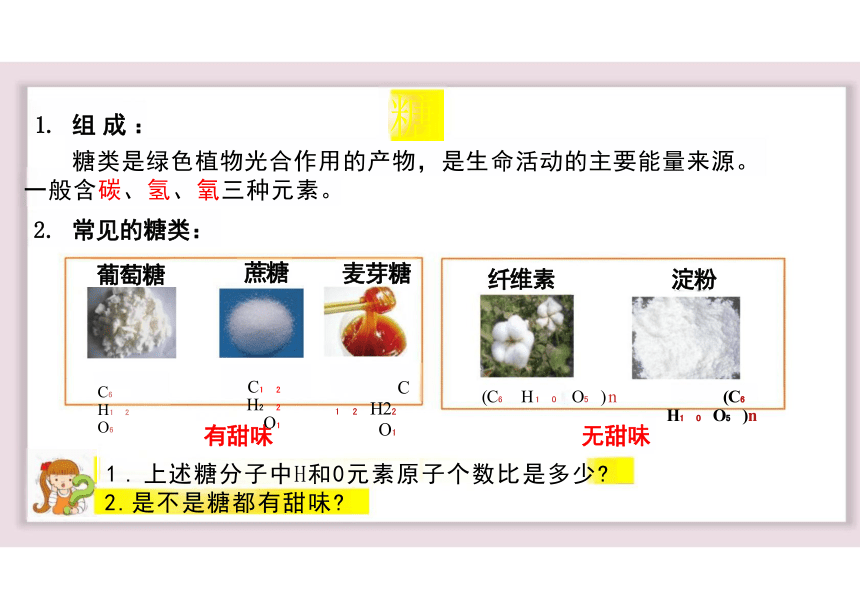
1. 组 成 : 糖
糖类是绿色植物光合作用的产物,是生命活动的主要能量来源。 一般含碳、氢、氧三种元素。
有甜味 无甜味
1 . 上述糖分子中H和0元素原子个数比是多少 2.是不是糖都有甜味
纤维素 淀粉
(C H O ) n (C H O )n
2. 常见的糖类:
麦芽糖
葡萄糖
C H2 O
蔗糖
C H O
C H O
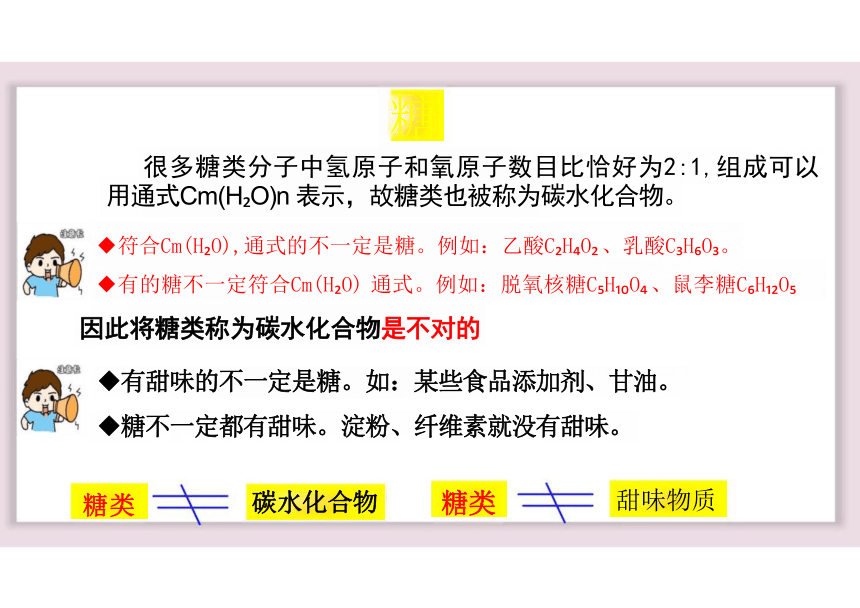
很多糖类分子中氢原子和氧原子数目比恰好为2:1,组成可以 用通式Cm(H O)n 表示,故糖类也被称为碳水化合物。
◆符合Cm(H O),通式的不一定是糖。例如:乙酸C H O 、乳酸C H O 。
◆有的糖不一定符合Cm(H O) 通式。例如:脱氧核糖C H O 、鼠李糖C H O
因此将糖类称为碳水化合物是不对的
◆有甜味的不一定是糖。如:某些食品添加剂、甘油。
◆糖不一定都有甜味。淀粉、纤维素就没有甜味。
甜味物质
碳水化合物
糖
糖类
糖类
单糖 寡糖(低聚糖)
多糖
概念 不能 水解的糖 1 mol糖水解后能产生 2~10_mol单糖的糖
1 mol糖水解后能产 生10 mol以上单糖的 糖
代表物 葡萄糖、果糖 蔗糖、麦芽糖
纤维素、_ 淀粉
分子式 C H 2O
(C H 0O )n
一、糖类的组成和分类
从结构上看,糖类是多羟基酮 多 羟 基 醛 或它们 的 脱 水 缩 合 物 0
单糖
(1)存在:
葡萄糖是自然界中分布最广的单糖,因最初是从葡萄汁中分 离得到而得名。葡萄糖存在于水果、蜂蜜,以及植物的种子、
叶、根、花中。动物的血液和淋巴液中也含有葡萄糖。
(2)物理性质:
无色晶体,熔点146℃,有甜味,但甜度不如
蔗糖,易溶于水,稍溶于乙醇,不溶于乙醚。
1、葡萄糖
(2)化学性质
【实验4-1】
a.葡萄糖与银氨溶液
光亮的银镜
A W njhoyuLGO回
b.葡萄糖与新制Cu(OH) 悬浊液
砖红色沉淀
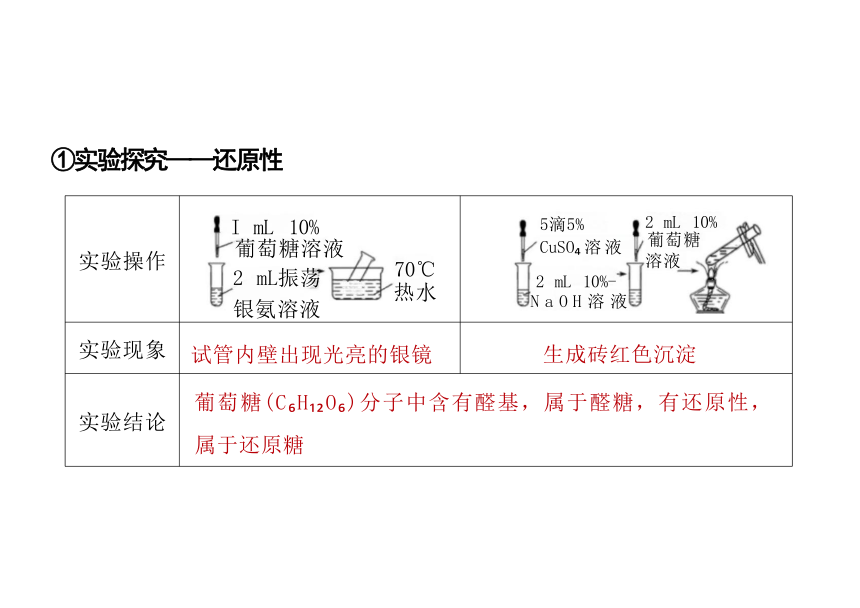
实验操作 I mL 10% 葡萄糖溶液 2 mL振荡 银氨溶液 70℃ 热水 5滴5% CuSO 溶液 2 mL 10%- N a O H 溶 液
2 mL 10%
葡萄糖
溶液
实验现象 试管内壁出现光亮的银镜 生成砖红色沉淀
实验结论 葡萄糖(C H O )分子中含有醛基,属于醛糖,有还原性, 属于还原糖
①实验探究——还原性
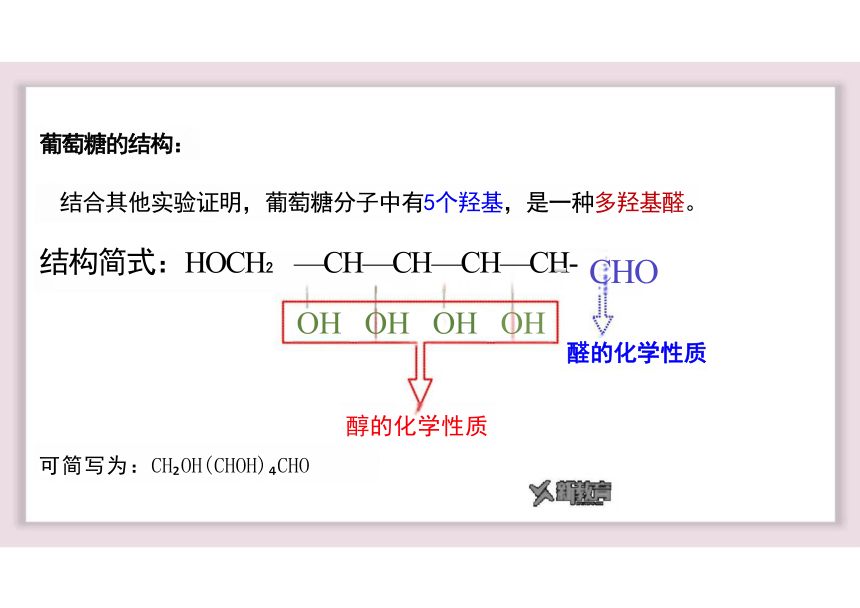
葡萄糖的结构:
结合其他实验证明,葡萄糖分子中有5个羟基,是一种多羟基醛。
结构简式:HOCH —CH—CH—CH—CH- CHO
OH OH OH OH
醛的化学性质
醇的化学性质
可简写为:CH OH(CHOH) CHO
置换反应
氧化反应一→使高锰酸钾溶液褪色
酯化反应
取代反应
与HX反应
消去反应
银镜反应
与新制Cu(OH) 悬浊液反应:
与高锰酸钾、溴水等强氧化剂反应
CH OH(CHOH) CHO+H NiCH OH(CHOH) CH OH
wwwsthjinoyLCO0o
氧化反应
加成反应
醛 基
羟 基
葡萄糖是种重要的营养物质,易于被人体吸收,经酶的催化发生氧化反应放出热
量,提供了维持生命活动所需要的能量。人生病不能正常饮食或低血糖时,医生 一般会静脉注射葡萄糖水溶液。
(2)葡萄糖的应用 wWsnjaoyuLE
①食品和医药工业
酒化酶
C H 2O →2C H OH+2CO 个
②工业上制镜
③制酒工业
制酒工业
镀银工业
【资料卡片】糖尿病患者的糖代谢功能紊乱,其
血液和尿液中的葡萄糖含量会超出正常范围。测 定患者血液或尿液中的葡萄糖含量有助于判断病 情,可使用根据葡萄糖特征反应原理制备的试纸 进行测试。
加入银氨溶液、加热 形成光亮的银镜
加入新制 H) 悬浊液产生砖红色沉淀
加热
Cu(O
检验 葡萄糖
葡萄糖—
资料卡片 葡萄糖的环状结构
葡萄糖分子中的醛基可以与分子内的羟基作用,形成两种六元环状结 构。在葡萄糖水溶液中,存在着链状和环状结构葡萄糖之间的平衡,其 中绝大部分葡萄糖为环状结构。很多单糖,以及寡糖和多糖中的单糖单 元多以环状结构的形式存在。
aD 吡喃葡萄糖 链状葡萄糖 βD吡喃葡萄糖
2. 果糖
存 在 :在水果和蜂蜜中含量较高
物理性质:纯净的果糖为无色晶 体 ,易溶 于 水 ,吸湿性强, 比蔗糖甜度高
;羟基酮
于酮糖
1葡萄糖互为同分异构体
C H 2O
结构简式:
分子式:
核糖:C H O H 0 脱氧核糖:C H O
C
H 一 OH
H 一 OH
OH OH
H OH
OH 0 OH 0
OH OH H C —OH OH
二者都含有醛基,均属于醛糖,均具有还原性,属于还原糖。
3. 核糖与脱氧核糖
核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA) 与脱氧核糖核酸 (DNA) 的重要组成部分。
H 0
C
H 一 -H
H 一 OH
H 一 OH
H C —OH
>最简单的醛糖是丙醛糖,又称甘油醛,其结构简式为:
CH -cH-CHO
>连有4个不同的原子或原子团的碳原子叫做不对称碳原子H 也叫手性碳原
子,如甘油醛分子中注*号的碳原子。
>有手性碳原子的分子存在对映异构体。人们把这样的分子称为手性分子。
D-甘油醛 L-甘油醛
糖类分子与手性
二糖
(1)分子式:C H O
(2)物理性质:无色晶体,熔点186℃,
(3)化学性质:
①水解反应 C H 2O +H O 酸 或 酶C H O +C H 2O 蔗糖 葡萄糖 果糖
蔗糖水解
蔗糖 水解液 中和液 产生
呈弱碱性
稀NaOH
如何检验蔗糖水
解后产生葡萄糖
1 .蔗糖
仟问学堂
0
白色晶体,易溶于水,有甜味,甜度约为蔗糖的
饴糖就是麦芽糖的粗制品。
主要存在于发芽的谷粒和麦芽中。
化学性质:
①水解反应 C H 2O +H O 酸或酶、2C H O
麦芽糖 葡萄糖
分子式:C H O 1
2 . 麦 芽 糖
0
实 验 步 骤 5%CuSO 溶液5滴 10%NaOH 溶液2mL 10%蔗糖 溶液2 mL 5%CuSO 溶液5滴 10%NaOH 溶液2 mL
10%麦芽糖
溶液2mL
现象 无 明 显 现 象 试 管 中 出 现 砖 红 色 沉 淀
结论 蔗糖不属于还原糖 , 麦芽糖属于还原糖
糖类的还原性
葡萄糖属于还原糖,蔗糖和麦芽槽是否属于还原糖
根据检验葡萄糖还原性的方法,设计实验方案进行探究
糖类还原性是指糖类中的醛基被氧化的性质。某些糖类有较强的
还原性,能被银氨溶液或新制Cu(OH) 氧化。若糖类不能发生银镜反应 或不与新制Cu(OH) 反应,则该糖不具有还原性,为非还原糖,如蔗糖。
资料卡片
乳糖
乳糖也是一种常见的二糖,主要存在于哺乳动物的乳汁中,可 用于婴儿食品、糖果、药物等的生产。乳糖经发酵产生的乳酸是酸 奶酸味的主要来源。部分人群由于肠道内缺乏乳糖酶导致乳糖消化 吸收障碍,饮用牛奶后容易出现腹胀、腹泻等乳糖不耐受的症状。
多糖
1.淀粉 (C H oO )。
(1)存在:
淀粉是绿色植物光合作用的产物,是植物储存营养 物质的一种形式,在种子、块根和块茎中含量丰富。天 然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高 的一些谷物,如糯米、糯玉米等有比较黏的口感。
1.淀粉 (C H O )n
(2)物理性质:
白色粉末状物质,没有甜味,不溶于冷水。在热水 中,淀粉会部分溶解,形成胶状的淀粉糊
1.淀粉
绿色植物光合作用的产物;
存在:植物种子或块根中,如大米、小麦、马铃薯等
天然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高 的一些谷物,如糯米、糯玉米等有比较黏的口感。
支链淀粉
直链淀粉
①淀粉的物理性质:
淀粉有直链淀粉和支链淀粉两类。前者为无分支的螺旋结构;后者以24~30个葡萄糖残基 以α-1,4-糖苷键首尾相连而成,在支链处为α-1,6-糖苷键。
直链淀粉遇碘呈监色,支链淀粉遇碘呈紫红色。这并非是淀粉与碘发生了化学反应,产 生相互作用,而是淀粉螺旋中央空穴恰能容下碘分子,通过范德华力,两者形成一种蓝 黑色络合物。具有可逆热色性
淀粉遇单质碘变蓝
②淀粉的化学性质:
●淀粉不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
●在淀粉中葡萄糖单元存在醇羟基,可以发生酯化反应。
●在酸或酶催化下,淀粉最终生成葡萄糖。
(C H O )n+nH O 或酶nC H 2O
淀粉 葡萄糖
5 min后
热水
淀粉水解反应
新制的 Cu(OH
淀粉 溶液
NaOH
溶液
稀硫酸
新制的
Cu(OH)
有砖红色沉 淀生成
NaOH
溶液
5min后
热水
催化剂
n C H 2O
葡萄糖
淀粉水解生成的葡萄糖,与新制的Cu(OH) 共热生成氧化亚铜(Cu O)
稀硫酸
淀粉
溶液
(C H 0O )n+nH O
淀粉
淀粉水解反应
现象A 现象B或现象C
结论
溶液呈蓝色 B:未产生砖红色沉淀C:未产生银镜
未水解
溶液呈蓝色 B:产生砖红色沉淀C:产生银镜
部分水解
溶液不呈蓝色 B:产生砖红色沉淀C:产生银镜
完全水解
如何判断淀粉的水解程度(完全水解、部分水解、未水解)
新制Cu(OH)
银氨溶液 水浴加热
现象A
中和液
碘水
NaOH
溶液
现 象B
现象C
淀粉 h 0 → 水解液
△
③淀粉用途:
淀粉是食物的一种重要成分,也是重要的工业原料。以淀粉或淀粉水解生成的葡 萄糖等为原料,经发酵可以得到多种产品,如燃料乙醇、白酒、食醋、味精,以 及氨基酸、抗生素等药物。淀粉经酯化后可用于生产食品添加剂、表面活性剂和 可降解塑料等。
2 . 纤维素
>物理性质: 白色、没有甜味的具有纤维状结构的物质。 不溶于水和一般的有机溶剂。
> 存 在 :纤维素存在于一些植物中(例如棉花、
木材、麻中)。纤维素参与构成植物的细胞壁, 是自然界分布最广泛的一种多糖。
2.纤维素
(3)化学性质:
①在酸或酶催化下最终水解成葡萄糖
酸或酶
n C H 2O
葡萄糖
②不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
(C H 0O )n+nH O
纤维素
+3n CH COOH 浓硫酸
纤维素醋酸酯(俗称醋酸纤维)
③纤维素的葡萄糖单元仍有三个羟基,所以也可表示为[C H O (OH) ]n, 能发生 酯化(或硝化)。
OH (C H O )—OH
OH
0oCCH
0OCCH 00CCH n
(C H O -
十 3nH O
2.纤维素
(3)化学性质:
③纤维素的葡萄糖单元仍有三个羟基,所以也可表示为[C H O (OH) ], 能发生 酯化(或硝化)。
十 3nH O
纤维素硝酸酯(俗称硝酸纤维)
(3)化学性质:
2.纤维素
1.人体内的葡萄糖是从哪里来呢
人体摄入其他糖类(如蔗糖、麦芽糖、淀粉)在酶的 催化作用下逐步水解,最终可生成葡萄糖。
2.某广告宣称新型糕点只含面粉、植物油和鸡蛋,不含糖,是糖尿病患者的理想
食品,你认为这种说法对吗
唾液淀粉酶
胰、肠淀粉酶
胰麦芽糖酶
肠麦芽糖酶
你知道吗
麦芽糖
葡萄糖
淀粉
食物中的纤维素有
利于人体的消化。
制造黏胶纤维:其中的长纤 维称人造丝,短纤维称人造 棉,都可用于纺织工业。
制造纤维素乙酸酯(醋酸纤维): 不易燃烧,可用于生产塑料、过 滤膜、胶片等。
棉和麻的纤维大
量用于纺织工业。
木材、稻草、秸杆、 蔗渣等用于造纸。
制造纤维素硝酸酯(硝酸纤 维):极易燃烧。可用于生 产火药、塑料和涂料等。
纤维素 的用途
> 用途
2
3
6
5
4
1
淀粉
纤维素
分子 结构 分子通式 (C H10O )n
相对分子质量 可达到几十万
可达到几百万
分子结构关系 都是由葡萄糖结构单元(C H 0O )构成的天然有机高分子, 但分子内葡萄糖结构单元数目不同,不是同分异构体。
化学 性质 共性 无还原性 水解最终生成葡萄糖
特性 遇碘变蓝
分子中含有醇羟基,能与醋酸、 硝酸等发生酯化反应
淀粉和纤维素
3. 多糖的知识拓展 — — 甲壳质
> 甲壳质是由乙酰氨基葡萄糖相互结合形成的一 种多糖,它是许多低等动物,特别是节肢动物 外壳的重要成分,是一种来源丰富的可再生资 源。
>壳聚糖是甲壳质在碱溶液中脱去乙酰基,生成 以氨基葡萄糖为单体的高聚物。可溶于酸溶液, 具有良好的生物相容性和一定的抑菌作用。
1.葡萄糖所不具有的性质是( D )
A. 和H 发生加成反应 醛基
B. 和银氨溶液发生氧化反应 醛基
C. 和酸发生酯化反应 羟 基
D. 和NaOH 溶液反应
随堂练习
随堂练习
2. 以下试剂不可以鉴别乙酸、葡萄糖溶液,这种试剂是( D )
A. 新制Cu(OH) 蓝色絮状沉淀消失砖红色沉淀
B.Na CO 溶液 放出二氧化碳 不反应
C. 石蕊试液 变红 不变色
D. 氢氧化钠溶液 无明显现象 不反应
随堂练习
3.有关葡萄糖与果糖的下列说法中,不正确的是( D )
A. 两者互为同分异构体
B. 两者都易溶于水
C. 两者都能发生酯化反应
D. 葡萄糖比果糖要甜 葡萄糖甜度比蔗糖低,果糖甜度比蔗糖高
THANK Y0U
感谢观看
第四章生物大分子
第一节 糖类
课时一糖类的组成和性质
01.从糖类的官能团微观探析糖类的结构
特点,了解糖类的分类,理解糖类的化学
性质,掌握糖类的特殊性
02.了解糖类在人体供能、储能等方面的 作用,了解糖类的摄入和代谢与人体健康
之间的关系,科学合理地搭配饮食。
学习
目标
们生活中的面粉,看到的棉花、小草、树皮中也含有大量的糖, 那么这些糖的成分一样吗 它们又有什么样的区别
说起糖,大家恐怕都不会陌生,其实除了我们吃的这些糖,我
1. 组 成 : 糖
糖类是绿色植物光合作用的产物,是生命活动的主要能量来源。 一般含碳、氢、氧三种元素。
有甜味 无甜味
1 . 上述糖分子中H和0元素原子个数比是多少 2.是不是糖都有甜味
纤维素 淀粉
(C H O ) n (C H O )n
2. 常见的糖类:
麦芽糖
葡萄糖
C H2 O
蔗糖
C H O
C H O
很多糖类分子中氢原子和氧原子数目比恰好为2:1,组成可以 用通式Cm(H O)n 表示,故糖类也被称为碳水化合物。
◆符合Cm(H O),通式的不一定是糖。例如:乙酸C H O 、乳酸C H O 。
◆有的糖不一定符合Cm(H O) 通式。例如:脱氧核糖C H O 、鼠李糖C H O
因此将糖类称为碳水化合物是不对的
◆有甜味的不一定是糖。如:某些食品添加剂、甘油。
◆糖不一定都有甜味。淀粉、纤维素就没有甜味。
甜味物质
碳水化合物
糖
糖类
糖类
单糖 寡糖(低聚糖)
多糖
概念 不能 水解的糖 1 mol糖水解后能产生 2~10_mol单糖的糖
1 mol糖水解后能产 生10 mol以上单糖的 糖
代表物 葡萄糖、果糖 蔗糖、麦芽糖
纤维素、_ 淀粉
分子式 C H 2O
(C H 0O )n
一、糖类的组成和分类
从结构上看,糖类是多羟基酮 多 羟 基 醛 或它们 的 脱 水 缩 合 物 0
单糖
(1)存在:
葡萄糖是自然界中分布最广的单糖,因最初是从葡萄汁中分 离得到而得名。葡萄糖存在于水果、蜂蜜,以及植物的种子、
叶、根、花中。动物的血液和淋巴液中也含有葡萄糖。
(2)物理性质:
无色晶体,熔点146℃,有甜味,但甜度不如
蔗糖,易溶于水,稍溶于乙醇,不溶于乙醚。
1、葡萄糖
(2)化学性质
【实验4-1】
a.葡萄糖与银氨溶液
光亮的银镜
A W njhoyuLGO回
b.葡萄糖与新制Cu(OH) 悬浊液
砖红色沉淀
实验操作 I mL 10% 葡萄糖溶液 2 mL振荡 银氨溶液 70℃ 热水 5滴5% CuSO 溶液 2 mL 10%- N a O H 溶 液
2 mL 10%
葡萄糖
溶液
实验现象 试管内壁出现光亮的银镜 生成砖红色沉淀
实验结论 葡萄糖(C H O )分子中含有醛基,属于醛糖,有还原性, 属于还原糖
①实验探究——还原性
葡萄糖的结构:
结合其他实验证明,葡萄糖分子中有5个羟基,是一种多羟基醛。
结构简式:HOCH —CH—CH—CH—CH- CHO
OH OH OH OH
醛的化学性质
醇的化学性质
可简写为:CH OH(CHOH) CHO
置换反应
氧化反应一→使高锰酸钾溶液褪色
酯化反应
取代反应
与HX反应
消去反应
银镜反应
与新制Cu(OH) 悬浊液反应:
与高锰酸钾、溴水等强氧化剂反应
CH OH(CHOH) CHO+H NiCH OH(CHOH) CH OH
wwwsthjinoyLCO0o
氧化反应
加成反应
醛 基
羟 基
葡萄糖是种重要的营养物质,易于被人体吸收,经酶的催化发生氧化反应放出热
量,提供了维持生命活动所需要的能量。人生病不能正常饮食或低血糖时,医生 一般会静脉注射葡萄糖水溶液。
(2)葡萄糖的应用 wWsnjaoyuLE
①食品和医药工业
酒化酶
C H 2O →2C H OH+2CO 个
②工业上制镜
③制酒工业
制酒工业
镀银工业
【资料卡片】糖尿病患者的糖代谢功能紊乱,其
血液和尿液中的葡萄糖含量会超出正常范围。测 定患者血液或尿液中的葡萄糖含量有助于判断病 情,可使用根据葡萄糖特征反应原理制备的试纸 进行测试。
加入银氨溶液、加热 形成光亮的银镜
加入新制 H) 悬浊液产生砖红色沉淀
加热
Cu(O
检验 葡萄糖
葡萄糖—
资料卡片 葡萄糖的环状结构
葡萄糖分子中的醛基可以与分子内的羟基作用,形成两种六元环状结 构。在葡萄糖水溶液中,存在着链状和环状结构葡萄糖之间的平衡,其 中绝大部分葡萄糖为环状结构。很多单糖,以及寡糖和多糖中的单糖单 元多以环状结构的形式存在。
aD 吡喃葡萄糖 链状葡萄糖 βD吡喃葡萄糖
2. 果糖
存 在 :在水果和蜂蜜中含量较高
物理性质:纯净的果糖为无色晶 体 ,易溶 于 水 ,吸湿性强, 比蔗糖甜度高
;羟基酮
于酮糖
1葡萄糖互为同分异构体
C H 2O
结构简式:
分子式:
核糖:C H O H 0 脱氧核糖:C H O
C
H 一 OH
H 一 OH
OH OH
H OH
OH 0 OH 0
OH OH H C —OH OH
二者都含有醛基,均属于醛糖,均具有还原性,属于还原糖。
3. 核糖与脱氧核糖
核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA) 与脱氧核糖核酸 (DNA) 的重要组成部分。
H 0
C
H 一 -H
H 一 OH
H 一 OH
H C —OH
>最简单的醛糖是丙醛糖,又称甘油醛,其结构简式为:
CH -cH-CHO
>连有4个不同的原子或原子团的碳原子叫做不对称碳原子H 也叫手性碳原
子,如甘油醛分子中注*号的碳原子。
>有手性碳原子的分子存在对映异构体。人们把这样的分子称为手性分子。
D-甘油醛 L-甘油醛
糖类分子与手性
二糖
(1)分子式:C H O
(2)物理性质:无色晶体,熔点186℃,
(3)化学性质:
①水解反应 C H 2O +H O 酸 或 酶C H O +C H 2O 蔗糖 葡萄糖 果糖
蔗糖水解
蔗糖 水解液 中和液 产生
呈弱碱性
稀NaOH
如何检验蔗糖水
解后产生葡萄糖
1 .蔗糖
仟问学堂
0
白色晶体,易溶于水,有甜味,甜度约为蔗糖的
饴糖就是麦芽糖的粗制品。
主要存在于发芽的谷粒和麦芽中。
化学性质:
①水解反应 C H 2O +H O 酸或酶、2C H O
麦芽糖 葡萄糖
分子式:C H O 1
2 . 麦 芽 糖
0
实 验 步 骤 5%CuSO 溶液5滴 10%NaOH 溶液2mL 10%蔗糖 溶液2 mL 5%CuSO 溶液5滴 10%NaOH 溶液2 mL
10%麦芽糖
溶液2mL
现象 无 明 显 现 象 试 管 中 出 现 砖 红 色 沉 淀
结论 蔗糖不属于还原糖 , 麦芽糖属于还原糖
糖类的还原性
葡萄糖属于还原糖,蔗糖和麦芽槽是否属于还原糖
根据检验葡萄糖还原性的方法,设计实验方案进行探究
糖类还原性是指糖类中的醛基被氧化的性质。某些糖类有较强的
还原性,能被银氨溶液或新制Cu(OH) 氧化。若糖类不能发生银镜反应 或不与新制Cu(OH) 反应,则该糖不具有还原性,为非还原糖,如蔗糖。
资料卡片
乳糖
乳糖也是一种常见的二糖,主要存在于哺乳动物的乳汁中,可 用于婴儿食品、糖果、药物等的生产。乳糖经发酵产生的乳酸是酸 奶酸味的主要来源。部分人群由于肠道内缺乏乳糖酶导致乳糖消化 吸收障碍,饮用牛奶后容易出现腹胀、腹泻等乳糖不耐受的症状。
多糖
1.淀粉 (C H oO )。
(1)存在:
淀粉是绿色植物光合作用的产物,是植物储存营养 物质的一种形式,在种子、块根和块茎中含量丰富。天 然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高 的一些谷物,如糯米、糯玉米等有比较黏的口感。
1.淀粉 (C H O )n
(2)物理性质:
白色粉末状物质,没有甜味,不溶于冷水。在热水 中,淀粉会部分溶解,形成胶状的淀粉糊
1.淀粉
绿色植物光合作用的产物;
存在:植物种子或块根中,如大米、小麦、马铃薯等
天然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高 的一些谷物,如糯米、糯玉米等有比较黏的口感。
支链淀粉
直链淀粉
①淀粉的物理性质:
淀粉有直链淀粉和支链淀粉两类。前者为无分支的螺旋结构;后者以24~30个葡萄糖残基 以α-1,4-糖苷键首尾相连而成,在支链处为α-1,6-糖苷键。
直链淀粉遇碘呈监色,支链淀粉遇碘呈紫红色。这并非是淀粉与碘发生了化学反应,产 生相互作用,而是淀粉螺旋中央空穴恰能容下碘分子,通过范德华力,两者形成一种蓝 黑色络合物。具有可逆热色性
淀粉遇单质碘变蓝
②淀粉的化学性质:
●淀粉不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
●在淀粉中葡萄糖单元存在醇羟基,可以发生酯化反应。
●在酸或酶催化下,淀粉最终生成葡萄糖。
(C H O )n+nH O 或酶nC H 2O
淀粉 葡萄糖
5 min后
热水
淀粉水解反应
新制的 Cu(OH
淀粉 溶液
NaOH
溶液
稀硫酸
新制的
Cu(OH)
有砖红色沉 淀生成
NaOH
溶液
5min后
热水
催化剂
n C H 2O
葡萄糖
淀粉水解生成的葡萄糖,与新制的Cu(OH) 共热生成氧化亚铜(Cu O)
稀硫酸
淀粉
溶液
(C H 0O )n+nH O
淀粉
淀粉水解反应
现象A 现象B或现象C
结论
溶液呈蓝色 B:未产生砖红色沉淀C:未产生银镜
未水解
溶液呈蓝色 B:产生砖红色沉淀C:产生银镜
部分水解
溶液不呈蓝色 B:产生砖红色沉淀C:产生银镜
完全水解
如何判断淀粉的水解程度(完全水解、部分水解、未水解)
新制Cu(OH)
银氨溶液 水浴加热
现象A
中和液
碘水
NaOH
溶液
现 象B
现象C
淀粉 h 0 → 水解液
△
③淀粉用途:
淀粉是食物的一种重要成分,也是重要的工业原料。以淀粉或淀粉水解生成的葡 萄糖等为原料,经发酵可以得到多种产品,如燃料乙醇、白酒、食醋、味精,以 及氨基酸、抗生素等药物。淀粉经酯化后可用于生产食品添加剂、表面活性剂和 可降解塑料等。
2 . 纤维素
>物理性质: 白色、没有甜味的具有纤维状结构的物质。 不溶于水和一般的有机溶剂。
> 存 在 :纤维素存在于一些植物中(例如棉花、
木材、麻中)。纤维素参与构成植物的细胞壁, 是自然界分布最广泛的一种多糖。
2.纤维素
(3)化学性质:
①在酸或酶催化下最终水解成葡萄糖
酸或酶
n C H 2O
葡萄糖
②不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
(C H 0O )n+nH O
纤维素
+3n CH COOH 浓硫酸
纤维素醋酸酯(俗称醋酸纤维)
③纤维素的葡萄糖单元仍有三个羟基,所以也可表示为[C H O (OH) ]n, 能发生 酯化(或硝化)。
OH (C H O )—OH
OH
0oCCH
0OCCH 00CCH n
(C H O -
十 3nH O
2.纤维素
(3)化学性质:
③纤维素的葡萄糖单元仍有三个羟基,所以也可表示为[C H O (OH) ], 能发生 酯化(或硝化)。
十 3nH O
纤维素硝酸酯(俗称硝酸纤维)
(3)化学性质:
2.纤维素
1.人体内的葡萄糖是从哪里来呢
人体摄入其他糖类(如蔗糖、麦芽糖、淀粉)在酶的 催化作用下逐步水解,最终可生成葡萄糖。
2.某广告宣称新型糕点只含面粉、植物油和鸡蛋,不含糖,是糖尿病患者的理想
食品,你认为这种说法对吗
唾液淀粉酶
胰、肠淀粉酶
胰麦芽糖酶
肠麦芽糖酶
你知道吗
麦芽糖
葡萄糖
淀粉
食物中的纤维素有
利于人体的消化。
制造黏胶纤维:其中的长纤 维称人造丝,短纤维称人造 棉,都可用于纺织工业。
制造纤维素乙酸酯(醋酸纤维): 不易燃烧,可用于生产塑料、过 滤膜、胶片等。
棉和麻的纤维大
量用于纺织工业。
木材、稻草、秸杆、 蔗渣等用于造纸。
制造纤维素硝酸酯(硝酸纤 维):极易燃烧。可用于生 产火药、塑料和涂料等。
纤维素 的用途
> 用途
2
3
6
5
4
1
淀粉
纤维素
分子 结构 分子通式 (C H10O )n
相对分子质量 可达到几十万
可达到几百万
分子结构关系 都是由葡萄糖结构单元(C H 0O )构成的天然有机高分子, 但分子内葡萄糖结构单元数目不同,不是同分异构体。
化学 性质 共性 无还原性 水解最终生成葡萄糖
特性 遇碘变蓝
分子中含有醇羟基,能与醋酸、 硝酸等发生酯化反应
淀粉和纤维素
3. 多糖的知识拓展 — — 甲壳质
> 甲壳质是由乙酰氨基葡萄糖相互结合形成的一 种多糖,它是许多低等动物,特别是节肢动物 外壳的重要成分,是一种来源丰富的可再生资 源。
>壳聚糖是甲壳质在碱溶液中脱去乙酰基,生成 以氨基葡萄糖为单体的高聚物。可溶于酸溶液, 具有良好的生物相容性和一定的抑菌作用。
1.葡萄糖所不具有的性质是( D )
A. 和H 发生加成反应 醛基
B. 和银氨溶液发生氧化反应 醛基
C. 和酸发生酯化反应 羟 基
D. 和NaOH 溶液反应
随堂练习
随堂练习
2. 以下试剂不可以鉴别乙酸、葡萄糖溶液,这种试剂是( D )
A. 新制Cu(OH) 蓝色絮状沉淀消失砖红色沉淀
B.Na CO 溶液 放出二氧化碳 不反应
C. 石蕊试液 变红 不变色
D. 氢氧化钠溶液 无明显现象 不反应
随堂练习
3.有关葡萄糖与果糖的下列说法中,不正确的是( D )
A. 两者互为同分异构体
B. 两者都易溶于水
C. 两者都能发生酯化反应
D. 葡萄糖比果糖要甜 葡萄糖甜度比蔗糖低,果糖甜度比蔗糖高
THANK Y0U
感谢观看
