2015-2016学年苏教版高中化学选修一:1.2《水资源的合理利用》ppt课件(共46张PPT)
文档属性
| 名称 | 2015-2016学年苏教版高中化学选修一:1.2《水资源的合理利用》ppt课件(共46张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 292.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-01-02 00:00:00 | ||
图片预览











文档简介
课件46张PPT。第二单元
水资源的合理利用知识点1 生活中的饮用水
【自主认知】
一、天然水中的杂质及城市自来水的获取
1.天然水中的杂质。
通常分为三类:_________、_________和_________。悬浮物质胶体物质溶解物质2.明矾的净水原理。
明矾溶于水后,铝离子发生_____,生成氢氧化铝胶体:_________
_______________________。
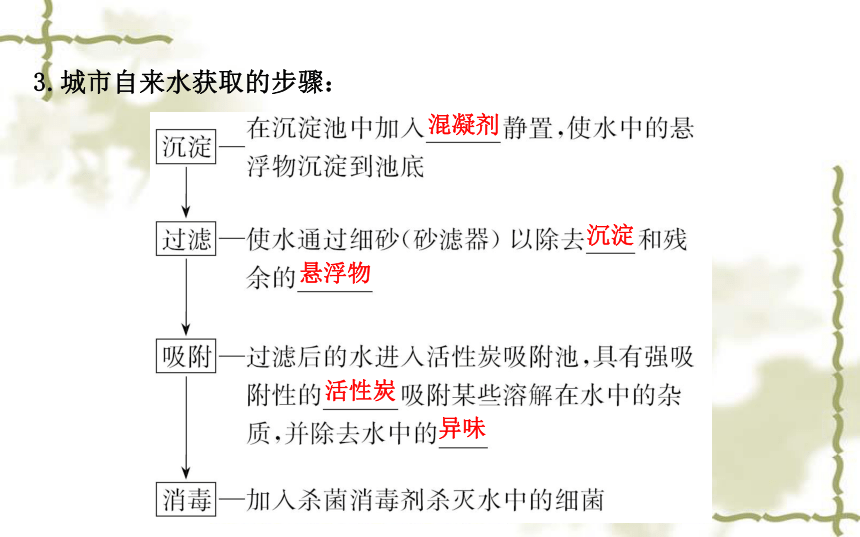
氢氧化铝胶体因吸附溶液中的阳离子而带正电荷。能吸附水中带负电荷的胶粒,并使杂质与氢氧化铝胶体一起凝聚而沉降。 水解Al3++3H2O Al(OH)3(胶体)+3H+3.城市自来水获取的步骤:混凝剂沉淀悬浮物活性炭异味二、硬水及其软化
1.有关概念。
硬水:含有_______________的水。
软水:不含或含少量___________的水。
硬水的软化:硬水软化的目的是减小水中_________________。较多钙、镁离子钙、镁离子钙、镁离子的浓度2.硬水软化的方法:
(1)煮沸法。
若硬水中的钙、镁离子以_________的形式存在时,可通过煮沸使钙、镁离子转化为沉淀。
反应的化学方程式为
______________________________,
_______________________________,
__________________________。 碳酸氢盐Ca(HCO3)2 CaCO3↓+CO2↑+H2OMg(HCO3)2 MgCO3↓+CO2↑+H2OMgCO3+H2O Mg(OH)2+CO2↑(2)离子交换法。
①用磺化煤软化硬水的原理(用反应方程式表示):
_____________________,
_____________________。
②磺化煤再生的原理:
CaR2+2Na+====2NaR+Ca2+,
MgR2+2Na+====2NaR+Mg2+。2NaR+Ca2+====CaR2+2Na+2NaR+Mg2+====MgR2+2Na+3.终端净水:
(1)水的二次污染:由于管道老化,储存水箱较脏,水箱内壁防腐材料不合格等引起的污染。
(2)终端净水及其优点。
①终端净水:在家中的出水点前加装净水设备。
②优点:能消除_________,使饮用水更安全。二次污染【释疑解惑】
1.硬水和软水的鉴别方法。
方法1:分别用两只烧杯取等量水样,向两只烧杯中分别滴加等量肥皂水。泡沫多、浮渣少的为软水;反之,为硬水。
方法2:用烧杯加热,在杯壁留下较多水垢的是硬水。因为硬水是含有较多的可溶性钙、镁物质的水,加热后,这些可溶性的钙、镁物质转化成不可溶的物质。
方法3:取一干净、干燥的玻璃片,分别在不同的位置滴等量水样。待其完全蒸发后,白色残留物多的为硬水;反之为软水。2.自来水的制取过程:【即时训练】
1.(2015·镇江高二检测)为了获取大量的生活饮用水,自来水厂需要用适宜、高效的方法和流程将天然水悬浮物、致病细菌等有害成分降低到规定的含量。
(1)要达到上述目的,一般要经过的基本步骤是①沉降、②______、③曝气、④ 。“曝气”的主要目的是 。
(2)在第①步中,下列物质可以使用的是 (用字母填空)。
A.明矾 B.膨润土 C.烧碱(3)在将天然水制成生活饮用水的过程中,水中不需要除去的成分是_________(至少答出一项)。
(4)经过上述四个步骤的处理之后,如果水中Ca2+、Mg2+的含量超标,还要将水进行 。 【解析】沉降之后必然是过滤。加消毒剂也是必不可少的步骤之一。“曝气”就是使水暴露在空气中,使水与空气接触的面积增大,增加水中的含氧量,以加速水中有机物的分解。明矾可作水的混凝剂,膨润土可作水的辅助混凝剂。对人体有益的矿物质等最好不要除去。降低水中Ca2+、Mg2+含量的过程叫作硬水的软化。
答案:(1)过滤 消毒 增加水中的含氧量,加速水中有机物的分解
(2)A、B (3)对人体有益的矿物质等
(4)软化2.(1)为了提高生活用水的卫生标准,自来水厂同时使用Cl2和FeSO4·7H2O对水进行消毒、净化,以改善水质,其原因是_______
, 。
(2)为了延长液氯的杀菌时间,某些自来水厂在用液氯进行消毒处理时,还加入少量液氨,其反应的化学方程式为NH3+HClOH2O+NH2Cl(一氯氨)。已知NH2Cl比HClO稳定,试分析加液氨能延长液氯杀菌时间的原因是? 。【解析】(1)Cl2的作用有两点:一是与H2O反应生成HClO,杀菌消毒;二是将Fe2+氧化成Fe3+,Fe3+水解生成Fe(OH)3胶体,吸附水中悬浮物。
(2)NH3+HClO H2O+NH2Cl是可逆反应,存在平衡,解题时要善于捕捉题目信息,由于NH2Cl比HClO稳定,因此在自来水中加入液氯,再加入液氨,上述平衡右移,随着HClO的杀菌,被消耗,浓度降低,平衡左移,所以可延长杀菌时间。答案:(1)Cl2溶于水生成的HClO能杀菌消毒
Cl2能氧化Fe2+为Fe3+,Fe3+的水解产物Fe(OH)3胶体可以吸附水中杂质
(2)HClO+NH3 H2O+NH2Cl,把不稳定的HClO转化为较稳定的NH2Cl,
消毒时,随HClO浓度降低,平衡向左移动,HClO得到补充【互动探究】
(1)题1(2)中的明矾的化学式是什么?明矾净水的原理是什么?
提示:明矾的化学式为KAl(SO4)2·12H2O,明矾净水的原理是明矾溶于水电离出Al3+,Al3+水解生成氢氧化铝胶体,能凝聚水中的悬浮物和吸附杂质。(2)自来水中含有少量余氯,在水管中停留可以起到有效的杀菌作用,故自来水厂杀菌消毒时充入的Cl2越多越好。这种说法对吗?为什么?
提示:不对。因为Cl2有毒,过量的Cl2会使自来水不适宜人饮用,而且还容易与水中的有机物反应,生成有毒的氯代烃。【补偿训练】1.以下是原水处理成自来水的工艺流程示意图。
(1)原水中含Ca2+、Mg2+、HC、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干反应,写出其中一个离子方程式:? 。(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂。它的
氧化性比KMnO4还强,反应中 被还原为Fe3+。
①已知高铁酸钠的制备反应如下:
2Fe(NO3)3+16NaOH+3Cl2====2Na2FeO4+6NaNO3+6NaCl+8H2O,则反应中
元素被氧化,反应中生成2 mol Na2FeO4转移电子物质的量
为 mol。
②高铁酸钠之所以能净水,除了能消毒杀菌外,另一个原因是
? 。 (3)通入二氧化碳的目的是? 和 。
(4)气体A的作用是 。
这种作用是基于气体A和水反应的产物具有? 性。
(5)下列物质中, 可以作为气体A的代用品。
①Ca(ClO)2 ②浓氨水 ③浓硫酸 ④SO2【解析】(1)Ca(OH)2可以与Mg2+发生反应:
Mg2++2OH-====Mg(OH)2↓;也可以与Mg2+、 发生反应:Mg2++
2 +4OH-+2Ca2+====Mg(OH)2↓+2CaCO3↓+2H2O;还可以与
发生反应:Ca2++ +OH-====CaCO3↓+H2O。
(2)①根据反应可知,反应过程中 铁元素化合
价升高,被氧化。根据2Fe(NO3)3 2Na2FeO4,故生成2 mol
Na2FeO4转移6 mol电子。
②Na2FeO4在净水时被还原为Fe3+,Fe3+能发生水解,生成Fe(OH)3胶
体,故可以作混凝剂,吸附水中杂质。(3)因为加入的CaO是过量的,溶液中Ca2+和OH-过量,通入CO2不仅能将多余的Ca2+生成沉淀,还能与OH-反应,调节溶液的pH,有利于沉淀的生成。
(4)原水处理成自来水一般经沉淀→过滤→吸附→杀菌消毒四步,题中流程中已经有了沉淀和过滤两步,而吸附一般是用活性炭固体,此处通入A只能是杀菌消毒,杀菌消毒一般用Cl2,Cl2与水反应生成HCl和HClO,HClO具有强氧化性,可以用来杀菌消毒。(5)气体A起杀菌消毒作用是因为与水反应生成的物质具有强氧化性,因此代用品也应具有强氧化性,①可以,②④没有强氧化性,③虽具有强氧化性,但不能用于饮用水的消毒。答案:(1)Mg2++2OH-====Mg(OH)2↓
[或Mg2++2 +2Ca2++4OH-====Mg(OH)2↓+2CaCO3↓+2H2O或
Ca2++ +OH-====CaCO3↓+H2O](任选一个即可)
(2)①铁 6
②还原产物Fe3+发生水解,生成Fe(OH)3胶体,能吸附杂质并沉降
(3)除去Ca2+ 调节pH
(4)杀菌消毒 强氧化
(5)①2.(2015·四平高二检测)有关硬水及其软化,下列说法正确的是
( )
A.含有Ca2+、Mg2+的水称为硬水
B.长期烧煮硬水的容器底部沉积的水垢主要成分是CaO和MgCO3
C.长期饮用硬度极低的软水,对人体的健康有利
D.目前使用离子交换法软化硬水比较普遍【解析】选D。溶有较多量的Ca2+和Mg2+的水叫作硬水,溶有少量或不含Ca2+和Mg2+的水叫作软水,因此A项不正确;水垢的主要成分是CaCO3和Mg(OH)2,因此B项不正确;长期饮用硬度极低的水可能会导致人体内缺乏某些元素,不利于身体健康,因此C项不正确。知识点2 水质评价与污水处理
【自主认知】
1.水质检测:
(1)常见的检测项目:水温、pH、导电率、___________、溶解氧
(DO)、化学需氧量(COD)、________________、一些有毒有害物质的
浓度等。
(2)测定水体的pH:先用广范pH试纸测得水样大致的pH范围,然后用
___________测得水样的pH。固体悬浮物生化需氧量(BOD)精密pH试纸(3)生物化学需氧量(BOD):单位体积水中耗氧有机物生化分解过程所
需消耗的氧气量(以mg·L-1为单位)。
2.污水处理:污水处理方法包括物理方法、化学方法和生物方法,其
中化学方法包括_______、___________、_______等。中和法氧化还原法沉淀法3.污水处理方法中的化学原理:【释疑解惑】
1.混凝剂的净水原理:混凝剂中的Al3+、Fe3+等水解生成氢氧化铝胶
体或氢氧化铁胶体,吸附水中的悬浮物而沉降,从而达到净水目的,
如Fe3++3H2O Fe(OH)3(胶体)+3H+。
2.杀菌消毒原理:杀菌消毒是利用消毒剂使蛋白质变性的原理,一些
强氧化剂、重金属盐、高温等都可使蛋白质变性。常见氧化剂如漂白
粉、液氯、二氧化氯、臭氧等;重金属盐的离子如Cu2+、Hg2+、Cd2+、
Ni2+等。【即时训练】
1.(2015·广州高二检测)如图是某市污水处理的工艺流程示意图:(1)污水处理的主要方法有①中和法;②化学沉淀法;③氧化还原法;④过滤法。其中属于化学方法的是 。
A.①②③ B.①②④
C.②③④ D.①②③④
(2)常用的混凝剂可以是 (任填一种混凝剂的名称)。
(3)加入熟石灰的目的是 ,
写出相关的化学方程式: 。
(4)加入Na2S的作用是 。【解析】过滤法属于物理方法,其他三种方法都属于化学方法。根据污水中的成分选择处理方法和所用试剂。水处理过程中常用的混凝剂有硫酸铝[Al2(SO4)3]、明矾[KAl(SO4)2·12H2O]、聚羟基氯化铝、聚丙烯酰胺等。该污水中含有H+和Hg2+,加入熟石灰目的是中和酸性废水,加入Na2S的目的是将Hg2+转化成HgS沉淀。答案:(1)A
(2)明矾(其他合理答案也可)
(3)中和酸性废水 Ca(OH)2+2HCl====CaCl2+2H2O
(4)除去Hg2+2.工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法类别都正确的是 ( )【解析】选C。处理酸性污水,应用生石灰中和,属于化学方法;处理含Cu2+等重金属离子污水,一般加S2-生成沉淀,属于化学方法;处理含苯废水,用活性炭吸附,属于物理方法;处理含纯碱的废水,应加入适量的酸处理,属于化学方法。【互动探究】(1)用混凝剂Al2(SO4)3净水时,只发生物理变化,没有
化学变化,这种说法正确吗?
提示:不正确。因为Al2(SO4)3净水时,Al3+发生水解反应:Al3++3H2O
Al(OH)3(胶体)+3H+,此过程是化学过程;Al(OH)3胶体吸附水
中的悬浮物质发生沉降是物理过程。
(2)若污水中含有油类、氰化物应该用什么方法处理?
提示:可用氧化还原反应将其除去。【补偿训练】1.(2015·芜湖高二检测)某黄金冶炼公司在处理尾矿废液过程中,发生有毒HCN外逸事故,造成人员中毒。已知HCN是一种无色剧毒气体,接触皮肤或通过呼吸道吸入均会造成严重的中毒或死亡,HCN在明火或强光条件下易燃或易爆。它是一种极弱、易挥发的酸。结合以上信息,判断下列说法中错误的是 ( )
A.为了防止冶金络合剂氰化钠产生HCN,废液排放前应加入足量石灰
B.检查HCN外逸时,必须穿特制防护服,并用特制的手电筒
C.河水有自净能力,冶金废水可直接排放到河流中进行稀释、降解
D.实验室配制氰化钠溶液时,最好在通风橱中进行【解析】选C。HCN是酸性物质,有剧毒,可被碱性物质石灰吸收,与其接触一定要加强自身保护,以防中毒。HCN排放到河水中不能很快分解,会对河水产生严重污染。2.(2015·金华高二检测)如图甲所示,X河流经其工业城市Y市。其中a处在上游,d处在下游。根据市环保局监测站对X河流的水质检测结果,绘制成图乙。请根据图乙回答下列问题。(1)造成X河流污染的主要污染源最可能分布在 。
A.ab段 B.bc段
C.cd段 D.bd段
(2)列举造成X河流污染的三种可能的污染源? 。
(3)对c处水样进行检测,发现其中含有Cu2+等重金属离子。若要把铜离子变为单质铜回收,请写出两种回收的方法。
方法Ⅰ: ;
方法Ⅱ: 。(4)d处的污染程度明显降低,请从物理学、化学、生物学三方面简单分析其原因? 。【解析】(1)根据图乙曲线可知,市区范围bc段污染程度最大,而在
市区上游ab段污染程度最小。(2)因该市为工业城市,故污染源应从
工业废水、生活污水及垃圾、废渣等方面考虑。(3)回收铜可采用置
换法(用铁置换铜)或还原法:Cu2+ Cu(OH)2 CuO
Cu。(4)河水在物理沉降、化学氧化、生物分解作用下,可自我净化。答案:(1)B
(2)工业污水排放造成的污染、生活污水排放造成的污染、生活垃圾造成的污染、酸雨造成的污染、工业废渣造成的污染等(填其中三项即可)(3)还原法:Cu2++2OH-====Cu(OH)2↓,
Cu(OH)2 CuO+H2O,
2CuO+C 2Cu+CO2↑
置换法:Fe+Cu2+====Fe2++Cu(其他答案合理也可)
(4)河水在物理沉降、化学氧化、生物分解作用下,可自我净化
水资源的合理利用知识点1 生活中的饮用水
【自主认知】
一、天然水中的杂质及城市自来水的获取
1.天然水中的杂质。
通常分为三类:_________、_________和_________。悬浮物质胶体物质溶解物质2.明矾的净水原理。
明矾溶于水后,铝离子发生_____,生成氢氧化铝胶体:_________
_______________________。
氢氧化铝胶体因吸附溶液中的阳离子而带正电荷。能吸附水中带负电荷的胶粒,并使杂质与氢氧化铝胶体一起凝聚而沉降。 水解Al3++3H2O Al(OH)3(胶体)+3H+3.城市自来水获取的步骤:混凝剂沉淀悬浮物活性炭异味二、硬水及其软化
1.有关概念。
硬水:含有_______________的水。
软水:不含或含少量___________的水。
硬水的软化:硬水软化的目的是减小水中_________________。较多钙、镁离子钙、镁离子钙、镁离子的浓度2.硬水软化的方法:
(1)煮沸法。
若硬水中的钙、镁离子以_________的形式存在时,可通过煮沸使钙、镁离子转化为沉淀。
反应的化学方程式为
______________________________,
_______________________________,
__________________________。 碳酸氢盐Ca(HCO3)2 CaCO3↓+CO2↑+H2OMg(HCO3)2 MgCO3↓+CO2↑+H2OMgCO3+H2O Mg(OH)2+CO2↑(2)离子交换法。
①用磺化煤软化硬水的原理(用反应方程式表示):
_____________________,
_____________________。
②磺化煤再生的原理:
CaR2+2Na+====2NaR+Ca2+,
MgR2+2Na+====2NaR+Mg2+。2NaR+Ca2+====CaR2+2Na+2NaR+Mg2+====MgR2+2Na+3.终端净水:
(1)水的二次污染:由于管道老化,储存水箱较脏,水箱内壁防腐材料不合格等引起的污染。
(2)终端净水及其优点。
①终端净水:在家中的出水点前加装净水设备。
②优点:能消除_________,使饮用水更安全。二次污染【释疑解惑】
1.硬水和软水的鉴别方法。
方法1:分别用两只烧杯取等量水样,向两只烧杯中分别滴加等量肥皂水。泡沫多、浮渣少的为软水;反之,为硬水。
方法2:用烧杯加热,在杯壁留下较多水垢的是硬水。因为硬水是含有较多的可溶性钙、镁物质的水,加热后,这些可溶性的钙、镁物质转化成不可溶的物质。
方法3:取一干净、干燥的玻璃片,分别在不同的位置滴等量水样。待其完全蒸发后,白色残留物多的为硬水;反之为软水。2.自来水的制取过程:【即时训练】
1.(2015·镇江高二检测)为了获取大量的生活饮用水,自来水厂需要用适宜、高效的方法和流程将天然水悬浮物、致病细菌等有害成分降低到规定的含量。
(1)要达到上述目的,一般要经过的基本步骤是①沉降、②______、③曝气、④ 。“曝气”的主要目的是 。
(2)在第①步中,下列物质可以使用的是 (用字母填空)。
A.明矾 B.膨润土 C.烧碱(3)在将天然水制成生活饮用水的过程中,水中不需要除去的成分是_________(至少答出一项)。
(4)经过上述四个步骤的处理之后,如果水中Ca2+、Mg2+的含量超标,还要将水进行 。 【解析】沉降之后必然是过滤。加消毒剂也是必不可少的步骤之一。“曝气”就是使水暴露在空气中,使水与空气接触的面积增大,增加水中的含氧量,以加速水中有机物的分解。明矾可作水的混凝剂,膨润土可作水的辅助混凝剂。对人体有益的矿物质等最好不要除去。降低水中Ca2+、Mg2+含量的过程叫作硬水的软化。
答案:(1)过滤 消毒 增加水中的含氧量,加速水中有机物的分解
(2)A、B (3)对人体有益的矿物质等
(4)软化2.(1)为了提高生活用水的卫生标准,自来水厂同时使用Cl2和FeSO4·7H2O对水进行消毒、净化,以改善水质,其原因是_______
, 。
(2)为了延长液氯的杀菌时间,某些自来水厂在用液氯进行消毒处理时,还加入少量液氨,其反应的化学方程式为NH3+HClOH2O+NH2Cl(一氯氨)。已知NH2Cl比HClO稳定,试分析加液氨能延长液氯杀菌时间的原因是? 。【解析】(1)Cl2的作用有两点:一是与H2O反应生成HClO,杀菌消毒;二是将Fe2+氧化成Fe3+,Fe3+水解生成Fe(OH)3胶体,吸附水中悬浮物。
(2)NH3+HClO H2O+NH2Cl是可逆反应,存在平衡,解题时要善于捕捉题目信息,由于NH2Cl比HClO稳定,因此在自来水中加入液氯,再加入液氨,上述平衡右移,随着HClO的杀菌,被消耗,浓度降低,平衡左移,所以可延长杀菌时间。答案:(1)Cl2溶于水生成的HClO能杀菌消毒
Cl2能氧化Fe2+为Fe3+,Fe3+的水解产物Fe(OH)3胶体可以吸附水中杂质
(2)HClO+NH3 H2O+NH2Cl,把不稳定的HClO转化为较稳定的NH2Cl,
消毒时,随HClO浓度降低,平衡向左移动,HClO得到补充【互动探究】
(1)题1(2)中的明矾的化学式是什么?明矾净水的原理是什么?
提示:明矾的化学式为KAl(SO4)2·12H2O,明矾净水的原理是明矾溶于水电离出Al3+,Al3+水解生成氢氧化铝胶体,能凝聚水中的悬浮物和吸附杂质。(2)自来水中含有少量余氯,在水管中停留可以起到有效的杀菌作用,故自来水厂杀菌消毒时充入的Cl2越多越好。这种说法对吗?为什么?
提示:不对。因为Cl2有毒,过量的Cl2会使自来水不适宜人饮用,而且还容易与水中的有机物反应,生成有毒的氯代烃。【补偿训练】1.以下是原水处理成自来水的工艺流程示意图。
(1)原水中含Ca2+、Mg2+、HC、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干反应,写出其中一个离子方程式:? 。(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂。它的
氧化性比KMnO4还强,反应中 被还原为Fe3+。
①已知高铁酸钠的制备反应如下:
2Fe(NO3)3+16NaOH+3Cl2====2Na2FeO4+6NaNO3+6NaCl+8H2O,则反应中
元素被氧化,反应中生成2 mol Na2FeO4转移电子物质的量
为 mol。
②高铁酸钠之所以能净水,除了能消毒杀菌外,另一个原因是
? 。 (3)通入二氧化碳的目的是? 和 。
(4)气体A的作用是 。
这种作用是基于气体A和水反应的产物具有? 性。
(5)下列物质中, 可以作为气体A的代用品。
①Ca(ClO)2 ②浓氨水 ③浓硫酸 ④SO2【解析】(1)Ca(OH)2可以与Mg2+发生反应:
Mg2++2OH-====Mg(OH)2↓;也可以与Mg2+、 发生反应:Mg2++
2 +4OH-+2Ca2+====Mg(OH)2↓+2CaCO3↓+2H2O;还可以与
发生反应:Ca2++ +OH-====CaCO3↓+H2O。
(2)①根据反应可知,反应过程中 铁元素化合
价升高,被氧化。根据2Fe(NO3)3 2Na2FeO4,故生成2 mol
Na2FeO4转移6 mol电子。
②Na2FeO4在净水时被还原为Fe3+,Fe3+能发生水解,生成Fe(OH)3胶
体,故可以作混凝剂,吸附水中杂质。(3)因为加入的CaO是过量的,溶液中Ca2+和OH-过量,通入CO2不仅能将多余的Ca2+生成沉淀,还能与OH-反应,调节溶液的pH,有利于沉淀的生成。
(4)原水处理成自来水一般经沉淀→过滤→吸附→杀菌消毒四步,题中流程中已经有了沉淀和过滤两步,而吸附一般是用活性炭固体,此处通入A只能是杀菌消毒,杀菌消毒一般用Cl2,Cl2与水反应生成HCl和HClO,HClO具有强氧化性,可以用来杀菌消毒。(5)气体A起杀菌消毒作用是因为与水反应生成的物质具有强氧化性,因此代用品也应具有强氧化性,①可以,②④没有强氧化性,③虽具有强氧化性,但不能用于饮用水的消毒。答案:(1)Mg2++2OH-====Mg(OH)2↓
[或Mg2++2 +2Ca2++4OH-====Mg(OH)2↓+2CaCO3↓+2H2O或
Ca2++ +OH-====CaCO3↓+H2O](任选一个即可)
(2)①铁 6
②还原产物Fe3+发生水解,生成Fe(OH)3胶体,能吸附杂质并沉降
(3)除去Ca2+ 调节pH
(4)杀菌消毒 强氧化
(5)①2.(2015·四平高二检测)有关硬水及其软化,下列说法正确的是
( )
A.含有Ca2+、Mg2+的水称为硬水
B.长期烧煮硬水的容器底部沉积的水垢主要成分是CaO和MgCO3
C.长期饮用硬度极低的软水,对人体的健康有利
D.目前使用离子交换法软化硬水比较普遍【解析】选D。溶有较多量的Ca2+和Mg2+的水叫作硬水,溶有少量或不含Ca2+和Mg2+的水叫作软水,因此A项不正确;水垢的主要成分是CaCO3和Mg(OH)2,因此B项不正确;长期饮用硬度极低的水可能会导致人体内缺乏某些元素,不利于身体健康,因此C项不正确。知识点2 水质评价与污水处理
【自主认知】
1.水质检测:
(1)常见的检测项目:水温、pH、导电率、___________、溶解氧
(DO)、化学需氧量(COD)、________________、一些有毒有害物质的
浓度等。
(2)测定水体的pH:先用广范pH试纸测得水样大致的pH范围,然后用
___________测得水样的pH。固体悬浮物生化需氧量(BOD)精密pH试纸(3)生物化学需氧量(BOD):单位体积水中耗氧有机物生化分解过程所
需消耗的氧气量(以mg·L-1为单位)。
2.污水处理:污水处理方法包括物理方法、化学方法和生物方法,其
中化学方法包括_______、___________、_______等。中和法氧化还原法沉淀法3.污水处理方法中的化学原理:【释疑解惑】
1.混凝剂的净水原理:混凝剂中的Al3+、Fe3+等水解生成氢氧化铝胶
体或氢氧化铁胶体,吸附水中的悬浮物而沉降,从而达到净水目的,
如Fe3++3H2O Fe(OH)3(胶体)+3H+。
2.杀菌消毒原理:杀菌消毒是利用消毒剂使蛋白质变性的原理,一些
强氧化剂、重金属盐、高温等都可使蛋白质变性。常见氧化剂如漂白
粉、液氯、二氧化氯、臭氧等;重金属盐的离子如Cu2+、Hg2+、Cd2+、
Ni2+等。【即时训练】
1.(2015·广州高二检测)如图是某市污水处理的工艺流程示意图:(1)污水处理的主要方法有①中和法;②化学沉淀法;③氧化还原法;④过滤法。其中属于化学方法的是 。
A.①②③ B.①②④
C.②③④ D.①②③④
(2)常用的混凝剂可以是 (任填一种混凝剂的名称)。
(3)加入熟石灰的目的是 ,
写出相关的化学方程式: 。
(4)加入Na2S的作用是 。【解析】过滤法属于物理方法,其他三种方法都属于化学方法。根据污水中的成分选择处理方法和所用试剂。水处理过程中常用的混凝剂有硫酸铝[Al2(SO4)3]、明矾[KAl(SO4)2·12H2O]、聚羟基氯化铝、聚丙烯酰胺等。该污水中含有H+和Hg2+,加入熟石灰目的是中和酸性废水,加入Na2S的目的是将Hg2+转化成HgS沉淀。答案:(1)A
(2)明矾(其他合理答案也可)
(3)中和酸性废水 Ca(OH)2+2HCl====CaCl2+2H2O
(4)除去Hg2+2.工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法类别都正确的是 ( )【解析】选C。处理酸性污水,应用生石灰中和,属于化学方法;处理含Cu2+等重金属离子污水,一般加S2-生成沉淀,属于化学方法;处理含苯废水,用活性炭吸附,属于物理方法;处理含纯碱的废水,应加入适量的酸处理,属于化学方法。【互动探究】(1)用混凝剂Al2(SO4)3净水时,只发生物理变化,没有
化学变化,这种说法正确吗?
提示:不正确。因为Al2(SO4)3净水时,Al3+发生水解反应:Al3++3H2O
Al(OH)3(胶体)+3H+,此过程是化学过程;Al(OH)3胶体吸附水
中的悬浮物质发生沉降是物理过程。
(2)若污水中含有油类、氰化物应该用什么方法处理?
提示:可用氧化还原反应将其除去。【补偿训练】1.(2015·芜湖高二检测)某黄金冶炼公司在处理尾矿废液过程中,发生有毒HCN外逸事故,造成人员中毒。已知HCN是一种无色剧毒气体,接触皮肤或通过呼吸道吸入均会造成严重的中毒或死亡,HCN在明火或强光条件下易燃或易爆。它是一种极弱、易挥发的酸。结合以上信息,判断下列说法中错误的是 ( )
A.为了防止冶金络合剂氰化钠产生HCN,废液排放前应加入足量石灰
B.检查HCN外逸时,必须穿特制防护服,并用特制的手电筒
C.河水有自净能力,冶金废水可直接排放到河流中进行稀释、降解
D.实验室配制氰化钠溶液时,最好在通风橱中进行【解析】选C。HCN是酸性物质,有剧毒,可被碱性物质石灰吸收,与其接触一定要加强自身保护,以防中毒。HCN排放到河水中不能很快分解,会对河水产生严重污染。2.(2015·金华高二检测)如图甲所示,X河流经其工业城市Y市。其中a处在上游,d处在下游。根据市环保局监测站对X河流的水质检测结果,绘制成图乙。请根据图乙回答下列问题。(1)造成X河流污染的主要污染源最可能分布在 。
A.ab段 B.bc段
C.cd段 D.bd段
(2)列举造成X河流污染的三种可能的污染源? 。
(3)对c处水样进行检测,发现其中含有Cu2+等重金属离子。若要把铜离子变为单质铜回收,请写出两种回收的方法。
方法Ⅰ: ;
方法Ⅱ: 。(4)d处的污染程度明显降低,请从物理学、化学、生物学三方面简单分析其原因? 。【解析】(1)根据图乙曲线可知,市区范围bc段污染程度最大,而在
市区上游ab段污染程度最小。(2)因该市为工业城市,故污染源应从
工业废水、生活污水及垃圾、废渣等方面考虑。(3)回收铜可采用置
换法(用铁置换铜)或还原法:Cu2+ Cu(OH)2 CuO
Cu。(4)河水在物理沉降、化学氧化、生物分解作用下,可自我净化。答案:(1)B
(2)工业污水排放造成的污染、生活污水排放造成的污染、生活垃圾造成的污染、酸雨造成的污染、工业废渣造成的污染等(填其中三项即可)(3)还原法:Cu2++2OH-====Cu(OH)2↓,
Cu(OH)2 CuO+H2O,
2CuO+C 2Cu+CO2↑
置换法:Fe+Cu2+====Fe2++Cu(其他答案合理也可)
(4)河水在物理沉降、化学氧化、生物分解作用下,可自我净化
