离子反应讲课说课高一上学期化学人教版(2019)必修第一册(共22张PPT)
文档属性
| 名称 | 离子反应讲课说课高一上学期化学人教版(2019)必修第一册(共22张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 11.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-03 00:00:00 | ||
图片预览



文档简介
(共22张PPT)
离子反应
烧水壶用一段时间之后,会有一 层厚厚的水垢
水垢如果不去除会对烧水壶导热 产生一定的影响,并且对我们的 健康也会有一定的危害,通常可 以用醋来去除水垢,这是什么原 因呢
接下来就让我们一起来探究这其 中的原理和奥秘
生活现象
实验 向硫酸钠溶液中滴加氯化 钾溶液
向硫酸钠溶液中滴加氯化钡溶
液
现象 无明显现象
有白色沉淀产生
反应物 KCl Na SO
BaCl Na SO
是否反应 否
是
产物
BaSO J
化学反应方程式
BaCl +Na SO =BaSO J+2NaCl
宏观分析
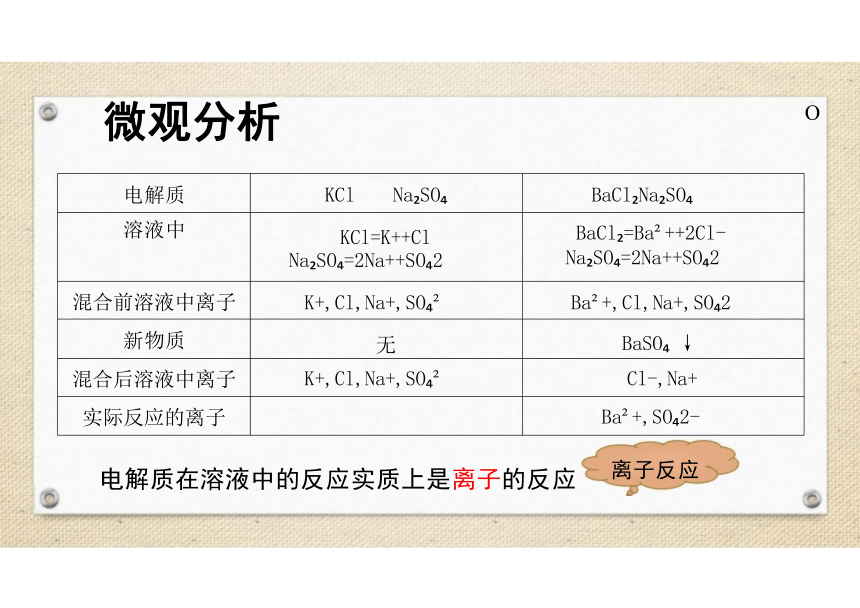
电解质 KCl Na SO
BaCl Na SO
溶液中 KCl=K++Cl Na SO =2Na++SO 2
BaCl =Ba ++2Cl-
Na SO =2Na++SO 2
混合前溶液中离子 K+,Cl,Na+,SO
Ba +,Cl,Na+,SO 2
新物质 无
BaSO ↓
混合后溶液中离子 K+,Cl,Na+,SO
Cl-,Na+
实际反应的离子
Ba +,SO 2-
电解质在溶液中的反应实质上是离子的反应
离子反应
微观分析
O
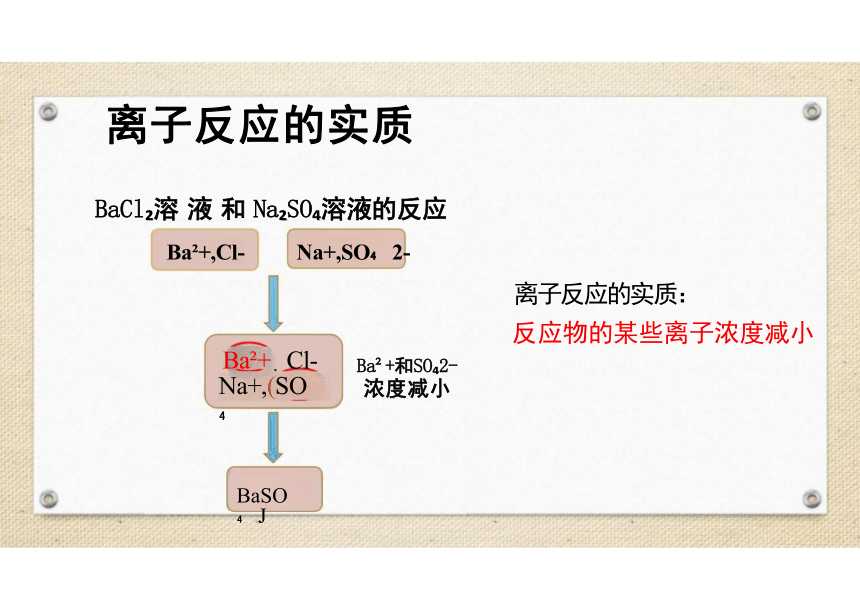
离子反应的实质
BaCl 溶 液 和 Na SO 溶液的反应
Ba +,Cl- Na+,SO 2-
离子反应的实质:
反应物的某些离子浓度减小
Ba + Cl- Na+,(SO
Ba +和SO 2- 浓度减小
BaSO J
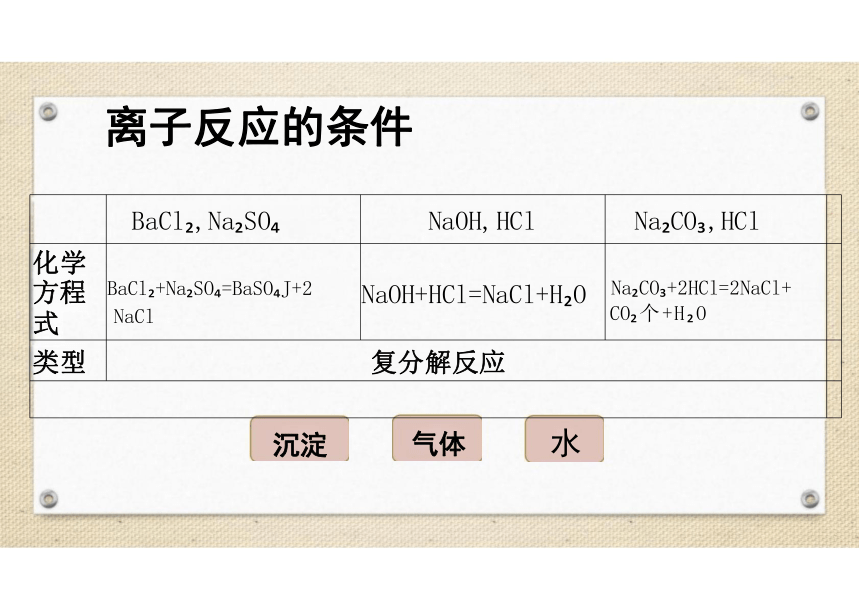
水
沉淀
气体
BaCl ,Na SO NaOH,HCl Na CO ,HCl
化学 方程 式 BaCl +Na SO =BaSO J+2 NaCl NaOH+HCl=NaCl+H O Na CO +2HCl=2NaCl+ CO 个+H O
类型 复分解反应
离子反应的条件
离子反应
本质 条件
总结
定义
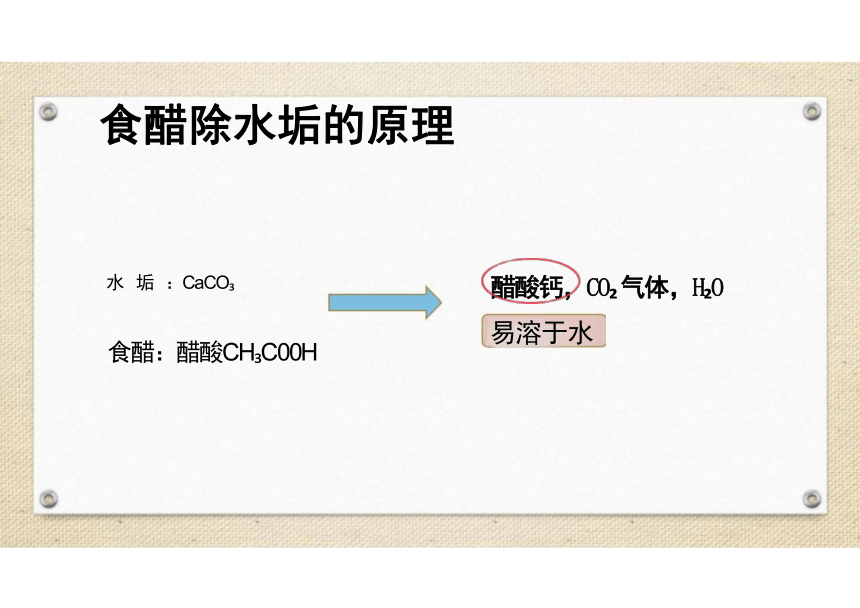
水 垢 :CaCO
食醋:醋酸CH C00H
食醋除水垢的原理
醋酸钙,CO 气体,H O
易溶于水
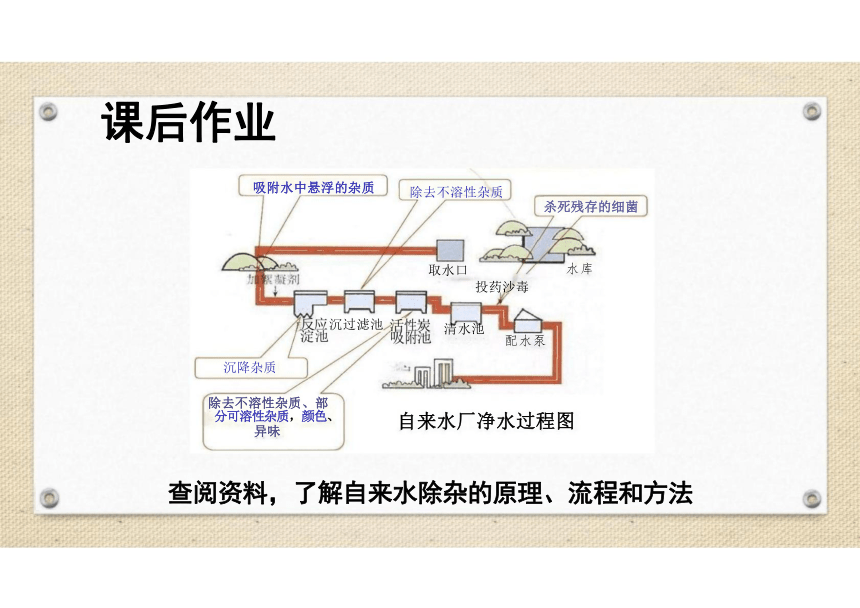
课后作业
吸附水中悬浮的杂质 除去不溶性杂质 杀死残存的细菌
沉过滤池 清水池
沉降杂质 用户
查阅资料,了解自来水除杂的原理、流程和方法
除去不溶性杂质、部
分可溶性杂质,颜色、
异味
自来水厂净水过程图
取水口
投药沙毒
配水泵
水库
离子反应说课
目录
01 教材分析
02 学情分析
03 教学目标
04 教学过程
05 板书设计
06 教学反思
选自人教版高中化学 必修一第一章第二节
揭示溶液中化学 反应的本质,巩 固前面学过的电 离初步知识
为后面元素化合 物知识电解质溶 液的学习奠定了 一定的基础
教材分析
学生已初步掌握电解质、电离等概 念,复分解反应相关知识,在初中 阶段具备一定的实验操作能力。
学生思维活跃,正处于由直观、形 象向逻辑、抽象思维的转变过程
学情分析
授课对象是高一年级的学生
知识储备
思维转变
密
通过对于溶液中离子移动和离子之间的 反应,形成离子反应的化学概念 重点
通过实验分析与总结,认识离子反应发 生的本质,以及复分解型离子反应的条 件。培养科学实验与探究意识 难点 通过生活中的问题,认识化学在生活中 的运用,并利用所学知识,解决生活中 的实际问题,增强社会责任感,养成科 学态度,培养责任担当。
宏观辨识与微观探析
证据推理与模型认知 变化观念与平衡思想 科学探究与创新意识 科学态度与社会责任
教学目标
教学过程
情景导入 实验分析
回归生活
探究总结
食醋除水垢导入
原理
问题导入
实验分析
对比实验:KCI溶液和Na SO 溶液 (BaCl 溶液和Na SO 溶液
观察现象 微观探析 探讨本质
宏观分析 引出概念
培养学生的宏观辨识与微观探 析的能力以及科学探究的精神
培养学生变化观念 和平衡思想的意识
NaOH和 HCI
Na CO 和 HCI
归纳所得产物
探究反应条件
培养学生证据推理与模型认知能力
探究总结
总结
探究
溶液
离子反应定义
本质和条件
吸 清水池
自来水厂净水过程图
池
炭
培养学生的科学态度与社会责任
回归生活
除去不溶性杂质
杀死残存的细菌
应沉
淀池
沉降杂质
除去不溶性杂质、部 分可溶性杂质,颜色、
异味
取水
投药游作
吸附水中悬浮的杂质
过滤池
配水泵
水库
本质 反应物某种离 子浓度减小
条件
有沉淀、气 体、水生成
BaCl 和Na SO 反 应
宏观:生成白色沉淀
微观:Ba +,SO 2-浓度减小
离子反应
离子反应
电解质
溶液中
离子
反应
改进
适当的增设与学生互动的环节,注重引 导学生,进一步了解学生知识掌握情况
教学设计具有逻辑性,教学思
路承上启下,联系生活实际
时间限制,讲授内容不够完
整,对学生了解不够确切
教学反思
亮 点
不 足
感谢聆听!
离子反应
烧水壶用一段时间之后,会有一 层厚厚的水垢
水垢如果不去除会对烧水壶导热 产生一定的影响,并且对我们的 健康也会有一定的危害,通常可 以用醋来去除水垢,这是什么原 因呢
接下来就让我们一起来探究这其 中的原理和奥秘
生活现象
实验 向硫酸钠溶液中滴加氯化 钾溶液
向硫酸钠溶液中滴加氯化钡溶
液
现象 无明显现象
有白色沉淀产生
反应物 KCl Na SO
BaCl Na SO
是否反应 否
是
产物
BaSO J
化学反应方程式
BaCl +Na SO =BaSO J+2NaCl
宏观分析
电解质 KCl Na SO
BaCl Na SO
溶液中 KCl=K++Cl Na SO =2Na++SO 2
BaCl =Ba ++2Cl-
Na SO =2Na++SO 2
混合前溶液中离子 K+,Cl,Na+,SO
Ba +,Cl,Na+,SO 2
新物质 无
BaSO ↓
混合后溶液中离子 K+,Cl,Na+,SO
Cl-,Na+
实际反应的离子
Ba +,SO 2-
电解质在溶液中的反应实质上是离子的反应
离子反应
微观分析
O
离子反应的实质
BaCl 溶 液 和 Na SO 溶液的反应
Ba +,Cl- Na+,SO 2-
离子反应的实质:
反应物的某些离子浓度减小
Ba + Cl- Na+,(SO
Ba +和SO 2- 浓度减小
BaSO J
水
沉淀
气体
BaCl ,Na SO NaOH,HCl Na CO ,HCl
化学 方程 式 BaCl +Na SO =BaSO J+2 NaCl NaOH+HCl=NaCl+H O Na CO +2HCl=2NaCl+ CO 个+H O
类型 复分解反应
离子反应的条件
离子反应
本质 条件
总结
定义
水 垢 :CaCO
食醋:醋酸CH C00H
食醋除水垢的原理
醋酸钙,CO 气体,H O
易溶于水
课后作业
吸附水中悬浮的杂质 除去不溶性杂质 杀死残存的细菌
沉过滤池 清水池
沉降杂质 用户
查阅资料,了解自来水除杂的原理、流程和方法
除去不溶性杂质、部
分可溶性杂质,颜色、
异味
自来水厂净水过程图
取水口
投药沙毒
配水泵
水库
离子反应说课
目录
01 教材分析
02 学情分析
03 教学目标
04 教学过程
05 板书设计
06 教学反思
选自人教版高中化学 必修一第一章第二节
揭示溶液中化学 反应的本质,巩 固前面学过的电 离初步知识
为后面元素化合 物知识电解质溶 液的学习奠定了 一定的基础
教材分析
学生已初步掌握电解质、电离等概 念,复分解反应相关知识,在初中 阶段具备一定的实验操作能力。
学生思维活跃,正处于由直观、形 象向逻辑、抽象思维的转变过程
学情分析
授课对象是高一年级的学生
知识储备
思维转变
密
通过对于溶液中离子移动和离子之间的 反应,形成离子反应的化学概念 重点
通过实验分析与总结,认识离子反应发 生的本质,以及复分解型离子反应的条 件。培养科学实验与探究意识 难点 通过生活中的问题,认识化学在生活中 的运用,并利用所学知识,解决生活中 的实际问题,增强社会责任感,养成科 学态度,培养责任担当。
宏观辨识与微观探析
证据推理与模型认知 变化观念与平衡思想 科学探究与创新意识 科学态度与社会责任
教学目标
教学过程
情景导入 实验分析
回归生活
探究总结
食醋除水垢导入
原理
问题导入
实验分析
对比实验:KCI溶液和Na SO 溶液 (BaCl 溶液和Na SO 溶液
观察现象 微观探析 探讨本质
宏观分析 引出概念
培养学生的宏观辨识与微观探 析的能力以及科学探究的精神
培养学生变化观念 和平衡思想的意识
NaOH和 HCI
Na CO 和 HCI
归纳所得产物
探究反应条件
培养学生证据推理与模型认知能力
探究总结
总结
探究
溶液
离子反应定义
本质和条件
吸 清水池
自来水厂净水过程图
池
炭
培养学生的科学态度与社会责任
回归生活
除去不溶性杂质
杀死残存的细菌
应沉
淀池
沉降杂质
除去不溶性杂质、部 分可溶性杂质,颜色、
异味
取水
投药游作
吸附水中悬浮的杂质
过滤池
配水泵
水库
本质 反应物某种离 子浓度减小
条件
有沉淀、气 体、水生成
BaCl 和Na SO 反 应
宏观:生成白色沉淀
微观:Ba +,SO 2-浓度减小
离子反应
离子反应
电解质
溶液中
离子
反应
改进
适当的增设与学生互动的环节,注重引 导学生,进一步了解学生知识掌握情况
教学设计具有逻辑性,教学思
路承上启下,联系生活实际
时间限制,讲授内容不够完
整,对学生了解不够确切
教学反思
亮 点
不 足
感谢聆听!
