人教版九下化学第九单元课题1 溶液的形成(共33张PPT)
文档属性
| 名称 | 人教版九下化学第九单元课题1 溶液的形成(共33张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-01-07 00:00:00 | ||
图片预览









文档简介
课件33张PPT。第九单元 溶液 课题1
溶液的形成第一课时创设情景:
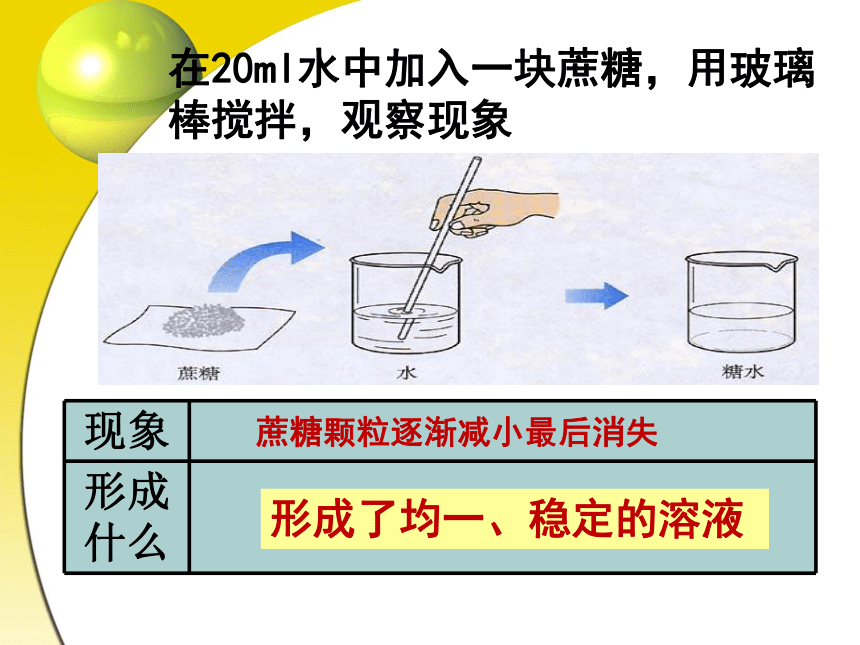
你生活中接触到的液体物质还有哪些? 这些液体物质都是混合物吗?它们是溶液吗?海洋是巨大的资源宝库,其中含有80多种元素海水是纯净物,还是混合物呢? 蔗糖颗粒逐渐减小最后消失形成了均一、稳定的溶液在20ml水中加入一块蔗糖,用玻璃棒搅拌,观察现象1、为什么这些固体会“消失”在水中?——分子在不停地运动蔗糖与氯化钠两种物质形成溶液后有什么区别与联系联系:两种溶液只要水分不被蒸发,温度不发生变化,蔗糖或氯化钠与水不会分离,取出其中任意一部分进行比较,它们的组成完全相同。区别蔗糖分散到水中食盐分散到水中形成蔗糖溶液形成食盐溶液蔗糖分子扩散到水分子的间隔之中。Na+和Cl- 扩散到水分子的间隔之中。探究思考:2、观察硫酸铜溶液颜色深浅是否各处相同?——溶液具有均一性3、形成溶液后,有固体与液体分离吗?——溶液具有稳定性 4、此时的溶液是纯净物还是混合物?——溶液是混合物通过上面的思考题,大家概括一下什么叫做溶液?1、定义:一种或几种物质分散到另一种物质
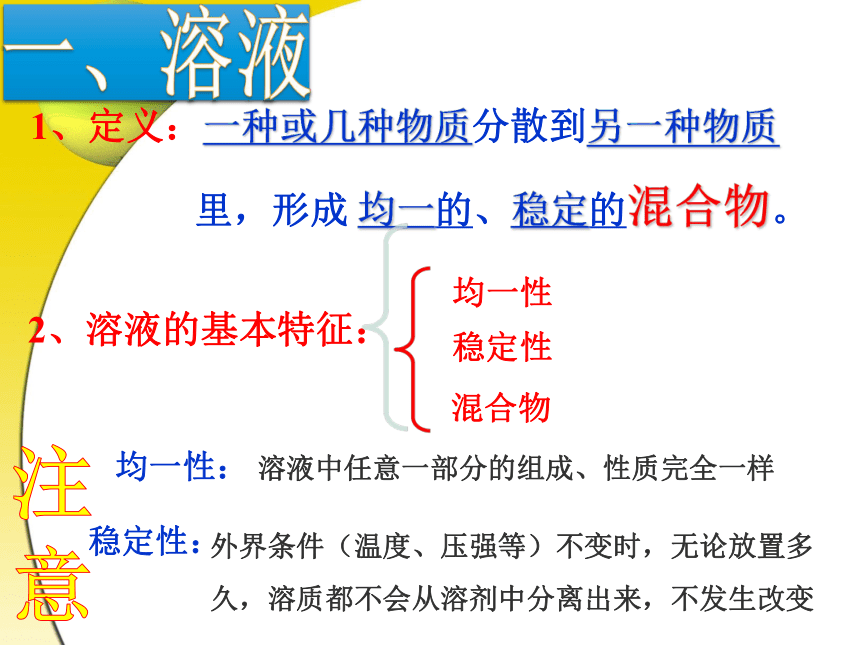
里,形成 均一的、稳定的混合物。 2、溶液的基本特征:一、溶液注
意关于溶液的认识(2)溶液一定是无色透明的吗?(3)均一、稳定的液体一定是溶液吗?(1)溶液的特征是什么?均一性、稳定性。不一定。如CuSO4溶液是蓝色的。不一定。如水就不是溶液、
酒精也不是溶液。能溶解其它物质的物质叫溶剂,水是最常见的溶剂
被溶解的物质叫溶质,可以是固体、液体、气体溶液是混合物,至少由两种物质组成。溶液质量=溶质质量+溶剂质量3、溶液的组成:
溶液体积 < 溶质体积 + 溶剂体积说明:
从微观上分析,溶液形成的过程是溶质的分子或离子分散到溶剂分子中的过程,因为粒子之间存在间隔,它们相互填充,所以溶液体积不等于溶质体积和溶剂体积之和。想一想:1、溶剂只可以是水吗?2、溶质可以是固体,还可以是?实验探究二:影响物质溶解性的因素有哪些?在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。 实验现象纪录碘几乎不溶,溶液略显棕黄色 碘溶解,溶液显棕色高锰酸钾溶解,溶液呈紫色高锰酸钾几乎不溶,溶液为无色物质的溶解性不仅与溶质有关,还与溶剂的性质有关。相同的溶质在不同的溶剂中溶解性不同
不同的溶质在相同的溶剂中溶解性不同探究实验三:水和乙醇能够互溶吗?不分层水和乙醇能够互溶试管里的液体出现了分层现象试管里的液体溶为一体,颜色均匀,不分层启示:溶液中溶质可以是多种!溶剂有多种(水、汽油、酒精等),水是一种最常用的溶剂,不指明溶剂的溶液,一般指的是水溶液。汽油也可能做溶剂,它可以溶解油脂——用汽油洗油污。酒精也可做溶剂,如溶解碘形成碘酒。
空气、合金也是溶液吗?分析与思考:它们具有均一性、稳定性、是混合物。因此是溶液!蔗糖水水食盐蔗糖的水溶液或蔗糖溶液食盐的水溶液或食盐溶液硫酸铜的水溶液或硫酸铜溶液水硫酸铜
练习与巩固:CuSO4 水H2SO4 水C2H5OH 水油脂汽油白磷二硫化碳HCl 水H2CO3 水碘(I2) 酒精汽油豆油酒精 水Ca(OH)2水(H2O )1、溶液是无色的。
2、无色、透明、澄清的液体就是溶液。
3、均一、稳定的液体一定是溶液。
4、把食盐溶液倒掉一半后,变稀了。
5、在温度不变,水不蒸发的条件下,
蔗糖溶液中蔗糖会从水中分离出来。 练习一:判断说明错!错!错!错!错! 课题1
溶液的形成第二课时探究实验四:洗涤剂在清洗油污时起的作用是什么?取两只试管,分别放入2~3mL水,再滴入几滴植物油;向其中一支试管中滴入几滴洗涤剂,振荡,观察现象;静置,观察现象;清洗,观察现象。分层分层浑浊浑浊分层不分层不干净干净植物油在水中形成的混合物是不均一、不稳定的,静置后会分层,混合物不稳定,但加了洗涤剂后可以稳定存在振 荡静 置1、乳浊液:小液滴分散到液体里形成的混合物叫做乳浊液。
乳浊液的特征:不稳定、不均一液体分层二、乳浊液和乳化现象2、乳化现象植物油大油滴洗涤剂分散成小油滴(乳化)水冲洗(乳浊液)随水流走用洗发剂洗去头发上的油脂用肥皂、洗衣粉洗去衣服上的污渍用洗涤剂洗餐具 洗涤剂具有乳化功能,加了洗涤剂后,乳浊液可以稳定存在! 1.洗涤剂有什么功能? 它的去污原理是什么?洗涤剂有乳化功能;洗涤剂的去污原理是:将油污分散成无数小液滴,然后随水流走。(这种现象称为洗涤剂的乳化作用。)2、修汽车的工人,当他的手上沾满油污时,他常用汽油洗去手上的油污.这说明汽油与洗涤剂一样能去油污,那么二者去油污的原理是否相同?若不同,汽油去油污的原理是什么?汽油去油污的原理是: 油污溶解在汽油中,形成溶液,从而除去油污.实验探究五:物质溶解时的热量变化 现有试管、烧杯、玻璃棒,温度计等仪器和固态NaCl、NH4NO3 、NaOH。
试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。温度基本不变温度降低温度升高物质溶解时可能吸热,也可能放热1、物质溶于水的过程吸收热量>放出热量,溶液温度降低 NH4NO3
吸收热量<放出热量,溶液温度升高 NaOH、CaO
吸收热量=放出热量,溶液温度不变 NaCl三、溶解时的吸热和放热现象2、溶解过程中温度变化的实质【典例精讲】
指出下列溶液中的溶质和溶剂。碘酒,稀硫酸,盐酸,酒精溶液
思路点拨:在溶液中,能溶解其他物质的物质叫做溶剂;被溶解的物质叫溶质。当固体、气体溶于液体时,固体、气体为溶质,液体作溶剂。如碘酒中碘为溶质,酒精为溶剂;盐酸中氯化氢气体为溶质,水为溶剂。两种液体互相溶解时,一般量少的一种作溶质,量多的一种作溶剂。但只要有水存在,水总作溶剂。
?
归纳:水是常用的溶剂,但生活中酒精有时也可做为溶剂。【易错易混提示】溶液和乳浊液是不同类别的混合物,溶液有均一、稳定的特性。达标检测1、下列与溶液有关的说法,正确的是( )
A.溶液均一稳定,且无色透明
B.一种溶液中只能含一种溶质
C.溶液中各部分的性质未必相同
D.如果外界条件不发生变化,食盐水溶液在密闭条件下久置也不会分离析出食盐晶体
2.物质在溶解时,溶液温度发生变化的原因是( )
A.吸收热量 B.放出热量
C.吸收热量等于放出热量 D.吸收热量和放出热量不相等
3.将下列物质分别混合后,经搅拌后得到的不是溶液的是( )
A.酒精中放入碘的晶体 B.水中放入蔗糖
C.水中放入细沙 D.汽油中放入油脂DCD达标检测4.一杯溶液里各部分的性质是( )
A.不相同的 B.相同的
C.上面跟下面不同 D.无法比较
5.把下列物质溶于适量的水中,溶液温度明显下降的是( )
A.硝酸铵 B.浓硫酸
C.氢氧化钠 D.食盐
6.下列说法不正确的是( )
A.当条件不变时,溶液放置时间稍长,溶质不会分离出来
B.溶液里各部分的性质是相同的
C.一种或一种以上的物质分散到另一种物质里形成的均一稳定的混合物叫溶液
D.凡是均匀、澄清、透明、稳定的液体就是溶液DAB
溶液的形成第一课时创设情景:
你生活中接触到的液体物质还有哪些? 这些液体物质都是混合物吗?它们是溶液吗?海洋是巨大的资源宝库,其中含有80多种元素海水是纯净物,还是混合物呢? 蔗糖颗粒逐渐减小最后消失形成了均一、稳定的溶液在20ml水中加入一块蔗糖,用玻璃棒搅拌,观察现象1、为什么这些固体会“消失”在水中?——分子在不停地运动蔗糖与氯化钠两种物质形成溶液后有什么区别与联系联系:两种溶液只要水分不被蒸发,温度不发生变化,蔗糖或氯化钠与水不会分离,取出其中任意一部分进行比较,它们的组成完全相同。区别蔗糖分散到水中食盐分散到水中形成蔗糖溶液形成食盐溶液蔗糖分子扩散到水分子的间隔之中。Na+和Cl- 扩散到水分子的间隔之中。探究思考:2、观察硫酸铜溶液颜色深浅是否各处相同?——溶液具有均一性3、形成溶液后,有固体与液体分离吗?——溶液具有稳定性 4、此时的溶液是纯净物还是混合物?——溶液是混合物通过上面的思考题,大家概括一下什么叫做溶液?1、定义:一种或几种物质分散到另一种物质
里,形成 均一的、稳定的混合物。 2、溶液的基本特征:一、溶液注
意关于溶液的认识(2)溶液一定是无色透明的吗?(3)均一、稳定的液体一定是溶液吗?(1)溶液的特征是什么?均一性、稳定性。不一定。如CuSO4溶液是蓝色的。不一定。如水就不是溶液、
酒精也不是溶液。能溶解其它物质的物质叫溶剂,水是最常见的溶剂
被溶解的物质叫溶质,可以是固体、液体、气体溶液是混合物,至少由两种物质组成。溶液质量=溶质质量+溶剂质量3、溶液的组成:
溶液体积 < 溶质体积 + 溶剂体积说明:
从微观上分析,溶液形成的过程是溶质的分子或离子分散到溶剂分子中的过程,因为粒子之间存在间隔,它们相互填充,所以溶液体积不等于溶质体积和溶剂体积之和。想一想:1、溶剂只可以是水吗?2、溶质可以是固体,还可以是?实验探究二:影响物质溶解性的因素有哪些?在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。 实验现象纪录碘几乎不溶,溶液略显棕黄色 碘溶解,溶液显棕色高锰酸钾溶解,溶液呈紫色高锰酸钾几乎不溶,溶液为无色物质的溶解性不仅与溶质有关,还与溶剂的性质有关。相同的溶质在不同的溶剂中溶解性不同
不同的溶质在相同的溶剂中溶解性不同探究实验三:水和乙醇能够互溶吗?不分层水和乙醇能够互溶试管里的液体出现了分层现象试管里的液体溶为一体,颜色均匀,不分层启示:溶液中溶质可以是多种!溶剂有多种(水、汽油、酒精等),水是一种最常用的溶剂,不指明溶剂的溶液,一般指的是水溶液。汽油也可能做溶剂,它可以溶解油脂——用汽油洗油污。酒精也可做溶剂,如溶解碘形成碘酒。
空气、合金也是溶液吗?分析与思考:它们具有均一性、稳定性、是混合物。因此是溶液!蔗糖水水食盐蔗糖的水溶液或蔗糖溶液食盐的水溶液或食盐溶液硫酸铜的水溶液或硫酸铜溶液水硫酸铜
练习与巩固:CuSO4 水H2SO4 水C2H5OH 水油脂汽油白磷二硫化碳HCl 水H2CO3 水碘(I2) 酒精汽油豆油酒精 水Ca(OH)2水(H2O )1、溶液是无色的。
2、无色、透明、澄清的液体就是溶液。
3、均一、稳定的液体一定是溶液。
4、把食盐溶液倒掉一半后,变稀了。
5、在温度不变,水不蒸发的条件下,
蔗糖溶液中蔗糖会从水中分离出来。 练习一:判断说明错!错!错!错!错! 课题1
溶液的形成第二课时探究实验四:洗涤剂在清洗油污时起的作用是什么?取两只试管,分别放入2~3mL水,再滴入几滴植物油;向其中一支试管中滴入几滴洗涤剂,振荡,观察现象;静置,观察现象;清洗,观察现象。分层分层浑浊浑浊分层不分层不干净干净植物油在水中形成的混合物是不均一、不稳定的,静置后会分层,混合物不稳定,但加了洗涤剂后可以稳定存在振 荡静 置1、乳浊液:小液滴分散到液体里形成的混合物叫做乳浊液。
乳浊液的特征:不稳定、不均一液体分层二、乳浊液和乳化现象2、乳化现象植物油大油滴洗涤剂分散成小油滴(乳化)水冲洗(乳浊液)随水流走用洗发剂洗去头发上的油脂用肥皂、洗衣粉洗去衣服上的污渍用洗涤剂洗餐具 洗涤剂具有乳化功能,加了洗涤剂后,乳浊液可以稳定存在! 1.洗涤剂有什么功能? 它的去污原理是什么?洗涤剂有乳化功能;洗涤剂的去污原理是:将油污分散成无数小液滴,然后随水流走。(这种现象称为洗涤剂的乳化作用。)2、修汽车的工人,当他的手上沾满油污时,他常用汽油洗去手上的油污.这说明汽油与洗涤剂一样能去油污,那么二者去油污的原理是否相同?若不同,汽油去油污的原理是什么?汽油去油污的原理是: 油污溶解在汽油中,形成溶液,从而除去油污.实验探究五:物质溶解时的热量变化 现有试管、烧杯、玻璃棒,温度计等仪器和固态NaCl、NH4NO3 、NaOH。
试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。温度基本不变温度降低温度升高物质溶解时可能吸热,也可能放热1、物质溶于水的过程吸收热量>放出热量,溶液温度降低 NH4NO3
吸收热量<放出热量,溶液温度升高 NaOH、CaO
吸收热量=放出热量,溶液温度不变 NaCl三、溶解时的吸热和放热现象2、溶解过程中温度变化的实质【典例精讲】
指出下列溶液中的溶质和溶剂。碘酒,稀硫酸,盐酸,酒精溶液
思路点拨:在溶液中,能溶解其他物质的物质叫做溶剂;被溶解的物质叫溶质。当固体、气体溶于液体时,固体、气体为溶质,液体作溶剂。如碘酒中碘为溶质,酒精为溶剂;盐酸中氯化氢气体为溶质,水为溶剂。两种液体互相溶解时,一般量少的一种作溶质,量多的一种作溶剂。但只要有水存在,水总作溶剂。
?
归纳:水是常用的溶剂,但生活中酒精有时也可做为溶剂。【易错易混提示】溶液和乳浊液是不同类别的混合物,溶液有均一、稳定的特性。达标检测1、下列与溶液有关的说法,正确的是( )
A.溶液均一稳定,且无色透明
B.一种溶液中只能含一种溶质
C.溶液中各部分的性质未必相同
D.如果外界条件不发生变化,食盐水溶液在密闭条件下久置也不会分离析出食盐晶体
2.物质在溶解时,溶液温度发生变化的原因是( )
A.吸收热量 B.放出热量
C.吸收热量等于放出热量 D.吸收热量和放出热量不相等
3.将下列物质分别混合后,经搅拌后得到的不是溶液的是( )
A.酒精中放入碘的晶体 B.水中放入蔗糖
C.水中放入细沙 D.汽油中放入油脂DCD达标检测4.一杯溶液里各部分的性质是( )
A.不相同的 B.相同的
C.上面跟下面不同 D.无法比较
5.把下列物质溶于适量的水中,溶液温度明显下降的是( )
A.硝酸铵 B.浓硫酸
C.氢氧化钠 D.食盐
6.下列说法不正确的是( )
A.当条件不变时,溶液放置时间稍长,溶质不会分离出来
B.溶液里各部分的性质是相同的
C.一种或一种以上的物质分散到另一种物质里形成的均一稳定的混合物叫溶液
D.凡是均匀、澄清、透明、稳定的液体就是溶液DAB
同课章节目录
