1.2.1电解质的电离 课件(共14张PPT)2024-2025学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 1.2.1电解质的电离 课件(共14张PPT)2024-2025学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 46.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-05 00:00:00 | ||
图片预览



文档简介
(共14张PPT)
电解质的电离
Ionization of electrolyte
刘琪
知识水平
··
教材位置
本次课程的内容在教材中位于人教版高中教科书必修一第一章第二节。
同学们刚刚升上高中,他们的认识情况,正在由具象认识转向抽象认识,可能对微观结构理解的不是很彻底。
认识水平
同学们在初中的时候已经接触过了,电解质的部分知识,有了一些模糊的概念。
环节一:新课导入
环节一:新课导入
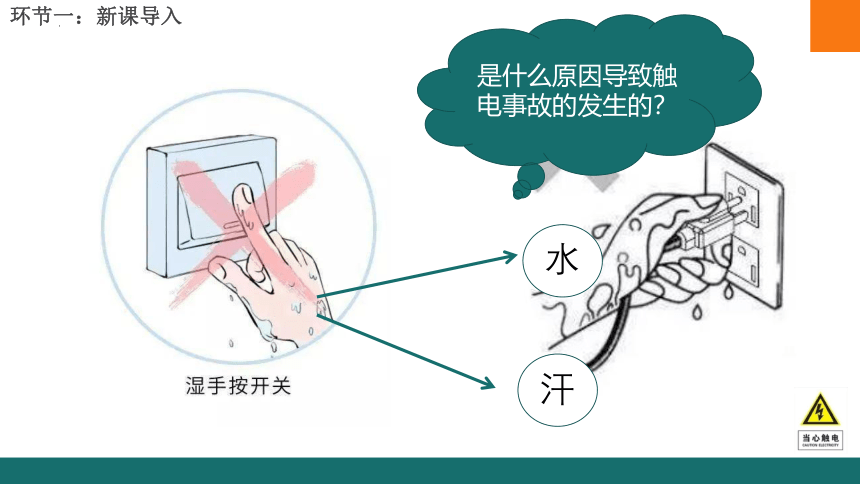
是什么原因导致触电事故的发生的?
水
汗
输入您的标题
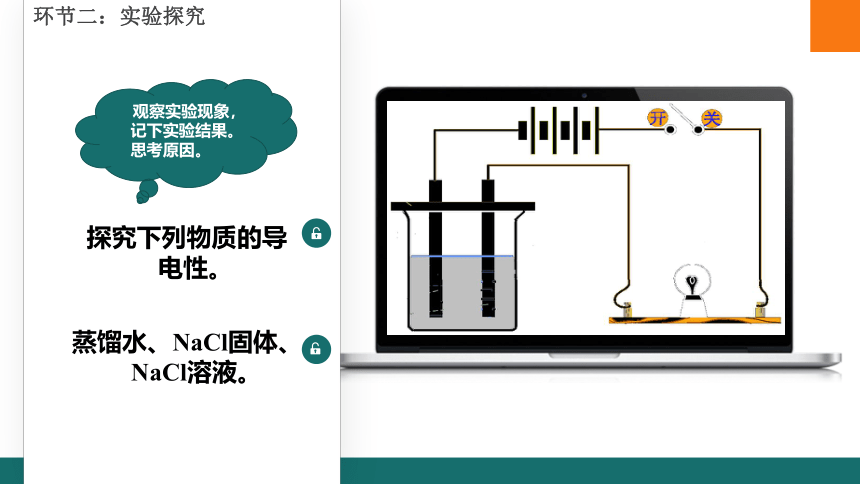
蒸馏水、NaCl固体、NaCl溶液。
探究下列物质的导电性。
观察实验现象,记下实验结果。思考原因。
环节二:实验探究
环节二:实验探究
NaCl固体
NaCl溶液
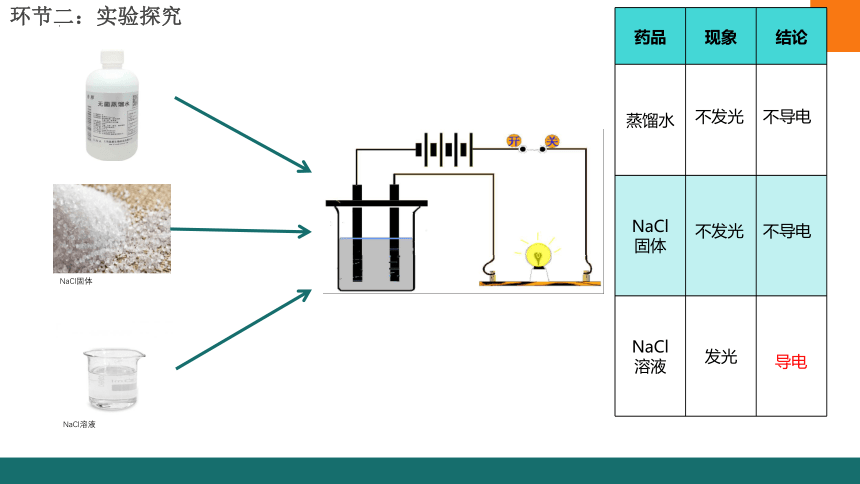
药品 现象 结论
蒸馏水
NaCl 固体
NaCl 溶液
不发光
不发光
发光
不导电
不导电
导电
铜和铁也可以导电,他么导电的原因是什么?
NaCl与他们的原因相同吗?
小组合作,思考并讨论
环节三:思考与讨论
NaCl溶液
实验探究3
NaCl溶液为什么能够导电?同学们观察并讨论。
NaCl溶液
实验探究
NaCl固体不导电,熔融的NaCl能导电吗?
这种在水溶液里或熔融状态下能导电的化合物叫做电解质。
纯净物
总结
实验探究2
NaCl固体为什么不导电?
综上所述,物质能否导电,取决于:
是否存在着自由移动的带电粒子。
人的手长上有汗水(含有NaCl溶液),存在自由移动的离子。因此,湿手直接接触电源容易发生触电事故!
NaCl固体中虽然有Na+和Cl-离子,但是它们按照一定的规则紧密的排列着,不能自由移动,所以固体NaCl不导电。
归纳总结
课下思考
1.同学们猜想熔融状态下的NaCl的微观结构,及导电原理
2.收集并记录电解质在生活中的应用。
谢谢观看
POWERPOINT TEMPLATE
刘琪
电解质的电离
Ionization of electrolyte
刘琪
知识水平
··
教材位置
本次课程的内容在教材中位于人教版高中教科书必修一第一章第二节。
同学们刚刚升上高中,他们的认识情况,正在由具象认识转向抽象认识,可能对微观结构理解的不是很彻底。
认识水平
同学们在初中的时候已经接触过了,电解质的部分知识,有了一些模糊的概念。
环节一:新课导入
环节一:新课导入
是什么原因导致触电事故的发生的?
水
汗
输入您的标题
蒸馏水、NaCl固体、NaCl溶液。
探究下列物质的导电性。
观察实验现象,记下实验结果。思考原因。
环节二:实验探究
环节二:实验探究
NaCl固体
NaCl溶液
药品 现象 结论
蒸馏水
NaCl 固体
NaCl 溶液
不发光
不发光
发光
不导电
不导电
导电
铜和铁也可以导电,他么导电的原因是什么?
NaCl与他们的原因相同吗?
小组合作,思考并讨论
环节三:思考与讨论
NaCl溶液
实验探究3
NaCl溶液为什么能够导电?同学们观察并讨论。
NaCl溶液
实验探究
NaCl固体不导电,熔融的NaCl能导电吗?
这种在水溶液里或熔融状态下能导电的化合物叫做电解质。
纯净物
总结
实验探究2
NaCl固体为什么不导电?
综上所述,物质能否导电,取决于:
是否存在着自由移动的带电粒子。
人的手长上有汗水(含有NaCl溶液),存在自由移动的离子。因此,湿手直接接触电源容易发生触电事故!
NaCl固体中虽然有Na+和Cl-离子,但是它们按照一定的规则紧密的排列着,不能自由移动,所以固体NaCl不导电。
归纳总结
课下思考
1.同学们猜想熔融状态下的NaCl的微观结构,及导电原理
2.收集并记录电解质在生活中的应用。
谢谢观看
POWERPOINT TEMPLATE
刘琪
