3.4第二课时 羧酸衍生物 课件(共23张PPT)2024-2025学年高二下学期化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.4第二课时 羧酸衍生物 课件(共23张PPT)2024-2025学年高二下学期化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-05 00:00:00 | ||
图片预览





文档简介
(共23张PPT)
第三章 烃的含氧衍生物
第四节 羧酸 羧酸衍生物
第二课时 羧酸衍生物
一.酯
1. 概念:
2. 官能团:
羧酸分子羧基中的—OH被—OR′取代后的产物,可简写为RCOOR′,R和R′可以相同,也可以不同。
酯基
O
=
—C-OR
或—COOR
3.分类:
根据分子中酯基的数目
酯
一元酯
二元酯
多元酯
有机酸酯
无机酸酯
根据生成酯的酸不同
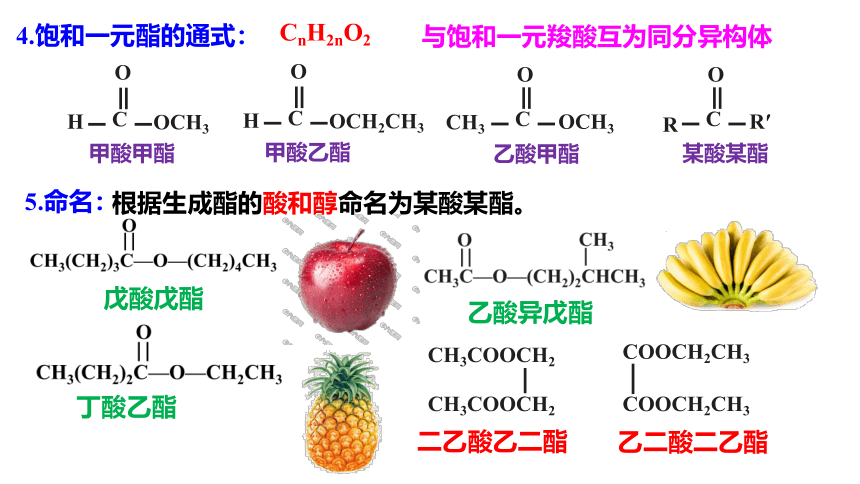
4.饱和一元酯的通式:
CnH2nO2
C
O
OCH3
H
甲酸甲酯
C
O
OCH2CH3
H
甲酸乙酯
C
O
OCH3
CH3
乙酸甲酯
C
O
R′
R
某酸某酯
与饱和一元羧酸互为同分异构体
根据生成酯的酸和醇命名为某酸某酯。
5.命名:
戊酸戊酯
乙酸异戊酯
丁酸乙酯
COOCH2CH3
COOCH2CH3
CH3COOCH2
CH3COOCH2
乙二酸二乙酯
二乙酸乙二酯
低级酯是具有芳香气味的液体,密度一般比水小,难溶于水,易溶于有机溶剂,许多酯也是常用的有机溶剂。
6.物理性质:
7.用途:
许多酯是常用的有机溶剂,酯类广泛存在于自然界,日常生活中的饮料、糖果和糕点等常使用酯类香料。
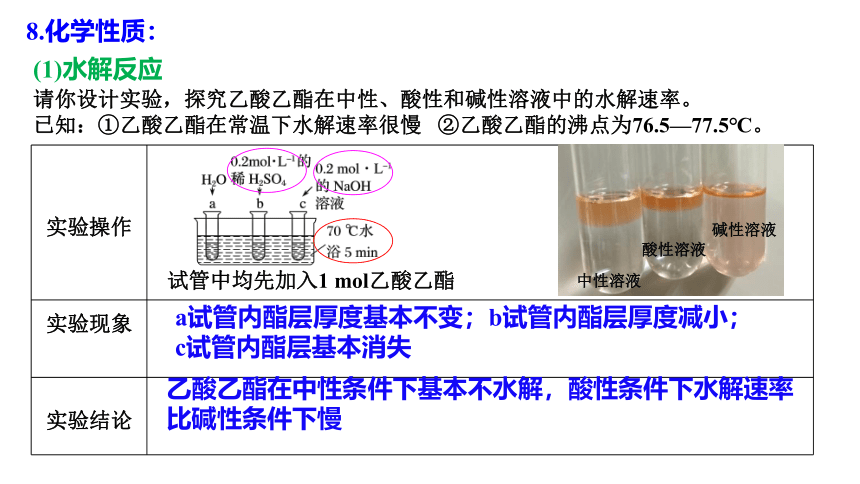
8.化学性质:
实验操作
实验现象
实验结论
a试管内酯层厚度基本不变;b试管内酯层厚度减小;c试管内酯层基本消失
乙酸乙酯在中性条件下基本不水解,酸性条件下水解速率比碱性条件下慢
中性溶液
碱性溶液
酸性溶液
试管中均先加入1 mol乙酸乙酯
(1)水解反应
请你设计实验,探究乙酸乙酯在中性、酸性和碱性溶液中的水解速率。
已知:①乙酸乙酯在常温下水解速率很慢 ②乙酸乙酯的沸点为76.5—77.5℃。
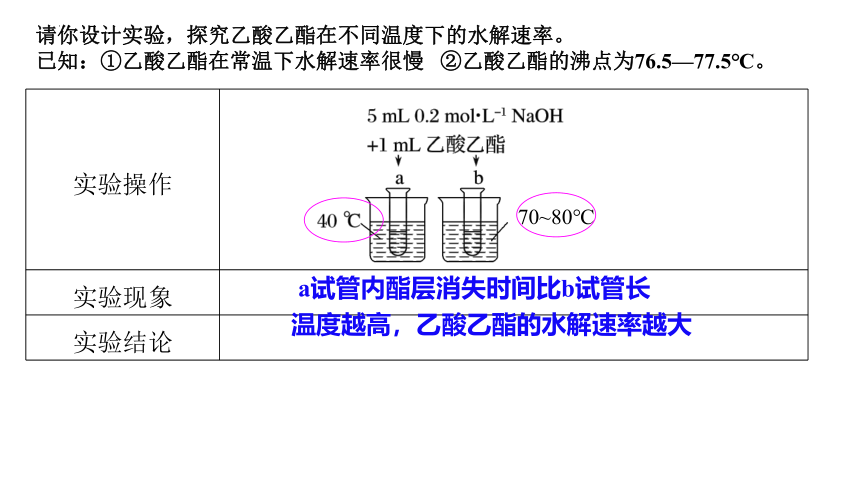
请你设计实验,探究乙酸乙酯在不同温度下的水解速率。
已知:①乙酸乙酯在常温下水解速率很慢 ②乙酸乙酯的沸点为76.5—77.5℃。
实验操作
实验现象
实验结论
a试管内酯层消失时间比b试管长
温度越高,乙酸乙酯的水解速率越大
70~80℃
【思考与讨论】
(1)为什么可以通过比较酯层消失的时间来判断水解速率的大小
因为羧基为亲水基,乙基为疏水基,所以乙酸易溶于水,乙酸乙酯在水中的溶解度较小。同时,乙酸乙酯的密度比水的小,酯层位于水层之上。故酯层消失即表示乙酸乙酯水解完全。
(2)为什么乙酸乙酯在酸性溶液中的水解速率大于中性溶液的水解速率?
无机酸作催化剂,加快反应速率。
(3)为什么乙酸乙酯在碱性溶液中能够水解完全(从平衡移动的角度进行分析)?
碱不仅起催化作用,而且能与水解生成的羧酸发生中和反应,使平衡右移,水解程度增大,直至完全。酯在碱性条件下的水解不可逆。
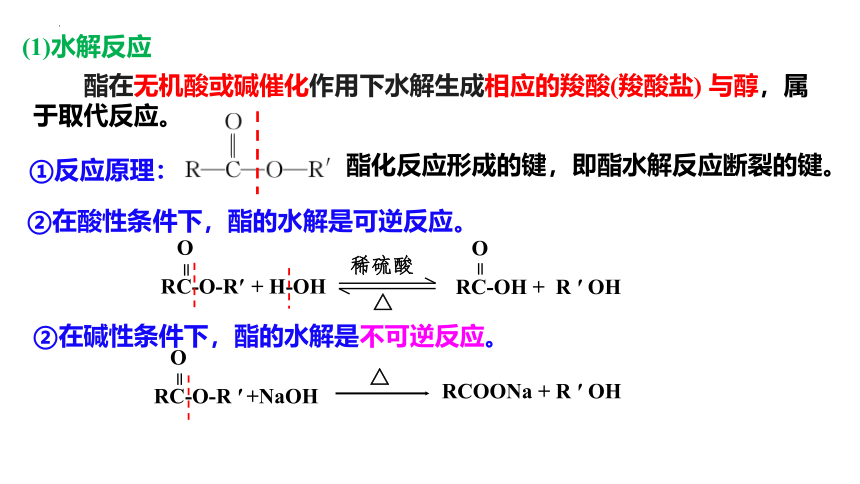
(1)水解反应
酯在无机酸或碱催化作用下水解生成相应的羧酸(羧酸盐) 与醇,属于取代反应。
①反应原理:
酯化反应形成的键,即酯水解反应断裂的键。
②在酸性条件下,酯的水解是可逆反应。
O
RC-O-R′ + H-OH
=
稀硫酸
△
O
RC-OH + R ′ OH
=
②在碱性条件下,酯的水解是不可逆反应。
O
RC-O-R ′ +NaOH
=
△
RCOONa + R ′ OH
酯化反应 酯的水解反应
反应关系
催化剂 浓硫酸 稀硫酸或NaOH溶液
催化剂的 其他作用 吸水、提高CH3COOH和C2H5OH的转化率 NaOH中和酯水解生成的羧酸、提高酯的水解效率
加热方式 酒精灯火焰加热 热水浴加热
反应类型 酯化反应、取代反应 水解反应、取代反应
酯化反应与酯的水解反应的比较
二.油脂
1.概念:
酯是由酸(有机羧酸或无机含氧酸)与醇相互作用失去水分子形成的一类化合物的总称。
油脂仅指高级脂肪酸与甘油所生成的酯,因而它是酯中特殊的一类物质。
2.结构:
R、R′、R″代表高级脂肪酸的烃基,可以相同也可以不同,可以是饱和烃基也可是是含碳碳双键的不饱和烃基。
油脂是由一分子甘油与三分子高级脂肪酸形成的酯,称为甘油三酯。
组成油脂的高级脂肪酸种类较多,其中以含16—18个碳原子的高级脂肪酸最为常见:
饱和高级脂肪酸:软脂酸(十六酸,棕榈酸) C15H31COOH
硬脂酸(十八酸) C17H35COOH
不饱和高级脂肪酸:油酸(9-十八碳烯酸) C17H33COOH
亚油酸(9,12-十八碳二烯酸) C17H31COOH
3.分类:
如果R、R‘、R’‘相同,称为 (简)单甘油酯(同酸甘油酯)
如果R、R‘、R’‘不同,称为混(合) 甘油酯(异酸甘油酯)
天然油脂大多数都是混甘油酯。
根据烃基是否饱和
油脂
根据烃基是否相同
饱和高级脂肪酸甘油酯
不饱和高级脂肪酸甘油酯
根据状态
油:常温下呈液态,如花生油、芝麻油、大豆油等植物油,含较多不饱和高级脂肪酸甘油酯。
脂肪:常温下呈固态,如牛油、羊油等动物油脂,含较多饱和高级脂肪酸甘油酯。
4.物理性质:
①色、味:纯净的油脂是无色、无味的,但一般因溶有维生素和色素等
而有颜色和气味。
②密度:比水小,黏度较大,触摸时有明显的油腻感。
③溶解性:难溶于水,易溶于汽油、乙醚、氯仿等有机溶剂。
④熔沸点:天然油脂都是由混甘油酯组成的混合物,没有恒定的熔、沸点。
5.化学性质:
(1)水解反应——以硬脂酸甘油酯为例
①在酸性条件下发生水解反应
+3H2O
3C17H35COOH+
②在碱性(NaOH或KOH溶液)条件下发生水解反应
+3NaOH
3C17H35COONa+
1 mol油脂完全水解生成3 mol高级脂肪酸(或盐)和1 mol甘油。
高级脂肪酸的盐常用于生产肥皂,油脂在碱性溶液中的水解反应又称为皂化反应。
乙酸乙酯在碱性条件下也能发生水解反应,但不是皂化反应。
肥皂的制取过程
油脂水解反应的应用:
热的纯碱溶液可以提高去除油脂的效果,因为热的纯碱水解程度大,碱性强使油脂易水解 。
(2)氢化反应(加成反应)
不饱和程度较高、熔点较低的液态油,通过催化加氢可提高饱和度,转变成半固态的脂肪,这个过程称为油脂的氢化,也称油脂的硬化。
由此制得的油脂叫人造脂肪,通常又称为硬化油。
+3H2
油酸甘油酯
硬脂酸甘油酯
硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂和人造奶油的原料。
油脂(酯)和矿物油的比较
物质 油脂 矿物油
油 脂肪
组成 不饱和高级脂肪酸甘油酯 饱和高级脂肪酸甘油酯 多种烃(石油及其分馏产品)
状态 液态 固态 液态
化学 性质 能水解,兼有烯烃的性质 能水解 具有烃的性质,不能水解
存在 芝麻等油料作物中 动物脂肪 石油
区分
取少量液体,加含酚酞的NaOH溶液,加热,红色变浅,最后不分层的为油脂(酯),否则为矿物油(烃)。
在油、脂肪、酯、汽油中一定能使酸性高锰酸钾溶液或溴水褪色的是哪种
油一定有碳碳双键,脂肪一般没有,酯可能有,直馏汽油一般没有而裂化汽油有。
三.酰胺
1.胺
①概念:
烃基取代氨分子中的氢原子而形成的化合物,一般写作R—NH2。
也可看作是烃分子中的氢原子被氨基(或取代的氨基—NRR`)所替代得到的化合物。
甲胺 CH3—NH2
苯胺
氨基 —NH2
②官能团:
③化学性质:
胺类化合物具有碱性
④用途:
胺的用途很广,是重要的化工原料。例如,甲胺和苯胺都是合成医药、农药和染料等的重要原料。
2.酰胺
①概念:
酰胺是羧酸分子中羟基被氨基(或取代的氨基)所替代得到的化合物。
②结构:
③常见的酰胺:
④用途
酰基
酰胺基
乙酰胺
苯甲酰胺
N,N-二甲基甲酰胺
酰胺常被用作溶剂和化工原料。例如,N,N-二甲基甲酰胺(DMF)是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等。
⑤化学性质:
酰胺在酸或碱存在并加热的条件下可以发生水解反应。
RCONH2+H2O+HCl RCOOH+NH4Cl
RCONH2+NaOH RCOONa+NH3↑
a.与盐酸
b.与NaOH
酰胺水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
组成 结构 性质 用途
氨 N、H 溶于水显碱性,能和酸或酸性物质发生反应 制冷剂、制造化肥和炸药
胺 C、N、H R—NH2 胺类化合物具有碱性 合成医药、农药和染料等的化工原料
酰胺 C、N、O、H 酰胺在酸或碱存在并加热的条件下可以发生水解反应 作溶剂和化工原料
铵盐 N、H等 和酸根阴离子 受热易分解,可与碱反应产生氨气 工业、农业及日常生活中都有用途
氨、胺、酰胺和铵盐的比较
第三章 烃的含氧衍生物
第四节 羧酸 羧酸衍生物
第二课时 羧酸衍生物
一.酯
1. 概念:
2. 官能团:
羧酸分子羧基中的—OH被—OR′取代后的产物,可简写为RCOOR′,R和R′可以相同,也可以不同。
酯基
O
=
—C-OR
或—COOR
3.分类:
根据分子中酯基的数目
酯
一元酯
二元酯
多元酯
有机酸酯
无机酸酯
根据生成酯的酸不同
4.饱和一元酯的通式:
CnH2nO2
C
O
OCH3
H
甲酸甲酯
C
O
OCH2CH3
H
甲酸乙酯
C
O
OCH3
CH3
乙酸甲酯
C
O
R′
R
某酸某酯
与饱和一元羧酸互为同分异构体
根据生成酯的酸和醇命名为某酸某酯。
5.命名:
戊酸戊酯
乙酸异戊酯
丁酸乙酯
COOCH2CH3
COOCH2CH3
CH3COOCH2
CH3COOCH2
乙二酸二乙酯
二乙酸乙二酯
低级酯是具有芳香气味的液体,密度一般比水小,难溶于水,易溶于有机溶剂,许多酯也是常用的有机溶剂。
6.物理性质:
7.用途:
许多酯是常用的有机溶剂,酯类广泛存在于自然界,日常生活中的饮料、糖果和糕点等常使用酯类香料。
8.化学性质:
实验操作
实验现象
实验结论
a试管内酯层厚度基本不变;b试管内酯层厚度减小;c试管内酯层基本消失
乙酸乙酯在中性条件下基本不水解,酸性条件下水解速率比碱性条件下慢
中性溶液
碱性溶液
酸性溶液
试管中均先加入1 mol乙酸乙酯
(1)水解反应
请你设计实验,探究乙酸乙酯在中性、酸性和碱性溶液中的水解速率。
已知:①乙酸乙酯在常温下水解速率很慢 ②乙酸乙酯的沸点为76.5—77.5℃。
请你设计实验,探究乙酸乙酯在不同温度下的水解速率。
已知:①乙酸乙酯在常温下水解速率很慢 ②乙酸乙酯的沸点为76.5—77.5℃。
实验操作
实验现象
实验结论
a试管内酯层消失时间比b试管长
温度越高,乙酸乙酯的水解速率越大
70~80℃
【思考与讨论】
(1)为什么可以通过比较酯层消失的时间来判断水解速率的大小
因为羧基为亲水基,乙基为疏水基,所以乙酸易溶于水,乙酸乙酯在水中的溶解度较小。同时,乙酸乙酯的密度比水的小,酯层位于水层之上。故酯层消失即表示乙酸乙酯水解完全。
(2)为什么乙酸乙酯在酸性溶液中的水解速率大于中性溶液的水解速率?
无机酸作催化剂,加快反应速率。
(3)为什么乙酸乙酯在碱性溶液中能够水解完全(从平衡移动的角度进行分析)?
碱不仅起催化作用,而且能与水解生成的羧酸发生中和反应,使平衡右移,水解程度增大,直至完全。酯在碱性条件下的水解不可逆。
(1)水解反应
酯在无机酸或碱催化作用下水解生成相应的羧酸(羧酸盐) 与醇,属于取代反应。
①反应原理:
酯化反应形成的键,即酯水解反应断裂的键。
②在酸性条件下,酯的水解是可逆反应。
O
RC-O-R′ + H-OH
=
稀硫酸
△
O
RC-OH + R ′ OH
=
②在碱性条件下,酯的水解是不可逆反应。
O
RC-O-R ′ +NaOH
=
△
RCOONa + R ′ OH
酯化反应 酯的水解反应
反应关系
催化剂 浓硫酸 稀硫酸或NaOH溶液
催化剂的 其他作用 吸水、提高CH3COOH和C2H5OH的转化率 NaOH中和酯水解生成的羧酸、提高酯的水解效率
加热方式 酒精灯火焰加热 热水浴加热
反应类型 酯化反应、取代反应 水解反应、取代反应
酯化反应与酯的水解反应的比较
二.油脂
1.概念:
酯是由酸(有机羧酸或无机含氧酸)与醇相互作用失去水分子形成的一类化合物的总称。
油脂仅指高级脂肪酸与甘油所生成的酯,因而它是酯中特殊的一类物质。
2.结构:
R、R′、R″代表高级脂肪酸的烃基,可以相同也可以不同,可以是饱和烃基也可是是含碳碳双键的不饱和烃基。
油脂是由一分子甘油与三分子高级脂肪酸形成的酯,称为甘油三酯。
组成油脂的高级脂肪酸种类较多,其中以含16—18个碳原子的高级脂肪酸最为常见:
饱和高级脂肪酸:软脂酸(十六酸,棕榈酸) C15H31COOH
硬脂酸(十八酸) C17H35COOH
不饱和高级脂肪酸:油酸(9-十八碳烯酸) C17H33COOH
亚油酸(9,12-十八碳二烯酸) C17H31COOH
3.分类:
如果R、R‘、R’‘相同,称为 (简)单甘油酯(同酸甘油酯)
如果R、R‘、R’‘不同,称为混(合) 甘油酯(异酸甘油酯)
天然油脂大多数都是混甘油酯。
根据烃基是否饱和
油脂
根据烃基是否相同
饱和高级脂肪酸甘油酯
不饱和高级脂肪酸甘油酯
根据状态
油:常温下呈液态,如花生油、芝麻油、大豆油等植物油,含较多不饱和高级脂肪酸甘油酯。
脂肪:常温下呈固态,如牛油、羊油等动物油脂,含较多饱和高级脂肪酸甘油酯。
4.物理性质:
①色、味:纯净的油脂是无色、无味的,但一般因溶有维生素和色素等
而有颜色和气味。
②密度:比水小,黏度较大,触摸时有明显的油腻感。
③溶解性:难溶于水,易溶于汽油、乙醚、氯仿等有机溶剂。
④熔沸点:天然油脂都是由混甘油酯组成的混合物,没有恒定的熔、沸点。
5.化学性质:
(1)水解反应——以硬脂酸甘油酯为例
①在酸性条件下发生水解反应
+3H2O
3C17H35COOH+
②在碱性(NaOH或KOH溶液)条件下发生水解反应
+3NaOH
3C17H35COONa+
1 mol油脂完全水解生成3 mol高级脂肪酸(或盐)和1 mol甘油。
高级脂肪酸的盐常用于生产肥皂,油脂在碱性溶液中的水解反应又称为皂化反应。
乙酸乙酯在碱性条件下也能发生水解反应,但不是皂化反应。
肥皂的制取过程
油脂水解反应的应用:
热的纯碱溶液可以提高去除油脂的效果,因为热的纯碱水解程度大,碱性强使油脂易水解 。
(2)氢化反应(加成反应)
不饱和程度较高、熔点较低的液态油,通过催化加氢可提高饱和度,转变成半固态的脂肪,这个过程称为油脂的氢化,也称油脂的硬化。
由此制得的油脂叫人造脂肪,通常又称为硬化油。
+3H2
油酸甘油酯
硬脂酸甘油酯
硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂和人造奶油的原料。
油脂(酯)和矿物油的比较
物质 油脂 矿物油
油 脂肪
组成 不饱和高级脂肪酸甘油酯 饱和高级脂肪酸甘油酯 多种烃(石油及其分馏产品)
状态 液态 固态 液态
化学 性质 能水解,兼有烯烃的性质 能水解 具有烃的性质,不能水解
存在 芝麻等油料作物中 动物脂肪 石油
区分
取少量液体,加含酚酞的NaOH溶液,加热,红色变浅,最后不分层的为油脂(酯),否则为矿物油(烃)。
在油、脂肪、酯、汽油中一定能使酸性高锰酸钾溶液或溴水褪色的是哪种
油一定有碳碳双键,脂肪一般没有,酯可能有,直馏汽油一般没有而裂化汽油有。
三.酰胺
1.胺
①概念:
烃基取代氨分子中的氢原子而形成的化合物,一般写作R—NH2。
也可看作是烃分子中的氢原子被氨基(或取代的氨基—NRR`)所替代得到的化合物。
甲胺 CH3—NH2
苯胺
氨基 —NH2
②官能团:
③化学性质:
胺类化合物具有碱性
④用途:
胺的用途很广,是重要的化工原料。例如,甲胺和苯胺都是合成医药、农药和染料等的重要原料。
2.酰胺
①概念:
酰胺是羧酸分子中羟基被氨基(或取代的氨基)所替代得到的化合物。
②结构:
③常见的酰胺:
④用途
酰基
酰胺基
乙酰胺
苯甲酰胺
N,N-二甲基甲酰胺
酰胺常被用作溶剂和化工原料。例如,N,N-二甲基甲酰胺(DMF)是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等。
⑤化学性质:
酰胺在酸或碱存在并加热的条件下可以发生水解反应。
RCONH2+H2O+HCl RCOOH+NH4Cl
RCONH2+NaOH RCOONa+NH3↑
a.与盐酸
b.与NaOH
酰胺水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
组成 结构 性质 用途
氨 N、H 溶于水显碱性,能和酸或酸性物质发生反应 制冷剂、制造化肥和炸药
胺 C、N、H R—NH2 胺类化合物具有碱性 合成医药、农药和染料等的化工原料
酰胺 C、N、O、H 酰胺在酸或碱存在并加热的条件下可以发生水解反应 作溶剂和化工原料
铵盐 N、H等 和酸根阴离子 受热易分解,可与碱反应产生氨气 工业、农业及日常生活中都有用途
氨、胺、酰胺和铵盐的比较
