4.1糖类 课件(共32张PPT)2024-2025学年高二下学期化学人教版(2019)选择性必修3
文档属性
| 名称 | 4.1糖类 课件(共32张PPT)2024-2025学年高二下学期化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-05 00:00:00 | ||
图片预览





文档简介
(共32张PPT)
第四章 生物大分子
第一节 糖类
葡萄糖(C6H12O6)
蔗糖(C12H22O11)
淀粉[(C6H10O5)n]
纤维素[(C6H10O5)n]
一.糖类的组成和分类
1.组成
糖类化合物一般由C、H、O三种元素组成,大多数可用通式Cm(H2O)n
表示,如葡萄糖(C6H12O6)、蔗糖(C12H22O11)、淀粉[(C6H10O5)n]等。也被称为碳水化合物。
▲并不是所有糖的组成都符合上述通式,如脱氧核糖(C5H10O4);而某些符合此通式的物质却不属于糖类,如乙酸(C2H4O2)、甲醛(CH2O)。因而碳水化合物这一名称并不准确,但因沿用已久,目前仍在使用。
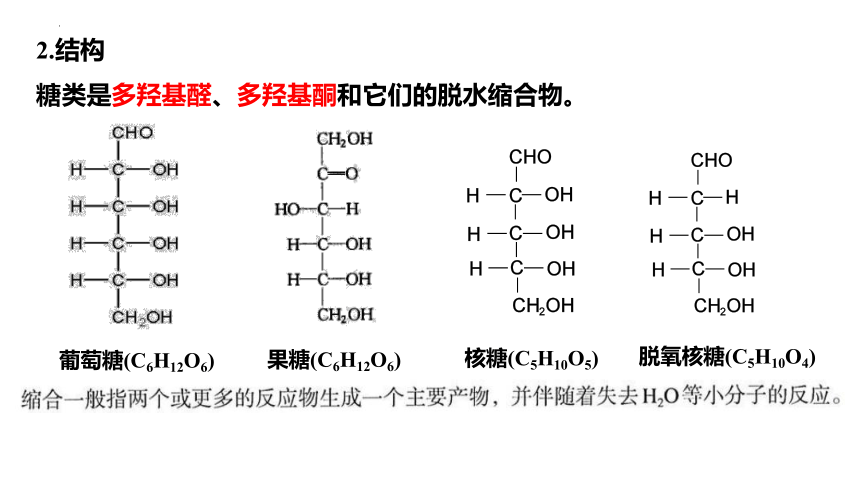
2.结构
糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
葡萄糖(C6H12O6)
果糖(C6H12O6)
核糖(C5H10O5)
脱氧核糖(C5H10O4)
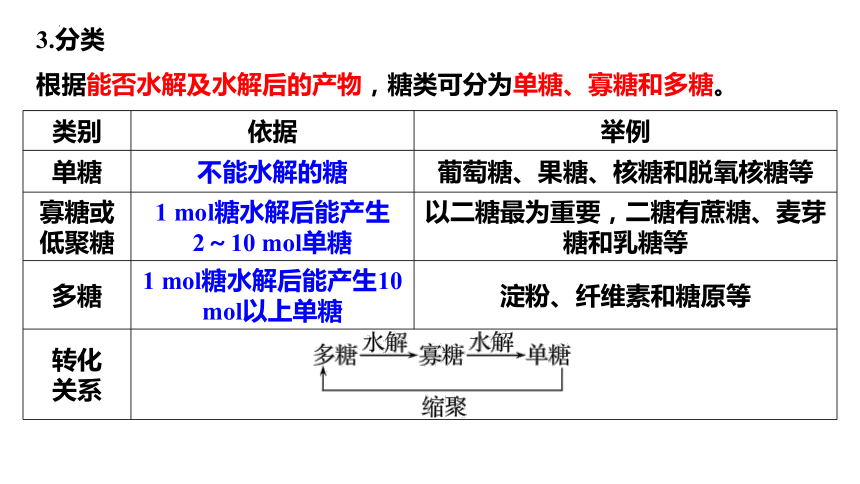
3.分类
根据能否水解及水解后的产物,糖类可分为单糖、寡糖和多糖。
类别 依据 举例
单糖 不能水解的糖 葡萄糖、果糖、核糖和脱氧核糖等
寡糖或 低聚糖 1 mol糖水解后能产生2~10 mol单糖 以二糖最为重要,二糖有蔗糖、麦芽糖和乳糖等
多糖 1 mol糖水解后能产生10 mol以上单糖 淀粉、纤维素和糖原等
转化 关系
二.单糖
1.葡萄糖
(1)存在
葡萄糖是自然界中分布最广的单糖,存在于水果、蜂蜜、植物的种子、叶、根、花,以及动物的血液和淋巴液中。
(2)物理性质
葡萄糖是易溶于水的无色晶体,熔点146℃,有甜味,但甜度不如蔗糖。
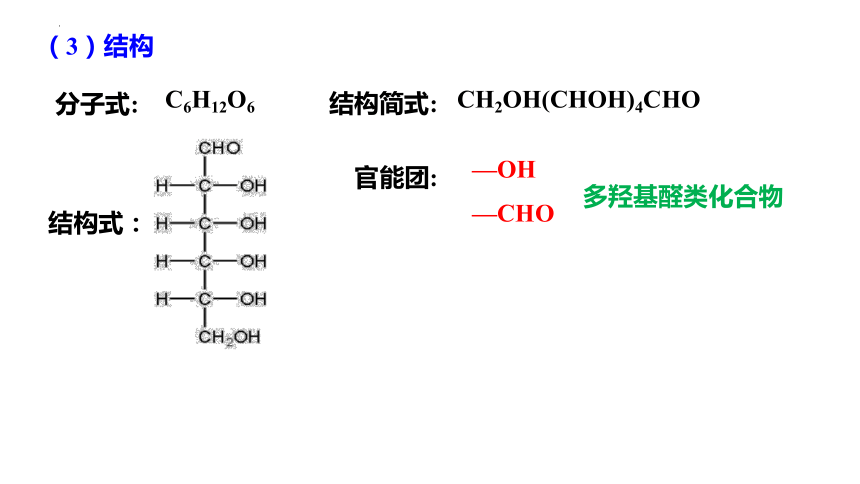
(3)结构
C6H12O6
CH2OH(CHOH)4CHO
—OH
—CHO
多羟基醛类化合物
分子式:
结构式:
结构简式:
官能团:
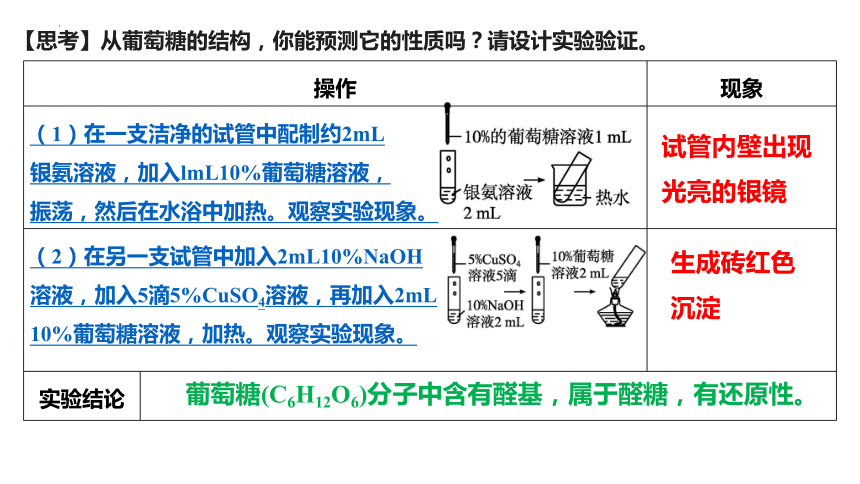
【思考】从葡萄糖的结构,你能预测它的性质吗?请设计实验验证。
操作 现象
(1)在一支洁净的试管中配制约2mL 银氨溶液,加入lmL10%葡萄糖溶液, 振荡,然后在水浴中加热。观察实验现象。
(2)在另一支试管中加入2mL10%NaOH 溶液,加入5滴5%CuSO4溶液,再加入2mL 10%葡萄糖溶液,加热。观察实验现象。
实验结论
试管内壁出现光亮的银镜
生成砖红色沉淀
葡萄糖(C6H12O6)分子中含有醛基,属于醛糖,有还原性。
(4)化学性质
c.使溴水、酸性高锰酸钾溶液褪色
a.银镜反应:
△
CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
b.与新制Cu(OH)2悬浊液的反应:
△
CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH CH2OH(CHOH)4COONa+Cu2O↓+3H2O
e.在酒化酶作用下发酵成酒精
d.生理氧化
C6H12O6+6O2CO2+6H2O
C6H12O62C2H5OH+2CO2↑
还
原
性
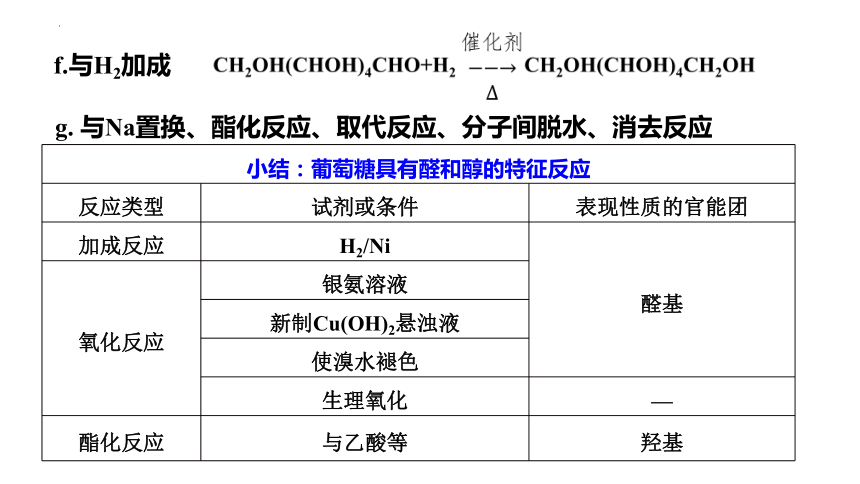
f.与H2加成
CH2OH(CHOH)4CHO+H2 CH2OH(CHOH)4CH2OH
g. 与Na置换、酯化反应、取代反应、分子间脱水、消去反应
小结:葡萄糖具有醛和醇的特征反应
反应类型 试剂或条件 表现性质的官能团
加成反应 H2/Ni 醛基
氧化反应 银氨溶液
新制Cu(OH)2悬浊液
使溴水褪色
生理氧化 —
酯化反应 与乙酸等 羟基
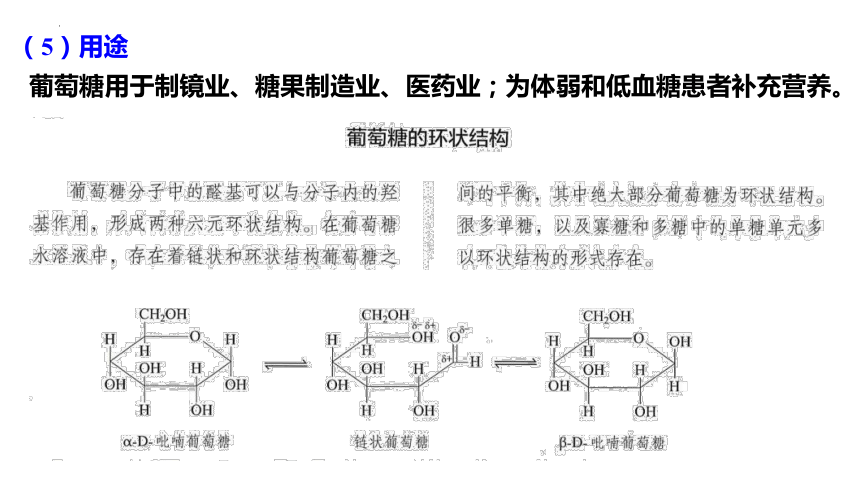
(5)用途
葡萄糖用于制镜业、糖果制造业、医药业;为体弱和低血糖患者补充营养。
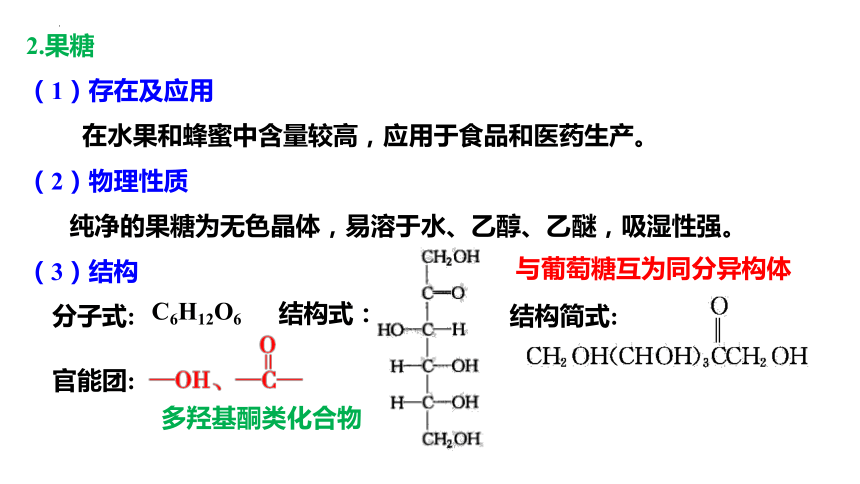
2.果糖
(1)存在及应用
在水果和蜂蜜中含量较高,应用于食品和医药生产。
(2)物理性质
纯净的果糖为无色晶体,易溶于水、乙醇、乙醚,吸湿性强。
(3)结构
分子式:
结构式:
C6H12O6
结构简式:
官能团:
与葡萄糖互为同分异构体
多羟基酮类化合物
【思考】从果糖的结构,你能预测它的性质吗?
(4)化学性质
a.与氢气加成生成醇
b.与Na置换、酯化反应、取代反应、分子间脱水、消去反应
c.果糖虽无醛基,但仍能同葡萄糖一样发生银镜反应、与新制的Cu(OH)2反应。
3.核糖与脱氧核糖
核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA)与脱氧核糖核酸(DNA)的重要组成部分。它们都是含有5个碳原子的单糖—— 戊糖,均为醛糖,具有还原性。
核糖(C5H10O5)
脱氧核糖(C5H10O4)
三.二糖
1.蔗糖和麦芽糖
(1)存在及应用
名称 存在 常见物质 分子式 用途 关系
蔗糖 大多数植物体中,甜菜、甘蔗中含量最高 红糖、白糖、冰糖 C12H22O11 甜味食品
麦芽糖 发芽的谷粒和麦芽中 饴糖 C12H22O11 甜味食品
互为同分异构体
蔗糖:无色晶体,易溶于水,熔点186℃,较难溶于乙醇,甜味仅次于果糖
麦芽糖:无色晶体,易溶于水,有甜味,但甜味不如蔗糖。
(2)物理性质
(3)化学性质
蔗糖:在酸和酶的作用下,蔗糖可水解生成葡萄糖和果糖
麦芽糖:在酸或酶催化下,麦芽糖发生水解反应生成葡萄糖
C12H22O11+H2O 2C6H12O6
麦芽糖
葡萄糖
【思考】根据蔗糖和麦芽糖的水解产物,预测蔗糖和麦芽糖结构上的差异,它们是否和葡萄糖一样属于还原性糖呢?如何验证?
实验内容 实验现象 结论
加蔗糖溶液的试管无明显现象,加麦芽糖溶液的试管内壁出现光亮的银镜
加蔗糖溶液的试管无明显现象,加麦芽糖溶液的试管中出现砖红色沉淀
蔗糖分子内无醛基,是非还原糖;麦芽糖分子内含有醛基,是还原糖
取两支洁净的试管,分别在试管中配制约2mL银氨溶液,分别加入1mL蔗糖溶液、麦芽糖溶液,振荡,然后在水浴中加热。观察实验现象。
另取两支试管,向其中分别加入2mL10%NaOH溶液,加入5滴5%CuSO4溶液,再分别加入2mL蔗糖溶液、麦芽糖溶液,加热。观察实验现象。
【讨论】以上实验操作中有哪些要注意的地方?
1.实验中各种试剂的浓度、用量,以及反应时间、反应温度等应尽可能相同。
2.为保证实验现象明显,操作中所使用的试管必须洁净。试管最好先用NaOH溶液清洗,再用水清洗。
3.银氨溶液和Cu(OH)2必须现用现制。反应混合液应及时处理,不可久置。生成的银镜可用少量硝酸去除。
4.进行蔗糖还原性的检验实验时,应注意市售的白糖中常混有少量的葡萄糖等杂质,会导致对比实验失败。因此,该实验最好使用化学纯以上级别的蔗糖试剂,以保证蔗糖的纯度和实验结果的准确性。
糖类不一定都有甜味,有甜味的不一定属于糖类。
四.多糖
淀粉和纤维素是最重要的多糖,它们都是由大量葡萄糖单元相互连接组成的,属于天然有机高分子,淀粉的相对分子质量可达到几十万,纤维素可达到几百万。
分子式可以表示为(C6H10O5)n,其中的葡萄糖单元中一般仍有三个羟基,也可表示为[C6H7O2(OH)3]n。
因为n值不同,二者不互为同分异构体。
1.淀粉
(1)存在:是绿色植物光合作用的产物,在种子、块根和块茎中含量丰富,谷类和薯类含淀粉较多。天然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高的一些谷物,如糯米、糯玉米等有比较黏的口感。
(2)物理性质:淀粉是白色粉末状物质,没有甜味,不溶于冷水。在热水中淀粉会部分溶解,形成胶状的淀粉糊(糊化)。
(3)用途:淀粉是食物的一种重要成分,也是重要的工业原料。以淀粉或淀粉水解生成的葡萄糖等为原料,经发酵可以得到多种产品,如燃料乙醇、白酒、食醋、味精,以及氨基酸、抗生素等药物。淀粉经酯化后可用于生产食品添加剂、表面活性剂和可降解塑料等。
(4)化学性质
a.不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
b.分子中存在醇羟基,可以发生酯化反应。
c.在酸或酶的作用下水解,最终生成葡萄糖。
d.淀粉遇碘变蓝,可以利用该现象检验淀粉的存在。
【思考】如何判断淀粉的水解程度
(1)实验原理:
淀粉在酸作用下发生水解反应最终生成葡萄糖,反应物淀粉遇碘变蓝色,不能发生银镜反应;产物葡萄糖遇碘不变蓝,能发生银镜反应。
(2)实验步骤:
现象B 现象A 结论
1 溶液变蓝色 未出现银镜 淀粉尚未水解
2 溶液变蓝色 出现银镜 淀粉部分水解
3 溶液不变蓝色 出现银镜 淀粉完全水解
(3)实验现象及结论:
【讨论】
①水解液中加入NaOH溶液的作用是什么
中和水解液中的稀硫酸,为醛基的检验创造碱性环境。
②能否向中和液中加入碘水检验淀粉的存在
不能,I2与NaOH反应,影响水解程度的判断。
▲①验证水解产物时,首先要向水解液中加入NaOH溶液中和至碱性后再进行实验。
②要验证混合液中是否还有淀粉应直接取水解后的混合液加碘水,而不能在加入NaOH中和后再加碘水,因碘水与NaOH溶液反应。
2.纤维素
(1)存在:
纤维素参与构成了植物的细胞壁,起着保护和支持作用。如自然界中的棉、麻、木材、秸秆中存在大量纤维素。
(2)物理性质:
纤维素是白色纤维状物质,没有甜味,不溶于水,也不溶于一般的有机溶剂。
(3)化学性质:
a.不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
b.酯化反应:可以与醋酸、硝酸发生酯化反应制备醋酸纤维、硝酸纤维。
c.在酸或酶的作用下水解,最终生成葡萄糖。
【思考】根据淀粉的水解实验,设计纤维素的水解实验。(提示:催化剂可使用浓硫酸)
实验方案:
在试管中放入少量脱脂棉,加入几滴蒸馏水和几滴浓硫酸,用玻璃棒将混合物搅拌成糊状。加入过量NaOH溶液中和至碱性,再滴入3滴5%CuSO4溶液,加热。观察并解释实验现象
实验现象:
结论:
溶液中产生砖红色沉淀;
纤维素能水解生成还原糖。
a.纺织工业、造纸业;
b.纤维素硝酸酯又称硝酸纤维,极易燃烧,可用于生产火药、塑料和涂料等。
c.纤维素乙酸酯又称醋酸纤维,不易燃烧,是一种纺织工业原料,可用于生产塑料、过滤膜、胶片等。
d.黏胶纤维是经化学处理后的纤维素。黏胶纤维中的长纤维一般称为人造丝,短纤维称为人造棉,都可用于纺织工业。
(4)纤维素的用途
淀粉 纤维素
分子式 (C6H10O5)n (C6H10O5)n
n值大小 大 更大
结构特点 ①无—CHO ②有—OH
水解最终产物 葡萄糖 葡萄糖
化学性质 溶液遇碘变蓝色 ——
可发生酯化反应
是否为纯净物 混合物
是否互为同 分异构体 否
第四章 生物大分子
第一节 糖类
葡萄糖(C6H12O6)
蔗糖(C12H22O11)
淀粉[(C6H10O5)n]
纤维素[(C6H10O5)n]
一.糖类的组成和分类
1.组成
糖类化合物一般由C、H、O三种元素组成,大多数可用通式Cm(H2O)n
表示,如葡萄糖(C6H12O6)、蔗糖(C12H22O11)、淀粉[(C6H10O5)n]等。也被称为碳水化合物。
▲并不是所有糖的组成都符合上述通式,如脱氧核糖(C5H10O4);而某些符合此通式的物质却不属于糖类,如乙酸(C2H4O2)、甲醛(CH2O)。因而碳水化合物这一名称并不准确,但因沿用已久,目前仍在使用。
2.结构
糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
葡萄糖(C6H12O6)
果糖(C6H12O6)
核糖(C5H10O5)
脱氧核糖(C5H10O4)
3.分类
根据能否水解及水解后的产物,糖类可分为单糖、寡糖和多糖。
类别 依据 举例
单糖 不能水解的糖 葡萄糖、果糖、核糖和脱氧核糖等
寡糖或 低聚糖 1 mol糖水解后能产生2~10 mol单糖 以二糖最为重要,二糖有蔗糖、麦芽糖和乳糖等
多糖 1 mol糖水解后能产生10 mol以上单糖 淀粉、纤维素和糖原等
转化 关系
二.单糖
1.葡萄糖
(1)存在
葡萄糖是自然界中分布最广的单糖,存在于水果、蜂蜜、植物的种子、叶、根、花,以及动物的血液和淋巴液中。
(2)物理性质
葡萄糖是易溶于水的无色晶体,熔点146℃,有甜味,但甜度不如蔗糖。
(3)结构
C6H12O6
CH2OH(CHOH)4CHO
—OH
—CHO
多羟基醛类化合物
分子式:
结构式:
结构简式:
官能团:
【思考】从葡萄糖的结构,你能预测它的性质吗?请设计实验验证。
操作 现象
(1)在一支洁净的试管中配制约2mL 银氨溶液,加入lmL10%葡萄糖溶液, 振荡,然后在水浴中加热。观察实验现象。
(2)在另一支试管中加入2mL10%NaOH 溶液,加入5滴5%CuSO4溶液,再加入2mL 10%葡萄糖溶液,加热。观察实验现象。
实验结论
试管内壁出现光亮的银镜
生成砖红色沉淀
葡萄糖(C6H12O6)分子中含有醛基,属于醛糖,有还原性。
(4)化学性质
c.使溴水、酸性高锰酸钾溶液褪色
a.银镜反应:
△
CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
b.与新制Cu(OH)2悬浊液的反应:
△
CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH CH2OH(CHOH)4COONa+Cu2O↓+3H2O
e.在酒化酶作用下发酵成酒精
d.生理氧化
C6H12O6+6O2CO2+6H2O
C6H12O62C2H5OH+2CO2↑
还
原
性
f.与H2加成
CH2OH(CHOH)4CHO+H2 CH2OH(CHOH)4CH2OH
g. 与Na置换、酯化反应、取代反应、分子间脱水、消去反应
小结:葡萄糖具有醛和醇的特征反应
反应类型 试剂或条件 表现性质的官能团
加成反应 H2/Ni 醛基
氧化反应 银氨溶液
新制Cu(OH)2悬浊液
使溴水褪色
生理氧化 —
酯化反应 与乙酸等 羟基
(5)用途
葡萄糖用于制镜业、糖果制造业、医药业;为体弱和低血糖患者补充营养。
2.果糖
(1)存在及应用
在水果和蜂蜜中含量较高,应用于食品和医药生产。
(2)物理性质
纯净的果糖为无色晶体,易溶于水、乙醇、乙醚,吸湿性强。
(3)结构
分子式:
结构式:
C6H12O6
结构简式:
官能团:
与葡萄糖互为同分异构体
多羟基酮类化合物
【思考】从果糖的结构,你能预测它的性质吗?
(4)化学性质
a.与氢气加成生成醇
b.与Na置换、酯化反应、取代反应、分子间脱水、消去反应
c.果糖虽无醛基,但仍能同葡萄糖一样发生银镜反应、与新制的Cu(OH)2反应。
3.核糖与脱氧核糖
核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA)与脱氧核糖核酸(DNA)的重要组成部分。它们都是含有5个碳原子的单糖—— 戊糖,均为醛糖,具有还原性。
核糖(C5H10O5)
脱氧核糖(C5H10O4)
三.二糖
1.蔗糖和麦芽糖
(1)存在及应用
名称 存在 常见物质 分子式 用途 关系
蔗糖 大多数植物体中,甜菜、甘蔗中含量最高 红糖、白糖、冰糖 C12H22O11 甜味食品
麦芽糖 发芽的谷粒和麦芽中 饴糖 C12H22O11 甜味食品
互为同分异构体
蔗糖:无色晶体,易溶于水,熔点186℃,较难溶于乙醇,甜味仅次于果糖
麦芽糖:无色晶体,易溶于水,有甜味,但甜味不如蔗糖。
(2)物理性质
(3)化学性质
蔗糖:在酸和酶的作用下,蔗糖可水解生成葡萄糖和果糖
麦芽糖:在酸或酶催化下,麦芽糖发生水解反应生成葡萄糖
C12H22O11+H2O 2C6H12O6
麦芽糖
葡萄糖
【思考】根据蔗糖和麦芽糖的水解产物,预测蔗糖和麦芽糖结构上的差异,它们是否和葡萄糖一样属于还原性糖呢?如何验证?
实验内容 实验现象 结论
加蔗糖溶液的试管无明显现象,加麦芽糖溶液的试管内壁出现光亮的银镜
加蔗糖溶液的试管无明显现象,加麦芽糖溶液的试管中出现砖红色沉淀
蔗糖分子内无醛基,是非还原糖;麦芽糖分子内含有醛基,是还原糖
取两支洁净的试管,分别在试管中配制约2mL银氨溶液,分别加入1mL蔗糖溶液、麦芽糖溶液,振荡,然后在水浴中加热。观察实验现象。
另取两支试管,向其中分别加入2mL10%NaOH溶液,加入5滴5%CuSO4溶液,再分别加入2mL蔗糖溶液、麦芽糖溶液,加热。观察实验现象。
【讨论】以上实验操作中有哪些要注意的地方?
1.实验中各种试剂的浓度、用量,以及反应时间、反应温度等应尽可能相同。
2.为保证实验现象明显,操作中所使用的试管必须洁净。试管最好先用NaOH溶液清洗,再用水清洗。
3.银氨溶液和Cu(OH)2必须现用现制。反应混合液应及时处理,不可久置。生成的银镜可用少量硝酸去除。
4.进行蔗糖还原性的检验实验时,应注意市售的白糖中常混有少量的葡萄糖等杂质,会导致对比实验失败。因此,该实验最好使用化学纯以上级别的蔗糖试剂,以保证蔗糖的纯度和实验结果的准确性。
糖类不一定都有甜味,有甜味的不一定属于糖类。
四.多糖
淀粉和纤维素是最重要的多糖,它们都是由大量葡萄糖单元相互连接组成的,属于天然有机高分子,淀粉的相对分子质量可达到几十万,纤维素可达到几百万。
分子式可以表示为(C6H10O5)n,其中的葡萄糖单元中一般仍有三个羟基,也可表示为[C6H7O2(OH)3]n。
因为n值不同,二者不互为同分异构体。
1.淀粉
(1)存在:是绿色植物光合作用的产物,在种子、块根和块茎中含量丰富,谷类和薯类含淀粉较多。天然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高的一些谷物,如糯米、糯玉米等有比较黏的口感。
(2)物理性质:淀粉是白色粉末状物质,没有甜味,不溶于冷水。在热水中淀粉会部分溶解,形成胶状的淀粉糊(糊化)。
(3)用途:淀粉是食物的一种重要成分,也是重要的工业原料。以淀粉或淀粉水解生成的葡萄糖等为原料,经发酵可以得到多种产品,如燃料乙醇、白酒、食醋、味精,以及氨基酸、抗生素等药物。淀粉经酯化后可用于生产食品添加剂、表面活性剂和可降解塑料等。
(4)化学性质
a.不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
b.分子中存在醇羟基,可以发生酯化反应。
c.在酸或酶的作用下水解,最终生成葡萄糖。
d.淀粉遇碘变蓝,可以利用该现象检验淀粉的存在。
【思考】如何判断淀粉的水解程度
(1)实验原理:
淀粉在酸作用下发生水解反应最终生成葡萄糖,反应物淀粉遇碘变蓝色,不能发生银镜反应;产物葡萄糖遇碘不变蓝,能发生银镜反应。
(2)实验步骤:
现象B 现象A 结论
1 溶液变蓝色 未出现银镜 淀粉尚未水解
2 溶液变蓝色 出现银镜 淀粉部分水解
3 溶液不变蓝色 出现银镜 淀粉完全水解
(3)实验现象及结论:
【讨论】
①水解液中加入NaOH溶液的作用是什么
中和水解液中的稀硫酸,为醛基的检验创造碱性环境。
②能否向中和液中加入碘水检验淀粉的存在
不能,I2与NaOH反应,影响水解程度的判断。
▲①验证水解产物时,首先要向水解液中加入NaOH溶液中和至碱性后再进行实验。
②要验证混合液中是否还有淀粉应直接取水解后的混合液加碘水,而不能在加入NaOH中和后再加碘水,因碘水与NaOH溶液反应。
2.纤维素
(1)存在:
纤维素参与构成了植物的细胞壁,起着保护和支持作用。如自然界中的棉、麻、木材、秸秆中存在大量纤维素。
(2)物理性质:
纤维素是白色纤维状物质,没有甜味,不溶于水,也不溶于一般的有机溶剂。
(3)化学性质:
a.不能被银氨溶液和氢氧化铜等弱氧化剂氧化,属于非还原糖。
b.酯化反应:可以与醋酸、硝酸发生酯化反应制备醋酸纤维、硝酸纤维。
c.在酸或酶的作用下水解,最终生成葡萄糖。
【思考】根据淀粉的水解实验,设计纤维素的水解实验。(提示:催化剂可使用浓硫酸)
实验方案:
在试管中放入少量脱脂棉,加入几滴蒸馏水和几滴浓硫酸,用玻璃棒将混合物搅拌成糊状。加入过量NaOH溶液中和至碱性,再滴入3滴5%CuSO4溶液,加热。观察并解释实验现象
实验现象:
结论:
溶液中产生砖红色沉淀;
纤维素能水解生成还原糖。
a.纺织工业、造纸业;
b.纤维素硝酸酯又称硝酸纤维,极易燃烧,可用于生产火药、塑料和涂料等。
c.纤维素乙酸酯又称醋酸纤维,不易燃烧,是一种纺织工业原料,可用于生产塑料、过滤膜、胶片等。
d.黏胶纤维是经化学处理后的纤维素。黏胶纤维中的长纤维一般称为人造丝,短纤维称为人造棉,都可用于纺织工业。
(4)纤维素的用途
淀粉 纤维素
分子式 (C6H10O5)n (C6H10O5)n
n值大小 大 更大
结构特点 ①无—CHO ②有—OH
水解最终产物 葡萄糖 葡萄糖
化学性质 溶液遇碘变蓝色 ——
可发生酯化反应
是否为纯净物 混合物
是否互为同 分异构体 否
