2.2气体的等温变化(第2课时)课件(共16张PPT)-2024-2025学年高二下学期物理人教版(2019)选择性必修第三册+
文档属性
| 名称 | 2.2气体的等温变化(第2课时)课件(共16张PPT)-2024-2025学年高二下学期物理人教版(2019)选择性必修第三册+ |

|
|
| 格式 | pptx | ||
| 文件大小 | 890.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2024-08-06 00:00:00 | ||
图片预览




文档简介
(共16张PPT)
第二章 气体、固体和液体
第2节 气体的等温变化
新教材人教版 物理(高中选择性必修第三册)
第二课时
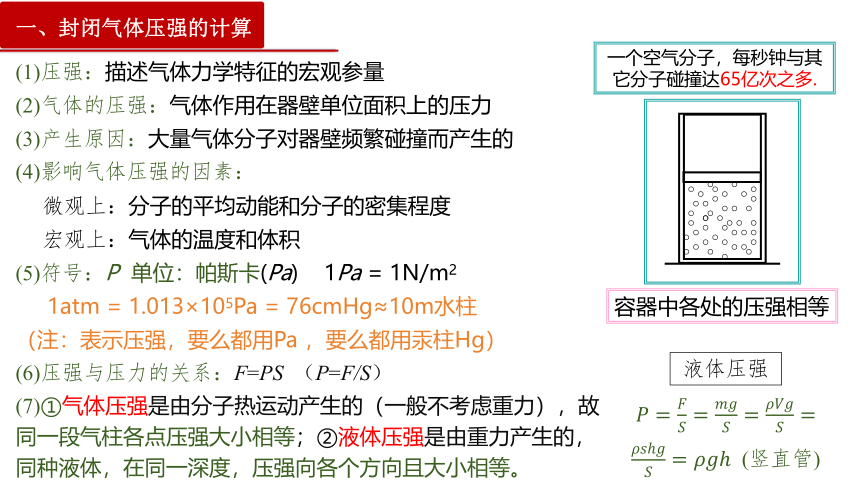
一、封闭气体压强的计算
(1)压强:描述气体力学特征的宏观参量
(2)气体的压强:气体作用在器壁单位面积上的压力
(3)产生原因:大量气体分子对器壁频繁碰撞而产生的
(4)影响气体压强的因素:
微观上:分子的平均动能和分子的密集程度
宏观上:气体的温度和体积
(5)符号:P 单位:帕斯卡(Pa) 1Pa = 1N/m2
1atm = 1.013×105Pa = 76cmHg≈10m水柱
(注:表示压强,要么都用Pa ,要么都用汞柱Hg)
(6)压强与压力的关系:F=PS (P=F/S)
一个空气分子,每秒钟与其它分子碰撞达65亿次之多.
容器中各处的压强相等
(7)①气体压强是由分子热运动产生的(一般不考虑重力),故同一段气柱各点压强大小相等;②液体压强是由重力产生的,同种液体,在同一深度,压强向各个方向且大小相等。
(竖直管)
液体压强
一、封闭气体压强的计算
问题一:平衡态下液体封闭气体压强的计算
h
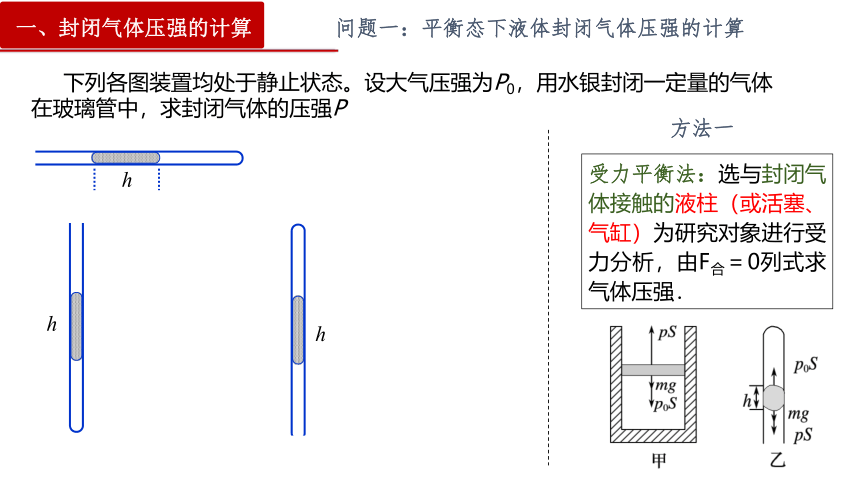
下列各图装置均处于静止状态。设大气压强为P0,用水银封闭一定量的气体在玻璃管中,求封闭气体的压强P
h
h
受力平衡法:选与封闭气体接触的液柱(或活塞、气缸)为研究对象进行受力分析,由F合=0列式求气体压强.
方法一
一、封闭气体压强的计算
问题一:平衡态下液体封闭气体压强的计算
h
h
h
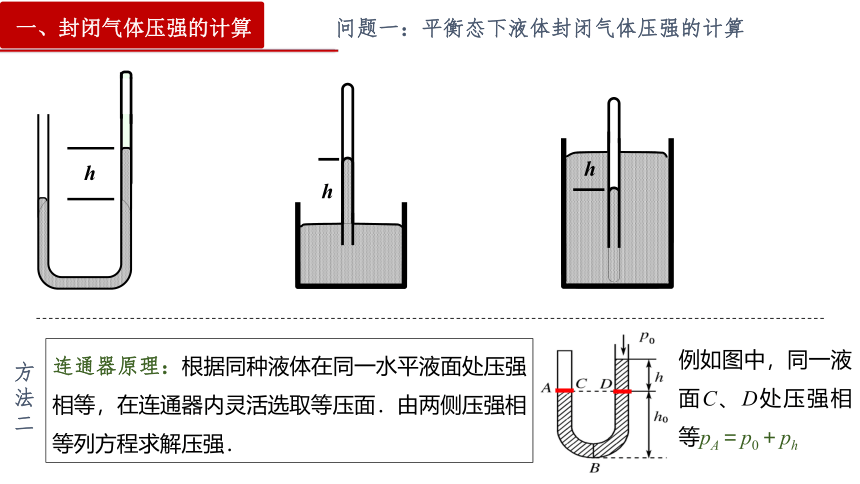
连通器原理:根据同种液体在同一水平液面处压强相等,在连通器内灵活选取等压面.由两侧压强相等列方程求解压强.
例如图中,同一液面C、D处压强相等pA=p0+ph
方法二
一、封闭气体压强的计算
问题一:平衡态下液体封闭气体压强的计算
液片平衡法(参考液片法):选取假想的液体薄片(自身重力不计)为研究对象,分析液片两侧受力情况,建立平衡方程消去面积S,得到液片两侧的压强平衡方程,进而求得气体压强.
例如,图中粗细均匀的U形管中封闭了一定质量的气体A,在其最低处取一液片B,由其两侧受力平衡可知
(pA+ph0)S=(p0+ph+ph0)S.即pA=p0+ph
★一般在D处取一液片,则有pA=pD=p0+ph
方法三
如图,U形管竖直放置.根据连通器原理可知,同一液体中的相同高度处压强一定相等,所以气体B和A的压强关系可由图中虚线联系起来.则有pB+ρgh2=pA.而pA=p0+ρgh1,所以气体B的压强为pB=p0+ρg(h1-h2).
根据所学知识,计算PA和PB的大小。
一、封闭气体压强的计算
问题二:非平衡态下液体封闭气体压强的计算
当容器加速运动时,通常选与气体相关联的液柱、汽缸或活塞为研究对象,并对其进行受力分析,然后由牛顿第二定律列方程,求出封闭气体的压强.
计算方法
如图所示,当竖直放置的玻璃管向上加速运动时,封闭气体的压强为多少?
思考与讨论:竖直放置的玻璃管向下加速运动时,封闭气体的压强为多少?
对液柱受力分析有: pS-p0S-mg=ma
二、活塞—气缸模型的气体压强
求用固体(如活塞)封闭在静止容器内的气体压强,应采用受力平衡法,对固体进行受力分析。然后根据平衡条件求解。
G
P0S
PS
PS = P0S+mg
G
PS
P0S′
PS =mg +P0S'cosθ
PS = mg+P0S
以活塞为研究对象
以气缸为研究对象
mg+PS = P0S
Mg+PS = P0S
例.如图为某压缩式喷雾器储液桶,其容量是5.7×10-3m3,往桶内倒入4.2×10-3 m3的药液后开始打气,假设打气过程中药液不会向外喷出.如果每次能打进2.5×10-4m3的空气,
(1)要使喷雾器内空气的压强达到4atm,应打气几次?
(2)这个压强能否使喷雾器内的药液全部喷完?
(设标准大气压为1 atm,打气过程中不考虑温度的变化)
三、气体变质量问题
每充或抽一次气,容器中空气的质量都会发生变化,但如果灵活选取研究对象,可将其转变为质量不变的问题。
(1)关于充气问题:如果打气时每一次打入的空气质量、体积和压强均相同,则可设想用一容积为nV0的打气筒将压强为p0的空气一次打入容器与打n次气等效代替。所以研究对象应为容器中原有的空气和n次打入的空气总和。这样充气过程可看作是气体的等温压缩过程。
(1)要使喷雾器内空气的压强达到4atm,应打气几次?
(设标准大气压为1 atm,打气过程中不考虑温度的变化)
4.2×10-3 m3
V
5.7×10-3m3
2.5×10-4m3
2.5×10-4m3
2.5×10-4m3
2.5×10-4m3
2.5×10-4m3
………………
变质量问题
4p0
一定质量气体的等温变化,可看成等温压缩问题!
p0V + p0×n×(2.5×10-4 m3) = 4p0 V
V=5.7×10-3 m3-4.2×10-3 m3=1.5×10-3 m3
n=18
(2)这个压强能否使喷雾器内的药液全部喷完?
假设空气完全充满药桶后(即液体全部喷完)
如果空气压强P仍然大于大气压,则药液可以全部喷出,否则不能完全喷出.
4.2×10-3 m3
V
5.7×10-3m3
5.7×10-3m3
4p0V=p×5.7×10-3
p=1.053p0>p0
所以药液可以全部喷出.
4p0
p
=1.5×10-3 m3
由玻意耳定律得:
(2)关于抽气问题:从容器内抽气的过程中,容器内的气体质量不断减小,这属于变质量的问题。分析时,将每次抽气过程中抽出的气体和剩余气体作为研究对象,质量不变,故抽气过程可看作是等温膨胀过程。
(3)关于灌气问题:一个大容器里的气体分装到多个小容器的问题,也是一个典型的变质量问题。分析这类问题时,可以把大容器的气体和多个小容器中的气体看作整体作为研究对象,可将变质量的问题转化为质量不变的问题。
例:容积V=20 L的钢瓶充满氧气后,压强p=30 atm,打开钢瓶阀门,让氧气分装到容积为V′=5 L的小瓶中去,小瓶子已抽成真空.分装完成后,每个小钢瓶的压强p′=2 atm.在分装过程中无漏气现象,且温度保持不变,那么最多可能装的瓶数是( )
A.4瓶
B.50瓶
C.56瓶
D.60瓶
三、气体变质量问题
p=30 atm
V=20 L
。。。。。
V′=5 L
V′=5 L
V′=5 L
变质量的问题
。。。。。
V′=5 L
V′=5 L
V′=5 L
p′=2 atm
p′=2 atm
p′=2 atm
p′=2 atm
V=20 L
一定质量气体的等温变化
p V =p′(V + nV′)
(4)漏气问题:容器漏气过程中气体的质量不断发生变化,属于变质量问题。如果选容器内剩余气体和漏出的气体组成的整体为研究对象,便可使问题变成一定质量的气体的状态变化问题。将漏出的气体利用波意耳定律“压缩”成与容器中剩余部分的气体有相同的压强,则放出的气体质量与体积成正比。
三、气体变质量问题
例题:某个容器的容积是10L,所装气体的压强是20×105Pa。如果温度保持不变,把容器的开关打开以后,经过足够长时间,容器里剩下的气体是原来的百分之几?设大气压是1.0×105Pa.
分析:由题意可知,打开开关后气体的压强等于外界大气压。本题解题的关键不是气体状态的确定,而是研究对象的选取。
解析:
初态 p1=20×105Pa V1=10L T1=T
剩下的气体为原来的
末态 p2=1.0×105Pa V2=?L T2=T
由玻意耳定律 p1V1=p2V2得 V2=200L
就容器而言,里面气体质量变了,但可视容器中气体出而不走,以原来容器中的气体为研究对象,就可以运用气体的等温变化规律求解。气体状态变化如图所示。
法一:
解析:
初态 p1=1.0×105Pa V1=10L T1=T
剩下的气体为原来的
末态 p2=20×105Pa V2=?L T2=T
由玻意耳定律 p1V1=p2V2得 V2=0.5L
以后来容器中的气体为研究对象。气体状态变化如图所示。
法二:
玻意耳等温分态公式
一般地,若将某气体(p,V,m)在保持总质量、温度不变的情况下分成了若干部分(p1,V1,m1)、(p2,V2,m2)、…、(pn、Vn、mn),则有pV=p1V1+p2V2+…+pnVn。
应用等温分态公式解答温度不变情况下,气体的分与合,部分气体质量有变化、气体总质量无变化、又不直接涉及气体质量的问题时,常常十分方便。
◎规律总结
求解变质量问题的方法技巧
三、气体变质量问题
推导过程:
例题:如图所示,一汽缸水平固定在静止的小车上,一质量为m,面积为S的活塞将一定量的气体封闭在汽缸内,平衡时活塞与汽缸底相距为L。现让小车以一较小的水平恒定加速度向右运动,稳定时发现活塞相对于汽缸移动了距离d。已知大气压强为p0,不计汽缸和活塞间的摩擦;且小车运动时,大气对活塞的压强仍可视为p0;整个过程温度保持不变。求小车加速度的大小。
【解析】设小车加速度大小为a,稳定时汽缸内气体的压强为p1,则活塞受到汽缸内、外气体的压力分别为:
F1=p1S,F0=p0S
由牛顿第二定律得:F1-F0=ma
小车静止时,在平衡状态下,汽缸内气体的压强应为p0。
由玻意耳定律得:
p1V1=p0V0
式中V0=SL,V1=S(L-d)
联立以上各式得:
答案:
典例分析
第二章 气体、固体和液体
第2节 气体的等温变化
新教材人教版 物理(高中选择性必修第三册)
第二课时
一、封闭气体压强的计算
(1)压强:描述气体力学特征的宏观参量
(2)气体的压强:气体作用在器壁单位面积上的压力
(3)产生原因:大量气体分子对器壁频繁碰撞而产生的
(4)影响气体压强的因素:
微观上:分子的平均动能和分子的密集程度
宏观上:气体的温度和体积
(5)符号:P 单位:帕斯卡(Pa) 1Pa = 1N/m2
1atm = 1.013×105Pa = 76cmHg≈10m水柱
(注:表示压强,要么都用Pa ,要么都用汞柱Hg)
(6)压强与压力的关系:F=PS (P=F/S)
一个空气分子,每秒钟与其它分子碰撞达65亿次之多.
容器中各处的压强相等
(7)①气体压强是由分子热运动产生的(一般不考虑重力),故同一段气柱各点压强大小相等;②液体压强是由重力产生的,同种液体,在同一深度,压强向各个方向且大小相等。
(竖直管)
液体压强
一、封闭气体压强的计算
问题一:平衡态下液体封闭气体压强的计算
h
下列各图装置均处于静止状态。设大气压强为P0,用水银封闭一定量的气体在玻璃管中,求封闭气体的压强P
h
h
受力平衡法:选与封闭气体接触的液柱(或活塞、气缸)为研究对象进行受力分析,由F合=0列式求气体压强.
方法一
一、封闭气体压强的计算
问题一:平衡态下液体封闭气体压强的计算
h
h
h
连通器原理:根据同种液体在同一水平液面处压强相等,在连通器内灵活选取等压面.由两侧压强相等列方程求解压强.
例如图中,同一液面C、D处压强相等pA=p0+ph
方法二
一、封闭气体压强的计算
问题一:平衡态下液体封闭气体压强的计算
液片平衡法(参考液片法):选取假想的液体薄片(自身重力不计)为研究对象,分析液片两侧受力情况,建立平衡方程消去面积S,得到液片两侧的压强平衡方程,进而求得气体压强.
例如,图中粗细均匀的U形管中封闭了一定质量的气体A,在其最低处取一液片B,由其两侧受力平衡可知
(pA+ph0)S=(p0+ph+ph0)S.即pA=p0+ph
★一般在D处取一液片,则有pA=pD=p0+ph
方法三
如图,U形管竖直放置.根据连通器原理可知,同一液体中的相同高度处压强一定相等,所以气体B和A的压强关系可由图中虚线联系起来.则有pB+ρgh2=pA.而pA=p0+ρgh1,所以气体B的压强为pB=p0+ρg(h1-h2).
根据所学知识,计算PA和PB的大小。
一、封闭气体压强的计算
问题二:非平衡态下液体封闭气体压强的计算
当容器加速运动时,通常选与气体相关联的液柱、汽缸或活塞为研究对象,并对其进行受力分析,然后由牛顿第二定律列方程,求出封闭气体的压强.
计算方法
如图所示,当竖直放置的玻璃管向上加速运动时,封闭气体的压强为多少?
思考与讨论:竖直放置的玻璃管向下加速运动时,封闭气体的压强为多少?
对液柱受力分析有: pS-p0S-mg=ma
二、活塞—气缸模型的气体压强
求用固体(如活塞)封闭在静止容器内的气体压强,应采用受力平衡法,对固体进行受力分析。然后根据平衡条件求解。
G
P0S
PS
PS = P0S+mg
G
PS
P0S′
PS =mg +P0S'cosθ
PS = mg+P0S
以活塞为研究对象
以气缸为研究对象
mg+PS = P0S
Mg+PS = P0S
例.如图为某压缩式喷雾器储液桶,其容量是5.7×10-3m3,往桶内倒入4.2×10-3 m3的药液后开始打气,假设打气过程中药液不会向外喷出.如果每次能打进2.5×10-4m3的空气,
(1)要使喷雾器内空气的压强达到4atm,应打气几次?
(2)这个压强能否使喷雾器内的药液全部喷完?
(设标准大气压为1 atm,打气过程中不考虑温度的变化)
三、气体变质量问题
每充或抽一次气,容器中空气的质量都会发生变化,但如果灵活选取研究对象,可将其转变为质量不变的问题。
(1)关于充气问题:如果打气时每一次打入的空气质量、体积和压强均相同,则可设想用一容积为nV0的打气筒将压强为p0的空气一次打入容器与打n次气等效代替。所以研究对象应为容器中原有的空气和n次打入的空气总和。这样充气过程可看作是气体的等温压缩过程。
(1)要使喷雾器内空气的压强达到4atm,应打气几次?
(设标准大气压为1 atm,打气过程中不考虑温度的变化)
4.2×10-3 m3
V
5.7×10-3m3
2.5×10-4m3
2.5×10-4m3
2.5×10-4m3
2.5×10-4m3
2.5×10-4m3
………………
变质量问题
4p0
一定质量气体的等温变化,可看成等温压缩问题!
p0V + p0×n×(2.5×10-4 m3) = 4p0 V
V=5.7×10-3 m3-4.2×10-3 m3=1.5×10-3 m3
n=18
(2)这个压强能否使喷雾器内的药液全部喷完?
假设空气完全充满药桶后(即液体全部喷完)
如果空气压强P仍然大于大气压,则药液可以全部喷出,否则不能完全喷出.
4.2×10-3 m3
V
5.7×10-3m3
5.7×10-3m3
4p0V=p×5.7×10-3
p=1.053p0>p0
所以药液可以全部喷出.
4p0
p
=1.5×10-3 m3
由玻意耳定律得:
(2)关于抽气问题:从容器内抽气的过程中,容器内的气体质量不断减小,这属于变质量的问题。分析时,将每次抽气过程中抽出的气体和剩余气体作为研究对象,质量不变,故抽气过程可看作是等温膨胀过程。
(3)关于灌气问题:一个大容器里的气体分装到多个小容器的问题,也是一个典型的变质量问题。分析这类问题时,可以把大容器的气体和多个小容器中的气体看作整体作为研究对象,可将变质量的问题转化为质量不变的问题。
例:容积V=20 L的钢瓶充满氧气后,压强p=30 atm,打开钢瓶阀门,让氧气分装到容积为V′=5 L的小瓶中去,小瓶子已抽成真空.分装完成后,每个小钢瓶的压强p′=2 atm.在分装过程中无漏气现象,且温度保持不变,那么最多可能装的瓶数是( )
A.4瓶
B.50瓶
C.56瓶
D.60瓶
三、气体变质量问题
p=30 atm
V=20 L
。。。。。
V′=5 L
V′=5 L
V′=5 L
变质量的问题
。。。。。
V′=5 L
V′=5 L
V′=5 L
p′=2 atm
p′=2 atm
p′=2 atm
p′=2 atm
V=20 L
一定质量气体的等温变化
p V =p′(V + nV′)
(4)漏气问题:容器漏气过程中气体的质量不断发生变化,属于变质量问题。如果选容器内剩余气体和漏出的气体组成的整体为研究对象,便可使问题变成一定质量的气体的状态变化问题。将漏出的气体利用波意耳定律“压缩”成与容器中剩余部分的气体有相同的压强,则放出的气体质量与体积成正比。
三、气体变质量问题
例题:某个容器的容积是10L,所装气体的压强是20×105Pa。如果温度保持不变,把容器的开关打开以后,经过足够长时间,容器里剩下的气体是原来的百分之几?设大气压是1.0×105Pa.
分析:由题意可知,打开开关后气体的压强等于外界大气压。本题解题的关键不是气体状态的确定,而是研究对象的选取。
解析:
初态 p1=20×105Pa V1=10L T1=T
剩下的气体为原来的
末态 p2=1.0×105Pa V2=?L T2=T
由玻意耳定律 p1V1=p2V2得 V2=200L
就容器而言,里面气体质量变了,但可视容器中气体出而不走,以原来容器中的气体为研究对象,就可以运用气体的等温变化规律求解。气体状态变化如图所示。
法一:
解析:
初态 p1=1.0×105Pa V1=10L T1=T
剩下的气体为原来的
末态 p2=20×105Pa V2=?L T2=T
由玻意耳定律 p1V1=p2V2得 V2=0.5L
以后来容器中的气体为研究对象。气体状态变化如图所示。
法二:
玻意耳等温分态公式
一般地,若将某气体(p,V,m)在保持总质量、温度不变的情况下分成了若干部分(p1,V1,m1)、(p2,V2,m2)、…、(pn、Vn、mn),则有pV=p1V1+p2V2+…+pnVn。
应用等温分态公式解答温度不变情况下,气体的分与合,部分气体质量有变化、气体总质量无变化、又不直接涉及气体质量的问题时,常常十分方便。
◎规律总结
求解变质量问题的方法技巧
三、气体变质量问题
推导过程:
例题:如图所示,一汽缸水平固定在静止的小车上,一质量为m,面积为S的活塞将一定量的气体封闭在汽缸内,平衡时活塞与汽缸底相距为L。现让小车以一较小的水平恒定加速度向右运动,稳定时发现活塞相对于汽缸移动了距离d。已知大气压强为p0,不计汽缸和活塞间的摩擦;且小车运动时,大气对活塞的压强仍可视为p0;整个过程温度保持不变。求小车加速度的大小。
【解析】设小车加速度大小为a,稳定时汽缸内气体的压强为p1,则活塞受到汽缸内、外气体的压力分别为:
F1=p1S,F0=p0S
由牛顿第二定律得:F1-F0=ma
小车静止时,在平衡状态下,汽缸内气体的压强应为p0。
由玻意耳定律得:
p1V1=p0V0
式中V0=SL,V1=S(L-d)
联立以上各式得:
答案:
典例分析
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
