广东省肇庆市2023-2024学年高一下学期期末考试 化学试题 (含答案)
文档属性
| 名称 | 广东省肇庆市2023-2024学年高一下学期期末考试 化学试题 (含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-07 00:00:00 | ||
图片预览


文档简介
肇庆市2023-2024学年高一下学期期末考试
化 学
注意事项:
1.本试卷共100分,考试时间75分钟。
2.答卷前,考生务必将自己的姓名、准考证号填写在试卷和答题卡上。回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H:1 C:12 N:14 O:16
一、选择题:本题共包括16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 广东省是岭南文化的重要传承地。下列非遗物品中材质不属于硅酸盐的是
A.石湾陶艺 B.潮州木雕 C.肇庆端砚 D.广东砖雕
A. A B. B C. C D. D
2. “神舟十八号”载人飞船发射圆满成功,中国人航天梦又向前迈进了一步。下列说法不正确的是
A. 为神舟系列飞船发射和返回提供保障特种玻璃纤维是一种无机非金属材料
B. 首次在飞船上采用的锂离子蓄电池是一种一次电池
C. 火箭燃料助燃剂是一种非金属氧化物
D. 航天员食用的燕麦片中所含的纤维素是一种人体所需的糖类物质
3. 下列化学用语表述正确的是
A. 甲烷的空间填充模型:
B. 聚丙烯的结构简式:
C. 四氯化碳的电子式:
D. 的名称:1,2-二溴乙烷
4. “劳动是人类生存和社会发展的基础”。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 环保工程师测定雨水的pH≈5.6 雨水中溶解了
B 某同学用热的碱性溶液洗涤沾有油脂的碗碟 油脂的饱和程度越高,熔点越高
C 面点师用含碳酸氢铵的膨松剂制作饼干 碳酸氢铵受热易分解
D 炼化工人将煤气化或液化后再利用 提高煤的利用率
A. A B. B C. C D. D
5. “绿水青山就是金山银山”。下列说法不正确的是
A. 在燃煤过程中加入石灰石,是为了减少温室气体的排放
B. 过量使用化肥可能造成水体富营养化,产生水华现象
C. 电池虽然应该回收利用,但不属于“可回收垃圾”
D. 滥用杀虫剂会破坏生态平衡,造成恶性循环
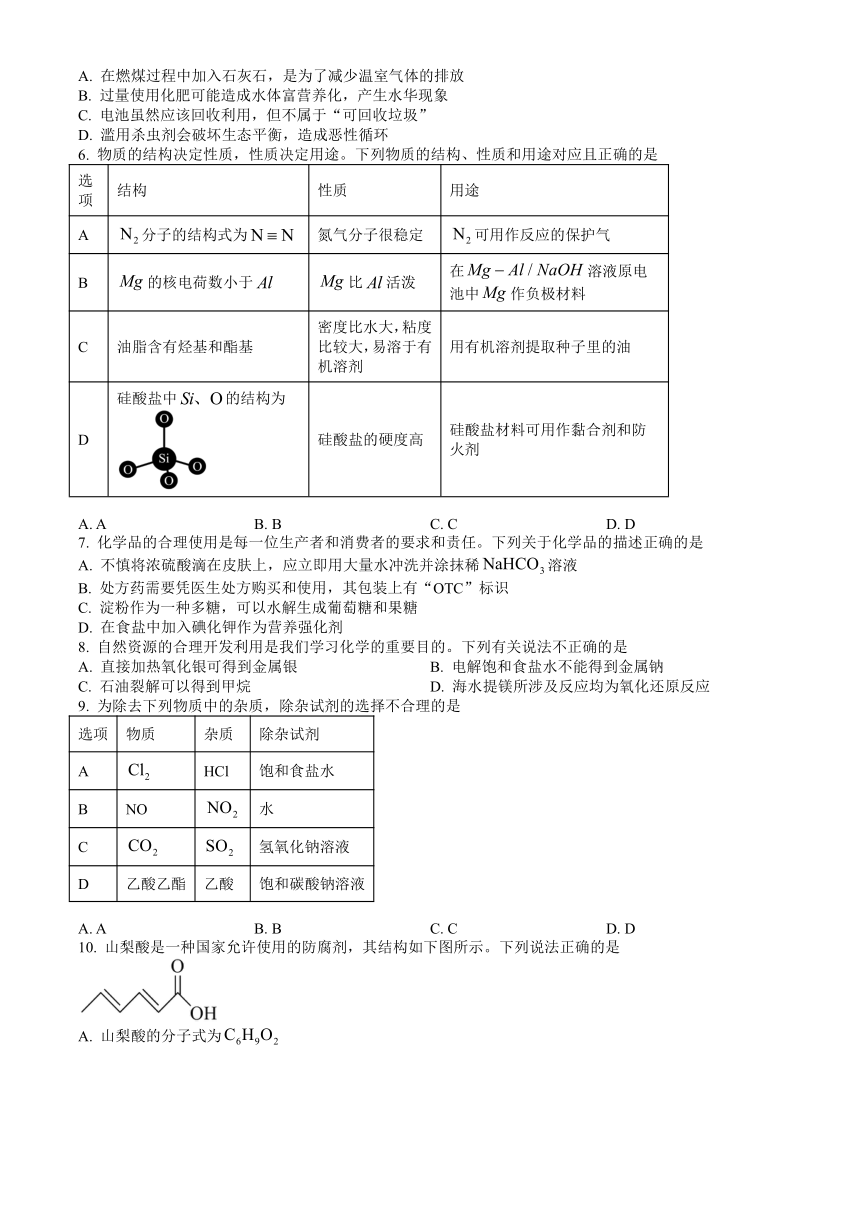
6. 物质的结构决定性质,性质决定用途。下列物质的结构、性质和用途对应且正确的是
选项 结构 性质 用途
A 分子的结构式为 氮气分子很稳定 可用作反应的保护气
B 的核电荷数小于 比活泼 在溶液原电池中作负极材料
C 油脂含有烃基和酯基 密度比水大,粘度比较大,易溶于有机溶剂 用有机溶剂提取种子里的油
D 硅酸盐中的结构为 硅酸盐的硬度高 硅酸盐材料可用作黏合剂和防火剂
A. A B. B C. C D. D
7. 化学品的合理使用是每一位生产者和消费者的要求和责任。下列关于化学品的描述正确的是
A. 不慎将浓硫酸滴在皮肤上,应立即用大量水冲洗并涂抹稀溶液
B. 处方药需要凭医生处方购买和使用,其包装上有“OTC”标识
C. 淀粉作为一种多糖,可以水解生成葡萄糖和果糖
D. 在食盐中加入碘化钾作为营养强化剂
8. 自然资源的合理开发利用是我们学习化学的重要目的。下列有关说法不正确的是
A. 直接加热氧化银可得到金属银 B. 电解饱和食盐水不能得到金属钠
C. 石油裂解可以得到甲烷 D. 海水提镁所涉及反应均为氧化还原反应
9. 为除去下列物质中的杂质,除杂试剂的选择不合理的是
选项 物质 杂质 除杂试剂
A HCl 饱和食盐水
B NO 水
C 氢氧化钠溶液
D 乙酸乙酯 乙酸 饱和碳酸钠溶液
A. A B. B C. C D. D
10. 山梨酸是一种国家允许使用的防腐剂,其结构如下图所示。下列说法正确的是
A. 山梨酸的分子式为
B. 山梨酸与丙烯酸()互为同系物
C. 1 mol山梨酸与Na反应最多生成0.5 mol
D. 1 mol山梨酸最多可以与3 mol 发生加成反应
11. 工业上以二氧化硫和空气混合制取三氧化硫:(放热反应)。在一定温度下向某刚性密闭容器中充入2mol 和2mol 发生反应,下列描述不能说明该反应达到平衡状态的是
A. 混合气体中的物质的量不再改变
B.
C. 混合气体中的含量不再改变
D. 混合气体中、和物质的量之比为2∶1∶2
12. 下列化学反应的化学方程式或离子方程式书写正确的是
A. Cu与浓硝酸反应:
B. 蔗糖的水解反应:
C. 将二氧化硫通入硫化氢溶液中:
D. 硫酸铁铵[]与过量氢氧化钡溶液的反应:
13. 下图所示的实验装置中,能达到实验目的的是
实验装置
实验目的 A.检验X溶液中含有 B.制备并收集
实验装置
实验目的 C.用喷泉实验验证溶解性 D.探究和发生取代反应
A. A B. B C. C D. D
14. 下列有关电池的描述不正确的是
选项 A.铜锌溶液原电池 B.铜锌溶液原电池
电池
描述 负极质量减小,正极质量几乎不变 负极质量减小,正极质量增大
选项 C.铅酸蓄电池 D.氢氧燃料电池
电池
描述 负极质量增大,正极质量减小 负极和正极质量均几乎不变
A. A B. B C. C D. D
15. 设为阿伏加德罗常数的值。下列说法正确的是
A. 足量Cu与1 mol S充分反应,转移电子的数目为
B. 常温下,将1 mol Cu放入足量稀硝酸中,生成NO分子的数目为2
C. 标准状况下,11.2 L乙酸中乙酸分子的数目为0.5
D. 1 mol正丁烷和异丁烷的混合物在空气中充分燃烧消耗分子的数目为6.5
16. 合成氨工业对农业、工业意义重大,随着科学技术的发展,人们对氨的需求量日益增长。已知:合成氨反应中,生成2 mol 时放出92.4 kJ的热量。下列说法正确的是
A. 若向容器中加入0.5 mol 和1.5 mol 充分反应,则放出的热量为46.2kJ
B. 断裂1 mol 键和3 mol 键需要吸收的能量之和小于形成6 mol 键放出的能量
C. 若升高温度合成氨的产率变高,说明升高温度合成氨的速率变快,氨分解的速率变慢
D. 不改变其他条件,延长反应时间有利于提高氢气的平衡转化率
二、非选择题:本题共4小题,共56分。
17. 是一种常见的无机物,它既是重要的物质资源,也是环境污染物之一,某学习小组改进教材中关于的制备和性质探究实验。回答下列问题:
(1)装置A中铜与浓硫酸反应的化学方程式为______。
(2)查阅资料可知,可以用固体(粉末状)和稀硫酸溶液反应制备,该反应的优点是无需使用加热装置,则可选择的发生装置为______(填序号)。
(3)小组同学通过记录实验现象探究了的性质,完成下列表格。
装置 现象 解释
C ①_____ 具有漂白性
D ②浅黄绿色变为无色 其中发生反应离子方程式为______
E ③_____ 具有______
(4)若直接将通入品红溶液中,容易发生“倒吸”现象,小组同学增加如图防倒吸装置B,请在虚线框中画出该装置______。
(5)装置F的作用是尾气处理,盛放的试剂为_____,其中发生反应的离子方程式为____。
18. 铝土矿(主要成分为,还含有和)是生产金属铝的最佳原料,其总产量的90%以上用于生产金属铝。工业上利用铝土矿制备金属铝的工艺流程如下:
回答下列问题:
(1)“浸取”时为了使转化为,试剂①可以选用______,发生反应的离子方程式为______,“浸渣1”为______。
(2)试剂②可以选用______,加入试剂②的用量应______(填“少量”或“足量”),分离的方法为______。
(3)“电解”过程发生反应的化学方程式为_______。
(4)利用铝热反应可以制备许多过渡金属单质,由制备的铝热反应的化学方程式为______。
19. 采用催化还原的处理方法可避免生产硝酸时产生的尾气()污染环境,回答下列问题。
(1)氮氧化物对环境的污染之一是形成酸雨,写出NO在空气中转化为的化学方程式:_____。
(2)一定温度下,向体积为2.0L的刚性密闭容器中充入0.45 mol 和0.50mol ,发生反应:。测得部分气体的物质的量随时间变化关系如图所示。
①该反应中作为还原剂的是______(填化学式,下同),曲线B表示______的物质的量,随时间的变化关系。
②0~5.0 min内,的物质的量浓度的变化量为______(保留2位有效数字,下同),的平均反应速率为_______;平衡时的转化率为_______。
③为了提高该氧化还原反应的速率,可以采取的措施是______(填序号)。
a.加入适宜的催化剂 b.降低温度 c.减小压强 d.提高的浓度
20. 有机玻璃(PMMA)俗称“亚克力”,是一种应用广泛的热塑性塑料。一种合成有机玻璃的工艺流程如下:
已知: (R、代表烃基或氢原子)
回答下列问题:
(1)A的名称为_______。
(2)A→B的反应中除了生成B,另一种副产物的结构简式为________,其与B的关系为______。
(3)C的结构简式为______。
(4)E中所含官能团名称为_______。
(5)E转化为F的化学方程式为_______,反应类型为________。
(6)F在一定条件下发生自身加成聚合反应得到pMMA,PMMA的结构简式为_______。
参考答案
一、选择题:本题共包括16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。
题号 1 2 3 4 5 6 7 8 9 10
答案 B B D B A A A D C C
题号 11 12 13 14 15 16
答案 D D C C D B
17. (1)
(2)b
(3)品红溶液褪色 紫红色变为无色 ④. 还原性
(4)
(5) 氢氧化钠溶液
18. (1) 氢氧化钠溶液 、
(2) 盐酸溶液 足量 过滤
(3)
(4)
19. (1)
(2)①.
②.
③ a、d
20. (1)丙烯
(2) 同分异构体
(3)
(4)碳碳双键、羧基
(5) 取代(酯化)反应
(6)
化 学
注意事项:
1.本试卷共100分,考试时间75分钟。
2.答卷前,考生务必将自己的姓名、准考证号填写在试卷和答题卡上。回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H:1 C:12 N:14 O:16
一、选择题:本题共包括16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 广东省是岭南文化的重要传承地。下列非遗物品中材质不属于硅酸盐的是
A.石湾陶艺 B.潮州木雕 C.肇庆端砚 D.广东砖雕
A. A B. B C. C D. D
2. “神舟十八号”载人飞船发射圆满成功,中国人航天梦又向前迈进了一步。下列说法不正确的是
A. 为神舟系列飞船发射和返回提供保障特种玻璃纤维是一种无机非金属材料
B. 首次在飞船上采用的锂离子蓄电池是一种一次电池
C. 火箭燃料助燃剂是一种非金属氧化物
D. 航天员食用的燕麦片中所含的纤维素是一种人体所需的糖类物质
3. 下列化学用语表述正确的是
A. 甲烷的空间填充模型:
B. 聚丙烯的结构简式:
C. 四氯化碳的电子式:
D. 的名称:1,2-二溴乙烷
4. “劳动是人类生存和社会发展的基础”。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 环保工程师测定雨水的pH≈5.6 雨水中溶解了
B 某同学用热的碱性溶液洗涤沾有油脂的碗碟 油脂的饱和程度越高,熔点越高
C 面点师用含碳酸氢铵的膨松剂制作饼干 碳酸氢铵受热易分解
D 炼化工人将煤气化或液化后再利用 提高煤的利用率
A. A B. B C. C D. D
5. “绿水青山就是金山银山”。下列说法不正确的是
A. 在燃煤过程中加入石灰石,是为了减少温室气体的排放
B. 过量使用化肥可能造成水体富营养化,产生水华现象
C. 电池虽然应该回收利用,但不属于“可回收垃圾”
D. 滥用杀虫剂会破坏生态平衡,造成恶性循环
6. 物质的结构决定性质,性质决定用途。下列物质的结构、性质和用途对应且正确的是
选项 结构 性质 用途
A 分子的结构式为 氮气分子很稳定 可用作反应的保护气
B 的核电荷数小于 比活泼 在溶液原电池中作负极材料
C 油脂含有烃基和酯基 密度比水大,粘度比较大,易溶于有机溶剂 用有机溶剂提取种子里的油
D 硅酸盐中的结构为 硅酸盐的硬度高 硅酸盐材料可用作黏合剂和防火剂
A. A B. B C. C D. D
7. 化学品的合理使用是每一位生产者和消费者的要求和责任。下列关于化学品的描述正确的是
A. 不慎将浓硫酸滴在皮肤上,应立即用大量水冲洗并涂抹稀溶液
B. 处方药需要凭医生处方购买和使用,其包装上有“OTC”标识
C. 淀粉作为一种多糖,可以水解生成葡萄糖和果糖
D. 在食盐中加入碘化钾作为营养强化剂
8. 自然资源的合理开发利用是我们学习化学的重要目的。下列有关说法不正确的是
A. 直接加热氧化银可得到金属银 B. 电解饱和食盐水不能得到金属钠
C. 石油裂解可以得到甲烷 D. 海水提镁所涉及反应均为氧化还原反应
9. 为除去下列物质中的杂质,除杂试剂的选择不合理的是
选项 物质 杂质 除杂试剂
A HCl 饱和食盐水
B NO 水
C 氢氧化钠溶液
D 乙酸乙酯 乙酸 饱和碳酸钠溶液
A. A B. B C. C D. D
10. 山梨酸是一种国家允许使用的防腐剂,其结构如下图所示。下列说法正确的是
A. 山梨酸的分子式为
B. 山梨酸与丙烯酸()互为同系物
C. 1 mol山梨酸与Na反应最多生成0.5 mol
D. 1 mol山梨酸最多可以与3 mol 发生加成反应
11. 工业上以二氧化硫和空气混合制取三氧化硫:(放热反应)。在一定温度下向某刚性密闭容器中充入2mol 和2mol 发生反应,下列描述不能说明该反应达到平衡状态的是
A. 混合气体中的物质的量不再改变
B.
C. 混合气体中的含量不再改变
D. 混合气体中、和物质的量之比为2∶1∶2
12. 下列化学反应的化学方程式或离子方程式书写正确的是
A. Cu与浓硝酸反应:
B. 蔗糖的水解反应:
C. 将二氧化硫通入硫化氢溶液中:
D. 硫酸铁铵[]与过量氢氧化钡溶液的反应:
13. 下图所示的实验装置中,能达到实验目的的是
实验装置
实验目的 A.检验X溶液中含有 B.制备并收集
实验装置
实验目的 C.用喷泉实验验证溶解性 D.探究和发生取代反应
A. A B. B C. C D. D
14. 下列有关电池的描述不正确的是
选项 A.铜锌溶液原电池 B.铜锌溶液原电池
电池
描述 负极质量减小,正极质量几乎不变 负极质量减小,正极质量增大
选项 C.铅酸蓄电池 D.氢氧燃料电池
电池
描述 负极质量增大,正极质量减小 负极和正极质量均几乎不变
A. A B. B C. C D. D
15. 设为阿伏加德罗常数的值。下列说法正确的是
A. 足量Cu与1 mol S充分反应,转移电子的数目为
B. 常温下,将1 mol Cu放入足量稀硝酸中,生成NO分子的数目为2
C. 标准状况下,11.2 L乙酸中乙酸分子的数目为0.5
D. 1 mol正丁烷和异丁烷的混合物在空气中充分燃烧消耗分子的数目为6.5
16. 合成氨工业对农业、工业意义重大,随着科学技术的发展,人们对氨的需求量日益增长。已知:合成氨反应中,生成2 mol 时放出92.4 kJ的热量。下列说法正确的是
A. 若向容器中加入0.5 mol 和1.5 mol 充分反应,则放出的热量为46.2kJ
B. 断裂1 mol 键和3 mol 键需要吸收的能量之和小于形成6 mol 键放出的能量
C. 若升高温度合成氨的产率变高,说明升高温度合成氨的速率变快,氨分解的速率变慢
D. 不改变其他条件,延长反应时间有利于提高氢气的平衡转化率
二、非选择题:本题共4小题,共56分。
17. 是一种常见的无机物,它既是重要的物质资源,也是环境污染物之一,某学习小组改进教材中关于的制备和性质探究实验。回答下列问题:
(1)装置A中铜与浓硫酸反应的化学方程式为______。
(2)查阅资料可知,可以用固体(粉末状)和稀硫酸溶液反应制备,该反应的优点是无需使用加热装置,则可选择的发生装置为______(填序号)。
(3)小组同学通过记录实验现象探究了的性质,完成下列表格。
装置 现象 解释
C ①_____ 具有漂白性
D ②浅黄绿色变为无色 其中发生反应离子方程式为______
E ③_____ 具有______
(4)若直接将通入品红溶液中,容易发生“倒吸”现象,小组同学增加如图防倒吸装置B,请在虚线框中画出该装置______。
(5)装置F的作用是尾气处理,盛放的试剂为_____,其中发生反应的离子方程式为____。
18. 铝土矿(主要成分为,还含有和)是生产金属铝的最佳原料,其总产量的90%以上用于生产金属铝。工业上利用铝土矿制备金属铝的工艺流程如下:
回答下列问题:
(1)“浸取”时为了使转化为,试剂①可以选用______,发生反应的离子方程式为______,“浸渣1”为______。
(2)试剂②可以选用______,加入试剂②的用量应______(填“少量”或“足量”),分离的方法为______。
(3)“电解”过程发生反应的化学方程式为_______。
(4)利用铝热反应可以制备许多过渡金属单质,由制备的铝热反应的化学方程式为______。
19. 采用催化还原的处理方法可避免生产硝酸时产生的尾气()污染环境,回答下列问题。
(1)氮氧化物对环境的污染之一是形成酸雨,写出NO在空气中转化为的化学方程式:_____。
(2)一定温度下,向体积为2.0L的刚性密闭容器中充入0.45 mol 和0.50mol ,发生反应:。测得部分气体的物质的量随时间变化关系如图所示。
①该反应中作为还原剂的是______(填化学式,下同),曲线B表示______的物质的量,随时间的变化关系。
②0~5.0 min内,的物质的量浓度的变化量为______(保留2位有效数字,下同),的平均反应速率为_______;平衡时的转化率为_______。
③为了提高该氧化还原反应的速率,可以采取的措施是______(填序号)。
a.加入适宜的催化剂 b.降低温度 c.减小压强 d.提高的浓度
20. 有机玻璃(PMMA)俗称“亚克力”,是一种应用广泛的热塑性塑料。一种合成有机玻璃的工艺流程如下:
已知: (R、代表烃基或氢原子)
回答下列问题:
(1)A的名称为_______。
(2)A→B的反应中除了生成B,另一种副产物的结构简式为________,其与B的关系为______。
(3)C的结构简式为______。
(4)E中所含官能团名称为_______。
(5)E转化为F的化学方程式为_______,反应类型为________。
(6)F在一定条件下发生自身加成聚合反应得到pMMA,PMMA的结构简式为_______。
参考答案
一、选择题:本题共包括16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。
题号 1 2 3 4 5 6 7 8 9 10
答案 B B D B A A A D C C
题号 11 12 13 14 15 16
答案 D D C C D B
17. (1)
(2)b
(3)品红溶液褪色 紫红色变为无色 ④. 还原性
(4)
(5) 氢氧化钠溶液
18. (1) 氢氧化钠溶液 、
(2) 盐酸溶液 足量 过滤
(3)
(4)
19. (1)
(2)①.
②.
③ a、d
20. (1)丙烯
(2) 同分异构体
(3)
(4)碳碳双键、羧基
(5) 取代(酯化)反应
(6)
同课章节目录
