2.2.3 化学平衡 课件(共29张ppt)高中化学人教版(2019)选择性必修1
文档属性
| 名称 | 2.2.3 化学平衡 课件(共29张ppt)高中化学人教版(2019)选择性必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 21.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-08 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
影响化学平衡的因素
——浓度、压强
第二章 化学反应速率与化学平衡
1.认识化学平衡的移动。
2.通过实验探究,掌握浓度、压强对化学平衡的影响规律。
3.学会用图示的方法表示在可逆反应中正逆反应速率随外界条件的变化,并分析平衡移动的方向。
化学平衡状态有哪些特征?
条件改变,平衡如何变化?
逆
等
动
定
变
v正=v逆
Q = K
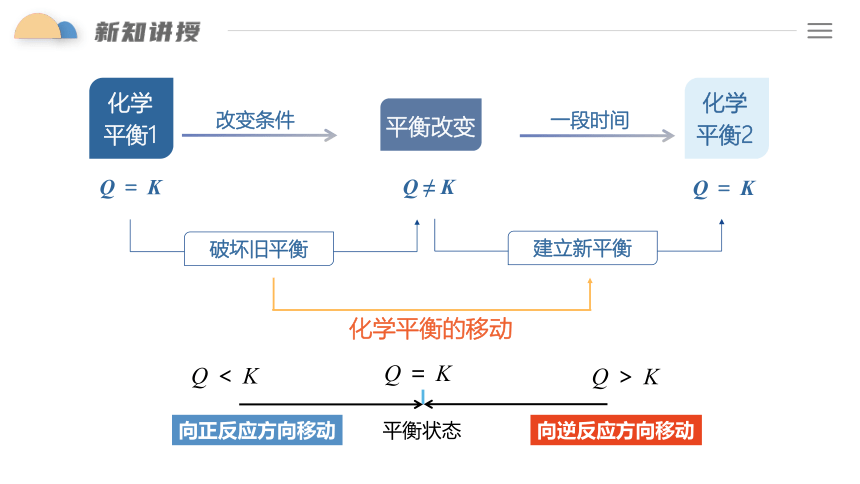
化学
平衡1
破坏旧平衡
建立新平衡
化学平衡的移动
改变条件
一段时间
Q ≠ K
平衡改变
向正反应方向移动
向逆反应方向移动
Q = K
Q < K
Q > K
平衡状态
化学
平衡2
Q = K
一、化学平衡的移动
v正= v逆≠0
条件改变
平衡1
建立新平衡
破坏旧平衡
一段时间
不平衡
平衡2
化学平衡的移动
实质引起了v正、 v逆的改变
v ′正≠ v ′逆
v ′′正= v ′′逆≠0
2. 移动的原因:外界条件发生变化
1.概念:改变外界条件,破坏原有的平衡状态,建立起新的平衡状态的过程。
一、化学平衡的移动
3.平衡移动与反应速率的关系
若外界条件的改变引起
v正> v逆
则平衡正向移动
v正< v逆
v正= v逆
则平衡逆向移动
则平衡不移动
【温故知新】影响化学反应速率的外界条件主要有哪些?
二、浓度对化学平衡的影响
Fe3+(浅黄色)+3SCN- Fe(SCN)3(红色)
[实验原理]
[实验操作]
溶液呈红色
溶液红色变浅
溶液红色加深
Fe+2Fe3+==3Fe2+
c(Fe3+)减小
c(SCN-)增大
平衡逆向移动
平衡正向移动
二、浓度对化学平衡的影响
1、结论:其他条件不变时
增大c(反应物)或减小c(生成物),会使平衡向正反应方向移动;
减小c(反应物)或增大c(生成物),会使平衡向逆反应方向移动。
2、理论解释——Q与K 大小判断
b溶液中 c溶液中
改变条件 发生反应:Fe+2Fe3+===3Fe2+, c(Fe3+)减小,即反应物浓度减小 c(SCN-)增大,即反应物浓度增大
从Q、K关系角度 Q= , Q= ,
Q>K,平衡逆向移动
Q<K,平衡正向移动
增大
减小
【注意】
①改变固态或纯液态的量,化学平衡不移动
②作为离子反应,只有改变实际参加反应的离子浓度,才对平衡有影响。
如:Fe3+ + 3SCN- Fe(SCN)3
加入KCl,对平衡无影响。
③反应物有两种或两种以上, 增加一种物质的浓度, 该物质的平衡转化率降低, 而其他物质的转化率提高。
【应用】
工业生产时,适当增大廉价反应物浓度来提高另一反应物的转
化率,以降低生产成本。
二、浓度对化学平衡的影响
●
●
v'正
v'逆
v'正=v'逆
●
●
v'正
v'逆
增大反应物的浓度
减小生成物的浓度
v'正=v'逆
平衡向正反应方向移动
v
t
0
●
●
v正
v逆
t1
v
t
0
●
●
v正
v逆
t1
3.用v –t 图像表示如下:
●
●
v'逆
v'正
v'正=v'逆
●
●
v'逆
v'正
增大生成物的浓度
减小反应物的浓度
v'正=v'逆
平衡向逆反应方向移动
v
t
0
●
●
v正
v逆
t1
v
t
0
●
●
v正
v逆
t1
图像具有连续性!
二、浓度对化学平衡的影响
3.用v –t 图像表示如下:
思考与讨论
讨论1:试用“浓度对化学平衡的影响”来解释“用排饱和食盐水法收集Cl2可以抑制Cl2的溶解”。
Cl2溶解于水,存在溶解平衡。
溶解的部分Cl2能与水反应: Cl2 + H2O H+ + Cl- + HClO
饱和食盐水增大Cl-浓度,使平衡向逆反应方向移动,从而使Cl2溶解度降低
思考与讨论
讨论2:H2O(g) +C(s) CO(g) + H2(g),在密闭容器中进行。一定条件下达到平衡状态,改变下列条件,能否引起平衡移动?CO浓度有何变化?
①增大水蒸汽浓度
②加入固体炭
③增加H2浓度
正向移动,CO浓度增大
逆向移动,CO浓度减小
不移动,CO浓度不变
结论:对平衡体系中的固态和纯液态物质,增加或减小固态或液态纯净物的量并不影响v正、v逆的大小,所以化学平衡不移动。
三、压强对化学平衡的影响
[实验原理]
[实验操作]
(红棕色)
(无色)
2NO2(g) N2O4(g)
用50 mL注射器吸入20 mL NO2与N2O4的混合气体,并将细管端用
橡皮塞封闭。然后将活塞向外拉,观察管内混合气体颜色的变化。当反复推拉活塞时,观察管内混合气体颜色的变化。
气体颜色先变深,后变浅
最终比原来深
气体颜色先变浅,后变深
最终比原来浅
实验 活塞往里推时,体系压强增大 活塞往外拉时,体系压强减小
现象
结论
增大压强,化学平衡向生成_______的方向移动
N2O4
减小压强,化学平衡向生成_______的方向移动
NO2
系数减小的方向
系数增大的方向
三、压强对化学平衡的影响
[理论解释]
2NO2(g) N2O4(g)
(温度不变) 压强 c(NO2) c(N2O4) 浓度商(Q )
原平衡容器容积为V p1 a b
缩小容积至V 瞬时
2p1
2a
b
=
Q=K
浓度增大,气体颜色先变深
平衡正向移动
达到新平衡(容积V)
p1< p新 < 2p1
a< c新 < 2a
2b< c新 < 2b+a
不变
颜色后变浅,但仍比原平衡颜色深
[结论]
对于有气体参加的可逆反应:
(1)若为反应前后气体体积不等的反应,如N2+3H2 2NH3:
增大压强后,平衡向 的方向移动;
减小压强后,平衡向 的方向移动。
气体体积减小
气体体积增大
(2)若为等体积反应,如H2+I2 2HI,改变压强后, 平衡 。
不移动
外界条件改变,平衡向着减弱这种改变的方向移动
三、压强对化学平衡的影响
用v –t 图像表示如下:
mA(g)+nB(g) pC(g)+qD(g)
v (正)
v (逆)
v'正=v'逆
v正=v逆
增大压强
v (正)
v (逆)
v'正=v'逆
v正=v逆
减小压强
①m+n>p+q
平衡正移
平衡逆移
三、压强对化学平衡的影响
用v –t 图像表示如下:
mA(g)+nB(g) pC(g)+qD(g)
v (逆)
v (正)
v'正=v'逆
增大压强
v (逆)
v (正)
v'正=v'逆
减小压强
②m+n平衡逆移
平衡正移
三、压强对化学平衡的影响
用v –t 图像表示如下:
mA(g)+nB(g) pC(g)+qD(g)
v'正=v'逆
增大压强
v'正=v'逆
减小压强
③m+n=p+q
平衡不移
平衡不移
“惰性气体”对化学平衡的影响
(1)恒温恒容条件
原平衡体系
体系总压强增大
体系中各组分的浓度
平衡 。
充入惰性气体
(2)恒温恒压条件
原平衡体系
容器容积 ,各反应气体的分压
各组分的浓度同倍数
充入惰性气体
体系中
平衡向气体体积 的方向移动。
(3)反应前后气体体积相等的反应[如H2(g)+I2(g) 2HI(g)]
当向平衡体系中充入“惰性”气体时,则无论任何情况下平衡都不发生移动。
不变
不移动
增大
减小
减小
增大
【特别提醒】
你能解释以下生活中的现象吗?
CO2+H2O H2CO3
【学以致用】
1.压强的变化不会使下列反应的平衡发生移动的是( )
A、H2(g)+I2(g) 2HI(g)
B、 N2(g)+3H2(g) 2NH3(g)
C、2SO2(g)+O2(g) 2SO3(g)
D、 C(s)+CO2(g) 2CO(g)
E 、 Fe3++n SCN- [Fe(SCN)n] 3-n
A E
固态或液态物质的体积受压强影响很小,可以忽略不计。
当平衡混合物中都是固态或液态物质时,改变压强后化学平衡一般不发生移动。
2.恒温下, 反应aX(g) bY(g)+cZ(g)达到平衡后, 把容器体积压缩到原来的一半且达到新平衡时, X的物质的量浓度由0.1mol/L增大到0.19mol/L, 下列判断正确的是( )
A、 a>b+c
B、 a<b+c
C、 a=b+c
D、 a=b=c
A
3.在N2(g)+3H2 (g) 2NH3 (g)密闭反应体系中,充入He气体:
⑴容积不变时,反应物质浓度—————,反应速率————,化学平衡——————;
⑵气体压强不变时,气体物质的浓度———,化学平衡向—————方向移动
不变
不变
不移动
减小
增体
压强变化若没有引起浓度的变化,
化学反应速率————,化学平衡____________。
不变
不移动
注意点:
4.一定量的混合气体在密闭容器中发生反应:
m A (g) + n B (g) p C (g)
达到平衡后,温度不变,将气体体积缩小到原来的1/2但达到平衡时,C的浓度为原来的1.8倍,则下列说法正确的是( )
A、m + n > p
B、A 的转化率降低
C、平衡向正反应方向移动
D、C的体积分数增加
B
V’正
v
t
V正
V逆
V’逆
V’正=V’逆
5.有反应aA + bB cC + dD其中反应物与生成物均为气体,达到平衡后其他条件不变,改变压强,则下图适合哪种情况( )
A、a+bc+d,加压
C、a+bc+d,减压
B
6.一定条件下,反应4NH3(g)+5O2 (g) 4NO(g)+6H2O(g)在一容器中达平衡状态,压强为P0,其它条件不变,将容器体积缩小为原来的一半,达平衡时压强为P1,则P0、P1、2P0的关系为____________
P1
P0
2P0
<
<
影响化学平衡的因素
——浓度、压强
第二章 化学反应速率与化学平衡
1.认识化学平衡的移动。
2.通过实验探究,掌握浓度、压强对化学平衡的影响规律。
3.学会用图示的方法表示在可逆反应中正逆反应速率随外界条件的变化,并分析平衡移动的方向。
化学平衡状态有哪些特征?
条件改变,平衡如何变化?
逆
等
动
定
变
v正=v逆
Q = K
化学
平衡1
破坏旧平衡
建立新平衡
化学平衡的移动
改变条件
一段时间
Q ≠ K
平衡改变
向正反应方向移动
向逆反应方向移动
Q = K
Q < K
Q > K
平衡状态
化学
平衡2
Q = K
一、化学平衡的移动
v正= v逆≠0
条件改变
平衡1
建立新平衡
破坏旧平衡
一段时间
不平衡
平衡2
化学平衡的移动
实质引起了v正、 v逆的改变
v ′正≠ v ′逆
v ′′正= v ′′逆≠0
2. 移动的原因:外界条件发生变化
1.概念:改变外界条件,破坏原有的平衡状态,建立起新的平衡状态的过程。
一、化学平衡的移动
3.平衡移动与反应速率的关系
若外界条件的改变引起
v正> v逆
则平衡正向移动
v正< v逆
v正= v逆
则平衡逆向移动
则平衡不移动
【温故知新】影响化学反应速率的外界条件主要有哪些?
二、浓度对化学平衡的影响
Fe3+(浅黄色)+3SCN- Fe(SCN)3(红色)
[实验原理]
[实验操作]
溶液呈红色
溶液红色变浅
溶液红色加深
Fe+2Fe3+==3Fe2+
c(Fe3+)减小
c(SCN-)增大
平衡逆向移动
平衡正向移动
二、浓度对化学平衡的影响
1、结论:其他条件不变时
增大c(反应物)或减小c(生成物),会使平衡向正反应方向移动;
减小c(反应物)或增大c(生成物),会使平衡向逆反应方向移动。
2、理论解释——Q与K 大小判断
b溶液中 c溶液中
改变条件 发生反应:Fe+2Fe3+===3Fe2+, c(Fe3+)减小,即反应物浓度减小 c(SCN-)增大,即反应物浓度增大
从Q、K关系角度 Q= , Q= ,
Q>K,平衡逆向移动
Q<K,平衡正向移动
增大
减小
【注意】
①改变固态或纯液态的量,化学平衡不移动
②作为离子反应,只有改变实际参加反应的离子浓度,才对平衡有影响。
如:Fe3+ + 3SCN- Fe(SCN)3
加入KCl,对平衡无影响。
③反应物有两种或两种以上, 增加一种物质的浓度, 该物质的平衡转化率降低, 而其他物质的转化率提高。
【应用】
工业生产时,适当增大廉价反应物浓度来提高另一反应物的转
化率,以降低生产成本。
二、浓度对化学平衡的影响
●
●
v'正
v'逆
v'正=v'逆
●
●
v'正
v'逆
增大反应物的浓度
减小生成物的浓度
v'正=v'逆
平衡向正反应方向移动
v
t
0
●
●
v正
v逆
t1
v
t
0
●
●
v正
v逆
t1
3.用v –t 图像表示如下:
●
●
v'逆
v'正
v'正=v'逆
●
●
v'逆
v'正
增大生成物的浓度
减小反应物的浓度
v'正=v'逆
平衡向逆反应方向移动
v
t
0
●
●
v正
v逆
t1
v
t
0
●
●
v正
v逆
t1
图像具有连续性!
二、浓度对化学平衡的影响
3.用v –t 图像表示如下:
思考与讨论
讨论1:试用“浓度对化学平衡的影响”来解释“用排饱和食盐水法收集Cl2可以抑制Cl2的溶解”。
Cl2溶解于水,存在溶解平衡。
溶解的部分Cl2能与水反应: Cl2 + H2O H+ + Cl- + HClO
饱和食盐水增大Cl-浓度,使平衡向逆反应方向移动,从而使Cl2溶解度降低
思考与讨论
讨论2:H2O(g) +C(s) CO(g) + H2(g),在密闭容器中进行。一定条件下达到平衡状态,改变下列条件,能否引起平衡移动?CO浓度有何变化?
①增大水蒸汽浓度
②加入固体炭
③增加H2浓度
正向移动,CO浓度增大
逆向移动,CO浓度减小
不移动,CO浓度不变
结论:对平衡体系中的固态和纯液态物质,增加或减小固态或液态纯净物的量并不影响v正、v逆的大小,所以化学平衡不移动。
三、压强对化学平衡的影响
[实验原理]
[实验操作]
(红棕色)
(无色)
2NO2(g) N2O4(g)
用50 mL注射器吸入20 mL NO2与N2O4的混合气体,并将细管端用
橡皮塞封闭。然后将活塞向外拉,观察管内混合气体颜色的变化。当反复推拉活塞时,观察管内混合气体颜色的变化。
气体颜色先变深,后变浅
最终比原来深
气体颜色先变浅,后变深
最终比原来浅
实验 活塞往里推时,体系压强增大 活塞往外拉时,体系压强减小
现象
结论
增大压强,化学平衡向生成_______的方向移动
N2O4
减小压强,化学平衡向生成_______的方向移动
NO2
系数减小的方向
系数增大的方向
三、压强对化学平衡的影响
[理论解释]
2NO2(g) N2O4(g)
(温度不变) 压强 c(NO2) c(N2O4) 浓度商(Q )
原平衡容器容积为V p1 a b
缩小容积至V 瞬时
2p1
2a
b
=
Q=K
浓度增大,气体颜色先变深
平衡正向移动
达到新平衡(容积V)
p1< p新 < 2p1
a< c新 < 2a
2b< c新 < 2b+a
不变
颜色后变浅,但仍比原平衡颜色深
[结论]
对于有气体参加的可逆反应:
(1)若为反应前后气体体积不等的反应,如N2+3H2 2NH3:
增大压强后,平衡向 的方向移动;
减小压强后,平衡向 的方向移动。
气体体积减小
气体体积增大
(2)若为等体积反应,如H2+I2 2HI,改变压强后, 平衡 。
不移动
外界条件改变,平衡向着减弱这种改变的方向移动
三、压强对化学平衡的影响
用v –t 图像表示如下:
mA(g)+nB(g) pC(g)+qD(g)
v (正)
v (逆)
v'正=v'逆
v正=v逆
增大压强
v (正)
v (逆)
v'正=v'逆
v正=v逆
减小压强
①m+n>p+q
平衡正移
平衡逆移
三、压强对化学平衡的影响
用v –t 图像表示如下:
mA(g)+nB(g) pC(g)+qD(g)
v (逆)
v (正)
v'正=v'逆
增大压强
v (逆)
v (正)
v'正=v'逆
减小压强
②m+n
平衡正移
三、压强对化学平衡的影响
用v –t 图像表示如下:
mA(g)+nB(g) pC(g)+qD(g)
v'正=v'逆
增大压强
v'正=v'逆
减小压强
③m+n=p+q
平衡不移
平衡不移
“惰性气体”对化学平衡的影响
(1)恒温恒容条件
原平衡体系
体系总压强增大
体系中各组分的浓度
平衡 。
充入惰性气体
(2)恒温恒压条件
原平衡体系
容器容积 ,各反应气体的分压
各组分的浓度同倍数
充入惰性气体
体系中
平衡向气体体积 的方向移动。
(3)反应前后气体体积相等的反应[如H2(g)+I2(g) 2HI(g)]
当向平衡体系中充入“惰性”气体时,则无论任何情况下平衡都不发生移动。
不变
不移动
增大
减小
减小
增大
【特别提醒】
你能解释以下生活中的现象吗?
CO2+H2O H2CO3
【学以致用】
1.压强的变化不会使下列反应的平衡发生移动的是( )
A、H2(g)+I2(g) 2HI(g)
B、 N2(g)+3H2(g) 2NH3(g)
C、2SO2(g)+O2(g) 2SO3(g)
D、 C(s)+CO2(g) 2CO(g)
E 、 Fe3++n SCN- [Fe(SCN)n] 3-n
A E
固态或液态物质的体积受压强影响很小,可以忽略不计。
当平衡混合物中都是固态或液态物质时,改变压强后化学平衡一般不发生移动。
2.恒温下, 反应aX(g) bY(g)+cZ(g)达到平衡后, 把容器体积压缩到原来的一半且达到新平衡时, X的物质的量浓度由0.1mol/L增大到0.19mol/L, 下列判断正确的是( )
A、 a>b+c
B、 a<b+c
C、 a=b+c
D、 a=b=c
A
3.在N2(g)+3H2 (g) 2NH3 (g)密闭反应体系中,充入He气体:
⑴容积不变时,反应物质浓度—————,反应速率————,化学平衡——————;
⑵气体压强不变时,气体物质的浓度———,化学平衡向—————方向移动
不变
不变
不移动
减小
增体
压强变化若没有引起浓度的变化,
化学反应速率————,化学平衡____________。
不变
不移动
注意点:
4.一定量的混合气体在密闭容器中发生反应:
m A (g) + n B (g) p C (g)
达到平衡后,温度不变,将气体体积缩小到原来的1/2但达到平衡时,C的浓度为原来的1.8倍,则下列说法正确的是( )
A、m + n > p
B、A 的转化率降低
C、平衡向正反应方向移动
D、C的体积分数增加
B
V’正
v
t
V正
V逆
V’逆
V’正=V’逆
5.有反应aA + bB cC + dD其中反应物与生成物均为气体,达到平衡后其他条件不变,改变压强,则下图适合哪种情况( )
A、a+b
C、a+b
B
6.一定条件下,反应4NH3(g)+5O2 (g) 4NO(g)+6H2O(g)在一容器中达平衡状态,压强为P0,其它条件不变,将容器体积缩小为原来的一半,达平衡时压强为P1,则P0、P1、2P0的关系为____________
P1
P0
2P0
<
<
