1.2物质的酸碱性 同步练习(含解析)
文档属性
| 名称 | 1.2物质的酸碱性 同步练习(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 334.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-08-08 00:00:00 | ||
图片预览




文档简介
1.2物质的酸碱性 同步练习
、选择题
把氯化氢、食盐、生石灰分别溶于水,往它们的溶液中分别滴入紫色石蕊试液,溶液呈现的颜色依次是( )
A.红色、紫色、蓝色 B.红色、蓝色、紫色
C.红色、无色、蓝色 D.蓝色、紫色、红色
高铁酸钾(K2FeO4)是一种新型的水处理剂,易溶于水,易与水反应,与水反应的化学方程式为4K2FeO4 + 10H2O===4Fe(OH)3↓ + 8KOH+ 3O2↑。该事例说明( )
A.高铁酸钾是一种氧化物
B.K2FeO4溶于水后有大量的FeO
C.高铁酸钾中铁的化合价是+3价
D.用高铁酸钾净化过的水,pH升高
取三种植物的花瓣分别放在研钵中,加入酒精研磨,得到花汁。各取少许花汁,用稀酸和稀碱进行检验,结果如下表所示:则下列说法中正确的是( )
花的种类 花汁在酒精中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
玫瑰 粉红色 粉红色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
A.上述三种花汁都能用作酸碱指示剂
B.可用雏菊花汁来区别H2SO4和K2SO4溶液
C.研磨花瓣过程中加入酒精是为了溶解其中的色素
D.25℃时,遇到pH=10的溶液,玫瑰花汁会变成粉红色
不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是( )
A.冼手液c的碱性比d弱
B.洗手液c能使石蕊试液变蓝色
C.洗手液a用蒸馏水稀释后pH减小
D.洗手液d和a混合液的pH可能等于7
婴儿纸尿裤的“尿显”试剂常用溴甲酚绿(pH试纸上的显色物质之一),其在pH≤3.8时呈黄色,pH≥5.4 时呈蓝绿色,pH=4.5 时开始有颜色的明显变化。已知婴儿尿液的pH范围为5.4-8.4,那么,当婴儿尿湿纸尿裤时,“尿显”试剂显示的颜色最有可能是( )
A.无色 B.黄色 C.蓝绿色 D.黄绿色
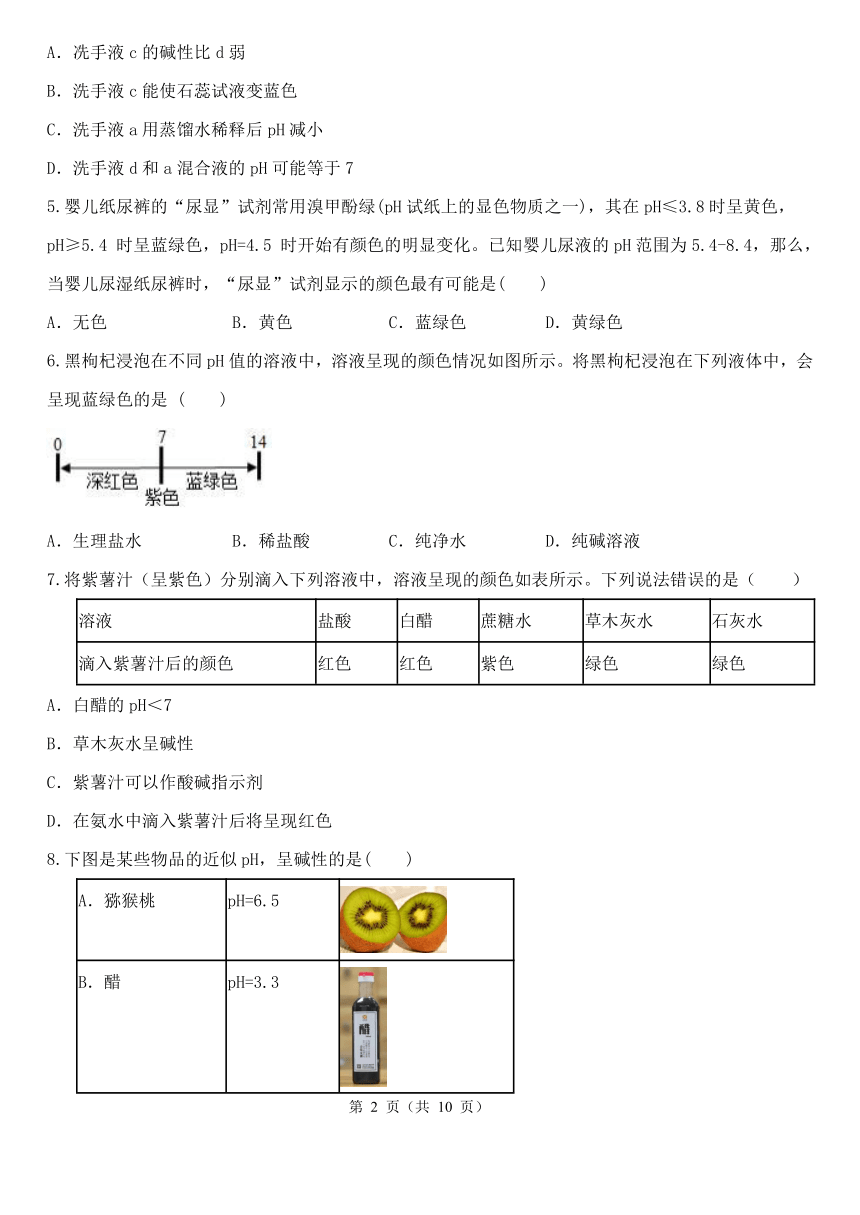
黑枸杞浸泡在不同pH值的溶液中,溶液呈现的颜色情况如图所示。将黑枸杞浸泡在下列液体中,会呈现蓝绿色的是 ( )
A.生理盐水 B.稀盐酸 C.纯净水 D.纯碱溶液
将紫薯汁(呈紫色)分别滴入下列溶液中,溶液呈现的颜色如表所示。下列说法错误的是( )
溶液 盐酸 白醋 蔗糖水 草木灰水 石灰水
滴入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
A.白醋的pH<7
B.草木灰水呈碱性
C.紫薯汁可以作酸碱指示剂
D.在氨水中滴入紫薯汁后将呈现红色
下图是某些物品的近似pH,呈碱性的是( )
A.猕猴桃 pH=6.5
B.醋 pH=3.3
C.纯牛奶 pH=3.2
D.小苏打 pH=9.1
A.A B.B C.C D.D
下列说法中正确的是( )
A.可以按溶解、过滤、蒸发的操作顺序将硝酸钾和硝酸钠分离出来
B.用氢气还原氧化铜实验中,先加热再通入氢气
C.用洁净玻璃棒蘸取少量某未知溶液滴在湿润的pH试纸上,判断未知溶液的酸碱度
D.利用紫色石落试液把氢氧化钠溶液、稀硫酸、氯化钠溶液、氯化钡溶液鉴别出来
经检验,四种溶液中除含有水分子外分别只含有以下离子,其中属于酸的水溶液的是( )
A.H+、Na+、SO42- B.Ca2+、Cl-
C.Ba2+、NO3- D.H+、Cl-
、填空题
碱在水中电离时,生成的阴离子都是相同的一种粒子 。常见的碱有氢氧化钠、氢氧化钙、氢氧化钡、氢氧化钾、氨水等。
根据生活经验,人体胃酸的pH 7(选填“>”“<”或“=”).维生素C溶液的pH小于7,显 性(选填“酸”“碱”或“中性”)
如下图所示:若关闭II阀打开I阀,紫色小花(用石蕊溶液染成)变红;若关闭I阀打开II阀,小花不变红。
(1)若甲瓶中未发生化学反应,则甲瓶中盛有的液体可能是
(2)若甲瓶中发生化学反应,但无明显现象,则甲瓶中发生的反应方程式可能为:
、实验探究题
在拓展性课程活动中,小明利用以下常见物品验证酸的一些性质:
白醋(含 3%的醋酸)、食品干燥剂(主要成分是 CaO)、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠)。
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝 色。
【实验过程】
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊。则鸡蛋 壳中一定含有 。(用离子符号表示)
(2)小明知道酸能够与铁发生反应产生氢气,但当他将足量的白醋加入放有铁钉的容器中, 没有看到明显的气泡产生.小明很疑惑,于是提出猜想:气泡不明显可能与酸的浓度有关.要验证与酸的浓度有关,应选择下例试剂中的 。(选填编号)
A.3%的盐酸 B.5%的醋酸 C.5%的盐酸
(3)小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计
步骤 操作 现象
1 将食品干燥剂加入适量清水中,搅拌后静置 放出大量的热
2 取步骤 1 中的上层清液,先加入牵牛花汁液, 溶液由无色变为蓝色,再变为紫色,最后变为红色
、解答题
2024年6月份公布的《2023年温州市环境状况公报》显示近5年我市酸雨率逐年降低,这与电动汽车的使用有一定的关系。自然降水因空气含二氧化碳而呈酸性,燃油汽车的使用会产生二氧化碳、氮氧化物等酸性气体,从而使降水的pH降低,pH小于5.6的降水称为酸雨。
(1)自然降水呈酸性的原因是 。
(2)使用纯电动汽车减少 排放,符合环保。
(3)小明想通过如图所示的实验寻找蒸馏水变成酸雨的证据,你认为下一步的实验操作是: 。
1.2物质的酸碱性 同步练习答案解析
、选择题
A
【解析】根据石蕊遇酸溶液变红,遇中性溶液呈紫色,遇碱性溶液变蓝分析。
氯化氢、食盐、生石灰分别溶于水后溶液分别呈酸性、中性和碱性,所以滴入紫色石蕊试液,溶液呈现的颜色依次是红色、紫色和蓝色;
故答案为:A.
D
【解析】(1)只由两种元素组成,且其中一种是氧元素的化合物,叫氧化物;
(2)根据反应产物判断;
(3)根据正负化合价的代数和为零计算;
(4)注意生成物中有氢氧化钾。
A.根据化学式K2FeO4可知,高铁酸钾由三种元素组成,肯定不是氧化物,故A错误;
B.根据方程式可知,生成物为氢氧化铁、氢氧化钾和氧气,故B错误;
C.根据化学式K2FeO4可知,(+1)×2+x+(-2)×4=0,解得:x=+6,故C错误;
D.因为生成物中有氢氧化钾,而氢氧化钾溶液呈碱性,因此pH升高,故D正确。
故选D。
C
【解析】根据三种植物的花的汁液在酸性、中性、碱性溶液中颜色的变化分析。
A.万寿菊在酸碱溶液中呈现颜色相同,不能作酸碱指示剂,不符合题意;
B、雏菊花汁在酸和中性的溶液中呈现相同颜色,不能区别硫酸和硫酸钾溶液 ,不符合题意;
C、酒精是一种常用的有机溶剂,研磨花瓣过程中加入酒精是为了溶解其中的色素,符合题意;
D、由玫瑰花汁在碱性溶液中的颜色可知,25℃时,遇到pH=10的溶液,玫瑰花汁会变成绿色 ,不符合题意;
故选C。
C
【解析】根据溶液的pH确定酸碱性,pH大于7呈碱性,小于7呈酸性,pH越小酸性越强,越大碱性越强分析。
A.洗手液cpH小于d, c的碱性比d弱 ,不符合题意;
B. 洗手液cpH大于7,呈碱性,能使石蕊试液变蓝色 ,不符合题意;
C. 洗手液apH小于7,呈酸性,用蒸馏水稀释后pH增大 ,符合题意;
D. 洗手液d呈碱性,a呈酸性,二者混合液的pH可能等于7 ,不符合题意;
故选C。
C
【解析】将婴儿尿液的pH范围与变色范围进行对比即可。
婴儿尿液的pH范围为5.4-8.4,而这种试剂pH≥5.4时呈蓝绿色,因此婴儿尿湿纸尿裤时最有可能呈现蓝绿色,故C正确,而A.B、D错误。
故选C。
D
【解析】根据生理盐水、纯净水呈中性,稀盐酸呈酸性,纯碱溶液呈碱性及图未中酸、碱、中性使枸杞的变色情况分析。
A.生理盐水呈中性,pH=7,使黑枸杞呈现紫色,不符合题意;
B.稀盐酸呈酸性,pH<7,使黑枸杞呈深红色,不符合题意;
C.纯净水呈中性,pH=7,使黑枸杞呈现紫色,不符合题意;
D.纯碱溶液呈碱性,pH>7,使黑枸杞呈现蓝绿色,符合题意;
故选D。
D
【解析】根据酸碱指示剂的用途分析判断。
根据表格可知,紫薯汁遇到酸呈红色,遇到中性溶液不变色,遇到碱性溶液时变成绿色。
A.紫薯汁遇到白醋变成红色,则白醋呈酸性,即白醋的pH<7,故A正确不合题意;
B.紫薯汁遇到草木灰变成绿色,即草木灰水呈碱性,故B正确不合题意;
C.紫薯汁遇到酸碱溶液时呈现不同的颜色,可以做酸碱指示剂,故C正确不合题意;
D.氨水呈碱性,则在氨水中滴入紫薯汁后将呈现绿色,故D错误符合题意。
故选D。
D
【解析】根据溶液pH与酸碱性关系分析,溶液pH<7时,呈酸性,且越小酸性越强,溶液pH>7时,呈碱性,且越大碱性越强,溶液pH=7时,呈中性。
A. 猕猴桃pH<7,呈酸性 ,不符合题意;
B、醋pH<7,呈酸性 ,不符合题意;
C、纯牛奶pH<7,呈酸性 ,不符合题意;
D、小苏打pH>7,呈碱性,符合题意;
故选D。
D
【解析】(1)使用溶解、过滤、蒸发分离物质,那么物质的溶解性的差异必须十分明显;
(2)用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH;
(3)酸或碱被稀释后,浓度减小,它们的pH值都会向7靠近;
(4)先用石蕊试液鉴别出酸和碱,再利用它们鉴别剩下的盐;A.硝酸钾和硝酸钠均易溶于水,不能用溶解、过滤、蒸发的操作顺序进行分离,故A错误;
B.用氢气还原氧化铜实验中,先通入氢气再加热,以排尽装置中的空气,防止发生爆炸,故B错误;
C.不能用水湿润pH试纸,若溶液显酸性或碱性,则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,故C错误;
D.氢氧化钠溶液、稀硫酸、氯化钠溶液、氯化钡溶液分别显碱性、酸性、中性、中性,分别能使紫色石蕊溶液显蓝色、红色、紫色、紫色,能鉴别出氢氧化钠溶液、稀硫酸,再将稀硫酸滴加至氯化钠、氯化钡溶液中,能与稀硫酸反应生成白色沉淀的是氯化钡溶液,可以鉴别,故D正确。
故选D。
D
【解析】根据酸的定义分析,酸是电离时产生的阳离子全部是氢离子的化合物。
A.阳离子还有钠离子,不属于酸,不符合题意;
B、阳离子不含氢离子,不属于酸,不符合题意;
C、阳离子不含氢离子,不属于酸,不符合题意;
D、阳离子全部是氢离子,属于酸,符合题意;
故选D。
、填空题
OH-
【解析】碱是指电离时电离出的阴离子全部是氢氧根离子的化合物。
电离时电离出的阴离子全部是氢氧根离子的化合物是碱。碱具有通性的原因是因为阴离子全部是氢氧根离子。
故答案为:OH-
<;酸
【解析】可以根据溶液的pH与溶液的酸碱性关系进行分析和判断,当pH=7时,呈中性,当pH<7时,呈酸性,当pH>7时,呈碱性.本题主要考查了溶液的酸碱性强弱与溶液pH大小的关系.
解:人体胃酸的主要成分是盐酸,所以pH<7,维生素C溶液的pH小于7,显酸性.
故答案为:<;酸.
(1)浓硫酸
(2)2NaOH+CO2=Na2CO3+H2O
【解析】(1)根据甲瓶中液体的用途分析;
(2)根据二氧化碳和氢氧化钠的反应解答。
(1)甲瓶中没有发生化学反应,即二氧化碳没有被吸收。根据紫色小花没有变色可知,甲对二氧化碳起干燥作用,那么应该是具有吸水性的浓硫酸。
(2)氢氧化钠和二氧化碳反应,生成碳酸钠和水,没有明显现象发生,
反应的方程式为:2NaOH+CO2=Na2CO3+H2O。
、实验探究题
(1)CO32-
(2)B
(3)滴加白醋至过量
【解析】(1)根据酸能够和碳酸根离子反应产生二氧化碳,二氧化碳能使澄清的石灰水变浑浊分析;
(2)根据控制变量法中提出的猜想可以选择试剂,题中研究与酸的浓度的关系,所以应选择浓度不同的同种溶液;
(3)由查阅的资料,根据牵牛花汁液作指示剂时溶液颜色的变化,由现象确定进行的操作。
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊,该气体是二氧化碳,因此说明鸡蛋壳中一定含有CO32-;故填:CO32-;
(2)该实验用的是3%的醋酸溶液,因此选择不同浓度的醋酸溶液即可对比实验;故填:B;
(3)向氢氧化钙的溶液中滴加牵牛花汁,溶液由无色变为蓝色,再变为紫色,最后变为红色,可知溶液由碱性变成中性,最后呈现酸性,因此向溶液中滴加醋酸最后醋酸过量;故填:再逐滴滴加白醋至过量
故答案为:(1)CO32-;(2)B;(3)滴加白醋至过量
、解答题
(1)二氧化碳与水反应形成碳酸
(2)二氧化硫、氮氧化物等酸性气体的产生
(3)用洁净的玻璃棒蘸取被测试的溶液,滴在 pH试纸上,将试纸显示的颜色与标准比色 卡对照
【解析】(1)根据“自然降水因空气含二氧化碳而呈酸性”解答;
(2)根据“燃油汽车的使用会产生二氧化碳、氮氧化物等酸性气体”解答;
(3)蒸馏水变成酸雨,它肯定呈酸性,可以用测定溶液pH的方法进行验证操作。
(1)自然降水呈酸性的原因是:二氧化碳与水反应形成碳酸。
(2)使用纯电动汽车减少二氧化硫、氮氧化物等酸性气体的产生排放,符合环保。
(3)小明想通过如图所示的实验寻找蒸馏水变成酸雨的证据,我认为下一步的实验操作是:用洁净的玻璃棒蘸取被测试的溶液,滴在 pH试纸上,将试纸显示的颜色与标准比色卡对照。
第 1 页(共 1 页)
、选择题
把氯化氢、食盐、生石灰分别溶于水,往它们的溶液中分别滴入紫色石蕊试液,溶液呈现的颜色依次是( )
A.红色、紫色、蓝色 B.红色、蓝色、紫色
C.红色、无色、蓝色 D.蓝色、紫色、红色
高铁酸钾(K2FeO4)是一种新型的水处理剂,易溶于水,易与水反应,与水反应的化学方程式为4K2FeO4 + 10H2O===4Fe(OH)3↓ + 8KOH+ 3O2↑。该事例说明( )
A.高铁酸钾是一种氧化物
B.K2FeO4溶于水后有大量的FeO
C.高铁酸钾中铁的化合价是+3价
D.用高铁酸钾净化过的水,pH升高
取三种植物的花瓣分别放在研钵中,加入酒精研磨,得到花汁。各取少许花汁,用稀酸和稀碱进行检验,结果如下表所示:则下列说法中正确的是( )
花的种类 花汁在酒精中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
玫瑰 粉红色 粉红色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
A.上述三种花汁都能用作酸碱指示剂
B.可用雏菊花汁来区别H2SO4和K2SO4溶液
C.研磨花瓣过程中加入酒精是为了溶解其中的色素
D.25℃时,遇到pH=10的溶液,玫瑰花汁会变成粉红色
不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是( )
A.冼手液c的碱性比d弱
B.洗手液c能使石蕊试液变蓝色
C.洗手液a用蒸馏水稀释后pH减小
D.洗手液d和a混合液的pH可能等于7
婴儿纸尿裤的“尿显”试剂常用溴甲酚绿(pH试纸上的显色物质之一),其在pH≤3.8时呈黄色,pH≥5.4 时呈蓝绿色,pH=4.5 时开始有颜色的明显变化。已知婴儿尿液的pH范围为5.4-8.4,那么,当婴儿尿湿纸尿裤时,“尿显”试剂显示的颜色最有可能是( )
A.无色 B.黄色 C.蓝绿色 D.黄绿色
黑枸杞浸泡在不同pH值的溶液中,溶液呈现的颜色情况如图所示。将黑枸杞浸泡在下列液体中,会呈现蓝绿色的是 ( )
A.生理盐水 B.稀盐酸 C.纯净水 D.纯碱溶液
将紫薯汁(呈紫色)分别滴入下列溶液中,溶液呈现的颜色如表所示。下列说法错误的是( )
溶液 盐酸 白醋 蔗糖水 草木灰水 石灰水
滴入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
A.白醋的pH<7
B.草木灰水呈碱性
C.紫薯汁可以作酸碱指示剂
D.在氨水中滴入紫薯汁后将呈现红色
下图是某些物品的近似pH,呈碱性的是( )
A.猕猴桃 pH=6.5
B.醋 pH=3.3
C.纯牛奶 pH=3.2
D.小苏打 pH=9.1
A.A B.B C.C D.D
下列说法中正确的是( )
A.可以按溶解、过滤、蒸发的操作顺序将硝酸钾和硝酸钠分离出来
B.用氢气还原氧化铜实验中,先加热再通入氢气
C.用洁净玻璃棒蘸取少量某未知溶液滴在湿润的pH试纸上,判断未知溶液的酸碱度
D.利用紫色石落试液把氢氧化钠溶液、稀硫酸、氯化钠溶液、氯化钡溶液鉴别出来
经检验,四种溶液中除含有水分子外分别只含有以下离子,其中属于酸的水溶液的是( )
A.H+、Na+、SO42- B.Ca2+、Cl-
C.Ba2+、NO3- D.H+、Cl-
、填空题
碱在水中电离时,生成的阴离子都是相同的一种粒子 。常见的碱有氢氧化钠、氢氧化钙、氢氧化钡、氢氧化钾、氨水等。
根据生活经验,人体胃酸的pH 7(选填“>”“<”或“=”).维生素C溶液的pH小于7,显 性(选填“酸”“碱”或“中性”)
如下图所示:若关闭II阀打开I阀,紫色小花(用石蕊溶液染成)变红;若关闭I阀打开II阀,小花不变红。
(1)若甲瓶中未发生化学反应,则甲瓶中盛有的液体可能是
(2)若甲瓶中发生化学反应,但无明显现象,则甲瓶中发生的反应方程式可能为:
、实验探究题
在拓展性课程活动中,小明利用以下常见物品验证酸的一些性质:
白醋(含 3%的醋酸)、食品干燥剂(主要成分是 CaO)、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠)。
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝 色。
【实验过程】
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊。则鸡蛋 壳中一定含有 。(用离子符号表示)
(2)小明知道酸能够与铁发生反应产生氢气,但当他将足量的白醋加入放有铁钉的容器中, 没有看到明显的气泡产生.小明很疑惑,于是提出猜想:气泡不明显可能与酸的浓度有关.要验证与酸的浓度有关,应选择下例试剂中的 。(选填编号)
A.3%的盐酸 B.5%的醋酸 C.5%的盐酸
(3)小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计
步骤 操作 现象
1 将食品干燥剂加入适量清水中,搅拌后静置 放出大量的热
2 取步骤 1 中的上层清液,先加入牵牛花汁液, 溶液由无色变为蓝色,再变为紫色,最后变为红色
、解答题
2024年6月份公布的《2023年温州市环境状况公报》显示近5年我市酸雨率逐年降低,这与电动汽车的使用有一定的关系。自然降水因空气含二氧化碳而呈酸性,燃油汽车的使用会产生二氧化碳、氮氧化物等酸性气体,从而使降水的pH降低,pH小于5.6的降水称为酸雨。
(1)自然降水呈酸性的原因是 。
(2)使用纯电动汽车减少 排放,符合环保。
(3)小明想通过如图所示的实验寻找蒸馏水变成酸雨的证据,你认为下一步的实验操作是: 。
1.2物质的酸碱性 同步练习答案解析
、选择题
A
【解析】根据石蕊遇酸溶液变红,遇中性溶液呈紫色,遇碱性溶液变蓝分析。
氯化氢、食盐、生石灰分别溶于水后溶液分别呈酸性、中性和碱性,所以滴入紫色石蕊试液,溶液呈现的颜色依次是红色、紫色和蓝色;
故答案为:A.
D
【解析】(1)只由两种元素组成,且其中一种是氧元素的化合物,叫氧化物;
(2)根据反应产物判断;
(3)根据正负化合价的代数和为零计算;
(4)注意生成物中有氢氧化钾。
A.根据化学式K2FeO4可知,高铁酸钾由三种元素组成,肯定不是氧化物,故A错误;
B.根据方程式可知,生成物为氢氧化铁、氢氧化钾和氧气,故B错误;
C.根据化学式K2FeO4可知,(+1)×2+x+(-2)×4=0,解得:x=+6,故C错误;
D.因为生成物中有氢氧化钾,而氢氧化钾溶液呈碱性,因此pH升高,故D正确。
故选D。
C
【解析】根据三种植物的花的汁液在酸性、中性、碱性溶液中颜色的变化分析。
A.万寿菊在酸碱溶液中呈现颜色相同,不能作酸碱指示剂,不符合题意;
B、雏菊花汁在酸和中性的溶液中呈现相同颜色,不能区别硫酸和硫酸钾溶液 ,不符合题意;
C、酒精是一种常用的有机溶剂,研磨花瓣过程中加入酒精是为了溶解其中的色素,符合题意;
D、由玫瑰花汁在碱性溶液中的颜色可知,25℃时,遇到pH=10的溶液,玫瑰花汁会变成绿色 ,不符合题意;
故选C。
C
【解析】根据溶液的pH确定酸碱性,pH大于7呈碱性,小于7呈酸性,pH越小酸性越强,越大碱性越强分析。
A.洗手液cpH小于d, c的碱性比d弱 ,不符合题意;
B. 洗手液cpH大于7,呈碱性,能使石蕊试液变蓝色 ,不符合题意;
C. 洗手液apH小于7,呈酸性,用蒸馏水稀释后pH增大 ,符合题意;
D. 洗手液d呈碱性,a呈酸性,二者混合液的pH可能等于7 ,不符合题意;
故选C。
C
【解析】将婴儿尿液的pH范围与变色范围进行对比即可。
婴儿尿液的pH范围为5.4-8.4,而这种试剂pH≥5.4时呈蓝绿色,因此婴儿尿湿纸尿裤时最有可能呈现蓝绿色,故C正确,而A.B、D错误。
故选C。
D
【解析】根据生理盐水、纯净水呈中性,稀盐酸呈酸性,纯碱溶液呈碱性及图未中酸、碱、中性使枸杞的变色情况分析。
A.生理盐水呈中性,pH=7,使黑枸杞呈现紫色,不符合题意;
B.稀盐酸呈酸性,pH<7,使黑枸杞呈深红色,不符合题意;
C.纯净水呈中性,pH=7,使黑枸杞呈现紫色,不符合题意;
D.纯碱溶液呈碱性,pH>7,使黑枸杞呈现蓝绿色,符合题意;
故选D。
D
【解析】根据酸碱指示剂的用途分析判断。
根据表格可知,紫薯汁遇到酸呈红色,遇到中性溶液不变色,遇到碱性溶液时变成绿色。
A.紫薯汁遇到白醋变成红色,则白醋呈酸性,即白醋的pH<7,故A正确不合题意;
B.紫薯汁遇到草木灰变成绿色,即草木灰水呈碱性,故B正确不合题意;
C.紫薯汁遇到酸碱溶液时呈现不同的颜色,可以做酸碱指示剂,故C正确不合题意;
D.氨水呈碱性,则在氨水中滴入紫薯汁后将呈现绿色,故D错误符合题意。
故选D。
D
【解析】根据溶液pH与酸碱性关系分析,溶液pH<7时,呈酸性,且越小酸性越强,溶液pH>7时,呈碱性,且越大碱性越强,溶液pH=7时,呈中性。
A. 猕猴桃pH<7,呈酸性 ,不符合题意;
B、醋pH<7,呈酸性 ,不符合题意;
C、纯牛奶pH<7,呈酸性 ,不符合题意;
D、小苏打pH>7,呈碱性,符合题意;
故选D。
D
【解析】(1)使用溶解、过滤、蒸发分离物质,那么物质的溶解性的差异必须十分明显;
(2)用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH;
(3)酸或碱被稀释后,浓度减小,它们的pH值都会向7靠近;
(4)先用石蕊试液鉴别出酸和碱,再利用它们鉴别剩下的盐;A.硝酸钾和硝酸钠均易溶于水,不能用溶解、过滤、蒸发的操作顺序进行分离,故A错误;
B.用氢气还原氧化铜实验中,先通入氢气再加热,以排尽装置中的空气,防止发生爆炸,故B错误;
C.不能用水湿润pH试纸,若溶液显酸性或碱性,则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,故C错误;
D.氢氧化钠溶液、稀硫酸、氯化钠溶液、氯化钡溶液分别显碱性、酸性、中性、中性,分别能使紫色石蕊溶液显蓝色、红色、紫色、紫色,能鉴别出氢氧化钠溶液、稀硫酸,再将稀硫酸滴加至氯化钠、氯化钡溶液中,能与稀硫酸反应生成白色沉淀的是氯化钡溶液,可以鉴别,故D正确。
故选D。
D
【解析】根据酸的定义分析,酸是电离时产生的阳离子全部是氢离子的化合物。
A.阳离子还有钠离子,不属于酸,不符合题意;
B、阳离子不含氢离子,不属于酸,不符合题意;
C、阳离子不含氢离子,不属于酸,不符合题意;
D、阳离子全部是氢离子,属于酸,符合题意;
故选D。
、填空题
OH-
【解析】碱是指电离时电离出的阴离子全部是氢氧根离子的化合物。
电离时电离出的阴离子全部是氢氧根离子的化合物是碱。碱具有通性的原因是因为阴离子全部是氢氧根离子。
故答案为:OH-
<;酸
【解析】可以根据溶液的pH与溶液的酸碱性关系进行分析和判断,当pH=7时,呈中性,当pH<7时,呈酸性,当pH>7时,呈碱性.本题主要考查了溶液的酸碱性强弱与溶液pH大小的关系.
解:人体胃酸的主要成分是盐酸,所以pH<7,维生素C溶液的pH小于7,显酸性.
故答案为:<;酸.
(1)浓硫酸
(2)2NaOH+CO2=Na2CO3+H2O
【解析】(1)根据甲瓶中液体的用途分析;
(2)根据二氧化碳和氢氧化钠的反应解答。
(1)甲瓶中没有发生化学反应,即二氧化碳没有被吸收。根据紫色小花没有变色可知,甲对二氧化碳起干燥作用,那么应该是具有吸水性的浓硫酸。
(2)氢氧化钠和二氧化碳反应,生成碳酸钠和水,没有明显现象发生,
反应的方程式为:2NaOH+CO2=Na2CO3+H2O。
、实验探究题
(1)CO32-
(2)B
(3)滴加白醋至过量
【解析】(1)根据酸能够和碳酸根离子反应产生二氧化碳,二氧化碳能使澄清的石灰水变浑浊分析;
(2)根据控制变量法中提出的猜想可以选择试剂,题中研究与酸的浓度的关系,所以应选择浓度不同的同种溶液;
(3)由查阅的资料,根据牵牛花汁液作指示剂时溶液颜色的变化,由现象确定进行的操作。
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊,该气体是二氧化碳,因此说明鸡蛋壳中一定含有CO32-;故填:CO32-;
(2)该实验用的是3%的醋酸溶液,因此选择不同浓度的醋酸溶液即可对比实验;故填:B;
(3)向氢氧化钙的溶液中滴加牵牛花汁,溶液由无色变为蓝色,再变为紫色,最后变为红色,可知溶液由碱性变成中性,最后呈现酸性,因此向溶液中滴加醋酸最后醋酸过量;故填:再逐滴滴加白醋至过量
故答案为:(1)CO32-;(2)B;(3)滴加白醋至过量
、解答题
(1)二氧化碳与水反应形成碳酸
(2)二氧化硫、氮氧化物等酸性气体的产生
(3)用洁净的玻璃棒蘸取被测试的溶液,滴在 pH试纸上,将试纸显示的颜色与标准比色 卡对照
【解析】(1)根据“自然降水因空气含二氧化碳而呈酸性”解答;
(2)根据“燃油汽车的使用会产生二氧化碳、氮氧化物等酸性气体”解答;
(3)蒸馏水变成酸雨,它肯定呈酸性,可以用测定溶液pH的方法进行验证操作。
(1)自然降水呈酸性的原因是:二氧化碳与水反应形成碳酸。
(2)使用纯电动汽车减少二氧化硫、氮氧化物等酸性气体的产生排放,符合环保。
(3)小明想通过如图所示的实验寻找蒸馏水变成酸雨的证据,我认为下一步的实验操作是:用洁净的玻璃棒蘸取被测试的溶液,滴在 pH试纸上,将试纸显示的颜色与标准比色卡对照。
第 1 页(共 1 页)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
