1.2.2 研究物质性质的方法和程序 课件(共21张ppt) 2024-2025学年高一化学鲁科版(2019)必修第一册
文档属性
| 名称 | 1.2.2 研究物质性质的方法和程序 课件(共21张ppt) 2024-2025学年高一化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 66.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-08 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
金属钠与氧气的反应
第1章 认识化学科学
1.会设计实验探究钠与氧气在不同条件下的反应。
2.通过比较的方法认识氧化钠和过氧化钠的性质。
思考:金属钠除了能与水发生反应外,还能与哪些物质反应?你能依据铁的化学性质,预测金属钠的化学性质吗?
分类法
金属:铁→钠
能与盐酸反应吗?
能与硫酸铜溶液发生置换反应吗?
能与氧气反应吗?
预测:能与氧气反应
活动 · 探究
金属钠与氧气的反应
1、探究金属钠与氧气的反应。
2、认识条件控制对实验研究的意义。
金属钠;
酒精灯、坩埚、三脚架、泥三角、坩埚钳、镊子、小刀、 玻璃片、滤纸、火柴。
【实验目的】
【实验用品】
【实验方案】
1、将切好的金属钠放置在空气中,观察现象。
2、将一小块金属钠放置在坩埚中加热,观察现象。
活动 · 探究
活动 · 探究
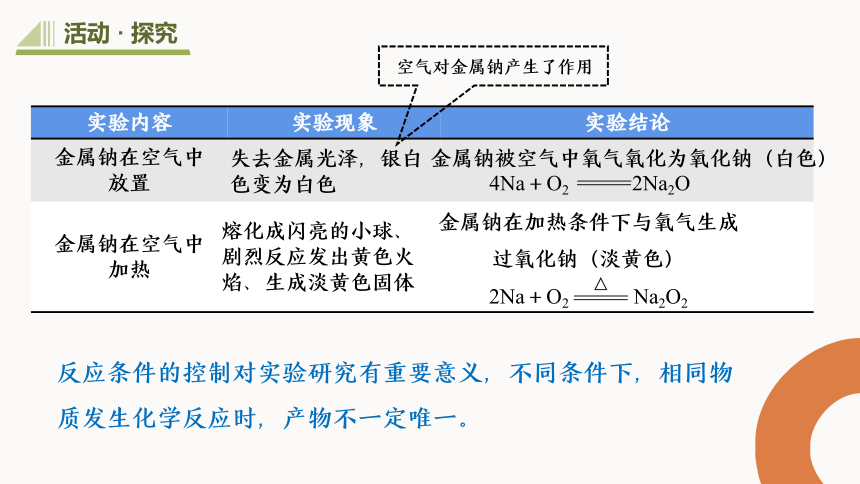
实验内容 实验现象 实验结论
金属钠在空气中 放置
金属钠在空气中 加热
空气对金属钠产生了作用
失去金属光泽,银白色变为白色
金属钠被空气中氧气氧化为氧化钠(白色)
4Na+O2 2Na2O
熔化成闪亮的小球、剧烈反应发出黄色火焰、生成淡黄色固体
△
金属钠在加热条件下与氧气生成
过氧化钠(淡黄色)
2Na+O2 Na2O2
反应条件的控制对实验研究有重要意义,不同条件下,相同物质发生化学反应时,产物不一定唯一。
过氧化钠可在呼吸面具或潜水艇中作供氧剂。
CO2
H2O
魔术实验
“滴水生火”
“吹气生火”
过氧化钠能与二氧化碳、水反应产生氧气并放出大量的热,故脱脂棉燃烧。
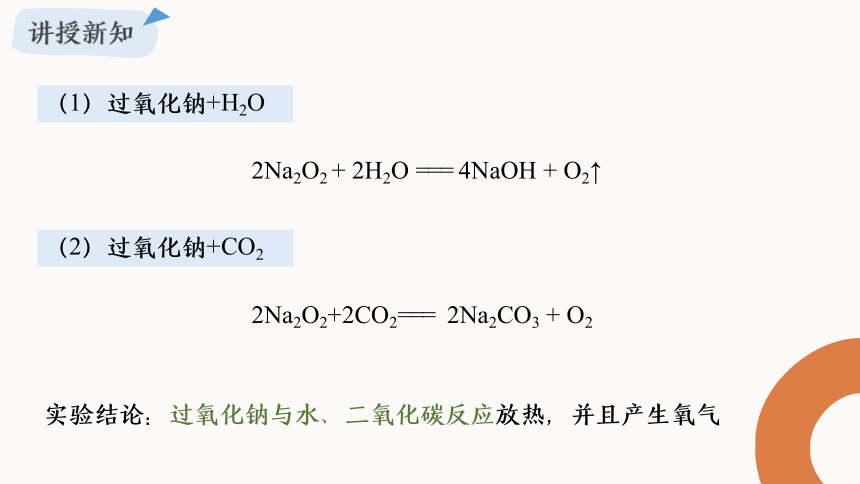
2Na2O2+2CO2=== 2Na2CO3 + O2
2Na2O2 + 2H2O === 4NaOH + O2↑
(1)过氧化钠+H2O
(2)过氧化钠+CO2
实验结论:过氧化钠与水、二氧化碳反应放热,并且产生氧气
思考:由Na2O+2HCl==2NaCl+H2O,推测Na2O2与盐酸如何反应?
过氧化钠是否是碱性氧化物吗?
2Na2O2 + 4HCl = 4NaCl +2H2O+ O2↑
能与酸反应生成盐和水的氧化物。
如氧化钠、氧化钙等
碱性氧化物:
Na2O Na2O2
颜色状态
化合价
构成微粒
与H2O反应
与盐酸反应
与CO2反应
氧化物类型
氧化性/漂白性
主要用途 制备NaOH 强氧化剂、漂白剂、供氧剂
白色固体
淡黄色固体
Na2O
+1
-2
Na2O2
+1
-1
Na+、O2-
Na+、O22-
Na2O + H2O = 2NaOH
2Na2O2+ 2H2O=4NaOH + O2↑
Na2O + HCl = NaCl + H2O
2Na2O2+4HCl = 4NaCl +2H2O+O2↑
Na2O + CO2 = Na2CO3
2Na2O2 +2CO2=2Na2CO3 + O2
碱性氧化物
过氧化物
无
有
特别提醒 ①Na2O2中的两个氧原子形成一个原子团过氧根离子。②加热时,不稳定的Na2O易转化成更稳定的Na2O2。其化学方程式为
2Na2O+O2===2Na2O2
思考:Na2O粉末中若混有少量的Na2O2,如何进行检验?
取少量粉末于试管中,滴加少量水,若有气体生成,则说明含有Na2O2。
思考:金属钠除了能与水发生反应外,还能与哪些物质反应?
你能依据铁的化学性质,预测金属钠的化学性质吗?
分类法
金属:铁→钠
能与盐酸反应吗?
能与硫酸铜溶液发生置换反应吗?
能与氧气反应吗?
2Na+2HCl === 2NaCl+H2↑
①若酸过量,只发生钠与酸的反应,反应程度比与水反应剧烈;
②若酸不足,钠将酸反应完后,剩余的钠再与水反应。
(1)钠与酸溶液的反应
(2)钠与盐溶液的反应(硫酸铜溶液)
Na浮在液面上
Na四处游动
发出嘶嘶响声
Na熔化成一个小球
产生蓝色絮状沉淀
2Na+2H2O===2NaOH+H2↑
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
思考:类比推理钠与氯化铁溶反应现象和反应方程式?
3NaOH+ FeCl3 === 3NaCl + Fe(OH) 3 ↓
2Na+2H2O === 2NaOH+H2↑
Na浮在液面上,熔化成小球,四处游动,发出嘶嘶响声,有红褐色沉淀生成。
由于钠与水剧烈反应,所以不能从溶液中置换出比它不活泼的金属
(3)钠与熔融盐反应
在熔融条件下,Na可以将钛、锆、铌等金属的氯化物中将金属置换出来
4Na+ TiCl4(熔融) == 4NaCl + Ti
700-800℃
金属钠长期露置于空气中,会发生什么变化?
提示 4Na+O2===2Na2O Na2O+H2O===2NaOH
2NaOH+CO2===Na2CO3+H2O Na2CO3+10H2O===Na2CO3·10H2O
Na2CO3·10H2O===Na2CO3+10H2O
1.判断正误
(1)Na2O2中阴、阳离子个数比为1∶1
(2)Na2O2在空气中放置后由淡黄色变为白色的化学方程式是2Na2O2===2Na2O+O2↑
(3)Na2O与Na2O2分别与CO2反应的产物完全相同
(4)Na2O与Na2O2均可与水反应产生氧气
(5)钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
×
×
×
×
√
2.回答下列问题:
(1)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,发生反应的化学方程式为___________________,生成物的颜色为______。
淡黄色
(2)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为________
(填化学式)。
Na2CO3
(3)过氧化钠常用于呼吸面具和潜水艇氧气的来源,其原理为_________
___________________________________________________(用化学方程式表示)。
2Na2O2+
2H2O===4NaOH+O2↑、2Na2O2+2CO2===2Na2CO3+O2
3.如图所示装置,试管b中盛有水,气球a中盛有干燥的Na2O2颗粒。U形管中注有浅红色的水。将气球用橡皮筋紧缚在试管口。实验时将气球中的Na2O2抖落到试管b的水中,下列说法正确的是
A.U形管内浅红色的水褪色
B.试管b内溶液变红
C.气球a膨胀,充满氢气
D.U形管水位:d>c
√
金属钠与氧气的反应
第1章 认识化学科学
1.会设计实验探究钠与氧气在不同条件下的反应。
2.通过比较的方法认识氧化钠和过氧化钠的性质。
思考:金属钠除了能与水发生反应外,还能与哪些物质反应?你能依据铁的化学性质,预测金属钠的化学性质吗?
分类法
金属:铁→钠
能与盐酸反应吗?
能与硫酸铜溶液发生置换反应吗?
能与氧气反应吗?
预测:能与氧气反应
活动 · 探究
金属钠与氧气的反应
1、探究金属钠与氧气的反应。
2、认识条件控制对实验研究的意义。
金属钠;
酒精灯、坩埚、三脚架、泥三角、坩埚钳、镊子、小刀、 玻璃片、滤纸、火柴。
【实验目的】
【实验用品】
【实验方案】
1、将切好的金属钠放置在空气中,观察现象。
2、将一小块金属钠放置在坩埚中加热,观察现象。
活动 · 探究
活动 · 探究
实验内容 实验现象 实验结论
金属钠在空气中 放置
金属钠在空气中 加热
空气对金属钠产生了作用
失去金属光泽,银白色变为白色
金属钠被空气中氧气氧化为氧化钠(白色)
4Na+O2 2Na2O
熔化成闪亮的小球、剧烈反应发出黄色火焰、生成淡黄色固体
△
金属钠在加热条件下与氧气生成
过氧化钠(淡黄色)
2Na+O2 Na2O2
反应条件的控制对实验研究有重要意义,不同条件下,相同物质发生化学反应时,产物不一定唯一。
过氧化钠可在呼吸面具或潜水艇中作供氧剂。
CO2
H2O
魔术实验
“滴水生火”
“吹气生火”
过氧化钠能与二氧化碳、水反应产生氧气并放出大量的热,故脱脂棉燃烧。
2Na2O2+2CO2=== 2Na2CO3 + O2
2Na2O2 + 2H2O === 4NaOH + O2↑
(1)过氧化钠+H2O
(2)过氧化钠+CO2
实验结论:过氧化钠与水、二氧化碳反应放热,并且产生氧气
思考:由Na2O+2HCl==2NaCl+H2O,推测Na2O2与盐酸如何反应?
过氧化钠是否是碱性氧化物吗?
2Na2O2 + 4HCl = 4NaCl +2H2O+ O2↑
能与酸反应生成盐和水的氧化物。
如氧化钠、氧化钙等
碱性氧化物:
Na2O Na2O2
颜色状态
化合价
构成微粒
与H2O反应
与盐酸反应
与CO2反应
氧化物类型
氧化性/漂白性
主要用途 制备NaOH 强氧化剂、漂白剂、供氧剂
白色固体
淡黄色固体
Na2O
+1
-2
Na2O2
+1
-1
Na+、O2-
Na+、O22-
Na2O + H2O = 2NaOH
2Na2O2+ 2H2O=4NaOH + O2↑
Na2O + HCl = NaCl + H2O
2Na2O2+4HCl = 4NaCl +2H2O+O2↑
Na2O + CO2 = Na2CO3
2Na2O2 +2CO2=2Na2CO3 + O2
碱性氧化物
过氧化物
无
有
特别提醒 ①Na2O2中的两个氧原子形成一个原子团过氧根离子。②加热时,不稳定的Na2O易转化成更稳定的Na2O2。其化学方程式为
2Na2O+O2===2Na2O2
思考:Na2O粉末中若混有少量的Na2O2,如何进行检验?
取少量粉末于试管中,滴加少量水,若有气体生成,则说明含有Na2O2。
思考:金属钠除了能与水发生反应外,还能与哪些物质反应?
你能依据铁的化学性质,预测金属钠的化学性质吗?
分类法
金属:铁→钠
能与盐酸反应吗?
能与硫酸铜溶液发生置换反应吗?
能与氧气反应吗?
2Na+2HCl === 2NaCl+H2↑
①若酸过量,只发生钠与酸的反应,反应程度比与水反应剧烈;
②若酸不足,钠将酸反应完后,剩余的钠再与水反应。
(1)钠与酸溶液的反应
(2)钠与盐溶液的反应(硫酸铜溶液)
Na浮在液面上
Na四处游动
发出嘶嘶响声
Na熔化成一个小球
产生蓝色絮状沉淀
2Na+2H2O===2NaOH+H2↑
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
思考:类比推理钠与氯化铁溶反应现象和反应方程式?
3NaOH+ FeCl3 === 3NaCl + Fe(OH) 3 ↓
2Na+2H2O === 2NaOH+H2↑
Na浮在液面上,熔化成小球,四处游动,发出嘶嘶响声,有红褐色沉淀生成。
由于钠与水剧烈反应,所以不能从溶液中置换出比它不活泼的金属
(3)钠与熔融盐反应
在熔融条件下,Na可以将钛、锆、铌等金属的氯化物中将金属置换出来
4Na+ TiCl4(熔融) == 4NaCl + Ti
700-800℃
金属钠长期露置于空气中,会发生什么变化?
提示 4Na+O2===2Na2O Na2O+H2O===2NaOH
2NaOH+CO2===Na2CO3+H2O Na2CO3+10H2O===Na2CO3·10H2O
Na2CO3·10H2O===Na2CO3+10H2O
1.判断正误
(1)Na2O2中阴、阳离子个数比为1∶1
(2)Na2O2在空气中放置后由淡黄色变为白色的化学方程式是2Na2O2===2Na2O+O2↑
(3)Na2O与Na2O2分别与CO2反应的产物完全相同
(4)Na2O与Na2O2均可与水反应产生氧气
(5)钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
×
×
×
×
√
2.回答下列问题:
(1)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,发生反应的化学方程式为___________________,生成物的颜色为______。
淡黄色
(2)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为________
(填化学式)。
Na2CO3
(3)过氧化钠常用于呼吸面具和潜水艇氧气的来源,其原理为_________
___________________________________________________(用化学方程式表示)。
2Na2O2+
2H2O===4NaOH+O2↑、2Na2O2+2CO2===2Na2CO3+O2
3.如图所示装置,试管b中盛有水,气球a中盛有干燥的Na2O2颗粒。U形管中注有浅红色的水。将气球用橡皮筋紧缚在试管口。实验时将气球中的Na2O2抖落到试管b的水中,下列说法正确的是
A.U形管内浅红色的水褪色
B.试管b内溶液变红
C.气球a膨胀,充满氢气
D.U形管水位:d>c
√
