浙教版科学九年级上册 2.6材料的利用与发展 同步练习(含答案)
文档属性
| 名称 | 浙教版科学九年级上册 2.6材料的利用与发展 同步练习(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 686.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-08-12 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
浙教版科学九上物质转化与材料利用2.6材料的利用与发展(含答案)
一、选择题
1.人类文明的进步离不开各种工具的发明与改进,下列工具主要由金属材料制成的是( )
A.石器 B.石斧 C.青铜器 D.瓷碗
2.下列成都出土的文物中,不属于金属材料的是( )
A.东汉说唱俑 B.“郫”字青铜戈
C.龙纹铅饼币 D.黄金面具
3.垃圾分类,从我做起。下列可回收物属于有机合成材料的是( )
A.旧报纸 B.塑料瓶 C.玻璃瓶 D.铝质易拉罐
4.不粘锅内表面通常使用特氟龙涂层,原料为聚四氟乙烯,其结构简式为[CF2CF2]n.对聚四氟乙烯的推断,不合理的是( )
A.属于有机合成材料 B.有较好的耐高温性
C.可耐酸腐蚀 D.可溶于酒精、食用油等有机溶剂
5.不粘锅内表面通常使用特氟龙涂层,原料为聚四氟乙烯,其结构简式为[CF2CF2]n.对聚四氟乙烯的推断,不合理的是( )
A.属于有机合成材料 B.有较好的耐高温性
C.可耐酸腐蚀 D.可溶于酒精、食用油等有机溶剂
6.考古发现,早在一万多年前我国已开始制造和使用陶器。现代人们已能生产新型陶瓷材料,如用氧化铝等为原料生产的陶瓷已制造发动机零件。下列有关氧化铝陶瓷的说法错误的是( )
A.该陶瓷属于无机非金属材料 B.该陶瓷中的原料氧化铝属于非金属氧化物
C.该陶瓷耐高温、强度高 D.该陶瓷耐酸、碱等化学物质的腐蚀
7.现代科技的发展,促使新型材料研究日益向微观层次深入,产生了纳米材料。纳米材料与普通材料相比,在机械强度、磁、光、声、热等方面都有很大的不同。下列关于纳米材料的叙述,错误的是( )
A.纳米材料是指其基本颗粒在0.01~1纳米范围内的材料
B.纳米陶瓷比普通陶瓷具有更好的韧性
C.用纳米油墨书写的字迹色泽更好
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快
8.现代科技的发展,促使新型材料研究日益向微观层次深入,产生了纳米材料。纳米材料与普通材料相比,在机械强度、磁、光、声、热等方面都有很大的不同。下列关于纳米材料的叙述,错误的是( )
A.纳米材料是指其基本颗粒在0.01~1纳米范围内的材料
B.纳米陶瓷比普通陶瓷具有更好的韧性
C.用纳米油墨书写的字迹色泽更好
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快
二、填空题
9.小舟归纳了金属及其化合物之间的部分转化关系,如图所示。
(1)请写出符合图中转化规律①的化学方程式 (写一个即可)。
(2)我国古代劳动人民最早发明使用湿法炼铜,其原理是:第一步用硫酸将铜矿中的铜转变为可溶性的硫酸铜,第二步将铁放入硫酸铜溶液中把铜置换出来。其中利用了图中转化规律⑧的是第 步。
10.眼镜是人们常用的护眼工具,如图所示是一款变色眼镜的示意图:
(1)所标物质中属于金属单质的是 ,属于有机合成材料的是 ,属于无机非金属材料的是 .
(2)夏天铜螺丝部位常出现一层绿色物质,这是由于铜生锈的原因,请完成该反应的化学方程式: Cu+O2+ +H2O═Cu2(OH)2CO3.防止铜螺丝生锈的一种方法是 .
(3)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜.在强光照射下,溴化银分解成溴和银,玻璃颜色变深,此反应类型属于 反应;当光线变暗时,溴和银在氧化铜作用下重新生成溴化银,玻璃颜色变浅,氧化铜在反应中起 作用.结合镜片材料从天然水晶、光学玻璃到光学树脂的变迁过程,请你谈一谈化学与生活的关系: .
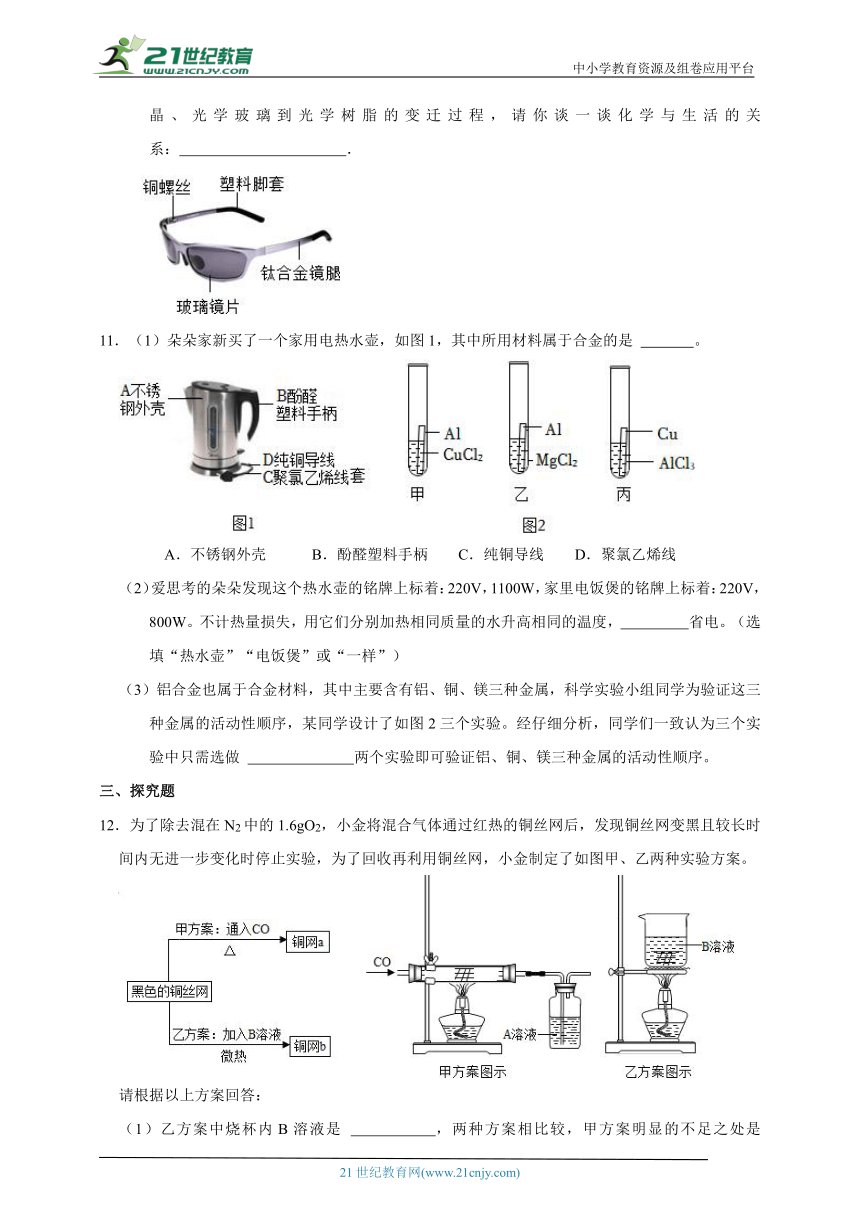
11.(1)朵朵家新买了一个家用电热水壶,如图1,其中所用材料属于合金的是 。
A.不锈钢外壳 B.酚醛塑料手柄 C.纯铜导线 D.聚氯乙烯线
(2)爱思考的朵朵发现这个热水壶的铭牌上标着:220V,1100W,家里电饭煲的铭牌上标着:220V,800W。不计热量损失,用它们分别加热相同质量的水升高相同的温度, 省电。(选填“热水壶”“电饭煲”或“一样”)
(3)铝合金也属于合金材料,其中主要含有铝、铜、镁三种金属,科学实验小组同学为验证这三种金属的活动性顺序,某同学设计了如图2三个实验。经仔细分析,同学们一致认为三个实验中只需选做 两个实验即可验证铝、铜、镁三种金属的活动性顺序。
三、探究题
12.为了除去混在N2中的1.6gO2,小金将混合气体通过红热的铜丝网后,发现铜丝网变黑且较长时间内无进一步变化时停止实验,为了回收再利用铜丝网,小金制定了如图甲、乙两种实验方案。
请根据以上方案回答:
(1)乙方案中烧杯内B溶液是 ,两种方案相比较,甲方案明显的不足之处是 (写出一种即可)。
(2)从理论上分析,若采用甲、乙两种方案处理此黑色铜丝网,则回收的铜丝网a的质量与铜丝网b的质量相差 克。
(3)小金发现乙方案反应后烧杯中的液体有腐蚀性,应加以适当的处理。小金加入过量的铁粉充分搅拌处理废液,最后得到的溶液中阳离子为 。(填化学符号)
四、解答题
13.氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上用粗铜渣(含CuO、Fe2O3、FeO以及少量不溶性杂所)为原料制取氯化铜(CuCl2)的为生产流程如图1:
(1)为了提高粗铜渣的利用率,可采取的措施是 。
(2)“盐酸浸出”中发生反应的化学方程式 (写1个)。铜的浸出率与浸出时间的关系如图2所示,由图可知:最佳浸出时间为 。
表一:几种离子生成氢氧化物沉淀的pH
开始沉淀的pH 沉淀完全的pH
Fe3+ 1.1 3.2
Fe2+ 5.8 8.8
Cu2+ 4.7 6.7
(3)“操作1”用到的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(4)依据“表一”分析:“除铁”中加入H2O2的作用是 。在下列试剂中选用适当试剂 (填选项字母)调节PH,调节PH的适宜范围是 。
A.CuSO4 B.CuO C.Cu2(OH)2CO3
(5)“操作2”包含过滤、洗涤滤渣、蒸发等多步实验基本操作,洗涤滤渣的目的是 ,过滤后滤渣为红褐色固体,该滤渣是 。(填化学式)。
(6)若不考虑“调节pH”对流程的影响,欲通过该方法生产CuCl2 13.5t,理论上至少需要含铜64%的粗铜渣 t。(精确到0.1,写出计算过程)
14.化学改变世界,科技改变生活。请回答:
(1)我国自主研发的复兴号动车组列车,领跑世界,其制造材料有铝合金等,在空气中铝制品耐腐蚀的原因是 。
(2)我国对石墨烯技术的研究居世界领先地位。石墨烯性能优良,用途独特,比如用作太阳能电池的电极,这主要是利用了它的 性。
(3)我国自主设计建造的港珠澳大桥是目前世界最长的跨海大桥,它使用了世界最大尺寸高阻尼橡胶隔震支座,其中橡胶属于 (填字母)。
a.金属材料 b.有机高分子材料 c.复合材料
(4)我国在氢能汽车研发领域取得重大突破,采用了第四代以氢为燃料的电池技术。
氢气作为理想能源前景广阔,现通过生物法制得的氢气中混有CO、O2和水蒸气等(氢气的体积分数通常为60%~90%),为了得到纯净的氢气,将混合气体依次通过NaOH溶液、灼热的Cu丝和干燥装置。该除杂方案是否正确? ,理由是 。
答案
1.解:A、石器是用天然石材制成的,故选项错误。
B、石斧是用天然石材制成的,故选项错误。
C、青铜器是用青铜制成的,青铜是铜的合金,属于金属材料,故选项正确。
D、瓷碗是用瓷土烧制而成的,属于无机非金属材料,故选项错误。
故选:C。
2.解:A.东汉说唱俑是一种陶瓷制品,属于无机非金属材料,符合题意;
B.“郫”字青铜戈是由合金制成的,属于金属材料,不合题意;
C.龙纹铅饼币是由合金制成的,属于金属材料,不合题意;
D.黄金面具是由金属制成的,属于金属材料,不合题意。
故选:A。
3.解:A、报纸不属于合成材料,故A错误;
B、塑料属于有机合成材料,故B正确,
C、玻璃属于无机非金属材料,故C错误;
D、铝制易拉罐属于金属材料制成的,故D错误;
故选:B。
4.解:A、聚四氟乙烯属于有机物,正确;
B、用在锅的表面,说明具有耐高温性,正确;
C、用在锅的表面,说明具有耐腐蚀性,正确;
D、若是溶于食用油等有机溶剂则会被破坏掉,错误;
故选:D。
5.解:A、聚四氟乙烯属于有机物,正确;
B、用在锅的表面,说明具有耐高温性,正确;
C、用在锅的表面,说明具有耐腐蚀性,正确;
D、若是溶于食用油等有机溶剂则会被破坏掉,错误;
故选:D。
6.解:题中信息为:氧化铝陶瓷为新型陶瓷材料,该陶瓷属于无机非金属材料(因氧化铝为无机物),该陶瓷,耐酸、碱等化学物质的腐蚀(陶瓷的性质),但该陶瓷中的原料氧化铝不属于非金属氧化物,而是金属氧化物。该陶瓷耐高温、强度高。
故选:B。
7.解:A.纳米材料是指其基本颗粒在1~100纳米范围内的材料,选项说法错误;
B.纳米陶瓷比普通陶瓷具有更好的韧性,选项说法正确;
C.用纳米油墨书写的字迹色泽更好,选项说法正确;
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快,选项说法正确。
故选:A。
8.解:A.纳米材料是指其基本颗粒在1~100纳米范围内的材料,选项说法错误;
B.纳米陶瓷比普通陶瓷具有更好的韧性,选项说法正确;
C.用纳米油墨书写的字迹色泽更好,选项说法正确;
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快,选项说法正确。
故选:A。
9.解:(1)转化规律①是金属转化为金属氧化物,如镁在氧气中燃烧生成氧化镁,反应的化学方程式为2Mg+O22MgO(合理即可)。
(2)转化规律⑧是盐转化为金属,铁放入硫酸铜溶液中把铜置换出来,铁与硫酸铜反应生成硫酸亚铁和铜,是盐转化为金属。
故答案为:
(1)2Mg+O22MgO(合理即可);
(2)二。
10.解:(1)铜螺丝是由一种元素组成的纯净物,属于单质;塑料属于有机合成材料;玻璃属于无机非金属材料;
故答案为:铜螺丝;塑料脚套;玻璃镜片;
(2)根据反应的化学方程式Cu+O2+____+H2O═Cu2(OH)2CO3,反应物中氧、氢原子个数分别为3、2,铜原子数未知,反应后的生成物中铜、氧、氢、碳原子个数分别为2、5、2、1,根据反应前后原子种类、数目不变,反应物中应该有2个铜原子,则每个____分子由1个碳原子和2个氧原子构成,则物质X的化学式为CO2;防止铜螺丝生锈可以保持螺丝的干燥;
故答案为:2;CO2;保持干燥;
(3)溴化银受强光照射时会分解为银和溴Br2,反应的化学方程式为:2AgBr2Ag+Br2,该反应属于分解反应;当光线变暗(弱)时,银和溴在催化剂氧化铜的作用下,又重新化合生成溴化银;从镜片材料从天然水晶、光学玻璃到光学树脂的变迁过程可以看出化学在材料的开发和利用中发挥着重要作用.
故答案为:分解;催化;化学在材料的开发和利用中发挥着重要作用.
11.(1)A.不锈钢属于合金,故A可选;
B.塑料属于有机高分子合成材料,故B不选;
C.纯铜属于金属,故C不选;
D.聚氯乙烯属于有机高分子材料,故D不选;
故选:A;
(2)分别加热相同质量的水升高相同的温度,需热量相同,所以两种用电器一样省电;
(3)甲试管中铝表面有紫红色固体析出,铝能够置换铜,能够证明铝的活动性大于铜;乙试管中没有明显现象,铝不能置换镁,乙试管可以证明铝的活动性小于镁;丙试管中没有明显现象,铜不能置换铝,可以证明铝的活动性大于铜;所以要验证铝、铜、镁三种金属的活动性,只需做甲和乙或乙和丙两个实验即可。
故答案为:
(1)A;
(2)一样;
(3)甲和乙或乙和丙。
12.解:(1)乙方案中烧杯内B溶液是稀硫酸(稀硫酸和氧化铜反应生成硫酸铜和水),两种方案相比较,甲方案明显的不足之处是没有处理尾气。
故答案为:稀硫酸;没有处理尾气。
(2)回收的铜丝网a的质量与原铜丝网质量相等,铜丝网b的质量减小,减小的质量与原铜丝网质量之差是与氧气反应的铜的质量,反应的化学方程式及其质量关系:
2Cu+O22CuO
128 32
6.4g 1.6g
则回收的铜丝网a的质量与铜丝网b的质量相差6.4g。
故答案为:6.4。
(3)小金加入过量的铁粉充分搅拌处理废液,过程中铁和硫酸铜反应生成硫酸亚铁和铜,最后得到的溶液中阳离子为Fe2+。
故答案为:Fe2+。
13.解:(1)根据图示分析可知,为了提高粗铜渣的利用率,可采取的措施是增加反应时间,故答案为:增加反应时间;
(2)CuO在“盐酸浸出”中和稀盐酸反应生成氯化铜和水,氧化铁和稀盐酸生成氯化铁和水,反应方程式为:CuO+2HCl=CuCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O;根据图象知,随着浸出时间的增加,Cu的浸出率相应的增加,浸出时间超过24h后,Cu的浸出率变化不明显,可知:最佳浸出时间为24h,故答案为:CuO+2HCl=CuCl2+H2O或Fe2O3+6HCl=2FeCl3+3H2O;24h;
(3)操作Ⅰ是分离固体和液体,是过滤操作,过滤中用到的玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是引流,故答案为:漏斗;引流。
(4)H2O2有强氧化性,能把Fe2+氧化为Fe3+;调节溶液pH值时加入的物质能和氢离子反应且不能引进新的杂质,A能引进杂质,只有BC能和氢离子反应且不引进杂质;根据Fe3+完全转化为沉淀时的pH可知,pH在3.2至4.7时Fe3+完全转化为沉淀且铜离子不沉淀;故答案为:把Fe2+氧化为Fe3;BC;3.2至4.7;
(5)操作2”包含过滤、洗涤滤渣、蒸发等多步实验基本操作,洗涤滤渣的目的是洗掉残留在滤渣表面的杂质离子,过滤后滤渣为红褐色固体,该滤渣是氢氧化铁,故答案为:洗掉残留在滤渣表面的杂质离子;Fe(OH)3;
(6)设粗铜渣质量为x,根据质量守恒,64%x=13.5t×,x=10.0t;由图可知铜的浸出率最多90%,所以精铜渣的质量为:10.0t÷90%≈11.1t;故答案为:11.1。
14.解:(1)在常温的条件下,铝易与空气的氧气反应生成致密的氧化铝保护膜,所以在空气中铝制品耐腐蚀;故答案为:在常温的条件下,铝易与空气的氧气反应生成致密的氧化铝保护膜;
(2)石墨烯性能优良,用途独特,比如用作太阳能电池的电极,这主要是利用了它的导电性;故答案为:导电;
(3)高阻尼橡胶是由合成橡胶制成的,合成橡胶是一种有机高分子材料;故答案为:b;
(4)氢气与氧气混合达到一定程度时遇明火或加热时会发生爆炸,所以该方案是错误的。故答案为:不正确;通过灼热的铜丝网时,混合气体可能发生爆炸。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
浙教版科学九上物质转化与材料利用2.6材料的利用与发展(含答案)
一、选择题
1.人类文明的进步离不开各种工具的发明与改进,下列工具主要由金属材料制成的是( )
A.石器 B.石斧 C.青铜器 D.瓷碗
2.下列成都出土的文物中,不属于金属材料的是( )
A.东汉说唱俑 B.“郫”字青铜戈
C.龙纹铅饼币 D.黄金面具
3.垃圾分类,从我做起。下列可回收物属于有机合成材料的是( )
A.旧报纸 B.塑料瓶 C.玻璃瓶 D.铝质易拉罐
4.不粘锅内表面通常使用特氟龙涂层,原料为聚四氟乙烯,其结构简式为[CF2CF2]n.对聚四氟乙烯的推断,不合理的是( )
A.属于有机合成材料 B.有较好的耐高温性
C.可耐酸腐蚀 D.可溶于酒精、食用油等有机溶剂
5.不粘锅内表面通常使用特氟龙涂层,原料为聚四氟乙烯,其结构简式为[CF2CF2]n.对聚四氟乙烯的推断,不合理的是( )
A.属于有机合成材料 B.有较好的耐高温性
C.可耐酸腐蚀 D.可溶于酒精、食用油等有机溶剂
6.考古发现,早在一万多年前我国已开始制造和使用陶器。现代人们已能生产新型陶瓷材料,如用氧化铝等为原料生产的陶瓷已制造发动机零件。下列有关氧化铝陶瓷的说法错误的是( )
A.该陶瓷属于无机非金属材料 B.该陶瓷中的原料氧化铝属于非金属氧化物
C.该陶瓷耐高温、强度高 D.该陶瓷耐酸、碱等化学物质的腐蚀
7.现代科技的发展,促使新型材料研究日益向微观层次深入,产生了纳米材料。纳米材料与普通材料相比,在机械强度、磁、光、声、热等方面都有很大的不同。下列关于纳米材料的叙述,错误的是( )
A.纳米材料是指其基本颗粒在0.01~1纳米范围内的材料
B.纳米陶瓷比普通陶瓷具有更好的韧性
C.用纳米油墨书写的字迹色泽更好
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快
8.现代科技的发展,促使新型材料研究日益向微观层次深入,产生了纳米材料。纳米材料与普通材料相比,在机械强度、磁、光、声、热等方面都有很大的不同。下列关于纳米材料的叙述,错误的是( )
A.纳米材料是指其基本颗粒在0.01~1纳米范围内的材料
B.纳米陶瓷比普通陶瓷具有更好的韧性
C.用纳米油墨书写的字迹色泽更好
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快
二、填空题
9.小舟归纳了金属及其化合物之间的部分转化关系,如图所示。
(1)请写出符合图中转化规律①的化学方程式 (写一个即可)。
(2)我国古代劳动人民最早发明使用湿法炼铜,其原理是:第一步用硫酸将铜矿中的铜转变为可溶性的硫酸铜,第二步将铁放入硫酸铜溶液中把铜置换出来。其中利用了图中转化规律⑧的是第 步。
10.眼镜是人们常用的护眼工具,如图所示是一款变色眼镜的示意图:
(1)所标物质中属于金属单质的是 ,属于有机合成材料的是 ,属于无机非金属材料的是 .
(2)夏天铜螺丝部位常出现一层绿色物质,这是由于铜生锈的原因,请完成该反应的化学方程式: Cu+O2+ +H2O═Cu2(OH)2CO3.防止铜螺丝生锈的一种方法是 .
(3)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜.在强光照射下,溴化银分解成溴和银,玻璃颜色变深,此反应类型属于 反应;当光线变暗时,溴和银在氧化铜作用下重新生成溴化银,玻璃颜色变浅,氧化铜在反应中起 作用.结合镜片材料从天然水晶、光学玻璃到光学树脂的变迁过程,请你谈一谈化学与生活的关系: .
11.(1)朵朵家新买了一个家用电热水壶,如图1,其中所用材料属于合金的是 。
A.不锈钢外壳 B.酚醛塑料手柄 C.纯铜导线 D.聚氯乙烯线
(2)爱思考的朵朵发现这个热水壶的铭牌上标着:220V,1100W,家里电饭煲的铭牌上标着:220V,800W。不计热量损失,用它们分别加热相同质量的水升高相同的温度, 省电。(选填“热水壶”“电饭煲”或“一样”)
(3)铝合金也属于合金材料,其中主要含有铝、铜、镁三种金属,科学实验小组同学为验证这三种金属的活动性顺序,某同学设计了如图2三个实验。经仔细分析,同学们一致认为三个实验中只需选做 两个实验即可验证铝、铜、镁三种金属的活动性顺序。
三、探究题
12.为了除去混在N2中的1.6gO2,小金将混合气体通过红热的铜丝网后,发现铜丝网变黑且较长时间内无进一步变化时停止实验,为了回收再利用铜丝网,小金制定了如图甲、乙两种实验方案。
请根据以上方案回答:
(1)乙方案中烧杯内B溶液是 ,两种方案相比较,甲方案明显的不足之处是 (写出一种即可)。
(2)从理论上分析,若采用甲、乙两种方案处理此黑色铜丝网,则回收的铜丝网a的质量与铜丝网b的质量相差 克。
(3)小金发现乙方案反应后烧杯中的液体有腐蚀性,应加以适当的处理。小金加入过量的铁粉充分搅拌处理废液,最后得到的溶液中阳离子为 。(填化学符号)
四、解答题
13.氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上用粗铜渣(含CuO、Fe2O3、FeO以及少量不溶性杂所)为原料制取氯化铜(CuCl2)的为生产流程如图1:
(1)为了提高粗铜渣的利用率,可采取的措施是 。
(2)“盐酸浸出”中发生反应的化学方程式 (写1个)。铜的浸出率与浸出时间的关系如图2所示,由图可知:最佳浸出时间为 。
表一:几种离子生成氢氧化物沉淀的pH
开始沉淀的pH 沉淀完全的pH
Fe3+ 1.1 3.2
Fe2+ 5.8 8.8
Cu2+ 4.7 6.7
(3)“操作1”用到的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(4)依据“表一”分析:“除铁”中加入H2O2的作用是 。在下列试剂中选用适当试剂 (填选项字母)调节PH,调节PH的适宜范围是 。
A.CuSO4 B.CuO C.Cu2(OH)2CO3
(5)“操作2”包含过滤、洗涤滤渣、蒸发等多步实验基本操作,洗涤滤渣的目的是 ,过滤后滤渣为红褐色固体,该滤渣是 。(填化学式)。
(6)若不考虑“调节pH”对流程的影响,欲通过该方法生产CuCl2 13.5t,理论上至少需要含铜64%的粗铜渣 t。(精确到0.1,写出计算过程)
14.化学改变世界,科技改变生活。请回答:
(1)我国自主研发的复兴号动车组列车,领跑世界,其制造材料有铝合金等,在空气中铝制品耐腐蚀的原因是 。
(2)我国对石墨烯技术的研究居世界领先地位。石墨烯性能优良,用途独特,比如用作太阳能电池的电极,这主要是利用了它的 性。
(3)我国自主设计建造的港珠澳大桥是目前世界最长的跨海大桥,它使用了世界最大尺寸高阻尼橡胶隔震支座,其中橡胶属于 (填字母)。
a.金属材料 b.有机高分子材料 c.复合材料
(4)我国在氢能汽车研发领域取得重大突破,采用了第四代以氢为燃料的电池技术。
氢气作为理想能源前景广阔,现通过生物法制得的氢气中混有CO、O2和水蒸气等(氢气的体积分数通常为60%~90%),为了得到纯净的氢气,将混合气体依次通过NaOH溶液、灼热的Cu丝和干燥装置。该除杂方案是否正确? ,理由是 。
答案
1.解:A、石器是用天然石材制成的,故选项错误。
B、石斧是用天然石材制成的,故选项错误。
C、青铜器是用青铜制成的,青铜是铜的合金,属于金属材料,故选项正确。
D、瓷碗是用瓷土烧制而成的,属于无机非金属材料,故选项错误。
故选:C。
2.解:A.东汉说唱俑是一种陶瓷制品,属于无机非金属材料,符合题意;
B.“郫”字青铜戈是由合金制成的,属于金属材料,不合题意;
C.龙纹铅饼币是由合金制成的,属于金属材料,不合题意;
D.黄金面具是由金属制成的,属于金属材料,不合题意。
故选:A。
3.解:A、报纸不属于合成材料,故A错误;
B、塑料属于有机合成材料,故B正确,
C、玻璃属于无机非金属材料,故C错误;
D、铝制易拉罐属于金属材料制成的,故D错误;
故选:B。
4.解:A、聚四氟乙烯属于有机物,正确;
B、用在锅的表面,说明具有耐高温性,正确;
C、用在锅的表面,说明具有耐腐蚀性,正确;
D、若是溶于食用油等有机溶剂则会被破坏掉,错误;
故选:D。
5.解:A、聚四氟乙烯属于有机物,正确;
B、用在锅的表面,说明具有耐高温性,正确;
C、用在锅的表面,说明具有耐腐蚀性,正确;
D、若是溶于食用油等有机溶剂则会被破坏掉,错误;
故选:D。
6.解:题中信息为:氧化铝陶瓷为新型陶瓷材料,该陶瓷属于无机非金属材料(因氧化铝为无机物),该陶瓷,耐酸、碱等化学物质的腐蚀(陶瓷的性质),但该陶瓷中的原料氧化铝不属于非金属氧化物,而是金属氧化物。该陶瓷耐高温、强度高。
故选:B。
7.解:A.纳米材料是指其基本颗粒在1~100纳米范围内的材料,选项说法错误;
B.纳米陶瓷比普通陶瓷具有更好的韧性,选项说法正确;
C.用纳米油墨书写的字迹色泽更好,选项说法正确;
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快,选项说法正确。
故选:A。
8.解:A.纳米材料是指其基本颗粒在1~100纳米范围内的材料,选项说法错误;
B.纳米陶瓷比普通陶瓷具有更好的韧性,选项说法正确;
C.用纳米油墨书写的字迹色泽更好,选项说法正确;
D.添加了纳米铅粉末的固体燃料会使火箭推进器的速度加快,选项说法正确。
故选:A。
9.解:(1)转化规律①是金属转化为金属氧化物,如镁在氧气中燃烧生成氧化镁,反应的化学方程式为2Mg+O22MgO(合理即可)。
(2)转化规律⑧是盐转化为金属,铁放入硫酸铜溶液中把铜置换出来,铁与硫酸铜反应生成硫酸亚铁和铜,是盐转化为金属。
故答案为:
(1)2Mg+O22MgO(合理即可);
(2)二。
10.解:(1)铜螺丝是由一种元素组成的纯净物,属于单质;塑料属于有机合成材料;玻璃属于无机非金属材料;
故答案为:铜螺丝;塑料脚套;玻璃镜片;
(2)根据反应的化学方程式Cu+O2+____+H2O═Cu2(OH)2CO3,反应物中氧、氢原子个数分别为3、2,铜原子数未知,反应后的生成物中铜、氧、氢、碳原子个数分别为2、5、2、1,根据反应前后原子种类、数目不变,反应物中应该有2个铜原子,则每个____分子由1个碳原子和2个氧原子构成,则物质X的化学式为CO2;防止铜螺丝生锈可以保持螺丝的干燥;
故答案为:2;CO2;保持干燥;
(3)溴化银受强光照射时会分解为银和溴Br2,反应的化学方程式为:2AgBr2Ag+Br2,该反应属于分解反应;当光线变暗(弱)时,银和溴在催化剂氧化铜的作用下,又重新化合生成溴化银;从镜片材料从天然水晶、光学玻璃到光学树脂的变迁过程可以看出化学在材料的开发和利用中发挥着重要作用.
故答案为:分解;催化;化学在材料的开发和利用中发挥着重要作用.
11.(1)A.不锈钢属于合金,故A可选;
B.塑料属于有机高分子合成材料,故B不选;
C.纯铜属于金属,故C不选;
D.聚氯乙烯属于有机高分子材料,故D不选;
故选:A;
(2)分别加热相同质量的水升高相同的温度,需热量相同,所以两种用电器一样省电;
(3)甲试管中铝表面有紫红色固体析出,铝能够置换铜,能够证明铝的活动性大于铜;乙试管中没有明显现象,铝不能置换镁,乙试管可以证明铝的活动性小于镁;丙试管中没有明显现象,铜不能置换铝,可以证明铝的活动性大于铜;所以要验证铝、铜、镁三种金属的活动性,只需做甲和乙或乙和丙两个实验即可。
故答案为:
(1)A;
(2)一样;
(3)甲和乙或乙和丙。
12.解:(1)乙方案中烧杯内B溶液是稀硫酸(稀硫酸和氧化铜反应生成硫酸铜和水),两种方案相比较,甲方案明显的不足之处是没有处理尾气。
故答案为:稀硫酸;没有处理尾气。
(2)回收的铜丝网a的质量与原铜丝网质量相等,铜丝网b的质量减小,减小的质量与原铜丝网质量之差是与氧气反应的铜的质量,反应的化学方程式及其质量关系:
2Cu+O22CuO
128 32
6.4g 1.6g
则回收的铜丝网a的质量与铜丝网b的质量相差6.4g。
故答案为:6.4。
(3)小金加入过量的铁粉充分搅拌处理废液,过程中铁和硫酸铜反应生成硫酸亚铁和铜,最后得到的溶液中阳离子为Fe2+。
故答案为:Fe2+。
13.解:(1)根据图示分析可知,为了提高粗铜渣的利用率,可采取的措施是增加反应时间,故答案为:增加反应时间;
(2)CuO在“盐酸浸出”中和稀盐酸反应生成氯化铜和水,氧化铁和稀盐酸生成氯化铁和水,反应方程式为:CuO+2HCl=CuCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O;根据图象知,随着浸出时间的增加,Cu的浸出率相应的增加,浸出时间超过24h后,Cu的浸出率变化不明显,可知:最佳浸出时间为24h,故答案为:CuO+2HCl=CuCl2+H2O或Fe2O3+6HCl=2FeCl3+3H2O;24h;
(3)操作Ⅰ是分离固体和液体,是过滤操作,过滤中用到的玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是引流,故答案为:漏斗;引流。
(4)H2O2有强氧化性,能把Fe2+氧化为Fe3+;调节溶液pH值时加入的物质能和氢离子反应且不能引进新的杂质,A能引进杂质,只有BC能和氢离子反应且不引进杂质;根据Fe3+完全转化为沉淀时的pH可知,pH在3.2至4.7时Fe3+完全转化为沉淀且铜离子不沉淀;故答案为:把Fe2+氧化为Fe3;BC;3.2至4.7;
(5)操作2”包含过滤、洗涤滤渣、蒸发等多步实验基本操作,洗涤滤渣的目的是洗掉残留在滤渣表面的杂质离子,过滤后滤渣为红褐色固体,该滤渣是氢氧化铁,故答案为:洗掉残留在滤渣表面的杂质离子;Fe(OH)3;
(6)设粗铜渣质量为x,根据质量守恒,64%x=13.5t×,x=10.0t;由图可知铜的浸出率最多90%,所以精铜渣的质量为:10.0t÷90%≈11.1t;故答案为:11.1。
14.解:(1)在常温的条件下,铝易与空气的氧气反应生成致密的氧化铝保护膜,所以在空气中铝制品耐腐蚀;故答案为:在常温的条件下,铝易与空气的氧气反应生成致密的氧化铝保护膜;
(2)石墨烯性能优良,用途独特,比如用作太阳能电池的电极,这主要是利用了它的导电性;故答案为:导电;
(3)高阻尼橡胶是由合成橡胶制成的,合成橡胶是一种有机高分子材料;故答案为:b;
(4)氢气与氧气混合达到一定程度时遇明火或加热时会发生爆炸,所以该方案是错误的。故答案为:不正确;通过灼热的铜丝网时,混合气体可能发生爆炸。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
