【高中化学人教版(2019必修第一册同步训练】 第三章铁金属材料综合检测题(含答案)
文档属性
| 名称 | 【高中化学人教版(2019必修第一册同步训练】 第三章铁金属材料综合检测题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-10 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
【高中化学人教版(2019必修第一册同步训练】
第三章铁金属材料
一、单选题
1.下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是( )
A.铝 B.钠 C.钙 D.铁
2.下列解释事实的方程式或离子方程式正确的是
A.铁与稀盐酸反应:
B.碳酸钙与稀盐酸反应:
C.常温下,新切开的钠表面很快变暗:
D.黄色FeCl3溶液加入铁粉溶液变成浅绿色:
3.2024年4月,中国空间站迎来两件事情,其中一件事情就是神舟十八号飞船的发射,另一件事情就是神舟十七号飞船返回舱的返航。下列涉及的系列材料中,主要成分为金属的是( )
A.返回舱与推进舱分离时使用的推进剂——液氧和液氢 B.返回舱侧壁壳体——高强度铝合金
C.返回舱减速伞材料——高强度锦纶纤维 D.航天员返回途中穿着的航天服——合成纤维及尼龙膜
A.A B.B C.C D.D
4.将铁屑溶于过量盐酸后,再加入下列物质:①硫酸 ②硝酸锌 ③氯化铜 ④氯水 产生Fe3+的是( )
A.①④ B.②④ C.只有④ D.①③
5.有关厨房铝制品的使用中,你认为合理的是()
A.烧煮开水 B.盛放食醋
C.用碱水洗涤 D.用金属丝擦表面的污垢
6.某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在ag HmX中所含质子的物质的量是( )
A. (A-N) mol B. mol
C. (A-N+m) mol D. (A-N+m) mol
二、多选题
7.在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是( )
A.两种气体A与B的相对分子质量之比为m:n
B.同质量气体A与B的分子数之比为m:n
C.同温同压下,A,B两气体的密度之比为n:m
D.相同状况下,同体积A,B两气体的质量之比为m:n
三、填空题
8.18gH2O的物质的量是 ,含有 个氢原子.
9.已知某植物营养液配方为0.3mol KCl,0.2mol K2SO4,0.1mol ZnSO4和1L水.若以KCl,K2SO4,ZnCl2和1L水为原料配得相同组成的营养液,需三种溶质KCl mol,K2SO4 mol,ZnCl2 mol.
10.目前用量最大、用途最广泛的合金是 .
11.请根据题意选择下列物质:
A.明矾[KAI(SO4)2 12H2O]B.Fe2O3
C.NaHCO3 D.熟石灰[Ca(OH)2],
并用其字母代号填空:
(1)一种红棕色粉末,常用作红色油漆和涂料的是
(2)要使含泥沙的洪水变澄清,可使用 ;
(3)要中和钢铁厂、电镀厂产生的酸性废水,可使用 ;
(4)使焙制糕点松软可以添加 .
12.把 17.1g 固体氢氧化钡溶于水,配成 250mL 溶液,则该溶液的物质的量浓度是 mol/L;取出 10mL溶液,其中 c(Ba2+)= mol/L;把取出的 10mL 溶液加水稀释到 100mL,稀释后溶液物质的量浓度是 mol/L,其中所含溶质质量为 g。
四、解答题
13.已知某混和气体的体积百分组成中有80.0%的CH4、15.0%C2H2、5.0%的C2H4,请计算0.5摩尔该混和气体的质量和在标准状态下的密度(克/升).
14.成人每天从食物中摄取的几中元素的质量分别为:0.8gCa、0.3gMg、0.2gCu和0.01gFe,这4种元素的物质的量之比为多少?
五、实验探究题
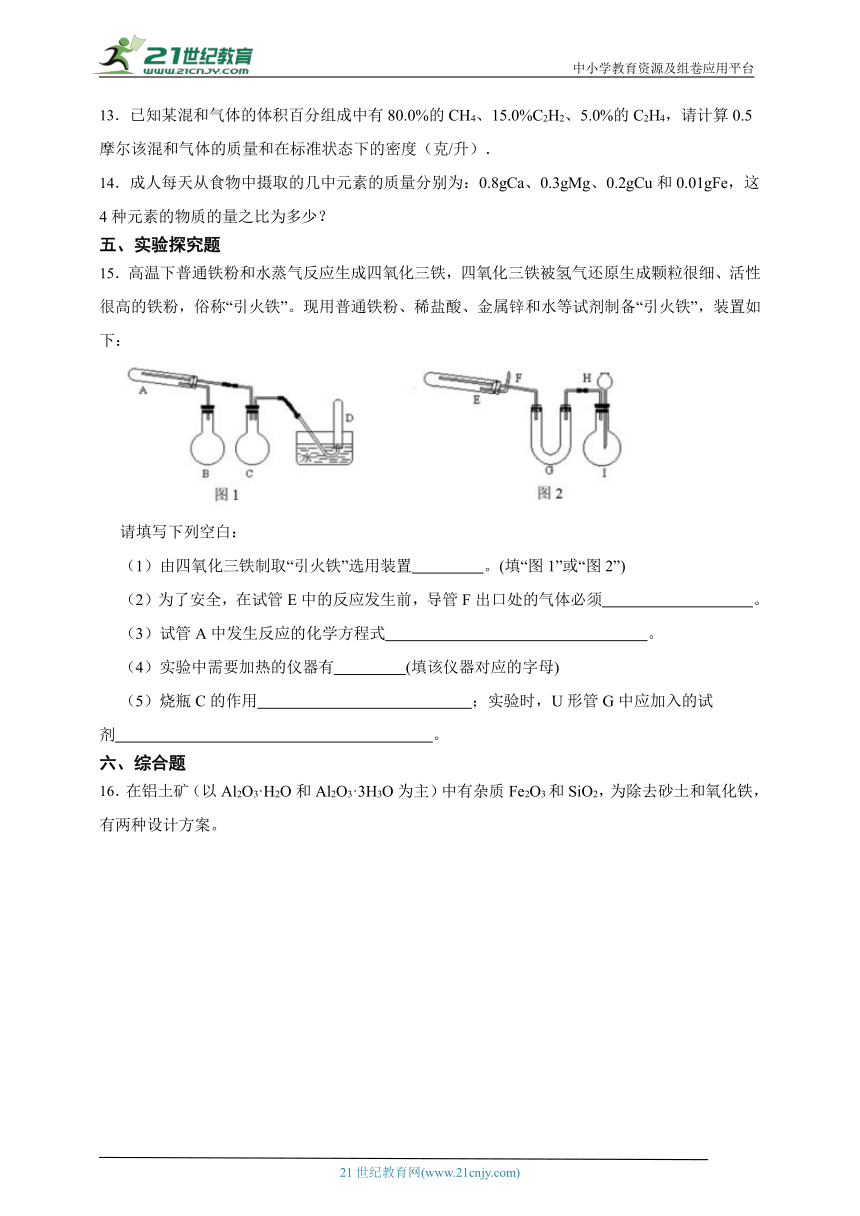
15.高温下普通铁粉和水蒸气反应生成四氧化三铁,四氧化三铁被氢气还原生成颗粒很细、活性很高的铁粉,俗称“引火铁”。现用普通铁粉、稀盐酸、金属锌和水等试剂制备“引火铁”,装置如下:
请填写下列空白:
(1)由四氧化三铁制取“引火铁”选用装置 。(填“图1”或“图2”)
(2)为了安全,在试管E中的反应发生前,导管F出口处的气体必须 。
(3)试管A中发生反应的化学方程式 。
(4)实验中需要加热的仪器有 (填该仪器对应的字母)
(5)烧瓶C的作用 ;实验时,U形管G中应加入的试剂 。
六、综合题
16.在铝土矿(以Al2O3·H2O和Al2O3·3H3O为主)中有杂质Fe2O3和SiO2,为除去砂土和氧化铁,有两种设计方案。
(1)以上设计的两种方案中,合理而又考虑经济效益的是(填编号) 。
(2)若提纯时用的原料除铝土矿、水外,还需物质在下列物质中选择:①Na2CO3,②CaCO3,③H2SO4,④HCl,⑤KOH。试写出有关主要反应的化学方程式(是离子反应的要写离子方程式): 。
17.按要求填空
(1)相同物质的量的O2和O3的质量比 ,分子个数比为 ,所含氧原子的个数比为 .
(2)在200mL 2mol/L MgCl2溶液中,溶质的质量为 g.此溶液中Mg2+的物质的量浓度为 mol/L,Cl﹣的物质的量浓度为 mol/L.
七、推断题
18.如图所示是铁及其化合物的价类二维图。回答下列问题:
(1)X的化学式为 ,生铁在潮湿空气中主要发生 (填“析氢”或“吸氧”)腐蚀。
(2)工业上用赤铁矿(Fe2O3)冶炼Fe常用的方法是 (填标号)。
a.电解法 b.热还原法 c.热分解法 d.物理方法
(3)检验FeCl3和FeCl2混合溶液中Fe2+的操作是 ;除去FeCl2溶液中的少量FeCl3加入的最佳试剂为 。
(4)Z在空气中很容易变成Y,该反应的化学方程式为 。
(5)FeCl3和KI在水溶液中转化的离子反应有:2Fe3++2I-2Fe2++I2,为了探究该反应存在一定的限度,某化学兴趣小组取10mL0.5mol·L-1的KI溶液于试管中,再加入10mL0.2mol·L-1的FeCl3溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的____(填标号)。
A.淀粉溶液 B.KSCN溶液
C.硝酸银溶液 D.酸性高锰酸钾溶液
答案解析部分
1.【答案】A
【知识点】铝的化学性质
2.【答案】D
【知识点】钠的化学性质;铁的化学性质;离子方程式的书写
3.【答案】B
【知识点】合金及其应用
4.【答案】B
【知识点】铁的化学性质;铁盐和亚铁盐的相互转变
5.【答案】A
【知识点】铝的化学性质
6.【答案】C
【知识点】物质的量的相关计算
7.【答案】B,C
【知识点】物质的量的相关计算
8.【答案】1mol;NA或1.204×1024
【知识点】物质的量的相关计算
9.【答案】0.1;0.3;0.1
【知识点】物质的量的相关计算
10.【答案】钢
【知识点】合金及其应用
11.【答案】B;A;D;C
【知识点】镁、铝的重要化合物
12.【答案】4;4;0.4;6.84
【知识点】物质的量的相关计算
13.【答案】解:0.5摩尔该混和气体的质量=0.500mol×(16g/mol×80.0%+26g/mol×15.0%+28g/mol×5.0%)=9.05g;
混合气体的密度==0.808(g/l);
故答案为:9.05g;0.808(g/l).
【知识点】物质的量的相关计算
14.【答案】解:0.8gCa的物质的量为: ;
0.3gMg的物质的量为: ;
0.2gCu的物质的量为: ;
0.01gFe的物质的量为: ;
所以这4种元素的物质的量之比为:0.02mol:0.0125mol:0.003125mol:0.0001786mol=224:14:0.35:2
【知识点】摩尔质量;物质的量的相关计算
15.【答案】(1)图2
(2)检验氢气的纯度
(3)3Fe+4H2O(g)Fe3O4+4H2
(4)ABE
(5)防止倒吸(或用作安全瓶);体NaOH或碱石灰、CaO等碱性固体干燥剂
【知识点】铁的化学性质;铁的氧化物和氢氧化物
16.【答案】(1)A
(2)Al2O3+2OH-=2AlO2-+H2O,2AlO2-+3H2O+CO2=Al(OH)3↓+CO32-,2Al(OH)3Al2O3+3H2O,CaCO3CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+CO32-=CaCO3+2OH-
【知识点】镁、铝的重要化合物;两性氧化物和两性氢氧化物
17.【答案】(1)2:3;1:1;2:3
(2)38;2;4
【知识点】物质的量的相关计算
18.【答案】(1)FeO;吸氧
(2)b
(3)取少许溶液,滴加铁氰化钾溶液,有蓝色沉淀产生,证明有Fe2+存在;铁粉
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(5)B
【知识点】铁的氧化物和氢氧化物;铁盐和亚铁盐的相互转变;二价铁离子和三价铁离子的检验
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
【高中化学人教版(2019必修第一册同步训练】
第三章铁金属材料
一、单选题
1.下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是( )
A.铝 B.钠 C.钙 D.铁
2.下列解释事实的方程式或离子方程式正确的是
A.铁与稀盐酸反应:
B.碳酸钙与稀盐酸反应:
C.常温下,新切开的钠表面很快变暗:
D.黄色FeCl3溶液加入铁粉溶液变成浅绿色:
3.2024年4月,中国空间站迎来两件事情,其中一件事情就是神舟十八号飞船的发射,另一件事情就是神舟十七号飞船返回舱的返航。下列涉及的系列材料中,主要成分为金属的是( )
A.返回舱与推进舱分离时使用的推进剂——液氧和液氢 B.返回舱侧壁壳体——高强度铝合金
C.返回舱减速伞材料——高强度锦纶纤维 D.航天员返回途中穿着的航天服——合成纤维及尼龙膜
A.A B.B C.C D.D
4.将铁屑溶于过量盐酸后,再加入下列物质:①硫酸 ②硝酸锌 ③氯化铜 ④氯水 产生Fe3+的是( )
A.①④ B.②④ C.只有④ D.①③
5.有关厨房铝制品的使用中,你认为合理的是()
A.烧煮开水 B.盛放食醋
C.用碱水洗涤 D.用金属丝擦表面的污垢
6.某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在ag HmX中所含质子的物质的量是( )
A. (A-N) mol B. mol
C. (A-N+m) mol D. (A-N+m) mol
二、多选题
7.在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是( )
A.两种气体A与B的相对分子质量之比为m:n
B.同质量气体A与B的分子数之比为m:n
C.同温同压下,A,B两气体的密度之比为n:m
D.相同状况下,同体积A,B两气体的质量之比为m:n
三、填空题
8.18gH2O的物质的量是 ,含有 个氢原子.
9.已知某植物营养液配方为0.3mol KCl,0.2mol K2SO4,0.1mol ZnSO4和1L水.若以KCl,K2SO4,ZnCl2和1L水为原料配得相同组成的营养液,需三种溶质KCl mol,K2SO4 mol,ZnCl2 mol.
10.目前用量最大、用途最广泛的合金是 .
11.请根据题意选择下列物质:
A.明矾[KAI(SO4)2 12H2O]B.Fe2O3
C.NaHCO3 D.熟石灰[Ca(OH)2],
并用其字母代号填空:
(1)一种红棕色粉末,常用作红色油漆和涂料的是
(2)要使含泥沙的洪水变澄清,可使用 ;
(3)要中和钢铁厂、电镀厂产生的酸性废水,可使用 ;
(4)使焙制糕点松软可以添加 .
12.把 17.1g 固体氢氧化钡溶于水,配成 250mL 溶液,则该溶液的物质的量浓度是 mol/L;取出 10mL溶液,其中 c(Ba2+)= mol/L;把取出的 10mL 溶液加水稀释到 100mL,稀释后溶液物质的量浓度是 mol/L,其中所含溶质质量为 g。
四、解答题
13.已知某混和气体的体积百分组成中有80.0%的CH4、15.0%C2H2、5.0%的C2H4,请计算0.5摩尔该混和气体的质量和在标准状态下的密度(克/升).
14.成人每天从食物中摄取的几中元素的质量分别为:0.8gCa、0.3gMg、0.2gCu和0.01gFe,这4种元素的物质的量之比为多少?
五、实验探究题
15.高温下普通铁粉和水蒸气反应生成四氧化三铁,四氧化三铁被氢气还原生成颗粒很细、活性很高的铁粉,俗称“引火铁”。现用普通铁粉、稀盐酸、金属锌和水等试剂制备“引火铁”,装置如下:
请填写下列空白:
(1)由四氧化三铁制取“引火铁”选用装置 。(填“图1”或“图2”)
(2)为了安全,在试管E中的反应发生前,导管F出口处的气体必须 。
(3)试管A中发生反应的化学方程式 。
(4)实验中需要加热的仪器有 (填该仪器对应的字母)
(5)烧瓶C的作用 ;实验时,U形管G中应加入的试剂 。
六、综合题
16.在铝土矿(以Al2O3·H2O和Al2O3·3H3O为主)中有杂质Fe2O3和SiO2,为除去砂土和氧化铁,有两种设计方案。
(1)以上设计的两种方案中,合理而又考虑经济效益的是(填编号) 。
(2)若提纯时用的原料除铝土矿、水外,还需物质在下列物质中选择:①Na2CO3,②CaCO3,③H2SO4,④HCl,⑤KOH。试写出有关主要反应的化学方程式(是离子反应的要写离子方程式): 。
17.按要求填空
(1)相同物质的量的O2和O3的质量比 ,分子个数比为 ,所含氧原子的个数比为 .
(2)在200mL 2mol/L MgCl2溶液中,溶质的质量为 g.此溶液中Mg2+的物质的量浓度为 mol/L,Cl﹣的物质的量浓度为 mol/L.
七、推断题
18.如图所示是铁及其化合物的价类二维图。回答下列问题:
(1)X的化学式为 ,生铁在潮湿空气中主要发生 (填“析氢”或“吸氧”)腐蚀。
(2)工业上用赤铁矿(Fe2O3)冶炼Fe常用的方法是 (填标号)。
a.电解法 b.热还原法 c.热分解法 d.物理方法
(3)检验FeCl3和FeCl2混合溶液中Fe2+的操作是 ;除去FeCl2溶液中的少量FeCl3加入的最佳试剂为 。
(4)Z在空气中很容易变成Y,该反应的化学方程式为 。
(5)FeCl3和KI在水溶液中转化的离子反应有:2Fe3++2I-2Fe2++I2,为了探究该反应存在一定的限度,某化学兴趣小组取10mL0.5mol·L-1的KI溶液于试管中,再加入10mL0.2mol·L-1的FeCl3溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的____(填标号)。
A.淀粉溶液 B.KSCN溶液
C.硝酸银溶液 D.酸性高锰酸钾溶液
答案解析部分
1.【答案】A
【知识点】铝的化学性质
2.【答案】D
【知识点】钠的化学性质;铁的化学性质;离子方程式的书写
3.【答案】B
【知识点】合金及其应用
4.【答案】B
【知识点】铁的化学性质;铁盐和亚铁盐的相互转变
5.【答案】A
【知识点】铝的化学性质
6.【答案】C
【知识点】物质的量的相关计算
7.【答案】B,C
【知识点】物质的量的相关计算
8.【答案】1mol;NA或1.204×1024
【知识点】物质的量的相关计算
9.【答案】0.1;0.3;0.1
【知识点】物质的量的相关计算
10.【答案】钢
【知识点】合金及其应用
11.【答案】B;A;D;C
【知识点】镁、铝的重要化合物
12.【答案】4;4;0.4;6.84
【知识点】物质的量的相关计算
13.【答案】解:0.5摩尔该混和气体的质量=0.500mol×(16g/mol×80.0%+26g/mol×15.0%+28g/mol×5.0%)=9.05g;
混合气体的密度==0.808(g/l);
故答案为:9.05g;0.808(g/l).
【知识点】物质的量的相关计算
14.【答案】解:0.8gCa的物质的量为: ;
0.3gMg的物质的量为: ;
0.2gCu的物质的量为: ;
0.01gFe的物质的量为: ;
所以这4种元素的物质的量之比为:0.02mol:0.0125mol:0.003125mol:0.0001786mol=224:14:0.35:2
【知识点】摩尔质量;物质的量的相关计算
15.【答案】(1)图2
(2)检验氢气的纯度
(3)3Fe+4H2O(g)Fe3O4+4H2
(4)ABE
(5)防止倒吸(或用作安全瓶);体NaOH或碱石灰、CaO等碱性固体干燥剂
【知识点】铁的化学性质;铁的氧化物和氢氧化物
16.【答案】(1)A
(2)Al2O3+2OH-=2AlO2-+H2O,2AlO2-+3H2O+CO2=Al(OH)3↓+CO32-,2Al(OH)3Al2O3+3H2O,CaCO3CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+CO32-=CaCO3+2OH-
【知识点】镁、铝的重要化合物;两性氧化物和两性氢氧化物
17.【答案】(1)2:3;1:1;2:3
(2)38;2;4
【知识点】物质的量的相关计算
18.【答案】(1)FeO;吸氧
(2)b
(3)取少许溶液,滴加铁氰化钾溶液,有蓝色沉淀产生,证明有Fe2+存在;铁粉
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(5)B
【知识点】铁的氧化物和氢氧化物;铁盐和亚铁盐的相互转变;二价铁离子和三价铁离子的检验
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
