2.2烯烃高二下学期化学人教版2019选择性必修3(共26张PPT)
文档属性
| 名称 | 2.2烯烃高二下学期化学人教版2019选择性必修3(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-11 00:00:00 | ||
图片预览





文档简介
(共26张PPT)
第二章烃
第二节烯烃炔烃
2.2.1 烯烃
新冠疫情爆发之初,口罩一度成为畅销品,甚至脱销,而丙烯
CH -CH=CH 是制造N95 口罩的原料之一。
丙烯具有哪些性质呢
新课引入
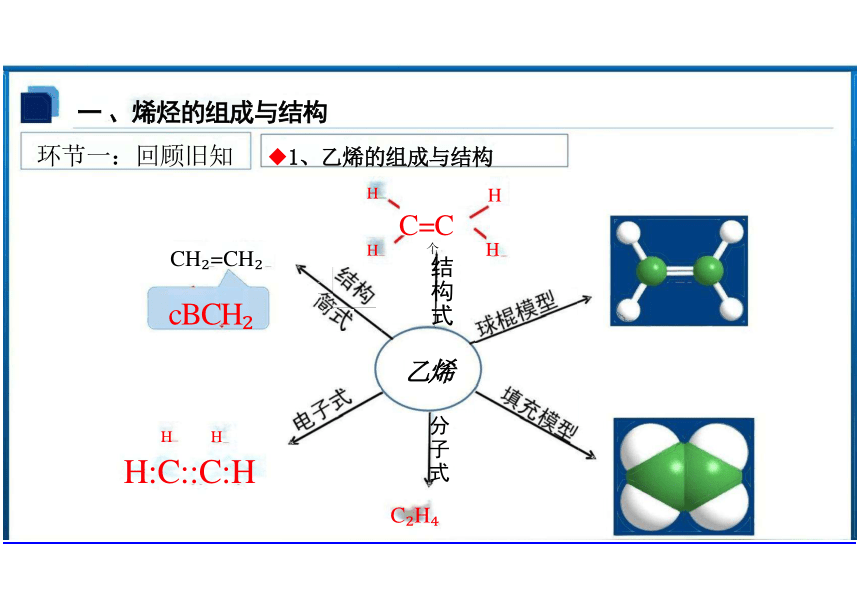
CH =CH
cBCH
H H
H:C::C:H
一 、烯烃的组成与结构
环节一:回顾旧知 ◆1、乙烯的组成与结构
乙烯
分 子
式
C H
个结构式
C=C
H
H
H
H
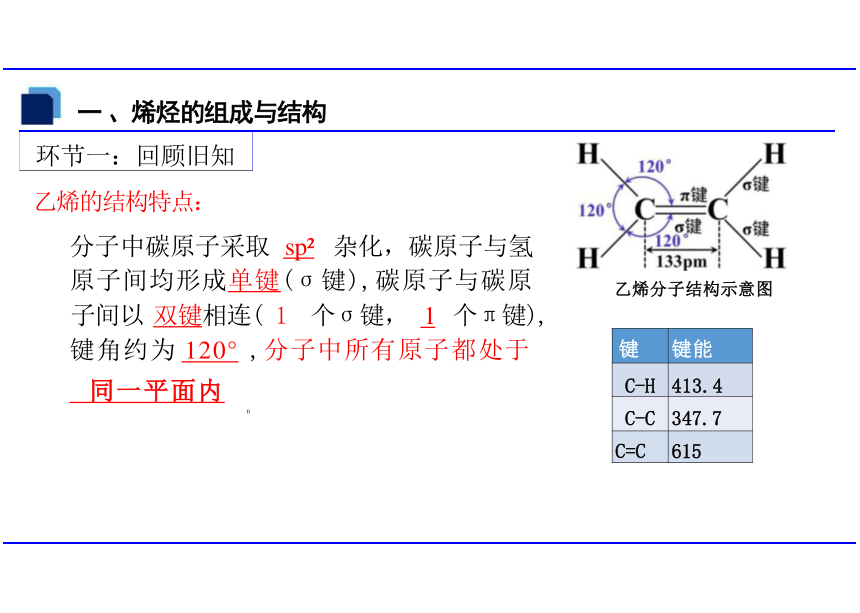
乙烯的结构特点:
分子中碳原子采取 sp 杂化,碳原子与氢 原子间均形成单键(σ键),碳原子与碳原
子间以 双键相连( 1 个σ键, 1 个π键),
键角约为 120° ,分子中所有原子都处于
同一平面内
0
键
键能
C-H
413.4
C-C
347.7
C=C
615
一 、烯烃的组成与结构
环节一:回顾旧知
乙烯分子结构示意图
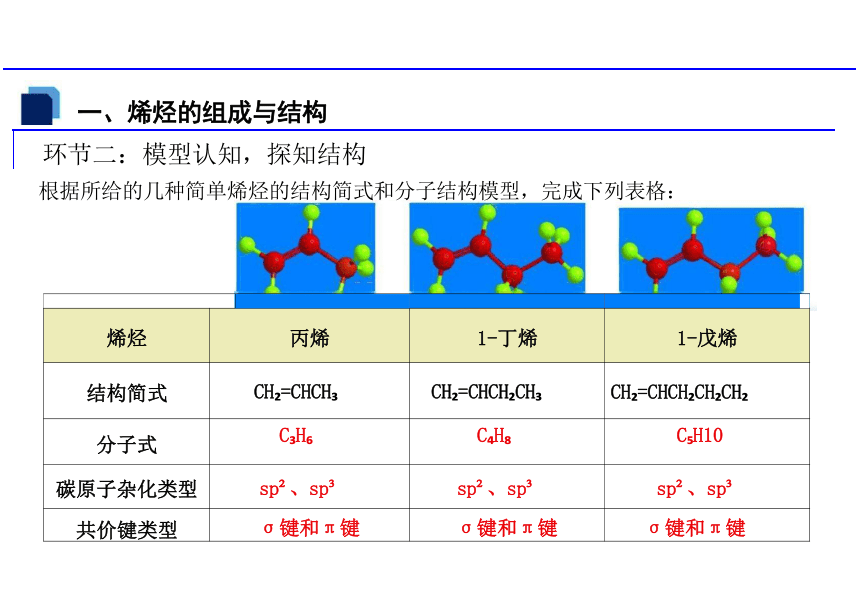
烯烃 丙烯 1-丁烯
1-戊烯
结构简式 CH =CHCH CH =CHCH CH
CH =CHCH CH CH
分子式 C H C H
C H10
碳原子杂化类型 sp 、sp sp 、sp
sp 、sp
共价键类型 σ键和π键 σ键和π键
σ键和π键
根据所给的几种简单烯烃的结构简式和分子结构模型,完成下列表格:
一、烯烃的组成与结构
环节二:模型认知,探知结构
(1)定义:分子中含有碳碳双键的烃,属于不饱和烃。
(2)官能团:碳碳双键 C-C
(3)结构特点:双键碳原子采取sp 杂化,以碳碳双键为中心的6个原子一定在同一平面。
(4)通式:链 状单烯烃C H n(n≥2) 注意
单烯烃与 同碳原子数的环烷烃是 同分异构体。
(5)分类: 如:丙烯CH =CHCH 、
环节二:模型认知,探知结构
◆2、烯烃的组成与结构
①累积二烯烃 C-C = C =C-C 不稳定
②共轭二烯烃 C = C-C =C-C 稳 定
③孤立二烯烃 C = C-C-C = C 性质同单烯烃
二烯烃 CH =CH-CH=CH 1,3- 丁二烯
多烯烃
一、烯烃的组成与结构
单烯烃 CH =CH 乙烯
=
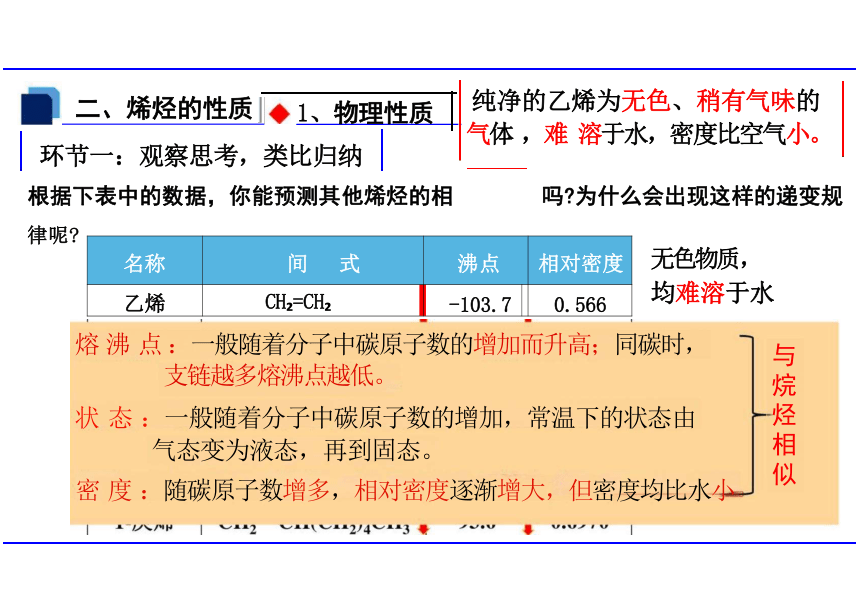
熔 沸 点 :一般随着分子中碳原子数的增加而升高;同碳时,
支链越多熔沸点越低。
状 态 :一般随着分子中碳原子数的增加,常温下的状态由 气态变为液态,再到固态。
密 度 :随碳原子数增多,相对密度逐渐增大,但密度均比水小
名称 间 式 沸点
相对密度
乙烯 CH =CH -103.7
0.566
纯净的乙烯为无色、稍有气味的
气体 ,难 溶于水,密度比空气小。
二、烯烃的性质 1、物理性质
根据下表中的数据,你能预测其他烯烃的相 吗 为什么会出现这样的递变规
环节一:观察思考,类比归纳
无色物质,
均难溶于水
与烷烃相似
律呢
二、烯烃的性质 环节二:回顾旧知,类比学习
①可燃性 ②使酸性KMnO 溶液褪色
2、化学性质
(1)氧化反应——乙烯
CH =cH KMnog(Hc O +H O
(1)氧化反应——烯烃
①可燃性
①有机物的含碳量越高,火焰越明亮,黑烟越浓;
②随着C数个:单烯烃含碳量相同,烷烃的含碳量增大,炔烃的含碳量降低 【思考与讨论】书写丙烯燃烧的方程式
②使酸性KMnO 溶液褪色
●能使酸性高锰酸钾溶液褪色,是由于碳碳双键的存在。
●可用酸性高锰酸钾溶液鉴别甲烷 (烷烃)和乙烯 (烯烃)。
●不能只用酸性高锰酸钾溶液除去甲烷中的乙烯。
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质 烯烃被氧化 的部位 CH = RCH= R R
C=
氧化产物 CO RCOOH R ~C=0 R
二、烯烃的性质 环节二:回顾旧知,类比学习 2、化学性质
烯烃与酸性高锰酸钾溶液反应的规律:
无氢成酮
C0LpC00H
C02TkCoon
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质
③臭氧氧化
烯烃经臭氧氧化后,在Zn 存在的条件下水解,可得到醛或酮。
如
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质
有机反应中:得 O失H的反应叫氧化反应;
得H失O 的反应叫还原反应。
④乙烯的催化氧化
催化剂
催化剂 0
2CH =CH +O 2
2CH =CH +O 加热加压2CH CHO
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质
或原子团直接结合生成新的物质的反应。
常与Br 、H 、HX 、H O
(2)加成反应 有机物分子中的不饱和碳原子(双键或三键等)与其它原子
无色液体,
密度比水大, 难溶于水。
1,2-二溴乙烷
CH,=CH,+Br,—
只进不出
CH,BrCH,Br
当分子结构不对称的烯烃与分子结构不对称的试剂发生加成时,加
成方向应如何决定 如丙烯与溴化氢反应后,会生成什么产物呢
二、烯烃的性质 ◆2、化学性质
①乙 烯 (对称单烯烃) 与H 、HX、H O 的加成反应:
啥 啥 啥
CH CH=CH +Br →CH CHBrCH Br
H C-CH=CH +HCl cCH 或
H C-CH=CH +H 或
H加H多
不对称烯烃和HX 、H O加成时,氢主要加在含氢多的双键碳原子上 ,这就是马氏规则。
思考:请同学们分析Br 、HCI、H O 分别与丙烯加成反应后产物的种类。
二、烯烃的性质 2、化学性质
②不对称烯烃
●区别乙烷和乙烯方法:
可用酸性高锰酸钾溶液或者溴水或者溴的四氯化碳溶液。
●除去乙烷中的乙烯方法:
①可用溴水
酸性KMnO4 溶液
不可以用溴的四氯化碳溶液
乙烷可以溶于四氯化碳
碱石灰或 浓硫酸
拓展延伸
NaOH 溶液
②混合 气体
Br (g)/ 光照
CH -CH=CH
Br
有机物A 的结构简式为CH =CHCH Br ;
生成B的化学方程式为:CH CH=CH +Br →CH CHBrCH Br 。
例1:丙烯在一定条件下能发生如图所示的转化:
(C 。H-Rr) 315D
D
D
课堂练习
CH —CH—CH—CH—C—CH
CH CH CH
是烯烃R和氢气发生加成反应后的产物,则R可能的
结构简式有( c )
A.4种 B.5 种 C.6 种 D.7 种
CH C H
课堂练习
2.烷烃
(a)1,3-丁二烯与氯气1:1发生加成反应有以下两种方式:
1,2-加成 CH =CH—CH=CH +Cl — CH —CH— CH=CH
竞争反应 Cl Cl
1,4-加成CH ÷CH—CH÷CH +Cl —→CH —CH=9H—CH
Cl Cl
(b)1,3-丁二烯与溴1:2全加成
③共轭二烯烃的加成反应
二、烯烃的性质
温度 较低
温度
较高
◆2、化学性质
④Diels-Alder 反应( 双烯合成) 二烯烃的加成反应
含活泼双键或叁键的化合物(亲双烯体)与含共轭双键的化合物 (双烯体)之间发生1,4 - 加成生 成六元环状化合物的反应,称为 Diels-Alder反应,也称双烯合成
二 、烯烃的性质
2、化学性质
二、烯烃的性质
◆2、化学性质
十
十
十
十
所用的原始原料可以是 ( A、D )
A.2一甲基一I,3 一丁二烯和2一丁炔
B.1,3 一戊二烯和2一丁炔
C.2,3 一二甲基一1,3一戊二烯和乙炔
D.2,3— 二甲基一1,3一丁二烯和丙炔
,如果要合成
例3、已知: 十
◆课堂练习
一定条件
二 、烯烃的性质
2、化学性质
(3)加聚反应
根据乙烯、氯乙烯发生的加聚,写出丙烯、异丁烯发生加聚反应的化学方程式。
PP 聚丙烯
聚异丁烯
二、烯烃的性质
练一练
(1)有碳碳双键
(2) 双键的每个碳原子必须连接两个不同的原子或原子团。
通过碳碳双键连接的原子或原子团不能绕键轴旋转会导致其空间排
三 、烯烃的立体异构
列方式不同,产生顺反异构现象。
形成顺反异构的条件:
三 、烯烃的立体异构
顺-2-丁烯 反-2-丁烯
相同的原子或原子团位于双键同一侧为顺式结构 相同的原子或原子团位于双键两侧为反式结构
H C=C H C H CH H C=C H C
CH
H
熔点/℃ —138.9 —105.5 沸点/℃ 3.7 0.9 密度/(g · cm-3) 0.621 0.604
互为顺反异构体的两种物质化学性质基本相同,物理性质有一定差异。
第二章烃
第二节烯烃炔烃
2.2.1 烯烃
新冠疫情爆发之初,口罩一度成为畅销品,甚至脱销,而丙烯
CH -CH=CH 是制造N95 口罩的原料之一。
丙烯具有哪些性质呢
新课引入
CH =CH
cBCH
H H
H:C::C:H
一 、烯烃的组成与结构
环节一:回顾旧知 ◆1、乙烯的组成与结构
乙烯
分 子
式
C H
个结构式
C=C
H
H
H
H
乙烯的结构特点:
分子中碳原子采取 sp 杂化,碳原子与氢 原子间均形成单键(σ键),碳原子与碳原
子间以 双键相连( 1 个σ键, 1 个π键),
键角约为 120° ,分子中所有原子都处于
同一平面内
0
键
键能
C-H
413.4
C-C
347.7
C=C
615
一 、烯烃的组成与结构
环节一:回顾旧知
乙烯分子结构示意图
烯烃 丙烯 1-丁烯
1-戊烯
结构简式 CH =CHCH CH =CHCH CH
CH =CHCH CH CH
分子式 C H C H
C H10
碳原子杂化类型 sp 、sp sp 、sp
sp 、sp
共价键类型 σ键和π键 σ键和π键
σ键和π键
根据所给的几种简单烯烃的结构简式和分子结构模型,完成下列表格:
一、烯烃的组成与结构
环节二:模型认知,探知结构
(1)定义:分子中含有碳碳双键的烃,属于不饱和烃。
(2)官能团:碳碳双键 C-C
(3)结构特点:双键碳原子采取sp 杂化,以碳碳双键为中心的6个原子一定在同一平面。
(4)通式:链 状单烯烃C H n(n≥2) 注意
单烯烃与 同碳原子数的环烷烃是 同分异构体。
(5)分类: 如:丙烯CH =CHCH 、
环节二:模型认知,探知结构
◆2、烯烃的组成与结构
①累积二烯烃 C-C = C =C-C 不稳定
②共轭二烯烃 C = C-C =C-C 稳 定
③孤立二烯烃 C = C-C-C = C 性质同单烯烃
二烯烃 CH =CH-CH=CH 1,3- 丁二烯
多烯烃
一、烯烃的组成与结构
单烯烃 CH =CH 乙烯
=
熔 沸 点 :一般随着分子中碳原子数的增加而升高;同碳时,
支链越多熔沸点越低。
状 态 :一般随着分子中碳原子数的增加,常温下的状态由 气态变为液态,再到固态。
密 度 :随碳原子数增多,相对密度逐渐增大,但密度均比水小
名称 间 式 沸点
相对密度
乙烯 CH =CH -103.7
0.566
纯净的乙烯为无色、稍有气味的
气体 ,难 溶于水,密度比空气小。
二、烯烃的性质 1、物理性质
根据下表中的数据,你能预测其他烯烃的相 吗 为什么会出现这样的递变规
环节一:观察思考,类比归纳
无色物质,
均难溶于水
与烷烃相似
律呢
二、烯烃的性质 环节二:回顾旧知,类比学习
①可燃性 ②使酸性KMnO 溶液褪色
2、化学性质
(1)氧化反应——乙烯
CH =cH KMnog(Hc O +H O
(1)氧化反应——烯烃
①可燃性
①有机物的含碳量越高,火焰越明亮,黑烟越浓;
②随着C数个:单烯烃含碳量相同,烷烃的含碳量增大,炔烃的含碳量降低 【思考与讨论】书写丙烯燃烧的方程式
②使酸性KMnO 溶液褪色
●能使酸性高锰酸钾溶液褪色,是由于碳碳双键的存在。
●可用酸性高锰酸钾溶液鉴别甲烷 (烷烃)和乙烯 (烯烃)。
●不能只用酸性高锰酸钾溶液除去甲烷中的乙烯。
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质 烯烃被氧化 的部位 CH = RCH= R R
C=
氧化产物 CO RCOOH R ~C=0 R
二、烯烃的性质 环节二:回顾旧知,类比学习 2、化学性质
烯烃与酸性高锰酸钾溶液反应的规律:
无氢成酮
C0LpC00H
C02TkCoon
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质
③臭氧氧化
烯烃经臭氧氧化后,在Zn 存在的条件下水解,可得到醛或酮。
如
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质
有机反应中:得 O失H的反应叫氧化反应;
得H失O 的反应叫还原反应。
④乙烯的催化氧化
催化剂
催化剂 0
2CH =CH +O 2
2CH =CH +O 加热加压2CH CHO
二、烯烃的性质 环节二:回顾旧知,类比学习
◆2、化学性质
或原子团直接结合生成新的物质的反应。
常与Br 、H 、HX 、H O
(2)加成反应 有机物分子中的不饱和碳原子(双键或三键等)与其它原子
无色液体,
密度比水大, 难溶于水。
1,2-二溴乙烷
CH,=CH,+Br,—
只进不出
CH,BrCH,Br
当分子结构不对称的烯烃与分子结构不对称的试剂发生加成时,加
成方向应如何决定 如丙烯与溴化氢反应后,会生成什么产物呢
二、烯烃的性质 ◆2、化学性质
①乙 烯 (对称单烯烃) 与H 、HX、H O 的加成反应:
啥 啥 啥
CH CH=CH +Br →CH CHBrCH Br
H C-CH=CH +HCl cCH 或
H C-CH=CH +H 或
H加H多
不对称烯烃和HX 、H O加成时,氢主要加在含氢多的双键碳原子上 ,这就是马氏规则。
思考:请同学们分析Br 、HCI、H O 分别与丙烯加成反应后产物的种类。
二、烯烃的性质 2、化学性质
②不对称烯烃
●区别乙烷和乙烯方法:
可用酸性高锰酸钾溶液或者溴水或者溴的四氯化碳溶液。
●除去乙烷中的乙烯方法:
①可用溴水
酸性KMnO4 溶液
不可以用溴的四氯化碳溶液
乙烷可以溶于四氯化碳
碱石灰或 浓硫酸
拓展延伸
NaOH 溶液
②混合 气体
Br (g)/ 光照
CH -CH=CH
Br
有机物A 的结构简式为CH =CHCH Br ;
生成B的化学方程式为:CH CH=CH +Br →CH CHBrCH Br 。
例1:丙烯在一定条件下能发生如图所示的转化:
(C 。H-Rr) 315D
D
D
课堂练习
CH —CH—CH—CH—C—CH
CH CH CH
是烯烃R和氢气发生加成反应后的产物,则R可能的
结构简式有( c )
A.4种 B.5 种 C.6 种 D.7 种
CH C H
课堂练习
2.烷烃
(a)1,3-丁二烯与氯气1:1发生加成反应有以下两种方式:
1,2-加成 CH =CH—CH=CH +Cl — CH —CH— CH=CH
竞争反应 Cl Cl
1,4-加成CH ÷CH—CH÷CH +Cl —→CH —CH=9H—CH
Cl Cl
(b)1,3-丁二烯与溴1:2全加成
③共轭二烯烃的加成反应
二、烯烃的性质
温度 较低
温度
较高
◆2、化学性质
④Diels-Alder 反应( 双烯合成) 二烯烃的加成反应
含活泼双键或叁键的化合物(亲双烯体)与含共轭双键的化合物 (双烯体)之间发生1,4 - 加成生 成六元环状化合物的反应,称为 Diels-Alder反应,也称双烯合成
二 、烯烃的性质
2、化学性质
二、烯烃的性质
◆2、化学性质
十
十
十
十
所用的原始原料可以是 ( A、D )
A.2一甲基一I,3 一丁二烯和2一丁炔
B.1,3 一戊二烯和2一丁炔
C.2,3 一二甲基一1,3一戊二烯和乙炔
D.2,3— 二甲基一1,3一丁二烯和丙炔
,如果要合成
例3、已知: 十
◆课堂练习
一定条件
二 、烯烃的性质
2、化学性质
(3)加聚反应
根据乙烯、氯乙烯发生的加聚,写出丙烯、异丁烯发生加聚反应的化学方程式。
PP 聚丙烯
聚异丁烯
二、烯烃的性质
练一练
(1)有碳碳双键
(2) 双键的每个碳原子必须连接两个不同的原子或原子团。
通过碳碳双键连接的原子或原子团不能绕键轴旋转会导致其空间排
三 、烯烃的立体异构
列方式不同,产生顺反异构现象。
形成顺反异构的条件:
三 、烯烃的立体异构
顺-2-丁烯 反-2-丁烯
相同的原子或原子团位于双键同一侧为顺式结构 相同的原子或原子团位于双键两侧为反式结构
H C=C H C H CH H C=C H C
CH
H
熔点/℃ —138.9 —105.5 沸点/℃ 3.7 0.9 密度/(g · cm-3) 0.621 0.604
互为顺反异构体的两种物质化学性质基本相同,物理性质有一定差异。
