3.5有机合成 高二下化学人教版(2019)选择性必修3(共54张PPT)
文档属性
| 名称 | 3.5有机合成 高二下化学人教版(2019)选择性必修3(共54张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-11 00:00:00 | ||
图片预览







文档简介
(共54张PPT)
第三章 烃的衍生物
第五节 有机合成
利用简单、易得的原料,通过有机反应,生成具有
有机合成反应的常见装置
一、有机合成的过程
特定结构和功能的有机化合物。
恒压分液漏斗
三颈烧瓶
冷凝管
1.有机合成遵循的原则
1)原料选择
廉价、易得、低毒、低污染
通常采用4个碳以下的单官能团化合物或单取代苯。
尽量选择步骤最少__ 的合成路线
尽量选择与目标化合物 结构相似 的原料 步骤越少,最后 产率 越高。
2)合成路线
1.有机合成遵循的原则
最大限度的利用原料分子的每个原子,达到 零排放。
尊重客观事实,按一定反应顺序和规律引入 官 能 团。
操作简单、条件温和、能耗低、易实现
4)合成优势
5)尊重事实
3)绿色化学
有机合成的意义
①制备天然有机物,弥补自然资源的不足;
②对天然有机物进行局部的结构改造和修饰,使其性能更加完美;
③合成具有特定性质的、自然界并不存在的有机物, 以满足人类的特殊需要
制 各 的 维 生 责C 阿司匹林缓释片 隐形眼镜材料
三氯蔗糖
者食用,被认为是近乎完美的甜味剂。
分子结构修饰在药物设计与合成中有广 泛的应用。为提高药物的治疗效果,降低毒 副作用等,可将药物分子的结构进行修饰。 例如,布洛芬具有抗炎、镇痛、解热作用, 但口服该药对胃、肠道有刺激性,可以对该 分子进行如图2-23所示的成酯修饰。
图12-21 蔗糖和三氯蔗糖结构式
三氯蔗糖(如图2-22),又名蔗糖素, 其甜度是蔗糖的600倍,没有异味,具有热 量值极低、安全性好等优点,可供糖尿病患
构被修饰后,分子的性质发生了改变。例如, 用三个氯原子取代蔗糖分子(如图2-21)中 的三个羟基,就得到三 氯蔗糖(如图2-21)。
分子结构修饰是指不改变分子的主体骨 架,保持分子的基本结构不变,仅改变分子 结构中的某些基团而得到的新分子。分子结
分子结构修饰与分子的性质
科学 · 技术 · 社会
图2-23 布洛芬的成酯修饰
图2-22 三氯蔗糖
2.有机合成的任务
目标化合物分子 骨架的构建 和 官能团的转化。
①官能团的引入:C=C 、 卤素原子、-OH 等
②官能团的消除和衍变
碳链的增长或缩短、 成环或开环等
二、有机合成的方法
正合成法(正向思维)
逆合成法(逆向思维)
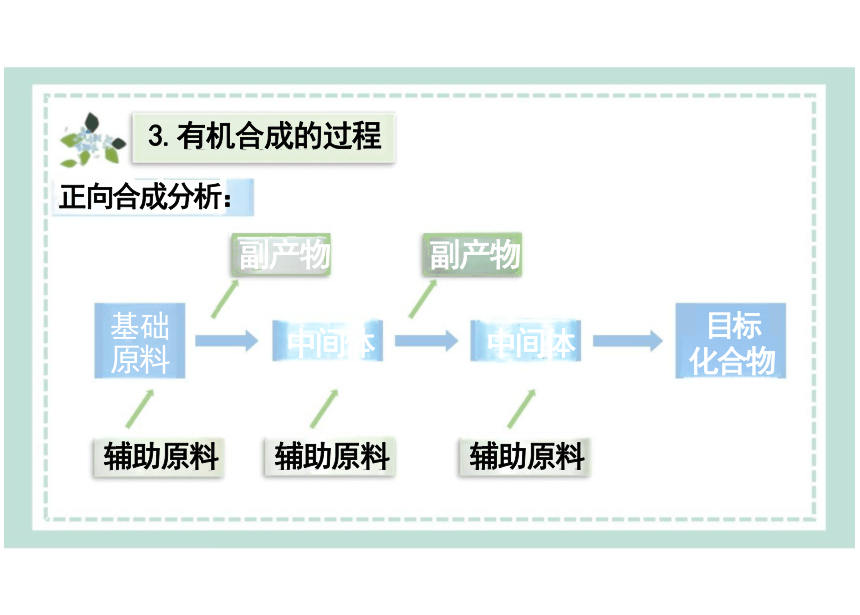
3.有机合成的过程
正向合成分析:
副产物 副产物
中间体 中间体
辅助原料 辅助原料 辅助原料
原料
基础
目标 化合物
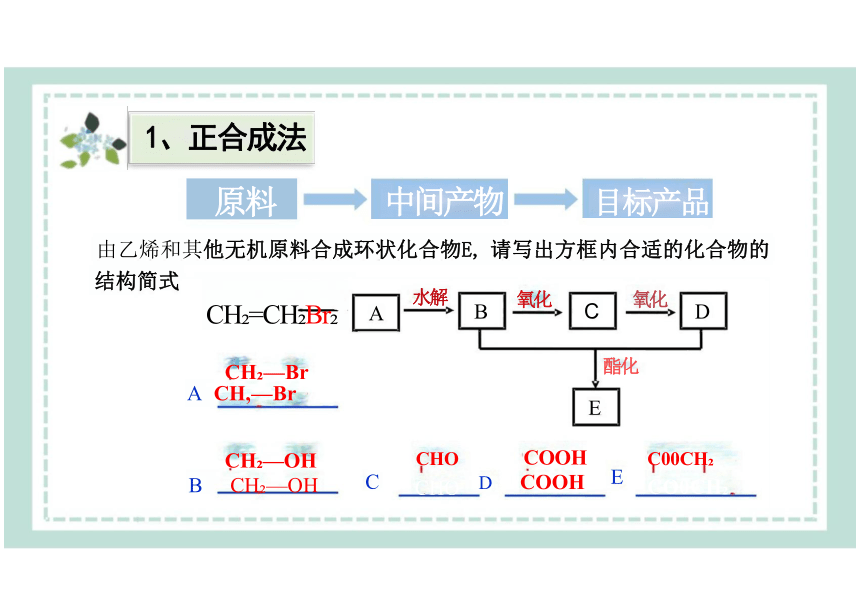
1、正合成法
由乙烯和其他无机原料合成环状化合物E, 请写出方框内合适的化合物的
结构简式
CH =CH Br
中间产物
目标产品
CH —OH
B CH —OH
CH —Br A CH,—Br
原料
COOH
D COOH
C00CH
CO0CH
酯化
E
CHO
CHO
水解
氧化
氧化
C
A
D
C
B
E
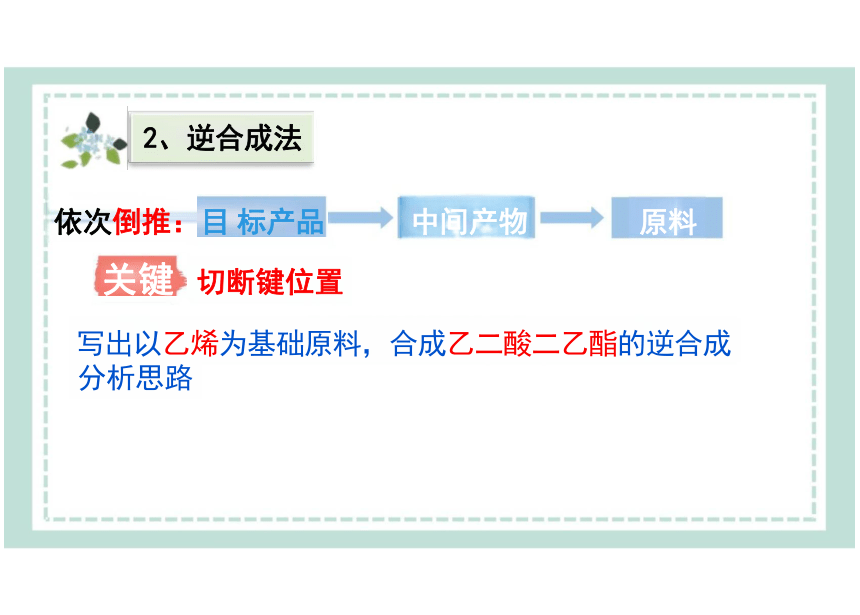
依次倒推:目 标产品 中间产物 原料
关键 切断键位置
写出以乙烯为基础原料,合成乙二酸二乙酯的逆合成 分析思路
2、逆合成法
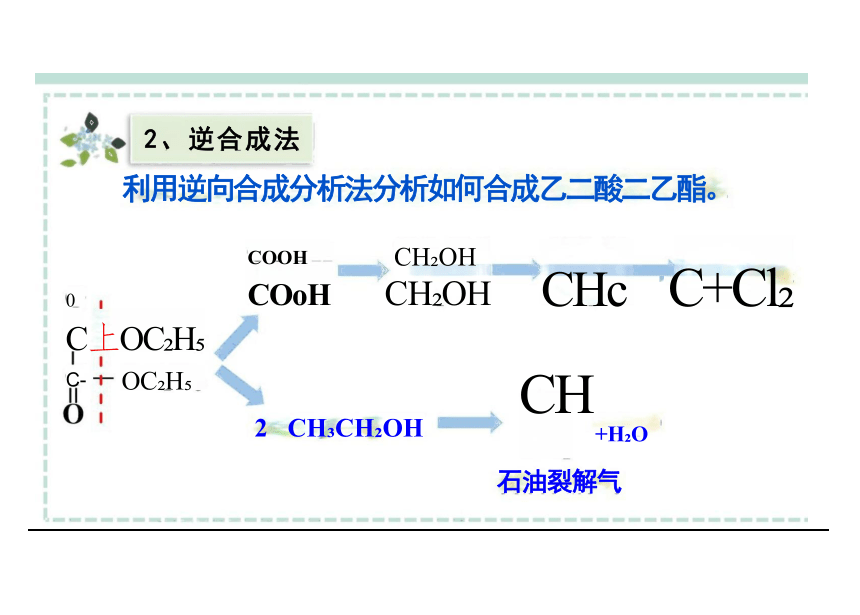
2、逆合成法
利用逆向合成分析法分析如何合成乙二酸二乙酯。
CH
+H O
石油裂解气
COOH CH OH
COoH CH OH
0
C上OC H
C- OC H
CHc C+Cl
2 CH CH OH
c00cH0H na一
酯化反应
+H O CH
2 CH CH OH 催化剂,△CH
石油裂解气
2、逆合成法
利用逆向合成分析法分析如何合成乙二酸二乙酯。
OC,H
_
c-OC H
0
【练习】
写出以乙烯为基础原料,合成乙二酸乙二酯的逆合成 分析思路
COOH CHO CH OH
I
C0OH CHO CH OH
CH OH CH Cl
CH OH CH CI
CH Cl
CH Cl
CH
COOCH
COOCH
四、有机合成解题方法
判断合成的有机物的类别
带有哪些官能团
逆推原料分子
官能团的:引入、转换、
衍变、保护方法
不同路线中,优选最佳路线
最佳合成路线,需考虑:
1、合成路线是否符合化学原理
2、合成操作是否安全可靠等
3、是否符合绿色化学的思想
1.写出合成 的逆合成分析思路并写出各步反应方程式:
有机物原料库
苯、甲苯、乙烯、
丙烯、乙炔、2一丁烯
官能团的转化
1)引入碳碳双键 —C=C—
NaOH/ 乙 醇
H X
浓硫酸
H OH
③炔烃不完全加成 -C=C- H /催化剂 H-C=C-H
①卤代烃消去
②醇消去
③ 烷烃/苯/苯的同系物 卤代
① 不饱和烃与HX 或X 加成
(特定情况下)甲苯产、 , 上引入卤原子
基
用
甲
常
子的
不
丙烯等分
物有多种
②醇与HX取代
官能团的转化
2 ) 引 入卤素原子:
X
光照
-H
FeX
官能团的转化
3)引入羟基-OH :
① 烯烃与H O加成 CH =CH +H O 压CH CH OH
加热加
催化剂
稀H SO
④酯水解 CH COOC H +H O△CH COOH+C H OH
水
C H BI +NaOH- △→ C H OH+NaBr
催化剂
△ →CH CH OH
③ 醛/酮 与 H 加 成 CH CHO+H
②卤代烃水解
4.引入碳氧双键(醛基,酮羰基)
2CH CH OH+O CuA2CH CHO+2H O
OH
2CH CHCH +o UAs 2CH CH +2H O
②某些烯烃被氧化
2CH =CH +O 一定条件 2CH CHO
官能团的转化
①醇的催化氧化
①O
②Zn/H O
OHCCH CH CH CH CHO
④某些卤代烃的水解反应
CH CHBrz+H O 催化剂
CH CHO
同一碳原子上联有 两个羟基会脱去一 分子水转化为醛基
③炔烃水化(加成反应)
催化剂
△
CH=CH+H O
CH CHO
①醛的氧化
CH CHO+2Ag(NH ) OH△H O+2AgJ+3NH +CH COONH
官能团的转化
5.引入羧基
+3H O
②某些烯烃、炔烃、芳香烃、醇等
被酸性高锰酸钾溶液氧化的反应
KMnO H+
R—CH OH
R— COOH
稀 硫 酸
CH CO0 C H +H O CH COOH +C H OH
△
(3)酯、酰胺、R—CN的水解(取代反应)
CH CH CNH O,H CH CH COOH
6、酯基的引入方法
①酯化反应 浓硫酸
CH COOH+C H OH= △ CH CO0C H +H O
②酰氯醇解
1.增长碳链(常考)
炔(烯)烃和醛(酮)中的不饱和键与HCN发生加成反应生成含有氰基(—CN)
①炔(烯)烃与HCN的加成反应
CH=CH催化剂 CH ==CHCNHO,H CH = OOH
酸
C
烯
H
丙
C
二、有机合成中碳骨架的构建
丙腈
将羧基、氨基等引入碳链的,产物较原料分子增加了 一个碳原子。
②醛 ( 或 酮 ) 与HCN的加成反应
羟基腈 氨基醇
1、碳 链 的增 长
二、有机合成中碳骨架的构建
② 羟醛缩合反应(极度常考)
+H O
(3)由卤代烃增长碳链
①2R—X+2Na →R—R+2NaX
②CH CH Cl+NaCN→CH CH CN+NaCl
③2CH C=CH+Na 液氮2CH C=CNa+H ^
CH C=CNa+CH CH Cl→CH C=CCH CH +NaCl
常见信息题会出现的
⑤由格氏试剂与卤代烃、醛、酮反应增长碳链
R'—Cl+RMgCl —R'—R +MgCl
练习
卤代烃与金属镁在无水乙醚中反应,可得格林试剂R—MgX, 它可与醛、酮等羰基化合物加成:
所得产物经水解可以得到醇,这是某些复杂醇的合成方法之 一。现欲 合成(CH ) C—OH, 下列所选用的卤代烃和羰基化合物的组合正确
的是( D )
A.乙 醛 和 氯 乙 烷 B. 甲醛和1 - 溴丙烷
C. 甲醛和2 - 溴丙烷 D. 丙酮和 一 氯甲烷
你知道哪些缩短碳链的方法
(1)烷烃的分解反应(烃的裂化、裂解)
(2)酯的水解反应(油脂的水解、蛋白质水解、多糖水解)
2、碳链的缩短
2.缩短碳链
(3)烯烃的氧化反应(常考)
KMnO4 氧化反应
RCH=CH KMnO /H+ RCOOH+CO,
二、有机合成中碳骨架的构建
烯烃
2、碳链的缩短
(4)炔烃及芳香烃的侧链被KMnO (H+)溶液氧化。
与苯环相连的碳原子上至少连有一个氢原子才能被酸性KMnO 氧化。
一 氢成气、无氢成酸
芳香烃:
3.成环反应
①烯烃炔烃成环
二、有机合成中碳骨架的构建
3CH=CH
十
所用的原料可以是( A )
①1,3-丁二烯和2-丁炔
②1,3-戊二烯和2-丁炔
③2,3-二甲基-1,3-丁二烯和乙炔
④2,4 - 己二烯和乙炔
A.①③ B.②③ C.②④ D.①④
练习
已知:
如果通过一步反应合成
十
二、有机合成中碳骨架的构建
3. 成环反应
②形成环酯
CH = CH 浓H SO CH CH +H O
OH OH
0
3CH =0
0 0
3、碳链的成 环
③形成环醚
o
3、碳链的成环
④形成环酸酐
练习
已知卤代烃可以和钠发生反应。例如溴乙烷与钠发生反应为2CH CH B r +2Na—→CH CH CH CH +2NaBr 应用这 一 反应,下列所给出的化合
物中可以与钠反应合成环丁烷 CH —CH 的是( Q
CH —CH
B.CH CH CH CH Br
D.CH CHBrCH CH Br
A.CH Br
C.CH BrCH Br
4.开环反应
①环酯的水解反应
二、有机合成中碳骨架的构建
②环烯烃的氧化开环
(2)环烯烃氧化开环 KMnOa HO0C
4
H+ HO0C
000 OHCCH CH CH CH CHO
coocH,+2H o 酸 coon+CH oOH
4、碳链的开环
(1)环酯水解开环
化合物丙是合成一种医药的中间体,可以通过如图反应制得。下列说法正
确的是 ( C )
A. 乙的分子式为C H 0O
B. 甲的一氯代物有4种(不考虑立体异构)
C. 乙可以发生取代反应、加成反应
D. 丙不能使酸性高锰酸钾溶液褪色
练习
已知:
由乙醇合成CH CH==CHCH (2-丁烯)的流程如下:
下列说法错误的是( D )
A.③发生氧化反应,⑥发生消去反应
B.M的结构简式为CH CH X
C.P的分子式为C H 00
D.2-丁烯与Br 以1:1加成可得三种不同产物
1.下列有机合成中①②步骤的目的是什么 提示①保护酚羟基不被氧化
② 引入羧基。
2.有机合成的设计流程中有如下环节,其目的是什么 提示保护羰基不被反应。
H
H+
COOH
三 、有机合成中官能团的保护
1. 酚羟基的保护
1、酚 羟 基的 保 护
因酚羟基易被氧化,故在加入氧化剂之前将-OH先转化为-ONa(或-OCH ), 待其他基氧化后,再酸化使其转化为-OH, 其过程表示为
胺基易被O 、O 、H O 等氧化, 一般采用下列方法保护
用甲苯制备对氨基苯甲酸,先氧化甲基后还原为氨基
2、氨基(-NH ) 的保护
三 、 官 能 团 的 保 护
2. 氨基的保护
胺基易被O 、O 、H O 等氧化, 一般采用下列方法保护
用甲苯制备对氨基苯甲酸,先氧化甲基后还原为氨基
三、有机合成中官能团的保护
碳碳双键也容易被氧化,在氧化其他基团前,可以利用其与HCl等的加 成反应将其保护起来,待氧化后再利用消去反应将其转变为碳碳双键。
NaOH,△CH =CHCOOH
三 、有机合成中官能团的保护
3. 碳碳双键的保护
醛基可被弱氧化剂氧化,为避免在反应过程中受到影响,保护一般是把 醛基制成缩醛,最后再将缩醛水解得到醛基(常用乙二醇)
缩醛
也可以先生成醇,然后再氧化恢复
四、官能团的保护04--醛基的保护
4、醛基的保护
H O -CHO
H
第三章 烃的衍生物
第五节 有机合成
利用简单、易得的原料,通过有机反应,生成具有
有机合成反应的常见装置
一、有机合成的过程
特定结构和功能的有机化合物。
恒压分液漏斗
三颈烧瓶
冷凝管
1.有机合成遵循的原则
1)原料选择
廉价、易得、低毒、低污染
通常采用4个碳以下的单官能团化合物或单取代苯。
尽量选择步骤最少__ 的合成路线
尽量选择与目标化合物 结构相似 的原料 步骤越少,最后 产率 越高。
2)合成路线
1.有机合成遵循的原则
最大限度的利用原料分子的每个原子,达到 零排放。
尊重客观事实,按一定反应顺序和规律引入 官 能 团。
操作简单、条件温和、能耗低、易实现
4)合成优势
5)尊重事实
3)绿色化学
有机合成的意义
①制备天然有机物,弥补自然资源的不足;
②对天然有机物进行局部的结构改造和修饰,使其性能更加完美;
③合成具有特定性质的、自然界并不存在的有机物, 以满足人类的特殊需要
制 各 的 维 生 责C 阿司匹林缓释片 隐形眼镜材料
三氯蔗糖
者食用,被认为是近乎完美的甜味剂。
分子结构修饰在药物设计与合成中有广 泛的应用。为提高药物的治疗效果,降低毒 副作用等,可将药物分子的结构进行修饰。 例如,布洛芬具有抗炎、镇痛、解热作用, 但口服该药对胃、肠道有刺激性,可以对该 分子进行如图2-23所示的成酯修饰。
图12-21 蔗糖和三氯蔗糖结构式
三氯蔗糖(如图2-22),又名蔗糖素, 其甜度是蔗糖的600倍,没有异味,具有热 量值极低、安全性好等优点,可供糖尿病患
构被修饰后,分子的性质发生了改变。例如, 用三个氯原子取代蔗糖分子(如图2-21)中 的三个羟基,就得到三 氯蔗糖(如图2-21)。
分子结构修饰是指不改变分子的主体骨 架,保持分子的基本结构不变,仅改变分子 结构中的某些基团而得到的新分子。分子结
分子结构修饰与分子的性质
科学 · 技术 · 社会
图2-23 布洛芬的成酯修饰
图2-22 三氯蔗糖
2.有机合成的任务
目标化合物分子 骨架的构建 和 官能团的转化。
①官能团的引入:C=C 、 卤素原子、-OH 等
②官能团的消除和衍变
碳链的增长或缩短、 成环或开环等
二、有机合成的方法
正合成法(正向思维)
逆合成法(逆向思维)
3.有机合成的过程
正向合成分析:
副产物 副产物
中间体 中间体
辅助原料 辅助原料 辅助原料
原料
基础
目标 化合物
1、正合成法
由乙烯和其他无机原料合成环状化合物E, 请写出方框内合适的化合物的
结构简式
CH =CH Br
中间产物
目标产品
CH —OH
B CH —OH
CH —Br A CH,—Br
原料
COOH
D COOH
C00CH
CO0CH
酯化
E
CHO
CHO
水解
氧化
氧化
C
A
D
C
B
E
依次倒推:目 标产品 中间产物 原料
关键 切断键位置
写出以乙烯为基础原料,合成乙二酸二乙酯的逆合成 分析思路
2、逆合成法
2、逆合成法
利用逆向合成分析法分析如何合成乙二酸二乙酯。
CH
+H O
石油裂解气
COOH CH OH
COoH CH OH
0
C上OC H
C- OC H
CHc C+Cl
2 CH CH OH
c00cH0H na一
酯化反应
+H O CH
2 CH CH OH 催化剂,△CH
石油裂解气
2、逆合成法
利用逆向合成分析法分析如何合成乙二酸二乙酯。
OC,H
_
c-OC H
0
【练习】
写出以乙烯为基础原料,合成乙二酸乙二酯的逆合成 分析思路
COOH CHO CH OH
I
C0OH CHO CH OH
CH OH CH Cl
CH OH CH CI
CH Cl
CH Cl
CH
COOCH
COOCH
四、有机合成解题方法
判断合成的有机物的类别
带有哪些官能团
逆推原料分子
官能团的:引入、转换、
衍变、保护方法
不同路线中,优选最佳路线
最佳合成路线,需考虑:
1、合成路线是否符合化学原理
2、合成操作是否安全可靠等
3、是否符合绿色化学的思想
1.写出合成 的逆合成分析思路并写出各步反应方程式:
有机物原料库
苯、甲苯、乙烯、
丙烯、乙炔、2一丁烯
官能团的转化
1)引入碳碳双键 —C=C—
NaOH/ 乙 醇
H X
浓硫酸
H OH
③炔烃不完全加成 -C=C- H /催化剂 H-C=C-H
①卤代烃消去
②醇消去
③ 烷烃/苯/苯的同系物 卤代
① 不饱和烃与HX 或X 加成
(特定情况下)甲苯产、 , 上引入卤原子
基
用
甲
常
子的
不
丙烯等分
物有多种
②醇与HX取代
官能团的转化
2 ) 引 入卤素原子:
X
光照
-H
FeX
官能团的转化
3)引入羟基-OH :
① 烯烃与H O加成 CH =CH +H O 压CH CH OH
加热加
催化剂
稀H SO
④酯水解 CH COOC H +H O△CH COOH+C H OH
水
C H BI +NaOH- △→ C H OH+NaBr
催化剂
△ →CH CH OH
③ 醛/酮 与 H 加 成 CH CHO+H
②卤代烃水解
4.引入碳氧双键(醛基,酮羰基)
2CH CH OH+O CuA2CH CHO+2H O
OH
2CH CHCH +o UAs 2CH CH +2H O
②某些烯烃被氧化
2CH =CH +O 一定条件 2CH CHO
官能团的转化
①醇的催化氧化
①O
②Zn/H O
OHCCH CH CH CH CHO
④某些卤代烃的水解反应
CH CHBrz+H O 催化剂
CH CHO
同一碳原子上联有 两个羟基会脱去一 分子水转化为醛基
③炔烃水化(加成反应)
催化剂
△
CH=CH+H O
CH CHO
①醛的氧化
CH CHO+2Ag(NH ) OH△H O+2AgJ+3NH +CH COONH
官能团的转化
5.引入羧基
+3H O
②某些烯烃、炔烃、芳香烃、醇等
被酸性高锰酸钾溶液氧化的反应
KMnO H+
R—CH OH
R— COOH
稀 硫 酸
CH CO0 C H +H O CH COOH +C H OH
△
(3)酯、酰胺、R—CN的水解(取代反应)
CH CH CNH O,H CH CH COOH
6、酯基的引入方法
①酯化反应 浓硫酸
CH COOH+C H OH= △ CH CO0C H +H O
②酰氯醇解
1.增长碳链(常考)
炔(烯)烃和醛(酮)中的不饱和键与HCN发生加成反应生成含有氰基(—CN)
①炔(烯)烃与HCN的加成反应
CH=CH催化剂 CH ==CHCNHO,H CH = OOH
酸
C
烯
H
丙
C
二、有机合成中碳骨架的构建
丙腈
将羧基、氨基等引入碳链的,产物较原料分子增加了 一个碳原子。
②醛 ( 或 酮 ) 与HCN的加成反应
羟基腈 氨基醇
1、碳 链 的增 长
二、有机合成中碳骨架的构建
② 羟醛缩合反应(极度常考)
+H O
(3)由卤代烃增长碳链
①2R—X+2Na →R—R+2NaX
②CH CH Cl+NaCN→CH CH CN+NaCl
③2CH C=CH+Na 液氮2CH C=CNa+H ^
CH C=CNa+CH CH Cl→CH C=CCH CH +NaCl
常见信息题会出现的
⑤由格氏试剂与卤代烃、醛、酮反应增长碳链
R'—Cl+RMgCl —R'—R +MgCl
练习
卤代烃与金属镁在无水乙醚中反应,可得格林试剂R—MgX, 它可与醛、酮等羰基化合物加成:
所得产物经水解可以得到醇,这是某些复杂醇的合成方法之 一。现欲 合成(CH ) C—OH, 下列所选用的卤代烃和羰基化合物的组合正确
的是( D )
A.乙 醛 和 氯 乙 烷 B. 甲醛和1 - 溴丙烷
C. 甲醛和2 - 溴丙烷 D. 丙酮和 一 氯甲烷
你知道哪些缩短碳链的方法
(1)烷烃的分解反应(烃的裂化、裂解)
(2)酯的水解反应(油脂的水解、蛋白质水解、多糖水解)
2、碳链的缩短
2.缩短碳链
(3)烯烃的氧化反应(常考)
KMnO4 氧化反应
RCH=CH KMnO /H+ RCOOH+CO,
二、有机合成中碳骨架的构建
烯烃
2、碳链的缩短
(4)炔烃及芳香烃的侧链被KMnO (H+)溶液氧化。
与苯环相连的碳原子上至少连有一个氢原子才能被酸性KMnO 氧化。
一 氢成气、无氢成酸
芳香烃:
3.成环反应
①烯烃炔烃成环
二、有机合成中碳骨架的构建
3CH=CH
十
所用的原料可以是( A )
①1,3-丁二烯和2-丁炔
②1,3-戊二烯和2-丁炔
③2,3-二甲基-1,3-丁二烯和乙炔
④2,4 - 己二烯和乙炔
A.①③ B.②③ C.②④ D.①④
练习
已知:
如果通过一步反应合成
十
二、有机合成中碳骨架的构建
3. 成环反应
②形成环酯
CH = CH 浓H SO CH CH +H O
OH OH
0
3CH =0
0 0
3、碳链的成 环
③形成环醚
o
3、碳链的成环
④形成环酸酐
练习
已知卤代烃可以和钠发生反应。例如溴乙烷与钠发生反应为2CH CH B r +2Na—→CH CH CH CH +2NaBr 应用这 一 反应,下列所给出的化合
物中可以与钠反应合成环丁烷 CH —CH 的是( Q
CH —CH
B.CH CH CH CH Br
D.CH CHBrCH CH Br
A.CH Br
C.CH BrCH Br
4.开环反应
①环酯的水解反应
二、有机合成中碳骨架的构建
②环烯烃的氧化开环
(2)环烯烃氧化开环 KMnOa HO0C
4
H+ HO0C
000 OHCCH CH CH CH CHO
coocH,+2H o 酸 coon+CH oOH
4、碳链的开环
(1)环酯水解开环
化合物丙是合成一种医药的中间体,可以通过如图反应制得。下列说法正
确的是 ( C )
A. 乙的分子式为C H 0O
B. 甲的一氯代物有4种(不考虑立体异构)
C. 乙可以发生取代反应、加成反应
D. 丙不能使酸性高锰酸钾溶液褪色
练习
已知:
由乙醇合成CH CH==CHCH (2-丁烯)的流程如下:
下列说法错误的是( D )
A.③发生氧化反应,⑥发生消去反应
B.M的结构简式为CH CH X
C.P的分子式为C H 00
D.2-丁烯与Br 以1:1加成可得三种不同产物
1.下列有机合成中①②步骤的目的是什么 提示①保护酚羟基不被氧化
② 引入羧基。
2.有机合成的设计流程中有如下环节,其目的是什么 提示保护羰基不被反应。
H
H+
COOH
三 、有机合成中官能团的保护
1. 酚羟基的保护
1、酚 羟 基的 保 护
因酚羟基易被氧化,故在加入氧化剂之前将-OH先转化为-ONa(或-OCH ), 待其他基氧化后,再酸化使其转化为-OH, 其过程表示为
胺基易被O 、O 、H O 等氧化, 一般采用下列方法保护
用甲苯制备对氨基苯甲酸,先氧化甲基后还原为氨基
2、氨基(-NH ) 的保护
三 、 官 能 团 的 保 护
2. 氨基的保护
胺基易被O 、O 、H O 等氧化, 一般采用下列方法保护
用甲苯制备对氨基苯甲酸,先氧化甲基后还原为氨基
三、有机合成中官能团的保护
碳碳双键也容易被氧化,在氧化其他基团前,可以利用其与HCl等的加 成反应将其保护起来,待氧化后再利用消去反应将其转变为碳碳双键。
NaOH,△CH =CHCOOH
三 、有机合成中官能团的保护
3. 碳碳双键的保护
醛基可被弱氧化剂氧化,为避免在反应过程中受到影响,保护一般是把 醛基制成缩醛,最后再将缩醛水解得到醛基(常用乙二醇)
缩醛
也可以先生成醇,然后再氧化恢复
四、官能团的保护04--醛基的保护
4、醛基的保护
H O -CHO
H
