糖类高一下学期化学人教版(2019)必修二(共30张PPT)
文档属性
| 名称 | 糖类高一下学期化学人教版(2019)必修二(共30张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-11 00:00:00 | ||
图片预览










文档简介
(共30张PPT)
7.4基本营养物质
营养物质主要包括:
糖类、蛋白质、油脂、维生素、无机盐、水
L
有机物 无机物
基本营养物质
化学 ·必修第二册
生命活动需要一系列复杂的化学过程来 维持,食物中的营养物质是这些过程的物质 和能量基础。
第一课时
糖类
教学目标与重难点
·教学目标:
·掌握糖的分类、性质和用途
·教学重点:
·葡萄糖的化学性质
·教学难点:
·还原糖鉴定与多糖水解的实验操作要点
化学 ·必修第二册
化学 ·必修第二册
学习任务一
糖类物质及其分类
· 白砂糖、糖果、葡萄糖注射液......生活中随处可见含糖的商品。 然而,“糖”的内涵到底是什么
糖类
化学 ·必修第二册
·糖是一类由C 、H 、O元素组成的有机物,因大部分糖类物质的分
子式可写为C (H O)m表示,糖也被称为碳水化合物。
一葡萄糖( C H O )
蔗糖 (C H O )→
果糖 (C H 2O )
麦芽糖(C H O ) →
糖类
化学 ·必修第二册
概念辨析:
1. 糖类不一定符合通式C,(H O)m, 如鼠李糖的分子式为C H O ,
脱氧核糖的分子式为C H O ; 符合通式C,(H O)m的也不一定是 糖类,如乙酸分子式C H O 可写为C (H O)
2.人食用糖类时不一定产生甜味感觉,如淀粉、纤维素;产生甜 味感觉的物质也不一定是糖,如糖精(C H NO S)
糖类
化学 ·必修第二册
类别 特点 代表物 代表物的分子式
代表物在自然界的存在
单糖 不能水解为更 简单的糖分子 葡萄糖 果糖 C H 2O
葡萄糖和果糖:水果、蜂蜜
二糖 水解后生成两 分子单糖 蔗糖 麦芽糖 乳糖 C H O
蔗糖:甘蔗、甜菜 乳糖:哺乳动物的乳汁
多糖 水解后能生成 多分子单糖 淀粉 纤维素 (C H O )n
淀粉:植物的种子或块根 纤维素:植物的茎、叶
·根据能否水解及水解后的产物,糖类可分为单糖、二糖、多糖。
糖类
化学 ·必修第二册
化学 ·必修第二册
糖类
· 淀粉与纤维素是高分子有机物,其分子式内的n值会随着分子大 小而变化。由于自然产生的淀粉和纤维素是大量n值不同的分子 混合在一起构成的,因此淀粉、纤维素属于混 合 物,二者也不 能 称为同分异构体。
CoS56
(C HOs504
CgH9Jas8
C H o5649
(CHHOsgG5
Cgho0s783
化学 ·必修第二册
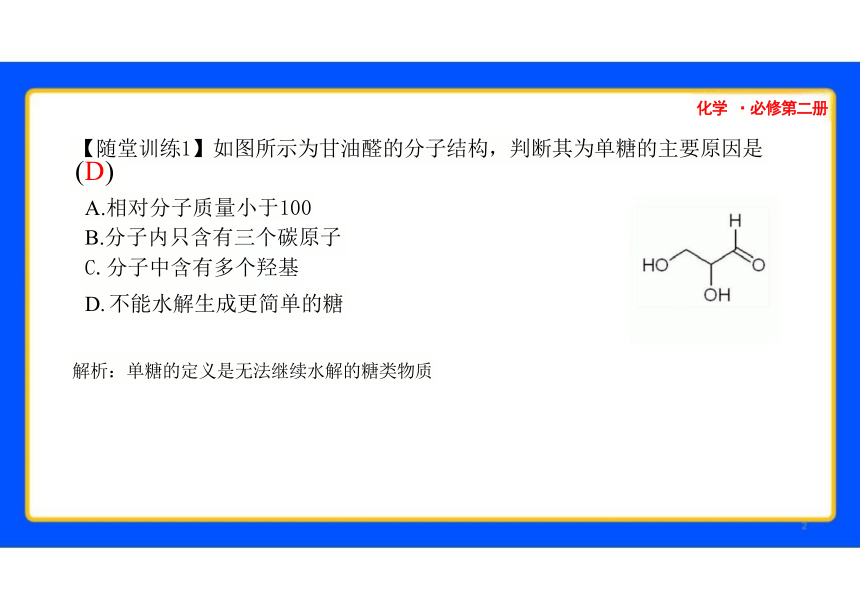
【随堂训练1】如图所示为甘油醛的分子结构,判断其为单糖的主要原因是 (D)
A.相对分子质量小于100
B.分子内只含有三个碳原子
C.分子中含有多个羟基
D. 不能水解生成更简单的糖
解析:单糖的定义是无法继续水解的糖类物质
化学 ·必修第二册
学习任务二
单糖的性质
·葡萄糖是一种有甜味的无色晶体,能溶于水,分子式为C H O , 分子结构如下图所示。它是植物光合作用的主要产物之一,也是 生物体内的主要供能物质。
能团 醛基
CH —CH-CH-CH-CH-C- 耳
(OH) OH) ( 0H)(OH ) OH)
羟基
葡萄糖
葡萄糖含 有哪些官
化学 ·必修第二册
· 由于葡萄糖中含有羟基,我们可以推测葡萄糖的化学性质包括:
氧化反应
-OH
酯化反应 置换反应
葡萄糖
化学 ·必修第二册
·葡萄糖内含有的醛基可以发生哪些化学反应 -CHO 1.加成反应/还原反应
醛类物质可以和氢气发生加成反应,以乙醛为例:
与醇生成醛的反应命名为氧化反应类似,可将醛到醇的反应 命名为还原反应
葡萄糖
化学 ·必修第二册
2. 氧化反应
醛类物质具有很强的还原性,氧气、酸性高锰酸钾溶液、酸 性重铬酸钾溶液等强氧化剂均将其氧化为羧酸。
此外,氧化性较弱的物质也可与醛类物质发生反应,如氢 氧 化铜悬浊液和银氨溶液,其中前者可以与醛反应生成砖红色的氧化 亚铜沉淀,后者则生成银单质。这两个反应可以用来鉴定醛基的存 在,而葡萄糖内含醛基,故也可作为葡萄糖的鉴定方法。
葡萄糖
化学 ·必修第二册
【实验1】在试管中加入2mL10%NaOH 溶液,滴加5滴5%CuSO 溶 液,得到新制的Cu(OH)2。再加入2 mL 10%葡萄糖溶液,加热,观 察现象。
葡萄糖的鉴定实验
5滴
5%CuSO 溶液
2mL
10%葡 萄糖
10%NaOH 溶液
化学 ·必修第二册
·本实验的注意事项如下:
1. 氢氧化铜的稳定性较差,长期放置的过程中会分解生成黑色的 氧化铜,故氢氧化铜悬浊液需要现配现用
2.该反应需要在碱性条件下发生,且黑色的氧化铜沉淀会影响砖 红色氧化亚铜沉淀的观察,因此需要将少量的硫酸铜溶液滴入 过量的氢氧化钠溶液中,防止产生太多的氢氧化铜干扰实验
葡萄糖的鉴定实验
化学 ·必修第二册
【实验2】在洁净的试管中加入1mL2%AgNO 溶液,然后一边振荡 试管,一边逐滴加入2%稀氨水,直到最初产生的沉淀恰好溶解为 止,得到银氨溶液。再加入1mL10% 葡萄糖溶液,振荡,然后放在 水浴中加热,观察现象。
葡萄糖的鉴定实验
1 mL2%
AgNO
溶液
I mL
10%葡 萄糖
澄清溶液 热水
化学 ·必修第二册
2%稀氨水
·本实验的注意事项如下:
1.配制银氨溶液时,必须将稀氨水逐渐滴入硝酸银溶液中,直到 产生的沉淀完全溶解,且需现配现用
2.为保证生成光亮的银镜镀层,试管的内壁必须保持洁净,且采 用水浴加热方式,明火加热或加热过程中振荡试管均可能对实 验结果造成负面影响
葡萄糖的鉴定实验
化学 ·必修第二册
化学 ·必修第二册
【随堂训练2】下列试剂中,不与葡萄糖反应的是( A )
A.氢氧化钠溶液
B.氢氧化铜悬浊液
C.银氨溶液
D. 酸性高锰酸钾溶液
解析:葡萄糖内含有羟基与醛基,但二者均不与氢氧化钠溶液反应
果糖
·果糖是葡萄糖的同分异构体,其官能团为 羟基与酮羰基。酮羰基也可以与氢气发生 加成/还原反应,但是不能发生氧化反应。
·果糖在碱性条件下,分子内部的酮羰基和 羟基会自发重整为醛基,因此也可以与氢 氧化铜悬浊液、银氨溶液发生相应的特征 反应,体现出还原性。
化学 ·必修第二册
酮羰基
化学 ·必修第二册
学习任务三
二糖与多糖的化学性质
· 实验表明,淀粉遇到碘液会变蓝,这一性质除检验淀粉的存在外, 还可以用于氧化性物质的检验,如湿润的淀粉-碘化钾试纸遇到氯 气便会变为蓝色。
淀粉的鉴定
2I-+Cl =2Cl-+I
化学 ·必修第二册
·蔗糖、麦芽糖、淀粉、纤维素在催化剂(一般用稀硫酸)、水浴 加热条件下,可以水解为单糖,其中蔗糖水解后得到葡萄糖和果 糖,麦芽糖、淀粉、纤维素彻底水解后只得到葡萄糖。
C H O +H O 催化剂C H O +C H O
蔗糖 葡萄糖 果糖
(C H O )n+nH O 催化剂 nC H O
淀粉(或纤维素) 葡萄糖
二糖与多糖的水解
化学 ·必修第二册
·思考与讨论:
(1)某学生设计了如下实验方案用以判断淀粉的水解效果,他得 到的结论是“淀粉没有水解”,该结论是否正确
二糖与多糖的水解
新制的
Cu(OH)
加热至沸腾
加热
液
解
水
无砖红色
沉淀产生
化学 ·必修第二册
稀硫酸、
淀粉液
·思考与讨论:
(2)他再次用改进后的实验方案(如下)得到结论“淀粉已完全 水解”,该结论是否正确
二糖与多糖的水解
新制的
Cu(OH)
加热至沸腾
过量NaOH 溶液
至碱性
稀硫酸、 加热
砖红色 沉淀
化学 ·必修第二册
溶液不变蓝
水解液
淀粉液
混合液
碘水
·淀粉在被人体摄入后,会在消化系统中由酶催化水解,依次生成 糊精、麦芽糖,最后水解为葡萄糖,在吸收后通过呼吸作用(氧 化反应)为人体提供能量。然而人体内没有可以水解纤维素的酶, 故纤维素无法为人体提供能量,但纤维素能刺激肠道蠕动,促进 消化和排泄,因此推荐每日摄取一定量的瓜果蔬菜与粗粮。
二糖与多糖的水解
化学 ·必修第二册
·此外,微生物发酵也是一种有效的糖类利用方式,如以淀粉为原 料酿酒,纤维素为原料生产乙醇燃料等。
C H O 酶 2C H OH+2CO 个
二糖与多糖的水解
化学 ·必修第二册
课时小结
C、H、O 组成元素
纤维素
淀粉 多糖
水解程度的实验
化学 ·必修第二册
无色晶体能溶于水
结构 CH —(CHOH) —CHO
葡萄糖 简式 OH
C H O
具有醇的 OH 性质
CHO 具有还原性
水解生成葡萄糖和果糖
水解生成葡萄糖
分子式
果糖
官能团
蔗糖
二糖
麦芽糖
单糖
糖类
7.4基本营养物质
营养物质主要包括:
糖类、蛋白质、油脂、维生素、无机盐、水
L
有机物 无机物
基本营养物质
化学 ·必修第二册
生命活动需要一系列复杂的化学过程来 维持,食物中的营养物质是这些过程的物质 和能量基础。
第一课时
糖类
教学目标与重难点
·教学目标:
·掌握糖的分类、性质和用途
·教学重点:
·葡萄糖的化学性质
·教学难点:
·还原糖鉴定与多糖水解的实验操作要点
化学 ·必修第二册
化学 ·必修第二册
学习任务一
糖类物质及其分类
· 白砂糖、糖果、葡萄糖注射液......生活中随处可见含糖的商品。 然而,“糖”的内涵到底是什么
糖类
化学 ·必修第二册
·糖是一类由C 、H 、O元素组成的有机物,因大部分糖类物质的分
子式可写为C (H O)m表示,糖也被称为碳水化合物。
一葡萄糖( C H O )
蔗糖 (C H O )→
果糖 (C H 2O )
麦芽糖(C H O ) →
糖类
化学 ·必修第二册
概念辨析:
1. 糖类不一定符合通式C,(H O)m, 如鼠李糖的分子式为C H O ,
脱氧核糖的分子式为C H O ; 符合通式C,(H O)m的也不一定是 糖类,如乙酸分子式C H O 可写为C (H O)
2.人食用糖类时不一定产生甜味感觉,如淀粉、纤维素;产生甜 味感觉的物质也不一定是糖,如糖精(C H NO S)
糖类
化学 ·必修第二册
类别 特点 代表物 代表物的分子式
代表物在自然界的存在
单糖 不能水解为更 简单的糖分子 葡萄糖 果糖 C H 2O
葡萄糖和果糖:水果、蜂蜜
二糖 水解后生成两 分子单糖 蔗糖 麦芽糖 乳糖 C H O
蔗糖:甘蔗、甜菜 乳糖:哺乳动物的乳汁
多糖 水解后能生成 多分子单糖 淀粉 纤维素 (C H O )n
淀粉:植物的种子或块根 纤维素:植物的茎、叶
·根据能否水解及水解后的产物,糖类可分为单糖、二糖、多糖。
糖类
化学 ·必修第二册
化学 ·必修第二册
糖类
· 淀粉与纤维素是高分子有机物,其分子式内的n值会随着分子大 小而变化。由于自然产生的淀粉和纤维素是大量n值不同的分子 混合在一起构成的,因此淀粉、纤维素属于混 合 物,二者也不 能 称为同分异构体。
CoS56
(C HOs504
CgH9Jas8
C H o5649
(CHHOsgG5
Cgho0s783
化学 ·必修第二册
【随堂训练1】如图所示为甘油醛的分子结构,判断其为单糖的主要原因是 (D)
A.相对分子质量小于100
B.分子内只含有三个碳原子
C.分子中含有多个羟基
D. 不能水解生成更简单的糖
解析:单糖的定义是无法继续水解的糖类物质
化学 ·必修第二册
学习任务二
单糖的性质
·葡萄糖是一种有甜味的无色晶体,能溶于水,分子式为C H O , 分子结构如下图所示。它是植物光合作用的主要产物之一,也是 生物体内的主要供能物质。
能团 醛基
CH —CH-CH-CH-CH-C- 耳
(OH) OH) ( 0H)(OH ) OH)
羟基
葡萄糖
葡萄糖含 有哪些官
化学 ·必修第二册
· 由于葡萄糖中含有羟基,我们可以推测葡萄糖的化学性质包括:
氧化反应
-OH
酯化反应 置换反应
葡萄糖
化学 ·必修第二册
·葡萄糖内含有的醛基可以发生哪些化学反应 -CHO 1.加成反应/还原反应
醛类物质可以和氢气发生加成反应,以乙醛为例:
与醇生成醛的反应命名为氧化反应类似,可将醛到醇的反应 命名为还原反应
葡萄糖
化学 ·必修第二册
2. 氧化反应
醛类物质具有很强的还原性,氧气、酸性高锰酸钾溶液、酸 性重铬酸钾溶液等强氧化剂均将其氧化为羧酸。
此外,氧化性较弱的物质也可与醛类物质发生反应,如氢 氧 化铜悬浊液和银氨溶液,其中前者可以与醛反应生成砖红色的氧化 亚铜沉淀,后者则生成银单质。这两个反应可以用来鉴定醛基的存 在,而葡萄糖内含醛基,故也可作为葡萄糖的鉴定方法。
葡萄糖
化学 ·必修第二册
【实验1】在试管中加入2mL10%NaOH 溶液,滴加5滴5%CuSO 溶 液,得到新制的Cu(OH)2。再加入2 mL 10%葡萄糖溶液,加热,观 察现象。
葡萄糖的鉴定实验
5滴
5%CuSO 溶液
2mL
10%葡 萄糖
10%NaOH 溶液
化学 ·必修第二册
·本实验的注意事项如下:
1. 氢氧化铜的稳定性较差,长期放置的过程中会分解生成黑色的 氧化铜,故氢氧化铜悬浊液需要现配现用
2.该反应需要在碱性条件下发生,且黑色的氧化铜沉淀会影响砖 红色氧化亚铜沉淀的观察,因此需要将少量的硫酸铜溶液滴入 过量的氢氧化钠溶液中,防止产生太多的氢氧化铜干扰实验
葡萄糖的鉴定实验
化学 ·必修第二册
【实验2】在洁净的试管中加入1mL2%AgNO 溶液,然后一边振荡 试管,一边逐滴加入2%稀氨水,直到最初产生的沉淀恰好溶解为 止,得到银氨溶液。再加入1mL10% 葡萄糖溶液,振荡,然后放在 水浴中加热,观察现象。
葡萄糖的鉴定实验
1 mL2%
AgNO
溶液
I mL
10%葡 萄糖
澄清溶液 热水
化学 ·必修第二册
2%稀氨水
·本实验的注意事项如下:
1.配制银氨溶液时,必须将稀氨水逐渐滴入硝酸银溶液中,直到 产生的沉淀完全溶解,且需现配现用
2.为保证生成光亮的银镜镀层,试管的内壁必须保持洁净,且采 用水浴加热方式,明火加热或加热过程中振荡试管均可能对实 验结果造成负面影响
葡萄糖的鉴定实验
化学 ·必修第二册
化学 ·必修第二册
【随堂训练2】下列试剂中,不与葡萄糖反应的是( A )
A.氢氧化钠溶液
B.氢氧化铜悬浊液
C.银氨溶液
D. 酸性高锰酸钾溶液
解析:葡萄糖内含有羟基与醛基,但二者均不与氢氧化钠溶液反应
果糖
·果糖是葡萄糖的同分异构体,其官能团为 羟基与酮羰基。酮羰基也可以与氢气发生 加成/还原反应,但是不能发生氧化反应。
·果糖在碱性条件下,分子内部的酮羰基和 羟基会自发重整为醛基,因此也可以与氢 氧化铜悬浊液、银氨溶液发生相应的特征 反应,体现出还原性。
化学 ·必修第二册
酮羰基
化学 ·必修第二册
学习任务三
二糖与多糖的化学性质
· 实验表明,淀粉遇到碘液会变蓝,这一性质除检验淀粉的存在外, 还可以用于氧化性物质的检验,如湿润的淀粉-碘化钾试纸遇到氯 气便会变为蓝色。
淀粉的鉴定
2I-+Cl =2Cl-+I
化学 ·必修第二册
·蔗糖、麦芽糖、淀粉、纤维素在催化剂(一般用稀硫酸)、水浴 加热条件下,可以水解为单糖,其中蔗糖水解后得到葡萄糖和果 糖,麦芽糖、淀粉、纤维素彻底水解后只得到葡萄糖。
C H O +H O 催化剂C H O +C H O
蔗糖 葡萄糖 果糖
(C H O )n+nH O 催化剂 nC H O
淀粉(或纤维素) 葡萄糖
二糖与多糖的水解
化学 ·必修第二册
·思考与讨论:
(1)某学生设计了如下实验方案用以判断淀粉的水解效果,他得 到的结论是“淀粉没有水解”,该结论是否正确
二糖与多糖的水解
新制的
Cu(OH)
加热至沸腾
加热
液
解
水
无砖红色
沉淀产生
化学 ·必修第二册
稀硫酸、
淀粉液
·思考与讨论:
(2)他再次用改进后的实验方案(如下)得到结论“淀粉已完全 水解”,该结论是否正确
二糖与多糖的水解
新制的
Cu(OH)
加热至沸腾
过量NaOH 溶液
至碱性
稀硫酸、 加热
砖红色 沉淀
化学 ·必修第二册
溶液不变蓝
水解液
淀粉液
混合液
碘水
·淀粉在被人体摄入后,会在消化系统中由酶催化水解,依次生成 糊精、麦芽糖,最后水解为葡萄糖,在吸收后通过呼吸作用(氧 化反应)为人体提供能量。然而人体内没有可以水解纤维素的酶, 故纤维素无法为人体提供能量,但纤维素能刺激肠道蠕动,促进 消化和排泄,因此推荐每日摄取一定量的瓜果蔬菜与粗粮。
二糖与多糖的水解
化学 ·必修第二册
·此外,微生物发酵也是一种有效的糖类利用方式,如以淀粉为原 料酿酒,纤维素为原料生产乙醇燃料等。
C H O 酶 2C H OH+2CO 个
二糖与多糖的水解
化学 ·必修第二册
课时小结
C、H、O 组成元素
纤维素
淀粉 多糖
水解程度的实验
化学 ·必修第二册
无色晶体能溶于水
结构 CH —(CHOH) —CHO
葡萄糖 简式 OH
C H O
具有醇的 OH 性质
CHO 具有还原性
水解生成葡萄糖和果糖
水解生成葡萄糖
分子式
果糖
官能团
蔗糖
二糖
麦芽糖
单糖
糖类
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
