【高效备课】2024人教新版九上化学--2.3.1 实验室制取氧气的原理 分解反应教学设计
文档属性
| 名称 | 【高效备课】2024人教新版九上化学--2.3.1 实验室制取氧气的原理 分解反应教学设计 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-12 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2.3.1 制取氧气(教学设计)
第1课时 实验室制取氧气的原理 分解反应
新课导入
[图片导入] 展示木炭、硫和铁丝分别在氧气中燃烧的实验装置图。上节课我们研究氧气的性质时用到了几瓶较纯净的氧气,你想不想自己制取一瓶氧气呢 这节课我们就开始学习制取氧气的方法。需要提醒同学们注意的是,我们不仅要学习制取氧气的相关知识,还要体会实验室中制取气体的一般思路和方法。
[复习导入] 我们学习了氧气的性质和用途,了解到氧气是一种化学性质比较活泼的气体,它能与许多物质发生氧化反应,能支持物质的燃烧,在反应中放出热量,物质在纯净的氧气中燃烧要比在空气中燃烧剧烈得多。氧气在日常生活、工农业生产和科学研究方面有许多用途,如氧气可用来供给病人呼吸,供给登山、潜水运动员呼吸,用于气焊、气割,还用于火箭的发射等。氧气有这么多重要的用途,所以我们要知道氧气是怎样制得的。
教学建言
[建言1] 制取原理中渗透元素守恒的学科思想
展示实验室中可以制取氧气的三种常见物质以后,板书书写高锰酸钾和过氧化氢两种物质的名称和化学式,通过化学式引导学生分析两种制取氧气的物质在组成上有什么共同特点,从而让学生能初步体会化学反应中元素守恒的思想。
[建言2] 探究过氧化氢分解制取氧气的反应中二氧化锰的作用的实验改进
(1)为解决二氧化锰粉末反应前后不好称量的问题,可将二氧化锰粉末混上适量水泥(二氧化锰与水泥的质量比为4∶1)制成小颗粒状或胶囊凝块。流程如图所示:
(2)也可以用砖块负载二氧化锰进行实验,具体操作方法是:取适量的高锰酸钾溶液,将砖块浸没其中,10~15 min后取出,对砖块进行充分灼烧,冷却并充分洗涤后用于实验。砖块价格比较便宜,贴近学生生活,实验的操作性强,对比也很明显。利用砖块的吸附性(多孔)来吸附高锰酸钾,再借助高锰酸钾加热分解产生的二氧化锰具有大的表面积,可有效地提高二氧化锰的催化效率,再加上砖块对于过氧化氢也具有一定的催化作用,负载后作为一种复合型催化剂,它的催化效果非常好。另外,砖块的质量较大,体积也较大,很容易从反应后的混合物中分离出来。
(3)用微型数字化设备测氧仪证明过氧化氢在不加二氧化锰的时候也能产生氧气,只是产生氧气缓慢。方法是:上课前先向试管1中加入5 mL 5%的过氧化氢溶液,塞紧橡胶塞放置。探究二氧化锰的催化作用之后,提出问题:实验开始时将有带火星的木条伸入盛有5 mL 5%的过氧化氢溶液的试管中,没观察到木条复燃的现象,是没有产生氧气还是产生氧气缓慢 然后用测氧仪分别测定空气、试管1和长期放置过氧化氢溶液的试剂瓶中氧气的含量,测试结果是氧气含量依次增大,从而说明了过氧化氢常温下就能分解,但分解缓慢。
以上三个改进点,引导学生通过“体验”“探究”“归纳”主动把握事物的本质,并渗透了控制变量的学科方法和证据推理的学科核心素养。
视频资源
[视频1] 加热高锰酸钾制取氧气
[视频2] 过氧化氢分解制取氧气的反应中二氧化锰的作用
板书设计
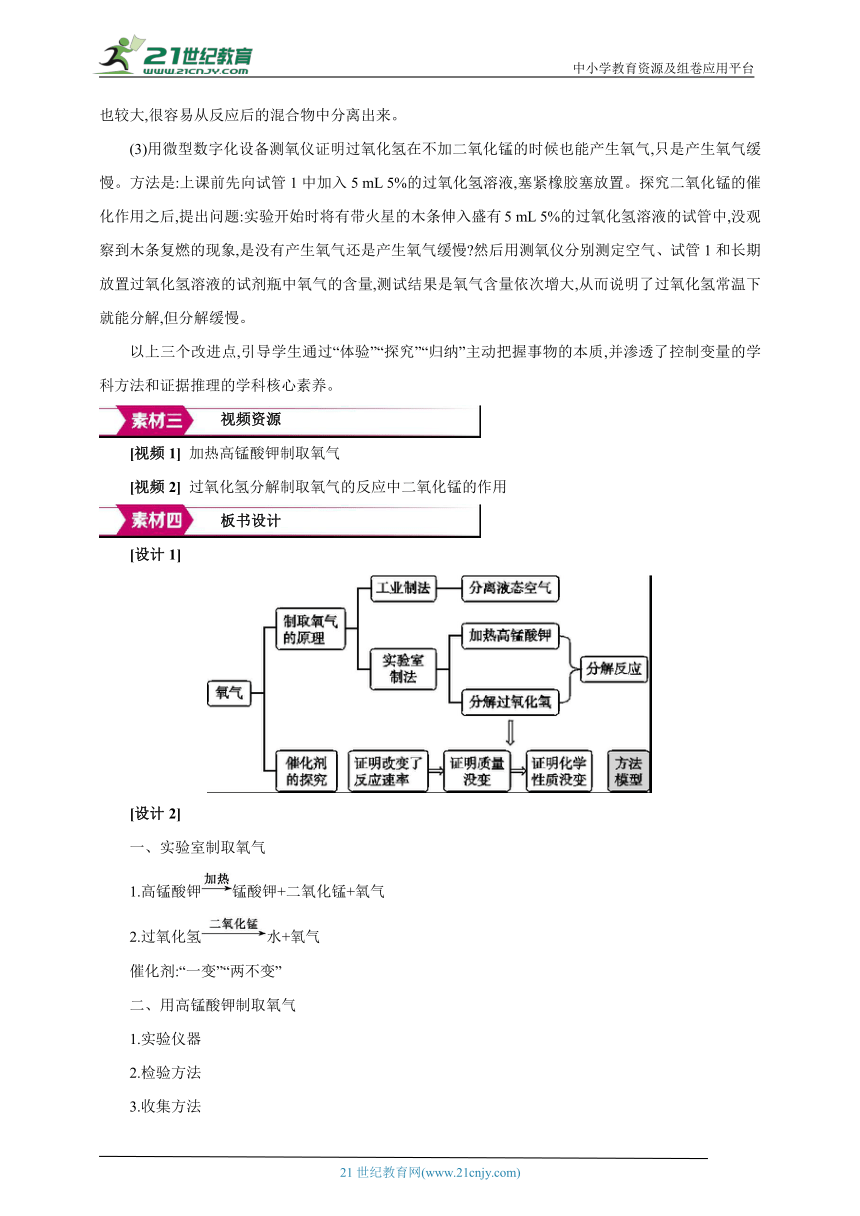
[设计1]
[设计2]
一、实验室制取氧气
1.高锰酸钾锰酸钾+二氧化锰+氧气
2.过氧化氢水+氧气
催化剂:“一变”“两不变”
二、用高锰酸钾制取氧气
1.实验仪器
2.检验方法
3.收集方法
4.验满方法
三、分解反应:“一变多”
课题3 制取氧气
第1课时 实验室制取氧气的原理 分解反应
教学设计
教学分析: 本课题的内容分两部分:第一部分让学生系统学习实验室制取氧气的方法,教材以高锰酸钾分解制取氧气为例,侧重对实验原理的介绍,过程和细节交代不多,对过氧化氢分解制取氧气的装置和过程也没有介绍。第二部分是探究过氧化氢分解制取氧气的反应中二氧化锰的作用,介绍了催化剂的概念和作用。所以本课题建议用两课时,第1课时侧重讲解原理,第2课时侧重动手操作。第1课时:着重讲解用高锰酸钾等物质制取氧气的反应原理;通过过氧化氢分解的实验探究,了解催化剂的作用。根据实验室制氧气的两个反应原理的分析,引出分解反应这一新的反应类型。第2课时:结合“实验活动1 氧气的实验室制取与性质”,具体探究制取氧气的实验步骤及操作规范,培养学生动手操作能力。
在本单元课题1和课题2的学习中,学生已经知道了氧气的性质并能利用氧气的性质设计实验检验氧气的存在,为学习氧气的制备原理奠定了基础。但由于这是学生学习化学以来第一次接触到具体气体物质的制法,需要教师引导学生初步形成实验室中制取气体的思路和方法,从而培养学生的分析能力和判断能力,并为以后探究二氧化碳的制取方法奠定坚实的基础。
教学目标: 1.通过实验,理解用高锰酸钾和过氧化氢溶液制取氧气的反应原理,能书写反应的文字表达式。初步总结实验室制取气体原理的一般思路。 2.通过分析实验室中制取氧气的原理,学习辨别常见的分解反应。 3.通过对过氧化氢分解反应中二氧化锰的催化作用的探究,初步学习探究催化剂的一般步骤,体验科学探究的方法,提升科学探究的能力。初步形成尊重事实、科学求证的意识。 4.通过观看图片,认识催化剂在化工生产中重要而广泛的应用。
教学重点:实验室中制取氧气的原理。
教学难点:过氧化氢分解反应中二氧化锰的催化作用的探究。
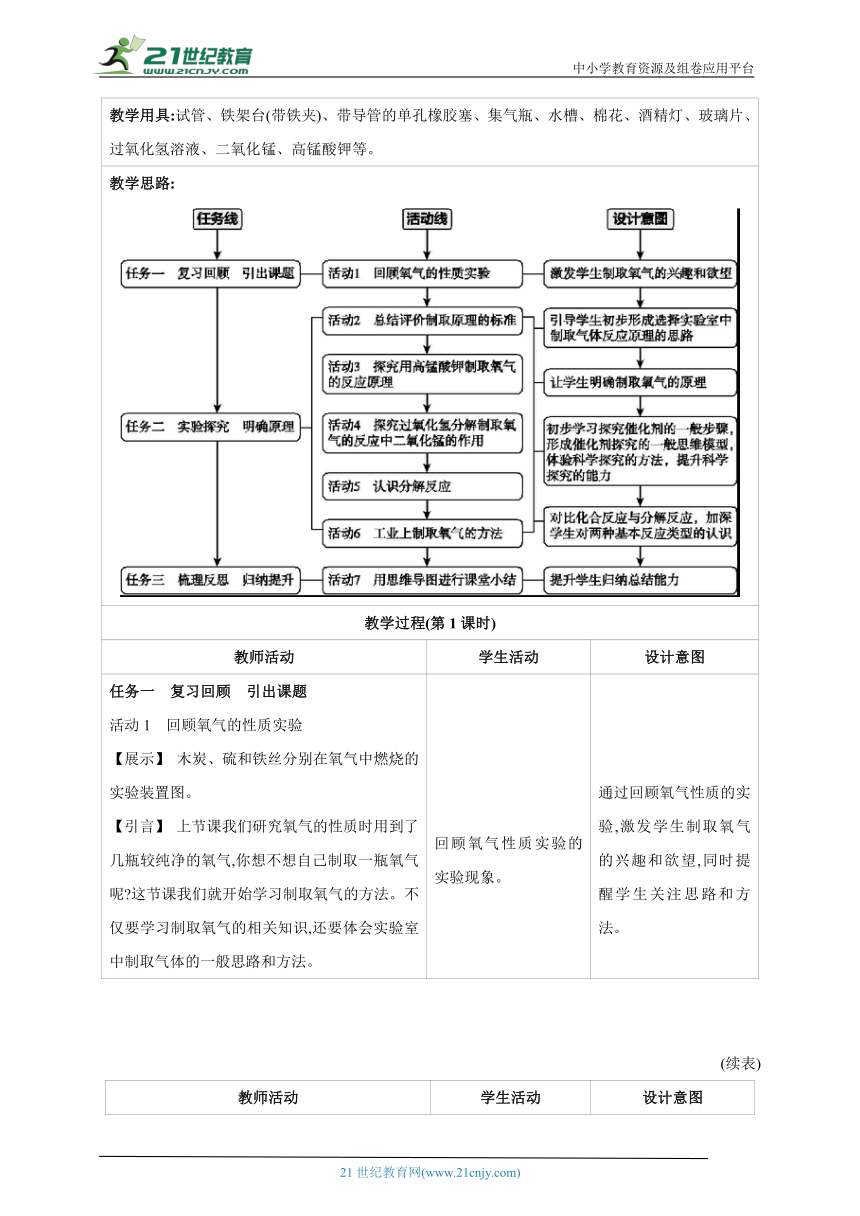
教学用具:试管、铁架台(带铁夹)、带导管的单孔橡胶塞、集气瓶、水槽、棉花、酒精灯、玻璃片、过氧化氢溶液、二氧化锰、高锰酸钾等。
教学思路:
教学过程(第1课时)
教师活动 学生活动 设计意图
任务一 复习回顾 引出课题 活动1 回顾氧气的性质实验 【展示】 木炭、硫和铁丝分别在氧气中燃烧的实验装置图。 【引言】 上节课我们研究氧气的性质时用到了几瓶较纯净的氧气,你想不想自己制取一瓶氧气呢 这节课我们就开始学习制取氧气的方法。不仅要学习制取氧气的相关知识,还要体会实验室中制取气体的一般思路和方法。 回顾氧气性质实验的实验现象。 通过回顾氧气性质的实验,激发学生制取氧气的兴趣和欲望,同时提醒学生关注思路和方法。
(续表)
教师活动 学生活动 设计意图
任务二 实验探究 明确原理 活动2 总结评价制取原理的标准 【讲述】 研究一种气体的实验室制法,我们首先要确定实验原理,即在实验条件下,选择什么试剂,通过发生什么反应就能制取该气体。 【提问】 制取氧气的方法有哪些 它们适合在实验室中制取氧气吗 为什么 【追问】 选择或评价反应原理的标准有哪些 【小结】 评价反应原理的优劣标准。 活动3 探究用高锰酸钾制取氧气的反应原理 【演示实验】 加热高锰酸钾制取氧气。 【提问】 (1)什么现象能证明加热高锰酸钾时有氧气生成 (2)试管口放一团棉花的作用是什么 【板书】 书写反应的文字表达式。 活动4 探究过氧化氢分解制取氧气的反应中二氧化锰的作用 【资料展示】 认识过氧化氢:纯过氧化氢是淡蓝色的黏稠液体,其水溶液俗称“双氧水”,为无色透明液体。过氧化氢可用作鱼塘增氧剂、种子引发剂、医用消毒剂等,在一般情况下会分解成水和氧气,但分解极其缓慢。 【提出问题】 在实验室里还常常用过氧化氢分解的方法制取氧气。实验中通常还要加入少量二氧化锰,这是为什么呢 【作出猜想】 请同学们作出猜想。 【设计实验并进行实验】 ①在试管中加入5 mL 5%过氧化氢溶液,把带有火星的木条插入试管。 ②称量负载二氧化锰的砖块后,加入上述试管中,把带有火星的木条插入试管。 回顾:植物的光合作用,不方便收集气体,不适合;加热氧化汞,会生成有毒的汞,不环保,不适合。 分组讨论并交流:一般从原理是否正确、操作是否简单安全、是否节能环保、反应速率是否适中以及是否造价低廉等方面考虑。 观察并在学案上记录实验现象。 思考并交流:(1)带有火星的木条复燃,证明有氧气生成。(2)防止加热时试管内的粉末状物质进入导管。 观察过氧化氢溶液和二氧化锰的颜色和状态。 讨论并作出猜想:过氧化氢分解放出氧气缓慢,二氧化锰可以加快反应进行。 观察并记录实验现象。 引导学生思考选择实验室中制取气体反应原理的思路。 培养学生证据推理能力。 初步学习探究催化剂的一般步骤,体验科学探究的方法,提升科学探究的能力。
③待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带有火星的木条插入试管,观察现象。待试管中又没有现象发生时,再重复上述操作。 ④将负载二氧化锰的砖块取出,烘干后再次称量。 【实验分析】 (1)实验①和②对比,能说明什么问题 (2)实验③中二氧化锰还能加快过氧化氢的分解,能不能说明二氧化锰的化学性质没有发生改变 (3)两次称量负载二氧化锰的砖块,称量结果相同,说明了什么 (4)实验①中带有火星的木条没有复燃,是过氧化氢没有产生氧气还是产生氧气缓慢 【演示实验】 用测氧仪分别测空气、试管①和长期放置过氧化氢溶液的试剂瓶中氧气的含量。 【得出结论】 二氧化锰能加快过氧化氢的分解,其质量和化学性质都未改变。 【讲述】 在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫催化剂。 【提问】 通过上述探究活动,你能总结出探究催化剂的一般思路和方法吗 【资料展示】 催化剂在化工生产中重要的作用。 活动5 认识分解反应 【提问】 思考两个制取氧气的反应,它们有什么共同特征 与化合反应有什么不同 活动6 工业上制取氧气的方法 【播放视频】 氧气的工业制取方法。 【提问】 工业上制备氧气的原理是什么 分组讨论并交流:(1)二氧化锰能加快过氧化氢的分解。(2)能说明二氧化锰的化学性质没有发生改变。(3)说明二氧化锰的质量在反应前后没有发生改变。(4)是产生氧气缓慢。 分析数据:测量结果依次增大,说明过氧化氢常温下就能分解,但分解缓慢。 通过引导写出反应的文字表达式。 分组讨论并交流。 阅读资料。 讨论并交流。 结合视频,简单总结工业上制取氧气的方法。 思考并回答。 通过驱动性问题的设置和讨论,引导学生认识在过氧化氢分解的反应中二氧化锰的作用。 形成探究催化剂的一般思维模型。 对比化合反应与分解反应,加深学生对两种基本反应类型的认识。
任务三 梳理反思 归纳提升 【提问】 通过这节课的学习,请你说说自己学到了哪些知识和方法。 思考并在学案上绘制思维导图。 让学生学习归纳和总结方法。
教学反思:
1.设定的教学目标有没有基本达成
2.学生有没有形成探究催化剂的一般思维模型
3.通过对过氧化氢分解的实验探究,学生是否理解了催化剂的概念
4.分解反应是否讲清楚 是否对比化合反应进行了教学
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2.3.1 制取氧气(教学设计)
第1课时 实验室制取氧气的原理 分解反应
新课导入
[图片导入] 展示木炭、硫和铁丝分别在氧气中燃烧的实验装置图。上节课我们研究氧气的性质时用到了几瓶较纯净的氧气,你想不想自己制取一瓶氧气呢 这节课我们就开始学习制取氧气的方法。需要提醒同学们注意的是,我们不仅要学习制取氧气的相关知识,还要体会实验室中制取气体的一般思路和方法。
[复习导入] 我们学习了氧气的性质和用途,了解到氧气是一种化学性质比较活泼的气体,它能与许多物质发生氧化反应,能支持物质的燃烧,在反应中放出热量,物质在纯净的氧气中燃烧要比在空气中燃烧剧烈得多。氧气在日常生活、工农业生产和科学研究方面有许多用途,如氧气可用来供给病人呼吸,供给登山、潜水运动员呼吸,用于气焊、气割,还用于火箭的发射等。氧气有这么多重要的用途,所以我们要知道氧气是怎样制得的。
教学建言
[建言1] 制取原理中渗透元素守恒的学科思想
展示实验室中可以制取氧气的三种常见物质以后,板书书写高锰酸钾和过氧化氢两种物质的名称和化学式,通过化学式引导学生分析两种制取氧气的物质在组成上有什么共同特点,从而让学生能初步体会化学反应中元素守恒的思想。
[建言2] 探究过氧化氢分解制取氧气的反应中二氧化锰的作用的实验改进
(1)为解决二氧化锰粉末反应前后不好称量的问题,可将二氧化锰粉末混上适量水泥(二氧化锰与水泥的质量比为4∶1)制成小颗粒状或胶囊凝块。流程如图所示:
(2)也可以用砖块负载二氧化锰进行实验,具体操作方法是:取适量的高锰酸钾溶液,将砖块浸没其中,10~15 min后取出,对砖块进行充分灼烧,冷却并充分洗涤后用于实验。砖块价格比较便宜,贴近学生生活,实验的操作性强,对比也很明显。利用砖块的吸附性(多孔)来吸附高锰酸钾,再借助高锰酸钾加热分解产生的二氧化锰具有大的表面积,可有效地提高二氧化锰的催化效率,再加上砖块对于过氧化氢也具有一定的催化作用,负载后作为一种复合型催化剂,它的催化效果非常好。另外,砖块的质量较大,体积也较大,很容易从反应后的混合物中分离出来。
(3)用微型数字化设备测氧仪证明过氧化氢在不加二氧化锰的时候也能产生氧气,只是产生氧气缓慢。方法是:上课前先向试管1中加入5 mL 5%的过氧化氢溶液,塞紧橡胶塞放置。探究二氧化锰的催化作用之后,提出问题:实验开始时将有带火星的木条伸入盛有5 mL 5%的过氧化氢溶液的试管中,没观察到木条复燃的现象,是没有产生氧气还是产生氧气缓慢 然后用测氧仪分别测定空气、试管1和长期放置过氧化氢溶液的试剂瓶中氧气的含量,测试结果是氧气含量依次增大,从而说明了过氧化氢常温下就能分解,但分解缓慢。
以上三个改进点,引导学生通过“体验”“探究”“归纳”主动把握事物的本质,并渗透了控制变量的学科方法和证据推理的学科核心素养。
视频资源
[视频1] 加热高锰酸钾制取氧气
[视频2] 过氧化氢分解制取氧气的反应中二氧化锰的作用
板书设计
[设计1]
[设计2]
一、实验室制取氧气
1.高锰酸钾锰酸钾+二氧化锰+氧气
2.过氧化氢水+氧气
催化剂:“一变”“两不变”
二、用高锰酸钾制取氧气
1.实验仪器
2.检验方法
3.收集方法
4.验满方法
三、分解反应:“一变多”
课题3 制取氧气
第1课时 实验室制取氧气的原理 分解反应
教学设计
教学分析: 本课题的内容分两部分:第一部分让学生系统学习实验室制取氧气的方法,教材以高锰酸钾分解制取氧气为例,侧重对实验原理的介绍,过程和细节交代不多,对过氧化氢分解制取氧气的装置和过程也没有介绍。第二部分是探究过氧化氢分解制取氧气的反应中二氧化锰的作用,介绍了催化剂的概念和作用。所以本课题建议用两课时,第1课时侧重讲解原理,第2课时侧重动手操作。第1课时:着重讲解用高锰酸钾等物质制取氧气的反应原理;通过过氧化氢分解的实验探究,了解催化剂的作用。根据实验室制氧气的两个反应原理的分析,引出分解反应这一新的反应类型。第2课时:结合“实验活动1 氧气的实验室制取与性质”,具体探究制取氧气的实验步骤及操作规范,培养学生动手操作能力。
在本单元课题1和课题2的学习中,学生已经知道了氧气的性质并能利用氧气的性质设计实验检验氧气的存在,为学习氧气的制备原理奠定了基础。但由于这是学生学习化学以来第一次接触到具体气体物质的制法,需要教师引导学生初步形成实验室中制取气体的思路和方法,从而培养学生的分析能力和判断能力,并为以后探究二氧化碳的制取方法奠定坚实的基础。
教学目标: 1.通过实验,理解用高锰酸钾和过氧化氢溶液制取氧气的反应原理,能书写反应的文字表达式。初步总结实验室制取气体原理的一般思路。 2.通过分析实验室中制取氧气的原理,学习辨别常见的分解反应。 3.通过对过氧化氢分解反应中二氧化锰的催化作用的探究,初步学习探究催化剂的一般步骤,体验科学探究的方法,提升科学探究的能力。初步形成尊重事实、科学求证的意识。 4.通过观看图片,认识催化剂在化工生产中重要而广泛的应用。
教学重点:实验室中制取氧气的原理。
教学难点:过氧化氢分解反应中二氧化锰的催化作用的探究。
教学用具:试管、铁架台(带铁夹)、带导管的单孔橡胶塞、集气瓶、水槽、棉花、酒精灯、玻璃片、过氧化氢溶液、二氧化锰、高锰酸钾等。
教学思路:
教学过程(第1课时)
教师活动 学生活动 设计意图
任务一 复习回顾 引出课题 活动1 回顾氧气的性质实验 【展示】 木炭、硫和铁丝分别在氧气中燃烧的实验装置图。 【引言】 上节课我们研究氧气的性质时用到了几瓶较纯净的氧气,你想不想自己制取一瓶氧气呢 这节课我们就开始学习制取氧气的方法。不仅要学习制取氧气的相关知识,还要体会实验室中制取气体的一般思路和方法。 回顾氧气性质实验的实验现象。 通过回顾氧气性质的实验,激发学生制取氧气的兴趣和欲望,同时提醒学生关注思路和方法。
(续表)
教师活动 学生活动 设计意图
任务二 实验探究 明确原理 活动2 总结评价制取原理的标准 【讲述】 研究一种气体的实验室制法,我们首先要确定实验原理,即在实验条件下,选择什么试剂,通过发生什么反应就能制取该气体。 【提问】 制取氧气的方法有哪些 它们适合在实验室中制取氧气吗 为什么 【追问】 选择或评价反应原理的标准有哪些 【小结】 评价反应原理的优劣标准。 活动3 探究用高锰酸钾制取氧气的反应原理 【演示实验】 加热高锰酸钾制取氧气。 【提问】 (1)什么现象能证明加热高锰酸钾时有氧气生成 (2)试管口放一团棉花的作用是什么 【板书】 书写反应的文字表达式。 活动4 探究过氧化氢分解制取氧气的反应中二氧化锰的作用 【资料展示】 认识过氧化氢:纯过氧化氢是淡蓝色的黏稠液体,其水溶液俗称“双氧水”,为无色透明液体。过氧化氢可用作鱼塘增氧剂、种子引发剂、医用消毒剂等,在一般情况下会分解成水和氧气,但分解极其缓慢。 【提出问题】 在实验室里还常常用过氧化氢分解的方法制取氧气。实验中通常还要加入少量二氧化锰,这是为什么呢 【作出猜想】 请同学们作出猜想。 【设计实验并进行实验】 ①在试管中加入5 mL 5%过氧化氢溶液,把带有火星的木条插入试管。 ②称量负载二氧化锰的砖块后,加入上述试管中,把带有火星的木条插入试管。 回顾:植物的光合作用,不方便收集气体,不适合;加热氧化汞,会生成有毒的汞,不环保,不适合。 分组讨论并交流:一般从原理是否正确、操作是否简单安全、是否节能环保、反应速率是否适中以及是否造价低廉等方面考虑。 观察并在学案上记录实验现象。 思考并交流:(1)带有火星的木条复燃,证明有氧气生成。(2)防止加热时试管内的粉末状物质进入导管。 观察过氧化氢溶液和二氧化锰的颜色和状态。 讨论并作出猜想:过氧化氢分解放出氧气缓慢,二氧化锰可以加快反应进行。 观察并记录实验现象。 引导学生思考选择实验室中制取气体反应原理的思路。 培养学生证据推理能力。 初步学习探究催化剂的一般步骤,体验科学探究的方法,提升科学探究的能力。
③待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带有火星的木条插入试管,观察现象。待试管中又没有现象发生时,再重复上述操作。 ④将负载二氧化锰的砖块取出,烘干后再次称量。 【实验分析】 (1)实验①和②对比,能说明什么问题 (2)实验③中二氧化锰还能加快过氧化氢的分解,能不能说明二氧化锰的化学性质没有发生改变 (3)两次称量负载二氧化锰的砖块,称量结果相同,说明了什么 (4)实验①中带有火星的木条没有复燃,是过氧化氢没有产生氧气还是产生氧气缓慢 【演示实验】 用测氧仪分别测空气、试管①和长期放置过氧化氢溶液的试剂瓶中氧气的含量。 【得出结论】 二氧化锰能加快过氧化氢的分解,其质量和化学性质都未改变。 【讲述】 在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫催化剂。 【提问】 通过上述探究活动,你能总结出探究催化剂的一般思路和方法吗 【资料展示】 催化剂在化工生产中重要的作用。 活动5 认识分解反应 【提问】 思考两个制取氧气的反应,它们有什么共同特征 与化合反应有什么不同 活动6 工业上制取氧气的方法 【播放视频】 氧气的工业制取方法。 【提问】 工业上制备氧气的原理是什么 分组讨论并交流:(1)二氧化锰能加快过氧化氢的分解。(2)能说明二氧化锰的化学性质没有发生改变。(3)说明二氧化锰的质量在反应前后没有发生改变。(4)是产生氧气缓慢。 分析数据:测量结果依次增大,说明过氧化氢常温下就能分解,但分解缓慢。 通过引导写出反应的文字表达式。 分组讨论并交流。 阅读资料。 讨论并交流。 结合视频,简单总结工业上制取氧气的方法。 思考并回答。 通过驱动性问题的设置和讨论,引导学生认识在过氧化氢分解的反应中二氧化锰的作用。 形成探究催化剂的一般思维模型。 对比化合反应与分解反应,加深学生对两种基本反应类型的认识。
任务三 梳理反思 归纳提升 【提问】 通过这节课的学习,请你说说自己学到了哪些知识和方法。 思考并在学案上绘制思维导图。 让学生学习归纳和总结方法。
教学反思:
1.设定的教学目标有没有基本达成
2.学生有没有形成探究催化剂的一般思维模型
3.通过对过氧化氢分解的实验探究,学生是否理解了催化剂的概念
4.分解反应是否讲清楚 是否对比化合反应进行了教学
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
