醇高二下学期化学人教版(2019)选择性必修三(共24张PPT)
文档属性
| 名称 | 醇高二下学期化学人教版(2019)选择性必修三(共24张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-14 10:14:00 | ||
图片预览




文档简介
(共24张PPT)
烃的衍生物
第 二 节 醇 酚
第一课时 醇
第三章
CH CH OH 乙醇
CH CHCH
OH
异丙醇
【思考】观察以上消毒剂的结构,从官能团看,它们分别属于哪些类别
新型冠状病毒
灭活甲型流感病毒
灭活率达99 .99%
生活中的消毒剂
对氯间二甲基苯酚
CH CH OH CH CH CH CH CHCH
OH OH
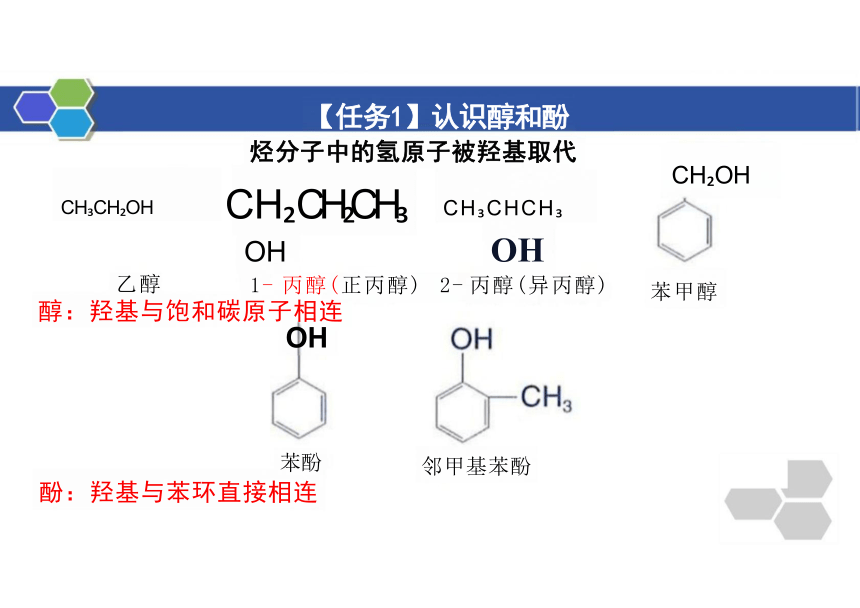
乙醇 1- 丙醇(正丙醇) 2- 丙醇(异丙醇)
醇:羟基与饱和碳原子相连
OH
【任务1】认识醇和酚
烃分子中的氢原子被羟基取代
苯酚
酚:羟基与苯环直接相连
CH OH
苯甲醇
邻甲基苯酚
CH —OH
CH —OH CH—OH
CH —OH CH —OH
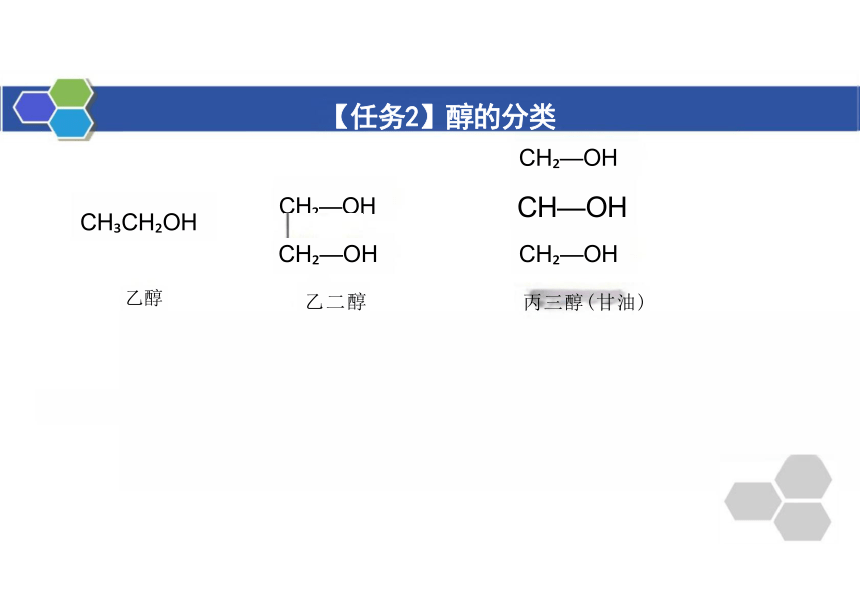
乙二醇 丙三醇(甘油)
CH CH OH
乙醇
【任务2】醇的分类
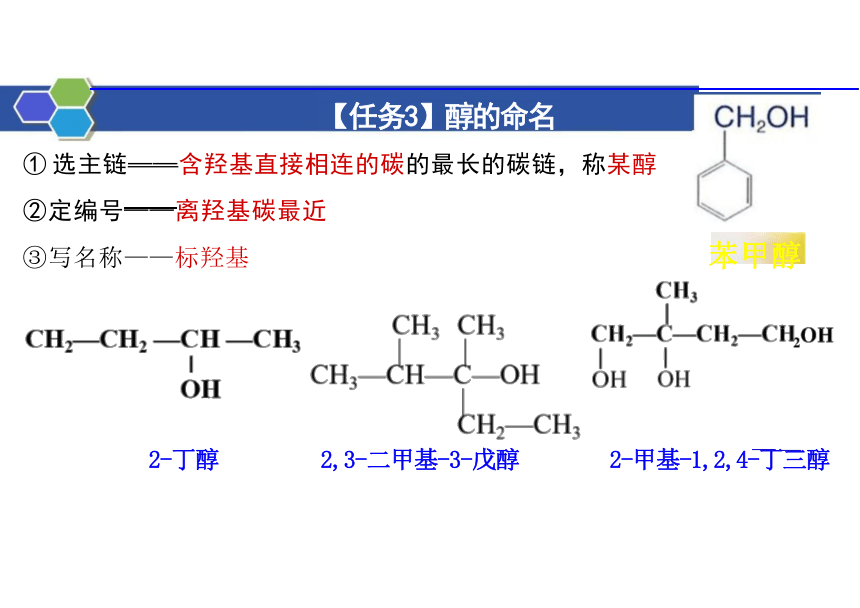
【任务3】醇的命名
① 选主链——含羟基直接相连的碳的最长的碳链,称某醇
②定编号——离羟基碳最近
③写名称——标羟基 苯甲醇
2-丁醇 2,3-二甲基-3-戊醇 2-甲基-1,2,4-丁三醇
乙二醇、丙三醇都是无色、黏稠的液体,
易溶于水和乙醇,是重要的化工原料
【思考】低级醇为什么均易溶于水 “相似相溶”规律、氢键
颜色:无色 挥发性:易挥发
状态:液 体 毒性:有毒 溶解性.易溶于水
用途: 化工生产、车用燃料
【任务3】醇类的物理性质
【思考】回顾乙醇的物理性质,类推甲醇的物理性质
工业酒精,燃料 俗称“假酒”
乙二醇
汽车防冻剂
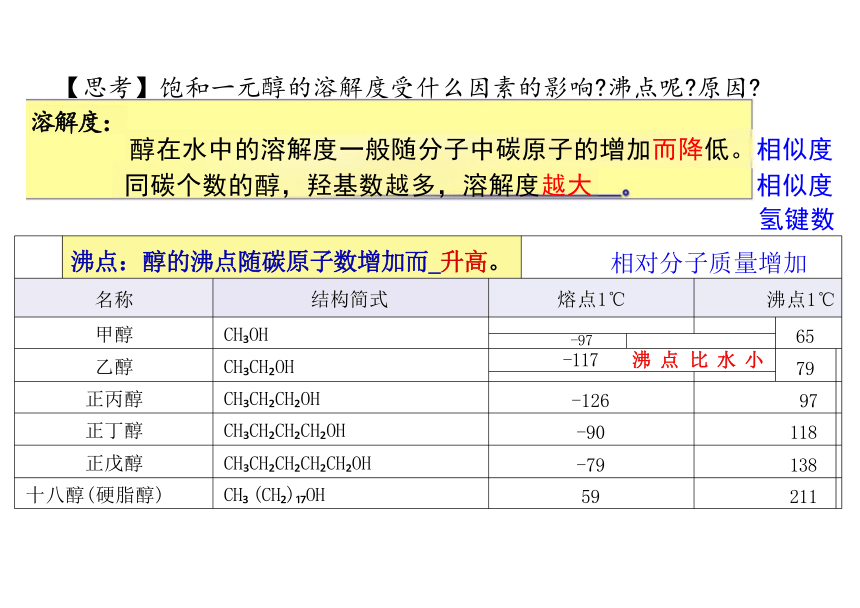
沸点:醇的沸点随碳原子数增加而_升高。 相对分子质量增加 名称 结构简式 熔点1℃ 沸点1℃ 甲醇 CH OH
65
-97 乙醇 CH CH OH -117 沸 点 比 水 小
79
正丙醇 CH CH CH OH -126 97 正丁醇 CH CH CH CH OH -90 118 正戊醇 CH CH CH CH CH OH -79 138 十八醇(硬脂醇) CH (CH ) OH 59 211
【思考】饱和一元醇的溶解度受什么因素的影响 沸点呢 原因
溶解度:
醇在水中的溶解度一般随分子中碳原子的增加而降低。相似度
同碳个数的醇,羟基数越多,溶解度越大 相似度
氢键数
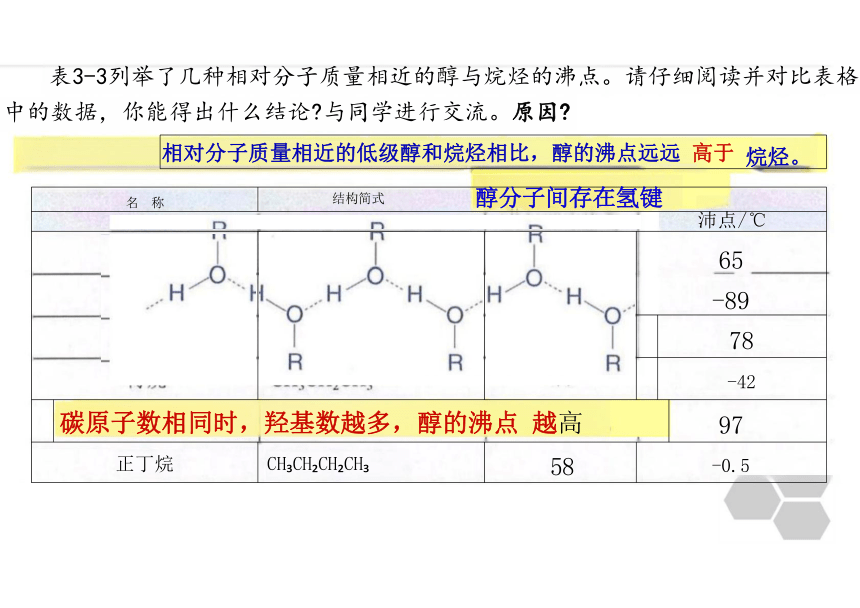
名 称 结构简式 醇分子间存在氢键 沛点/℃ 65 -89 78 -42 碳原子数相同时,羟基数越多,醇的沸点 越高
97
正丁烷 CH CH CH CH 58 -0.5
表3-3列举了几种相对分子质量相近的醇与烷烃的沸点。请仔细阅读并对比表格
中的数据,你能得出什么结论 与同学进行交流。原因
相对分子质量相近的低级醇和烷烃相比,醇的沸点远远 高于 烷烃。
【任务4】醇类的化学性质
【思考】请你回顾高一所学的乙醇的化学性质,并从官能团及化学键的角度 分析断键位置
乙醇的置换反应2CH CH OH+2Na→2CH CH ONa +H 个
★酯化反应(酸脱羟基、 氢酸)
CH COOH+HOCH CH 云 CH COOCH CH +H
0-
硫
脱
浓
醇
1、取代反应
电负性:H2.1 C2.503.5
极性较强易断裂
———取代反应或消去反应
结构
分子式
官能团
化学键
H—
【任务4】醇的化学性质
—OH
羟基
H H
δ+ δ-
H H
性质
决定
H
δ+
1、取代反应
CH CH OH+H-Br△> C H Br+H O
δ+ δ- δ+
C+ 0 —H -Br
【实验3 -2】
如图3-9所示,在圆底烧瓶中加入乙醇和浓硫酸(体
积比约为1:3)的混合液20 mL, 放入几片碎瓷片,以避 免混合液在受热时暴沸。加热混合液,使液体温度迅速升 到170℃,将生成的气体先通入氢氧化钠溶液除去杂质, 再分别通入酸性高锰酸钾溶液和溴的四氯化碳溶液中, 观察实验现象。
酸性高锰
酸钾溶液
溴的四氯 化碳溶液
2、消去反应
乙醇的消去反应
氧化
酸性KMnO 溶液、溴的四氯化碳溶液_ 褪色
产生含有不饱和碳碳键的 气体
实验现象:圆底烧瓶中的液体变黑
2、消 去 反 应 脱羟基和邻碳氢 分子内脱水
CH CH OH 170℃ CH =CH 个+H O
(1)溴乙烷与乙醇
都能发生消去反应,二
者的反应有什么异同
思考与讨论
都要求邻C有H
浓硫酸
如图3-9所示,在圆底烧瓶中加入乙醇和浓硫 酸 体 积比约为1:3)的混合液20 mL, 放入几片碎瓷片,以避 免混合液在受热时暴沸。加热混合液,使液体温度迅速 升 到170℃, 将生成的气体先通入氡氧化钠溶液除去杂质
乙醇和浓硫酸混合的顺序 先加乙醇,再加浓硫酸,相当于浓硫酸稀释 浓硫酸的作用 浓硫酸为脱水剂和催化剂
为什么圆底烧瓶中液体变黑 浓硫酸的脱水性使乙醇碳化
NaOH 溶液用于除去SO 和乙醇
SO (与Br 反应),乙醇(与酸性KMnO 溶液反应)
NaOH 溶液除去什么杂质
为什么要迅速升温至170℃
乙醇和浓硫酸的混合物140℃左右,两个乙醇分子间脱水
乙醚:无色、易挥发的液体,有特殊气味,沸点为34.5℃,有麻醉作用 易溶于有机溶剂,本身是一种优良溶剂 官能团
醚键
【思考】请你写出甲醇和乙醇混合后发生分子间脱水的反应方程式
乙醇和浓硫酸的混合物140℃左右,两个乙醇分子间脱水
取代反应 分子间脱水
CH CH OCH CH +H O 乙醚
CH CH OH+HOCH CH
浓硫酸 140℃
【思考】请你回顾高一所学的乙醇所能发生的氧化反应
3、氧化反应
①燃烧
★②催化氧化2CH CH OH+O Cu 或As2CH CHO +2H O
乙
H H
【思考】请你写出2-丙醇催化氧化的方程式
H H
H H
乙醇使酸性K Cr O 溶液由橙色变为绿色
如图3-10所示,在试管中加入酸性重铬酸钾溶液,然
3、氧化反应:③被KMnO /H+和K Cr O /H+氧化成乙酸
乙醇使酸性KMnO 溶液褪色
酸性高锰酸钾溶液
(KMnO )
酸性重铬酸钾溶液
(K Cr O )
后滴加乙醇,充分振荡,观察实验现象。
【实验3 - 3】
检验酒驾
★醇 →醛 →酸(连续氧化)
CH CH OH 氧化 CH CHO 氧化
酸 性KMnO /K Cr O
氧化反应:失 H 得O
还原反应:得 H 失 0
CH COOH
) 资料卞万
在日常生活中,我们看到有些人喝酒后, 会产生脸部变红、呕吐、昏迷等醉酒症状; 有些人喝了一定量的酒,却并不会出现上述 症状。这是什么原因造成的呢
酒精在人体内的代谢主要靠两种酶: 一 种
醇月
90%
在肝脏代谢 乙醇
酒精
酶能使乙醛氧化为乙酸。乙酸参与体内代谢,
转化为二氧化碳和水排出体外。人体内如果 具备这两种酶,就能较快地分解酒精。 一般 人的体内都有乙醇脱氢酶,但不少人缺少乙 醛脱氢酶,这使体内的乙醛不易被氧化为乙 扩张充
水
乙醛 乙 酸一二氧化碳
热量
乙醇的置换反应2CH CH OH+2Na→2CH CH ONa +H 个
1、取代反应 浓 硫 酸
CH COOH+HOCH CH 云CH COOCH CH +H O
2、消去反应
3、氧化反应 CH CHOH+O Cu或Ag2CH CHO+2H,O
△
CH CH OH 氧化→CH CHo 氧化CH coo
酸 性KMnO /K Cr O
作业本
课本67页,不抄题
注意标明反应条件
10.以乙烯为基本原料,合成六元环状化合物D(C H O ) 的反应如下所示(部分试剂、产物及反应条
件略去):
6.写出下列物质间转化的化学方程式,并注明反应条件。
请写出各步反应的化学方程式和反应类型。
+Br +H O -H O
B C
A
乙烯
D
谢谢观看
烃的衍生物
第 二 节 醇 酚
第一课时 醇
第三章
CH CH OH 乙醇
CH CHCH
OH
异丙醇
【思考】观察以上消毒剂的结构,从官能团看,它们分别属于哪些类别
新型冠状病毒
灭活甲型流感病毒
灭活率达99 .99%
生活中的消毒剂
对氯间二甲基苯酚
CH CH OH CH CH CH CH CHCH
OH OH
乙醇 1- 丙醇(正丙醇) 2- 丙醇(异丙醇)
醇:羟基与饱和碳原子相连
OH
【任务1】认识醇和酚
烃分子中的氢原子被羟基取代
苯酚
酚:羟基与苯环直接相连
CH OH
苯甲醇
邻甲基苯酚
CH —OH
CH —OH CH—OH
CH —OH CH —OH
乙二醇 丙三醇(甘油)
CH CH OH
乙醇
【任务2】醇的分类
【任务3】醇的命名
① 选主链——含羟基直接相连的碳的最长的碳链,称某醇
②定编号——离羟基碳最近
③写名称——标羟基 苯甲醇
2-丁醇 2,3-二甲基-3-戊醇 2-甲基-1,2,4-丁三醇
乙二醇、丙三醇都是无色、黏稠的液体,
易溶于水和乙醇,是重要的化工原料
【思考】低级醇为什么均易溶于水 “相似相溶”规律、氢键
颜色:无色 挥发性:易挥发
状态:液 体 毒性:有毒 溶解性.易溶于水
用途: 化工生产、车用燃料
【任务3】醇类的物理性质
【思考】回顾乙醇的物理性质,类推甲醇的物理性质
工业酒精,燃料 俗称“假酒”
乙二醇
汽车防冻剂
沸点:醇的沸点随碳原子数增加而_升高。 相对分子质量增加 名称 结构简式 熔点1℃ 沸点1℃ 甲醇 CH OH
65
-97 乙醇 CH CH OH -117 沸 点 比 水 小
79
正丙醇 CH CH CH OH -126 97 正丁醇 CH CH CH CH OH -90 118 正戊醇 CH CH CH CH CH OH -79 138 十八醇(硬脂醇) CH (CH ) OH 59 211
【思考】饱和一元醇的溶解度受什么因素的影响 沸点呢 原因
溶解度:
醇在水中的溶解度一般随分子中碳原子的增加而降低。相似度
同碳个数的醇,羟基数越多,溶解度越大 相似度
氢键数
名 称 结构简式 醇分子间存在氢键 沛点/℃ 65 -89 78 -42 碳原子数相同时,羟基数越多,醇的沸点 越高
97
正丁烷 CH CH CH CH 58 -0.5
表3-3列举了几种相对分子质量相近的醇与烷烃的沸点。请仔细阅读并对比表格
中的数据,你能得出什么结论 与同学进行交流。原因
相对分子质量相近的低级醇和烷烃相比,醇的沸点远远 高于 烷烃。
【任务4】醇类的化学性质
【思考】请你回顾高一所学的乙醇的化学性质,并从官能团及化学键的角度 分析断键位置
乙醇的置换反应2CH CH OH+2Na→2CH CH ONa +H 个
★酯化反应(酸脱羟基、 氢酸)
CH COOH+HOCH CH 云 CH COOCH CH +H
0-
硫
脱
浓
醇
1、取代反应
电负性:H2.1 C2.503.5
极性较强易断裂
———取代反应或消去反应
结构
分子式
官能团
化学键
H—
【任务4】醇的化学性质
—OH
羟基
H H
δ+ δ-
H H
性质
决定
H
δ+
1、取代反应
CH CH OH+H-Br△> C H Br+H O
δ+ δ- δ+
C+ 0 —H -Br
【实验3 -2】
如图3-9所示,在圆底烧瓶中加入乙醇和浓硫酸(体
积比约为1:3)的混合液20 mL, 放入几片碎瓷片,以避 免混合液在受热时暴沸。加热混合液,使液体温度迅速升 到170℃,将生成的气体先通入氢氧化钠溶液除去杂质, 再分别通入酸性高锰酸钾溶液和溴的四氯化碳溶液中, 观察实验现象。
酸性高锰
酸钾溶液
溴的四氯 化碳溶液
2、消去反应
乙醇的消去反应
氧化
酸性KMnO 溶液、溴的四氯化碳溶液_ 褪色
产生含有不饱和碳碳键的 气体
实验现象:圆底烧瓶中的液体变黑
2、消 去 反 应 脱羟基和邻碳氢 分子内脱水
CH CH OH 170℃ CH =CH 个+H O
(1)溴乙烷与乙醇
都能发生消去反应,二
者的反应有什么异同
思考与讨论
都要求邻C有H
浓硫酸
如图3-9所示,在圆底烧瓶中加入乙醇和浓硫 酸 体 积比约为1:3)的混合液20 mL, 放入几片碎瓷片,以避 免混合液在受热时暴沸。加热混合液,使液体温度迅速 升 到170℃, 将生成的气体先通入氡氧化钠溶液除去杂质
乙醇和浓硫酸混合的顺序 先加乙醇,再加浓硫酸,相当于浓硫酸稀释 浓硫酸的作用 浓硫酸为脱水剂和催化剂
为什么圆底烧瓶中液体变黑 浓硫酸的脱水性使乙醇碳化
NaOH 溶液用于除去SO 和乙醇
SO (与Br 反应),乙醇(与酸性KMnO 溶液反应)
NaOH 溶液除去什么杂质
为什么要迅速升温至170℃
乙醇和浓硫酸的混合物140℃左右,两个乙醇分子间脱水
乙醚:无色、易挥发的液体,有特殊气味,沸点为34.5℃,有麻醉作用 易溶于有机溶剂,本身是一种优良溶剂 官能团
醚键
【思考】请你写出甲醇和乙醇混合后发生分子间脱水的反应方程式
乙醇和浓硫酸的混合物140℃左右,两个乙醇分子间脱水
取代反应 分子间脱水
CH CH OCH CH +H O 乙醚
CH CH OH+HOCH CH
浓硫酸 140℃
【思考】请你回顾高一所学的乙醇所能发生的氧化反应
3、氧化反应
①燃烧
★②催化氧化2CH CH OH+O Cu 或As2CH CHO +2H O
乙
H H
【思考】请你写出2-丙醇催化氧化的方程式
H H
H H
乙醇使酸性K Cr O 溶液由橙色变为绿色
如图3-10所示,在试管中加入酸性重铬酸钾溶液,然
3、氧化反应:③被KMnO /H+和K Cr O /H+氧化成乙酸
乙醇使酸性KMnO 溶液褪色
酸性高锰酸钾溶液
(KMnO )
酸性重铬酸钾溶液
(K Cr O )
后滴加乙醇,充分振荡,观察实验现象。
【实验3 - 3】
检验酒驾
★醇 →醛 →酸(连续氧化)
CH CH OH 氧化 CH CHO 氧化
酸 性KMnO /K Cr O
氧化反应:失 H 得O
还原反应:得 H 失 0
CH COOH
) 资料卞万
在日常生活中,我们看到有些人喝酒后, 会产生脸部变红、呕吐、昏迷等醉酒症状; 有些人喝了一定量的酒,却并不会出现上述 症状。这是什么原因造成的呢
酒精在人体内的代谢主要靠两种酶: 一 种
醇月
90%
在肝脏代谢 乙醇
酒精
酶能使乙醛氧化为乙酸。乙酸参与体内代谢,
转化为二氧化碳和水排出体外。人体内如果 具备这两种酶,就能较快地分解酒精。 一般 人的体内都有乙醇脱氢酶,但不少人缺少乙 醛脱氢酶,这使体内的乙醛不易被氧化为乙 扩张充
水
乙醛 乙 酸一二氧化碳
热量
乙醇的置换反应2CH CH OH+2Na→2CH CH ONa +H 个
1、取代反应 浓 硫 酸
CH COOH+HOCH CH 云CH COOCH CH +H O
2、消去反应
3、氧化反应 CH CHOH+O Cu或Ag2CH CHO+2H,O
△
CH CH OH 氧化→CH CHo 氧化CH coo
酸 性KMnO /K Cr O
作业本
课本67页,不抄题
注意标明反应条件
10.以乙烯为基本原料,合成六元环状化合物D(C H O ) 的反应如下所示(部分试剂、产物及反应条
件略去):
6.写出下列物质间转化的化学方程式,并注明反应条件。
请写出各步反应的化学方程式和反应类型。
+Br +H O -H O
B C
A
乙烯
D
谢谢观看
