3.2卤代烃高二化学人教版(2019)选择性必修3(共33张PPT)
文档属性
| 名称 | 3.2卤代烃高二化学人教版(2019)选择性必修3(共33张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-14 00:00:00 | ||
图片预览







文档简介
(共33张PPT)
核心素养
第三章烃的衍生物
第1节卤代烃
第1课时卤代烃的结构与性质
学习目标
1、能辨识卤代烃的官能团,并根据官能团对卤代烃进行分类。
2、能列举卤代烃的主要物理性质及应用。
3、能从溴乙烷的官能团和化学键特点预测可能的断键部位和 化学性质,结合实验了解溴乙烷与NaOH 水溶液的反应,能写出 相应的化学方程式。
4、通过了解卤代烃在生活中的应用,认识化学对满足人类生
活需要的积极贡献,树立保护环境和可持续发展的意识。
1.烃的衍生物
烃分子中的氢原子被其它原子或原子团取代而生成的化合物。 常见有卤代烃、醇、酚、醛、酮、羧酸、酯等。
2.卤代烃
烃分子中的氢原子被卤素原子取代后生成的化合物称为卤代烃。 可表示为R—X(X=F 、Cl 、Br 、I。
◆烃的衍生物
知识回顾
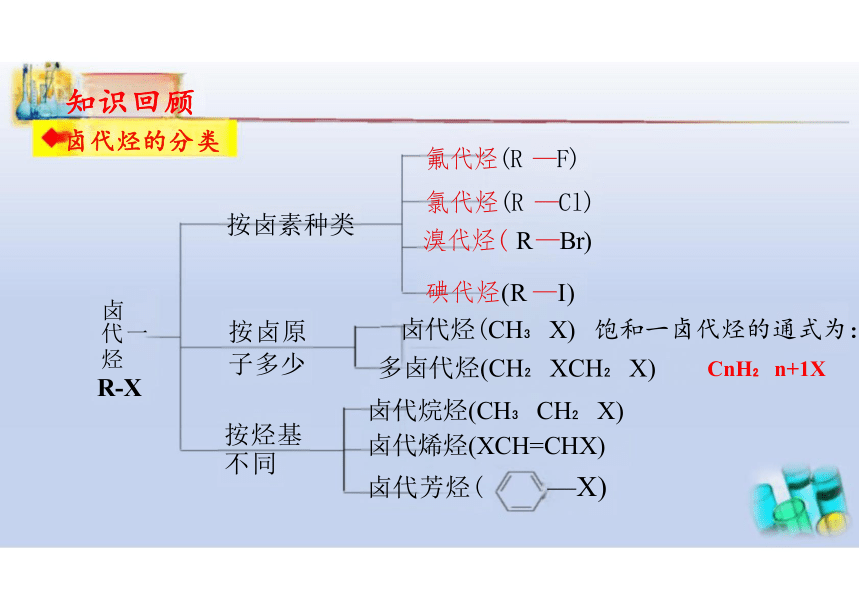
官能团:
碳卤键
氟代烃(R —F)
氯代烃(R —Cl)
溴代烃( R —Br)
碘代烃(R —I)
卤代烃(CH X) 饱和一卤代烃的通式为: 多卤代烃(CH XCH X) CnH n+1X
卤代烷烃(CH CH X)
卤代烯烃(XCH=CHX)
卤代芳烃( —X)
知识回顾
卤代烃的分类
按卤素种类
卤 代一 烃 R-X
按卤原 子多少
按烃基 不同
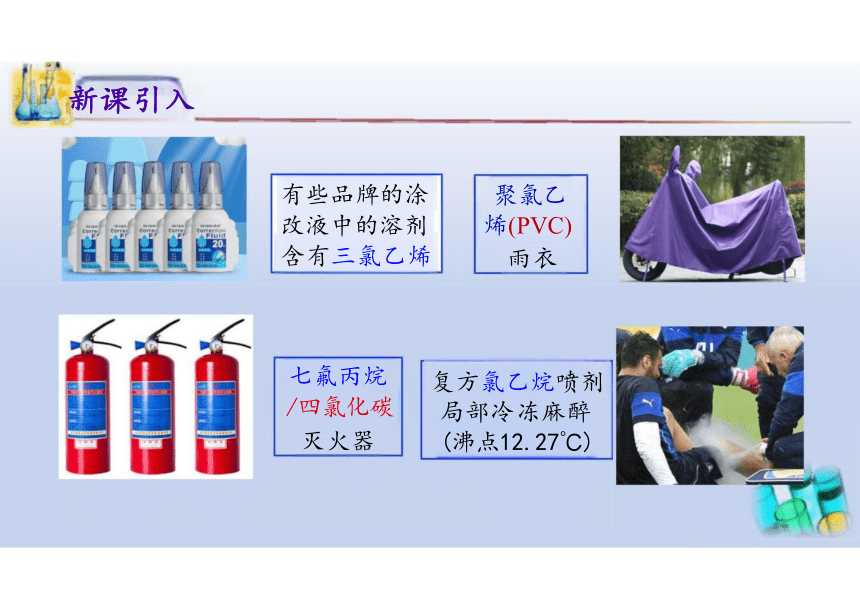
复方氯乙烷喷剂 局部冷冻麻醉 (沸点12.27℃)
有些品牌的涂 改液中的溶剂 含有三氯乙烯
七氟丙烷
/四氯化碳
灭火器
聚氯乙 烯(PVC)
雨衣
新课引入
知识精讲
卤代烃的命名
①定主链:选择含官能团的最长碳链作为主链
②编位号:卤素原子看做取代基,编号考虑“近、简、小” 有碳碳双键时从距离碳碳双键近的一端开始编号
③写名称:相对分子质量由小到大,和烷烃相似。
2,3-二氯-1-丙烯 3-甲基-1,3-二溴戊烷 3-甲基-2-氯丁烷
常温下除一氯甲烷、氯乙烯、氯乙烷等是气体外,
大多数为液体或固体。
熔沸点大 于同碳个数的烃,随碳原子数增多,沸点依次升高 (碳原子数相同时,支链越多沸点越低)。
除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大,
一般随着烃基中碳原子数目的增加而减小。
不溶于水,可溶于有机溶剂,某些卤代烃本身就是有机溶剂。
状态
沸 点
密度
溶解性
知识精讲
卤代烃的物理性质
知识精讲
卤代烃的化学性质
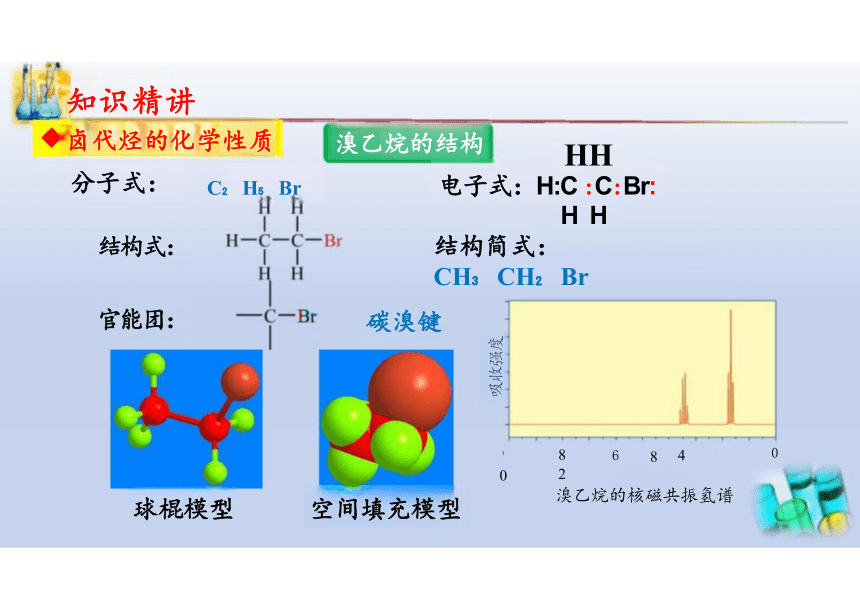
分子式: C H Br
结构式:
官能团:
电子式:H:C :C:Br: H H
结构简式: CH CH Br
球棍模型 空间填充模型
8 6 8 4 2
溴乙烷的核磁共振氢谱
溴乙烷的结构
碳溴键
吸收强度
HH
1
0
0
知识精讲
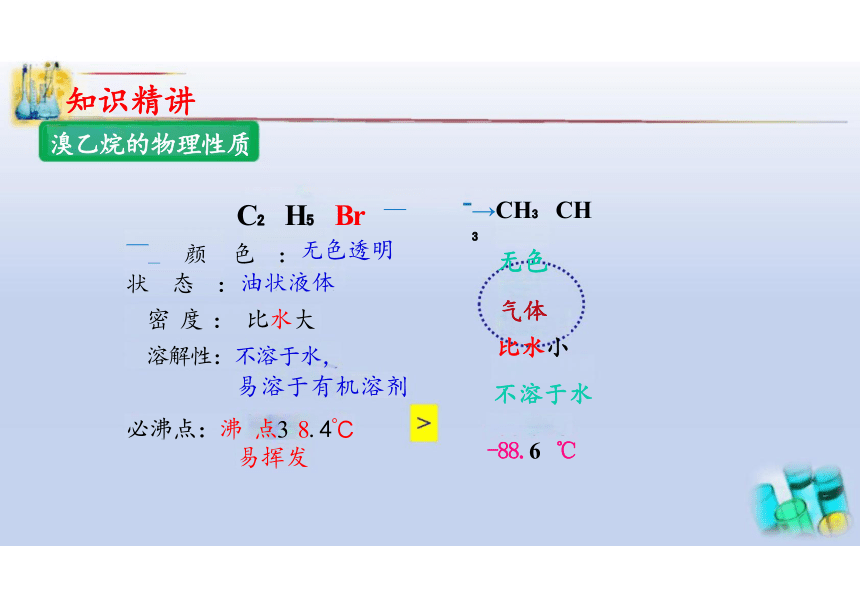
溴乙烷的物理性质
C H Br ——_ 颜 色 :无色透明
状 态 :油状液体
密 度 : 比水大
溶解性:不溶于水,
易溶于有机溶剂
必沸点:沸 点3 8.4℃ 易挥发
→CH CH
无色
气体
比水小
不溶于水
-88.6 ℃
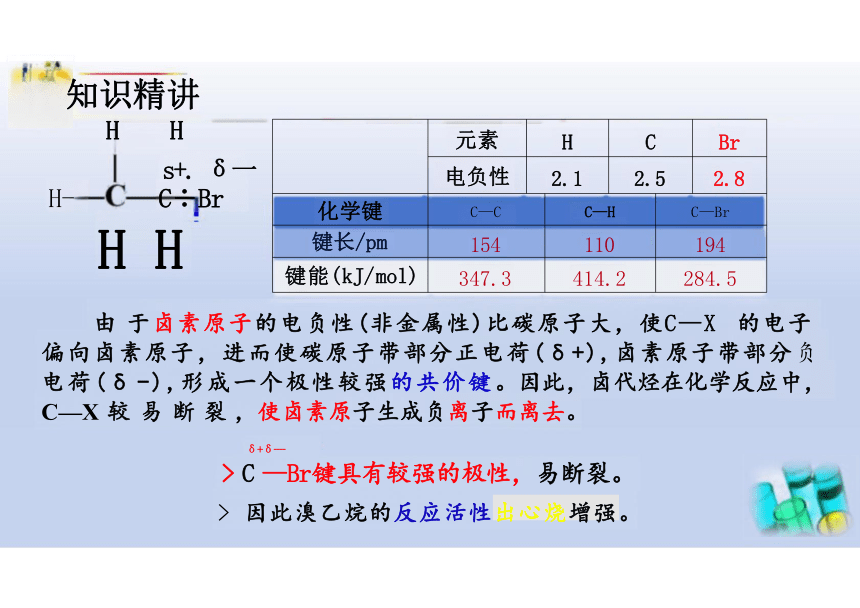
由 于卤素原子的电负性(非金属性)比碳原子大,使C—X 的电子 偏向卤素原子,进而使碳原子带部分正电荷(δ+),卤素原子带部分负 电荷(δ -),形成一个极性较强的共价键。因此,卤代烃在化学反应中, C—X 较 易 断 裂 ,使卤素原子生成负离子而离去。
元素 H C
Br
电负性 2.1 2.5
2.8
化学键 C—C C—H C—Br 键长/pm 154 110 194 键能(kJ/mol) 347.3 414.2 284.5
知识精讲
H H
s+. δ一 H- C÷Br
H H
δ+δ—
> C —Br键具有较强的极性,易断裂。
> 因此溴乙烷的反应活性出心烧增强。
提出问题1:溴乙烷 在水中能否电离出Br-
它是否为电解质 请设计实验证明。
AgNO (aq)+HNO
现 象 :—→无浅黄色沉淀
结论:C H Br是非电解质,
C H Br 不能电离出Br-
知识精讲
对CH CH Br 化学性质的探索
知识精讲
请同学们尝试写出溴乙烷与水发生反应的方程式。
资料卡片:
C H Br与水的反应要在 碱性环境下才容易进行
C-Br 键较易断裂,预测Br-离去后,碳原子易与带负电荷的
OH-结合而生成乙醇,这说明结构决定性 质。
HH
—9—
+H O
知识精讲
实验装置 ①
实验现象 ①中溶液分层。②中有机层厚度减小。④中有淡黄色沉淀生成。 实验解释 溴乙烷与NaOH溶液共热,产生了Br-
水
C H Br+NaOH ^ C H OH+NaBr
NaBr+AgNO —AgBrl+NaNO
实验条件:NaOH水溶液、加热
1 mL 5%
NaOH
溶液
振荡
10~15
滴溴乙
烷 ②
上层
-水溶液
2 滴 硝 酸银
静置 分层
l mL 稀硝
0 溶液
③ 酸
④
0
知识精讲
如何用实验证明该反应的发生
①C H Br AgNO 溶液。不合理
②C H Br Na 溶液 AgNO 溶液、 不合理
③C H Br NaO 溶液 AgNO 溶液 合理
溴乙烷中不存在溴离子,溴乙烷是非电解质,不能电离。
因 为Ag++OH-=AgOH ( 白 色) 2 AgOH=Ag O(褐色)+H O;
黑褐色掩蔽AgBr的浅黄色,干扰产物检验。所以必须用硝酸酸化!
硝酸酸化
上层清液
加
取
△
H
△
OH
小结卤代烃中卤元素的检验:
卤代烃 Na H (水) 取上层清液
液
溶
NO
H
AgNO
过量
白色
有沉淀产生→淡 黄 色
黄色
知识精讲
◆溴乙烷的取代反应(也叫水解反应)
反应条件:NaOH水溶液、加热
反应原理:羟 基取代溴原子
NaOH+HBr ==NaBr+H O
CH CH Br+NaOH CH CH OH+NaBr
推广:所有卤代烃在碱性水溶液中都会发生水解反应
总反应:
知识精讲
用何种波谱可以方便地检验产物中有乙醇生成
①红外光谱
②核磁共振氢谱
学以致用 1. 写出CH Cl 、CH CHCICH 、1,3- 二溴丙烷分别与NaOH的水溶液
发生反应的化学方程式。
②卤素原子直接与苯环相连的卤代芳香烃水解反应条件比较苛刻
①所有卤代烃在一定条件下都能发生水解。
规律:
知识精讲
溴乙烷的消去反应(也叫消除反应)
实验条件:与NaOH的醇溶液共热
C H Br
NaOH +乙 醇
作为溶剂
溴水
知识精讲
实 质:相邻的两个C 上脱去HX 形成不饱和键!
化学键的变化:断裂C-Br 和邻位碳原子上的C-H, 形 成 C=C
>消去反应:有机化合物在一 定条件下,从一个分子中脱去一个小分 子 ( 如H O、HX 等),而生成不饱和(含双键或三键)化合物的反应。P 4
知识精讲
(1)分析反应产生的气体中可能含有哪些杂质 会不会对乙烯。
的检验产生干扰 可能的杂质气体:溴乙烷(沸点:38.4℃)、乙醇、水蒸汽
(2)生成的气体通入高锰酸钾溶液前要先通入盛水的试管
(3)还可以用什么方法鉴别乙烯,这一方法还需要将生成的气体 先通入盛水的试管中吗
(2)乙醇能使酸性高锰酸钾溶液褪色,
除去乙醇,排除干扰。
(3)溴水或溴的四氯化碳溶液;不用 ,
因为乙醇不能使溴水褪色。 水
取反应后的液体加入稀硝酸酸化后,加硝酸银
溶液,有什么现象 不酸化可行吗
有浅黄色沉淀生成。不行,因 为反应环境呈碱性。
气体
水解反应(取代反应)
消去反应
反应物 CH CH Br 水
CH CH Br
反应条件 NaOH水溶液,加热
NaOH醇溶液,加热
断键 C一Br
C一Br,邻碳C一H
生成物 CH CH OH、 NaBr
CH =CH 、 NaBr、H O
结论 C H Br和NaOH在 不同条件下发生不同类型的反应
知识精讲
我们还学过哪个消去反应 CH —CH
…..
口诀:“有醇则无醇,无醇则有醇”
消去反应 水解反应
比较溴乙烷的取代反应和消去反应,并完成下表。
CH =CH 个+ H O
浓H SO 170℃
学 以致用
2.分析下列物质是否发生消去反应,消去产物有几种
①CH I ② ③
④ CH CHBr ⑤ ⑥
苯环上的H不能被消去!
消去反应的发生条件
1、邻位碳原子上必须有氢原子(β-H), 否 则不能发生消去反应。
2 、NaOH的乙醇溶液、加热。
归 纳 总 结
反应类型 取代反应 消去反应 反应物 CH CH CH CH Br +水 CH CH CH CH Br
反应条件 NaOH水溶液,加热 NaOH醇溶液,加热
生成物 CH CH CH CH OH、NaBr CH CH CH=CH 、NaBr、H
O
结论 1-溴丁烷和NaOH在不同条件下发生不同类型的反应
知识精讲
【比较与分析】
比较1-溴丁烷的取代反应和消去反应,完成下表,分析反应条件对化学反应的
影响。
知识精讲
【讨论】
(1)如图3-3所示,为什么要在气体通入酸性高锰酸钾溶液前先通入盛水的试 管 除了酸性高锰酸钾溶液,还可以用什么方法检验丁烯 此时还有必要将气体先
通入水中吗
因受热而挥发的乙醇也能使高锰酸钾褪色,
所以要先通过水除去乙醇,防止干扰实验。
还可以 利用溴水、溴 的CCl 溶液检验丁烯。
此时不需要先通入水中。
乙醇与溴不反应,不会干扰乙烯的检验。
知识精讲
(2)预测2-溴丁烷发生消去反应的可能产物。
消去反应规则:当有多个产物时,以消H少的C 原子上的H为主
2-丁烯(主产物)
1 -丁烯
CH -CH =CH-CH
CH -CH -CH=CH
“雪上加霜”
A、CH Cl 无相邻C
CH
(主产物)CH -CH =C-CH
CB-Ch-C-C
B、CH —CH一CH
Br CH =CH-CH
CI
苯环上为独特的碳碳键
Cl CH CI
CH
学 以致用
3.下列卤代烃能否发生消去反应 若能,请写出有机产物的结构简式:
关键:抓住断键方式
学 以致用
4.写出由CH BrCH Br 与NaOH醇溶液共热的反应化学方程式
规律:
二卤代烃发生消 去反应后可能在 有机化合物中引 入碳碳三键或两 个碳碳双键。
注意:不能同时消去2个卤素原子!!!
归纳总结
扩展: 卤代烃中卤素原子的检验方法:
①原理:通过水解反应将卤素原子转化为卤素离子
水溶液 过量HNO 溶液AgNO 溶液AgCl 酸化 AgBr
该步骤必不可少 AgI
> 不能 利用消去反应检验卤素原子;
因 为不是所有的卤代烃都能发生消去反应。
无沉淀
白色沉淀 浅黄色沉淀 黄色沉淀
②操作过程:
NaOH
R-X
△
能否改为“NaOH 醇 溶液”
取上层清液
笔记
AgF
3、有两个邻位碳原子,且碳原子上均有氢原子时,发生消去
反应可能生成多种产物。
例如: 发生消去反应的产物为:
—CH —CH CH —CH=CH—CH
1、没有邻位碳原子的卤代烃不能发生消去反应,如CH Br。
2、有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也 不能发生消去反应。
例如: CH Cl
卤代烃的消去反应规律
归纳总结
⑥
卤代烃的应用:
1.连接烃和烃的衍生物的桥梁
2.改变官能团的个数
3.改变官能团的位置
4.对官能团进行保护
归纳总结
烃、卤代烃、醇之间的衍变类系
⑤
③
CH =CH CH CH -Cl
CH CH - OH
随堂检测
1.下列化合物在一定条件下,
既能发生水解反应,又能发生消去反应的有 。
CH CHBrCH
CH =CHBr
CH I
CH CI
√③(CH ) CCI
CH Br
> 但卤代烃中无相邻C 或相邻C 上无H 的不 能发生消去反应
> 所有的卤代烃都能发生水解反应!
注意:
H , 催化剂 ① ④ Br 足量浓NaOH D乙醇溶液 △ E ⑤ 光照 ② 适量Br ⑥ HBr F1 ⑦ HBr F2 ⑧
G1
G2
G1
随堂检测
2.烯烃A在一定条件下可按下面的框图进行反应:
③HBr 已知D结构简式为:
H C CH
(1)A的结构简式为CH - C=C- CH
(2)框图中属于取代反应的是_②
(3)框图中①③⑥属于什么反应 加成反应
F1和F2是同分异构体;
G1 和G2互为同分异构体。
E 结构简式为:
H C CH
CH =C-C= CH
Br ,
C
B
核心素养
第三章烃的衍生物
第1节卤代烃
第1课时卤代烃的结构与性质
学习目标
1、能辨识卤代烃的官能团,并根据官能团对卤代烃进行分类。
2、能列举卤代烃的主要物理性质及应用。
3、能从溴乙烷的官能团和化学键特点预测可能的断键部位和 化学性质,结合实验了解溴乙烷与NaOH 水溶液的反应,能写出 相应的化学方程式。
4、通过了解卤代烃在生活中的应用,认识化学对满足人类生
活需要的积极贡献,树立保护环境和可持续发展的意识。
1.烃的衍生物
烃分子中的氢原子被其它原子或原子团取代而生成的化合物。 常见有卤代烃、醇、酚、醛、酮、羧酸、酯等。
2.卤代烃
烃分子中的氢原子被卤素原子取代后生成的化合物称为卤代烃。 可表示为R—X(X=F 、Cl 、Br 、I。
◆烃的衍生物
知识回顾
官能团:
碳卤键
氟代烃(R —F)
氯代烃(R —Cl)
溴代烃( R —Br)
碘代烃(R —I)
卤代烃(CH X) 饱和一卤代烃的通式为: 多卤代烃(CH XCH X) CnH n+1X
卤代烷烃(CH CH X)
卤代烯烃(XCH=CHX)
卤代芳烃( —X)
知识回顾
卤代烃的分类
按卤素种类
卤 代一 烃 R-X
按卤原 子多少
按烃基 不同
复方氯乙烷喷剂 局部冷冻麻醉 (沸点12.27℃)
有些品牌的涂 改液中的溶剂 含有三氯乙烯
七氟丙烷
/四氯化碳
灭火器
聚氯乙 烯(PVC)
雨衣
新课引入
知识精讲
卤代烃的命名
①定主链:选择含官能团的最长碳链作为主链
②编位号:卤素原子看做取代基,编号考虑“近、简、小” 有碳碳双键时从距离碳碳双键近的一端开始编号
③写名称:相对分子质量由小到大,和烷烃相似。
2,3-二氯-1-丙烯 3-甲基-1,3-二溴戊烷 3-甲基-2-氯丁烷
常温下除一氯甲烷、氯乙烯、氯乙烷等是气体外,
大多数为液体或固体。
熔沸点大 于同碳个数的烃,随碳原子数增多,沸点依次升高 (碳原子数相同时,支链越多沸点越低)。
除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大,
一般随着烃基中碳原子数目的增加而减小。
不溶于水,可溶于有机溶剂,某些卤代烃本身就是有机溶剂。
状态
沸 点
密度
溶解性
知识精讲
卤代烃的物理性质
知识精讲
卤代烃的化学性质
分子式: C H Br
结构式:
官能团:
电子式:H:C :C:Br: H H
结构简式: CH CH Br
球棍模型 空间填充模型
8 6 8 4 2
溴乙烷的核磁共振氢谱
溴乙烷的结构
碳溴键
吸收强度
HH
1
0
0
知识精讲
溴乙烷的物理性质
C H Br ——_ 颜 色 :无色透明
状 态 :油状液体
密 度 : 比水大
溶解性:不溶于水,
易溶于有机溶剂
必沸点:沸 点3 8.4℃ 易挥发
→CH CH
无色
气体
比水小
不溶于水
-88.6 ℃
由 于卤素原子的电负性(非金属性)比碳原子大,使C—X 的电子 偏向卤素原子,进而使碳原子带部分正电荷(δ+),卤素原子带部分负 电荷(δ -),形成一个极性较强的共价键。因此,卤代烃在化学反应中, C—X 较 易 断 裂 ,使卤素原子生成负离子而离去。
元素 H C
Br
电负性 2.1 2.5
2.8
化学键 C—C C—H C—Br 键长/pm 154 110 194 键能(kJ/mol) 347.3 414.2 284.5
知识精讲
H H
s+. δ一 H- C÷Br
H H
δ+δ—
> C —Br键具有较强的极性,易断裂。
> 因此溴乙烷的反应活性出心烧增强。
提出问题1:溴乙烷 在水中能否电离出Br-
它是否为电解质 请设计实验证明。
AgNO (aq)+HNO
现 象 :—→无浅黄色沉淀
结论:C H Br是非电解质,
C H Br 不能电离出Br-
知识精讲
对CH CH Br 化学性质的探索
知识精讲
请同学们尝试写出溴乙烷与水发生反应的方程式。
资料卡片:
C H Br与水的反应要在 碱性环境下才容易进行
C-Br 键较易断裂,预测Br-离去后,碳原子易与带负电荷的
OH-结合而生成乙醇,这说明结构决定性 质。
HH
—9—
+H O
知识精讲
实验装置 ①
实验现象 ①中溶液分层。②中有机层厚度减小。④中有淡黄色沉淀生成。 实验解释 溴乙烷与NaOH溶液共热,产生了Br-
水
C H Br+NaOH ^ C H OH+NaBr
NaBr+AgNO —AgBrl+NaNO
实验条件:NaOH水溶液、加热
1 mL 5%
NaOH
溶液
振荡
10~15
滴溴乙
烷 ②
上层
-水溶液
2 滴 硝 酸银
静置 分层
l mL 稀硝
0 溶液
③ 酸
④
0
知识精讲
如何用实验证明该反应的发生
①C H Br AgNO 溶液。不合理
②C H Br Na 溶液 AgNO 溶液、 不合理
③C H Br NaO 溶液 AgNO 溶液 合理
溴乙烷中不存在溴离子,溴乙烷是非电解质,不能电离。
因 为Ag++OH-=AgOH ( 白 色) 2 AgOH=Ag O(褐色)+H O;
黑褐色掩蔽AgBr的浅黄色,干扰产物检验。所以必须用硝酸酸化!
硝酸酸化
上层清液
加
取
△
H
△
OH
小结卤代烃中卤元素的检验:
卤代烃 Na H (水) 取上层清液
液
溶
NO
H
AgNO
过量
白色
有沉淀产生→淡 黄 色
黄色
知识精讲
◆溴乙烷的取代反应(也叫水解反应)
反应条件:NaOH水溶液、加热
反应原理:羟 基取代溴原子
NaOH+HBr ==NaBr+H O
CH CH Br+NaOH CH CH OH+NaBr
推广:所有卤代烃在碱性水溶液中都会发生水解反应
总反应:
知识精讲
用何种波谱可以方便地检验产物中有乙醇生成
①红外光谱
②核磁共振氢谱
学以致用 1. 写出CH Cl 、CH CHCICH 、1,3- 二溴丙烷分别与NaOH的水溶液
发生反应的化学方程式。
②卤素原子直接与苯环相连的卤代芳香烃水解反应条件比较苛刻
①所有卤代烃在一定条件下都能发生水解。
规律:
知识精讲
溴乙烷的消去反应(也叫消除反应)
实验条件:与NaOH的醇溶液共热
C H Br
NaOH +乙 醇
作为溶剂
溴水
知识精讲
实 质:相邻的两个C 上脱去HX 形成不饱和键!
化学键的变化:断裂C-Br 和邻位碳原子上的C-H, 形 成 C=C
>消去反应:有机化合物在一 定条件下,从一个分子中脱去一个小分 子 ( 如H O、HX 等),而生成不饱和(含双键或三键)化合物的反应。P 4
知识精讲
(1)分析反应产生的气体中可能含有哪些杂质 会不会对乙烯。
的检验产生干扰 可能的杂质气体:溴乙烷(沸点:38.4℃)、乙醇、水蒸汽
(2)生成的气体通入高锰酸钾溶液前要先通入盛水的试管
(3)还可以用什么方法鉴别乙烯,这一方法还需要将生成的气体 先通入盛水的试管中吗
(2)乙醇能使酸性高锰酸钾溶液褪色,
除去乙醇,排除干扰。
(3)溴水或溴的四氯化碳溶液;不用 ,
因为乙醇不能使溴水褪色。 水
取反应后的液体加入稀硝酸酸化后,加硝酸银
溶液,有什么现象 不酸化可行吗
有浅黄色沉淀生成。不行,因 为反应环境呈碱性。
气体
水解反应(取代反应)
消去反应
反应物 CH CH Br 水
CH CH Br
反应条件 NaOH水溶液,加热
NaOH醇溶液,加热
断键 C一Br
C一Br,邻碳C一H
生成物 CH CH OH、 NaBr
CH =CH 、 NaBr、H O
结论 C H Br和NaOH在 不同条件下发生不同类型的反应
知识精讲
我们还学过哪个消去反应 CH —CH
…..
口诀:“有醇则无醇,无醇则有醇”
消去反应 水解反应
比较溴乙烷的取代反应和消去反应,并完成下表。
CH =CH 个+ H O
浓H SO 170℃
学 以致用
2.分析下列物质是否发生消去反应,消去产物有几种
①CH I ② ③
④ CH CHBr ⑤ ⑥
苯环上的H不能被消去!
消去反应的发生条件
1、邻位碳原子上必须有氢原子(β-H), 否 则不能发生消去反应。
2 、NaOH的乙醇溶液、加热。
归 纳 总 结
反应类型 取代反应 消去反应 反应物 CH CH CH CH Br +水 CH CH CH CH Br
反应条件 NaOH水溶液,加热 NaOH醇溶液,加热
生成物 CH CH CH CH OH、NaBr CH CH CH=CH 、NaBr、H
O
结论 1-溴丁烷和NaOH在不同条件下发生不同类型的反应
知识精讲
【比较与分析】
比较1-溴丁烷的取代反应和消去反应,完成下表,分析反应条件对化学反应的
影响。
知识精讲
【讨论】
(1)如图3-3所示,为什么要在气体通入酸性高锰酸钾溶液前先通入盛水的试 管 除了酸性高锰酸钾溶液,还可以用什么方法检验丁烯 此时还有必要将气体先
通入水中吗
因受热而挥发的乙醇也能使高锰酸钾褪色,
所以要先通过水除去乙醇,防止干扰实验。
还可以 利用溴水、溴 的CCl 溶液检验丁烯。
此时不需要先通入水中。
乙醇与溴不反应,不会干扰乙烯的检验。
知识精讲
(2)预测2-溴丁烷发生消去反应的可能产物。
消去反应规则:当有多个产物时,以消H少的C 原子上的H为主
2-丁烯(主产物)
1 -丁烯
CH -CH =CH-CH
CH -CH -CH=CH
“雪上加霜”
A、CH Cl 无相邻C
CH
(主产物)CH -CH =C-CH
CB-Ch-C-C
B、CH —CH一CH
Br CH =CH-CH
CI
苯环上为独特的碳碳键
Cl CH CI
CH
学 以致用
3.下列卤代烃能否发生消去反应 若能,请写出有机产物的结构简式:
关键:抓住断键方式
学 以致用
4.写出由CH BrCH Br 与NaOH醇溶液共热的反应化学方程式
规律:
二卤代烃发生消 去反应后可能在 有机化合物中引 入碳碳三键或两 个碳碳双键。
注意:不能同时消去2个卤素原子!!!
归纳总结
扩展: 卤代烃中卤素原子的检验方法:
①原理:通过水解反应将卤素原子转化为卤素离子
水溶液 过量HNO 溶液AgNO 溶液AgCl 酸化 AgBr
该步骤必不可少 AgI
> 不能 利用消去反应检验卤素原子;
因 为不是所有的卤代烃都能发生消去反应。
无沉淀
白色沉淀 浅黄色沉淀 黄色沉淀
②操作过程:
NaOH
R-X
△
能否改为“NaOH 醇 溶液”
取上层清液
笔记
AgF
3、有两个邻位碳原子,且碳原子上均有氢原子时,发生消去
反应可能生成多种产物。
例如: 发生消去反应的产物为:
—CH —CH CH —CH=CH—CH
1、没有邻位碳原子的卤代烃不能发生消去反应,如CH Br。
2、有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也 不能发生消去反应。
例如: CH Cl
卤代烃的消去反应规律
归纳总结
⑥
卤代烃的应用:
1.连接烃和烃的衍生物的桥梁
2.改变官能团的个数
3.改变官能团的位置
4.对官能团进行保护
归纳总结
烃、卤代烃、醇之间的衍变类系
⑤
③
CH =CH CH CH -Cl
CH CH - OH
随堂检测
1.下列化合物在一定条件下,
既能发生水解反应,又能发生消去反应的有 。
CH CHBrCH
CH =CHBr
CH I
CH CI
√③(CH ) CCI
CH Br
> 但卤代烃中无相邻C 或相邻C 上无H 的不 能发生消去反应
> 所有的卤代烃都能发生水解反应!
注意:
H , 催化剂 ① ④ Br 足量浓NaOH D乙醇溶液 △ E ⑤ 光照 ② 适量Br ⑥ HBr F1 ⑦ HBr F2 ⑧
G1
G2
G1
随堂检测
2.烯烃A在一定条件下可按下面的框图进行反应:
③HBr 已知D结构简式为:
H C CH
(1)A的结构简式为CH - C=C- CH
(2)框图中属于取代反应的是_②
(3)框图中①③⑥属于什么反应 加成反应
F1和F2是同分异构体;
G1 和G2互为同分异构体。
E 结构简式为:
H C CH
CH =C-C= CH
Br ,
C
B
