2.3物质的量单位——摩尔高一化学人教版(2019)必修第一册(共20张PPT)
文档属性
| 名称 | 2.3物质的量单位——摩尔高一化学人教版(2019)必修第一册(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-14 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
第三节 物质的量
第1课时物质的量的单位——摩尔
3.运用物质的量、摩尔质量之间的相互关系进行简单计算
4.能从物质的量的角度认识物质的组成及变化
1 了解物质的量、阿伏加德罗常数、摩尔质量的含义
2.建立物质的量的概念
怎样称一个原子
原子太小 —
分割
集体
求和
求商
象太大
曹冲称象
1个O原子 2.6578×10-23g
不好称
1万个O原子 10 ×2.6578×10-23g=2.6578×10-18g
不好称
1023个O原子 102 ×2.6578×10-23g=2.6578g
能称但不方便
6.02×1023个O原子 6.02×102 ×2.6578×10-23g=16g
很好称
“集体”的数目选择多少呢
6.02×1023
日常生活中,当某物质的质量很大时,一般不会用两或克表示,而用吨等
更大的计量单位表示,如一辆汽车的质量为3吨,不会说是3×106克。再如做某 事化去10分钟时间,我们不会说成是用了1.9×10-5年。人们喜欢选用一个合适
能否在宏观(可测)量与微观量之间建立一个物理量和单位,用合适的数值表
示很大数目的微观粒子。
的计量单位,把很大或很小的数值变为适中,利于计算、使用。
物理量 单位名称
单位符号
长度 米
m
质量 千克
Kg
时间 秒
S
电流 安[培]
A
热力学温度 开[尔文]
K
物质的量 摩尔(简称摩)
mol
发光强度 坎[德拉]
cd
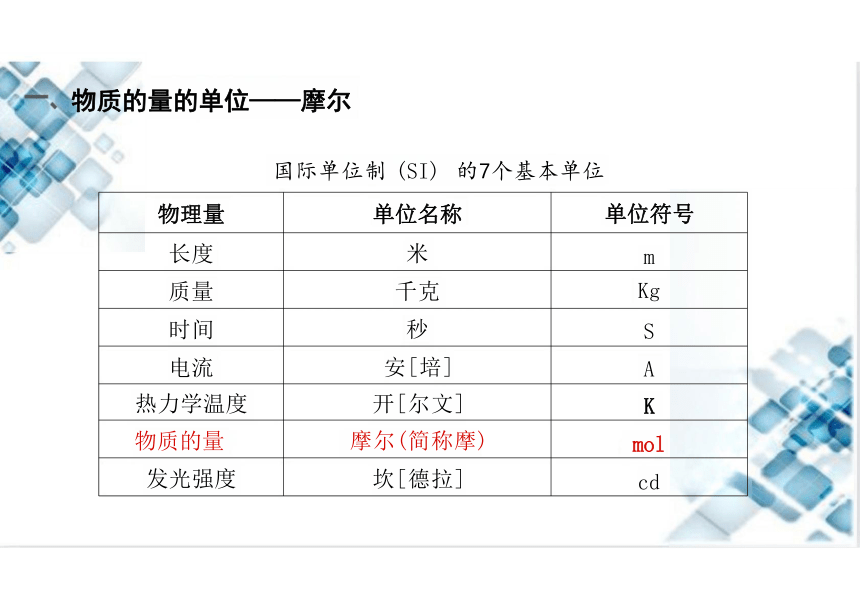
物质的量的单位——摩尔
国际单位制 (SI) 的7个基本单位
物质的量的单位——摩尔
0.012kg1 C的原子数目为1摩尔
表示含有一定数目粒子的集合体
②符号: n
③单位: 摩尔,简称摩(符号为mol)
1 mol氧 ×,指代不明,可指氧原子也可指氧分子
3 mol CO √
1 mol 空气 √,可以是混合物,指的是空气中的气体分子
1 mol质子 √
10 mol OH- √
判断下列说法是否正确
1 mol苹果 ×,不能指宏观物质
√,指氧原子
②符号: n
③单位: 摩尔,简称摩(符号为mol)
④适用范围: 原子、分子、离子、质子、中子、电子等微观粒子
1 . 物质的量 0.012kg1 C的原子数目为1摩尔
① 概念: 表示含有一定数目粒子的集合体
一、物质的量的单位——摩尔
6.02×1023个H的质量
1g
6.02×1023个O的质量
16g
6.02×1023个Fe的质量
56g
6.02×1023个C的质量
12g
6.02×1023个OH-的质量
17g
6.02×1023个SO 2-的质量
96g
物质的量的单位——摩尔
1mol微粒到底是多少呢 0.012kg
C的原子数目为1mol
一 、物质的量的单位——摩尔
2 .阿伏加德罗常数(NA)
国际上规定,1mol粒子集合体所含的粒子数约为6.02×1023。
1 mol任何粒子的粒子数叫做阿伏伽德罗常数。
② 符号:
③单位:
NA
m ol-1
一 、物质的量的单位——摩尔
下列说法正确吗
(1)6.02×1023就是阿伏加德罗常数.
(2)1molH O含有6.02×1023个分子。
注意
· 阿伏加德罗常数是一个物理量,有单位,而不是纯数,不能误认为NA就
是6.02×1023。
· 在应用时采用近似值6.02×1023mol
(1)1 mol O约含有6.02×1023_个氧原子
(2)5 molO约含有3.01×1024 个 氧 原 子
(3)6.02×1024个氧原子的物质的量约为10 mol 。
思考与交流:
粒子个数 (N)、
物质的量 (n)
微粒数目 (N)
阿伏加德罗常数(NA)
阿伏加德罗常数 (NA) 、 物质的量 (n) 三者的关系
(4)1.806×1023个硫酸分子的物质的量约为0.3mol 。
变式:N=n.NA或NA=N/n
二
6.02×1023个H的质量
1g
6.02×1023个O的质量
16g
6.02×1023个Fe的质量
56g
6.02×1023个C的质量
12g
6.02×1023个OH-的质量
17g
6.02×1023个SO 2-的质量
96g
相对原子(分子)质量
1
16
56
12
17
96
1mol 任何粒子或物质的质量以克为单位时,在数值都与该粒子的相对原子质量或相
对分子质量相等。
你知道500g水里面有多少个水分子吗
二 、摩尔质量
①概念: 单位物质的量的物质所具有的质量叫做摩尔质量
② 符号: M
③单位: g/mol(g·mol- )
④表达式:
二 、摩尔质量
AI的相对原子质量为 27 ,AI的摩尔质量为27gmor ,
1molA1的质量为 27g,2molAl 的 质 量 为 _ 5 4g ,
81gAl的物质的量为_3 mol。
2 、H O 的相对分子质量为18 , H O 的摩尔质量为18 g.mor ,
0.5molH O 的质量为 _9 g , 约 含 有 _3.01×1023 个水分子,
18g H O约含有6.02×1023 _个水分子。
请从定量角度描述这一化学反应的含义
C 十 O
宏观 12g碳 32g氧气
物质的量1mol 1mol
微观6.02×1023 6.02×1023
1mol
6.02×1023
1个二氧化碳分子
CO
44g二氧化碳
粒子数1个碳原子1个氧分子
物质的量
点燃 二二
C.1 mol 任何物质都含有阿伏加德罗常数个原子
D.物质的量适用于计量分子、原子、离子等粒子
2.已知硫酸中含有3.01×1023个氧原子,硫酸的物质的量是
A.0.500 mol B.1.00 mol
C.0.250 mol D.0.125 mol
1.下列说法中错误的是 C
A.物质的量是表示含有一定数目粒子的集合体的物理量
B.使用摩尔作单位时必须指明微粒的名称
3.下列关于阿伏加德罗常数的说法错误的是
A.6.02×1023 就是阿伏加德罗常数
B.1 mol水中约含有6.02×1023个水分子
C.含有阿伏加德罗常数个粒子的物质的量是1 mol
D.1 mol氨气所含的原子数约为2.408×1024
4.40.5 g某金属氯化物RCl 含有0.6 mol 氯离子,则金属R 的摩尔质量为
A.135 g B.135 g·mol-1 C.64 g D.64 g·mol-1
A
是阿伏加德罗常数的值。下列说法正确的是
A.该原子的摩尔质量是aNA
B.Wg 该原子的物质的量是
C.Wg 该原子中含有 个该原子
D.由已知信息可得
课堂反馈
5.科学家发现了某种元素的一个原子,其质量是a g, 一个12C 原子的质量是bg,NA
B
第三节 物质的量
第1课时物质的量的单位——摩尔
3.运用物质的量、摩尔质量之间的相互关系进行简单计算
4.能从物质的量的角度认识物质的组成及变化
1 了解物质的量、阿伏加德罗常数、摩尔质量的含义
2.建立物质的量的概念
怎样称一个原子
原子太小 —
分割
集体
求和
求商
象太大
曹冲称象
1个O原子 2.6578×10-23g
不好称
1万个O原子 10 ×2.6578×10-23g=2.6578×10-18g
不好称
1023个O原子 102 ×2.6578×10-23g=2.6578g
能称但不方便
6.02×1023个O原子 6.02×102 ×2.6578×10-23g=16g
很好称
“集体”的数目选择多少呢
6.02×1023
日常生活中,当某物质的质量很大时,一般不会用两或克表示,而用吨等
更大的计量单位表示,如一辆汽车的质量为3吨,不会说是3×106克。再如做某 事化去10分钟时间,我们不会说成是用了1.9×10-5年。人们喜欢选用一个合适
能否在宏观(可测)量与微观量之间建立一个物理量和单位,用合适的数值表
示很大数目的微观粒子。
的计量单位,把很大或很小的数值变为适中,利于计算、使用。
物理量 单位名称
单位符号
长度 米
m
质量 千克
Kg
时间 秒
S
电流 安[培]
A
热力学温度 开[尔文]
K
物质的量 摩尔(简称摩)
mol
发光强度 坎[德拉]
cd
物质的量的单位——摩尔
国际单位制 (SI) 的7个基本单位
物质的量的单位——摩尔
0.012kg1 C的原子数目为1摩尔
表示含有一定数目粒子的集合体
②符号: n
③单位: 摩尔,简称摩(符号为mol)
1 mol氧 ×,指代不明,可指氧原子也可指氧分子
3 mol CO √
1 mol 空气 √,可以是混合物,指的是空气中的气体分子
1 mol质子 √
10 mol OH- √
判断下列说法是否正确
1 mol苹果 ×,不能指宏观物质
√,指氧原子
②符号: n
③单位: 摩尔,简称摩(符号为mol)
④适用范围: 原子、分子、离子、质子、中子、电子等微观粒子
1 . 物质的量 0.012kg1 C的原子数目为1摩尔
① 概念: 表示含有一定数目粒子的集合体
一、物质的量的单位——摩尔
6.02×1023个H的质量
1g
6.02×1023个O的质量
16g
6.02×1023个Fe的质量
56g
6.02×1023个C的质量
12g
6.02×1023个OH-的质量
17g
6.02×1023个SO 2-的质量
96g
物质的量的单位——摩尔
1mol微粒到底是多少呢 0.012kg
C的原子数目为1mol
一 、物质的量的单位——摩尔
2 .阿伏加德罗常数(NA)
国际上规定,1mol粒子集合体所含的粒子数约为6.02×1023。
1 mol任何粒子的粒子数叫做阿伏伽德罗常数。
② 符号:
③单位:
NA
m ol-1
一 、物质的量的单位——摩尔
下列说法正确吗
(1)6.02×1023就是阿伏加德罗常数.
(2)1molH O含有6.02×1023个分子。
注意
· 阿伏加德罗常数是一个物理量,有单位,而不是纯数,不能误认为NA就
是6.02×1023。
· 在应用时采用近似值6.02×1023mol
(1)1 mol O约含有6.02×1023_个氧原子
(2)5 molO约含有3.01×1024 个 氧 原 子
(3)6.02×1024个氧原子的物质的量约为10 mol 。
思考与交流:
粒子个数 (N)、
物质的量 (n)
微粒数目 (N)
阿伏加德罗常数(NA)
阿伏加德罗常数 (NA) 、 物质的量 (n) 三者的关系
(4)1.806×1023个硫酸分子的物质的量约为0.3mol 。
变式:N=n.NA或NA=N/n
二
6.02×1023个H的质量
1g
6.02×1023个O的质量
16g
6.02×1023个Fe的质量
56g
6.02×1023个C的质量
12g
6.02×1023个OH-的质量
17g
6.02×1023个SO 2-的质量
96g
相对原子(分子)质量
1
16
56
12
17
96
1mol 任何粒子或物质的质量以克为单位时,在数值都与该粒子的相对原子质量或相
对分子质量相等。
你知道500g水里面有多少个水分子吗
二 、摩尔质量
①概念: 单位物质的量的物质所具有的质量叫做摩尔质量
② 符号: M
③单位: g/mol(g·mol- )
④表达式:
二 、摩尔质量
AI的相对原子质量为 27 ,AI的摩尔质量为27gmor ,
1molA1的质量为 27g,2molAl 的 质 量 为 _ 5 4g ,
81gAl的物质的量为_3 mol。
2 、H O 的相对分子质量为18 , H O 的摩尔质量为18 g.mor ,
0.5molH O 的质量为 _9 g , 约 含 有 _3.01×1023 个水分子,
18g H O约含有6.02×1023 _个水分子。
请从定量角度描述这一化学反应的含义
C 十 O
宏观 12g碳 32g氧气
物质的量1mol 1mol
微观6.02×1023 6.02×1023
1mol
6.02×1023
1个二氧化碳分子
CO
44g二氧化碳
粒子数1个碳原子1个氧分子
物质的量
点燃 二二
C.1 mol 任何物质都含有阿伏加德罗常数个原子
D.物质的量适用于计量分子、原子、离子等粒子
2.已知硫酸中含有3.01×1023个氧原子,硫酸的物质的量是
A.0.500 mol B.1.00 mol
C.0.250 mol D.0.125 mol
1.下列说法中错误的是 C
A.物质的量是表示含有一定数目粒子的集合体的物理量
B.使用摩尔作单位时必须指明微粒的名称
3.下列关于阿伏加德罗常数的说法错误的是
A.6.02×1023 就是阿伏加德罗常数
B.1 mol水中约含有6.02×1023个水分子
C.含有阿伏加德罗常数个粒子的物质的量是1 mol
D.1 mol氨气所含的原子数约为2.408×1024
4.40.5 g某金属氯化物RCl 含有0.6 mol 氯离子,则金属R 的摩尔质量为
A.135 g B.135 g·mol-1 C.64 g D.64 g·mol-1
A
是阿伏加德罗常数的值。下列说法正确的是
A.该原子的摩尔质量是aNA
B.Wg 该原子的物质的量是
C.Wg 该原子中含有 个该原子
D.由已知信息可得
课堂反馈
5.科学家发现了某种元素的一个原子,其质量是a g, 一个12C 原子的质量是bg,NA
B
