7.3 乙酸 高一化学人教版(2019)必修2(共32张PPT)
文档属性
| 名称 | 7.3 乙酸 高一化学人教版(2019)必修2(共32张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-14 00:00:00 | ||
图片预览









文档简介
(共32张PPT)
舌尖上的有机物 ——乙酸
1、掌握乙酸物理性质
2、能认识乙酸弱酸性并书写相关反应
3、能书写乙酸分子式、结构式、结构简式、 官能团等。
4、能推理酯化反应的断键情况并书写方程式。
学习目标
学习反馈——问题一
总结香醋的酿造的酿造过程;
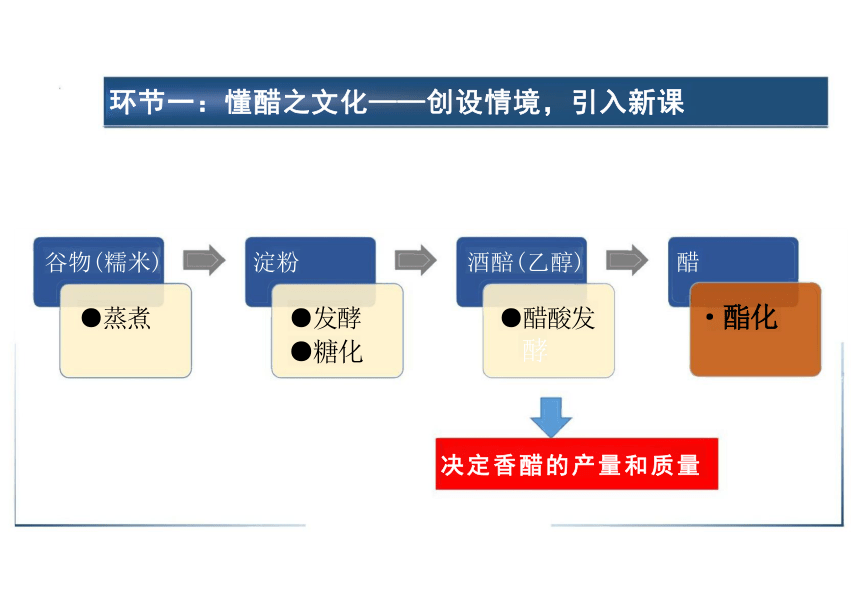
环节一:懂醋之文化——创设情境,引入新课
谷物(糯米) 淀粉 酒醅(乙醇) 醋
●蒸煮 ●发酵 ●醋酸发 ·酯化 ●糖化 酵
决定香醋的产量和质量
环节一:懂醋之文化——创设情境,引入新课
观察食用白醋,结合生活经验,总结乙酸有哪些物 理性质
作为常见调味品的食醋,其中含有3%~5%的乙酸, 乙酸又被称为醋酸
1.在洗澡水中加适量的醋,对毛孔起到缩小的作用。 可以使皮肤变得光滑细腻
2.白醋:甘油为5:1混合(即5滴白配1滴甘油),常 搽皮肤能使皮肤湿润,减少黑色素沉积。
3.民间偏方有熏蒸食醋一说,就是把醋放在容器里置 于火上,把醋烧开让它在室内挥发,杀灭房间的病 菌,来预防感冒。
醋中的重要成分——乙酸的物理性质
醋中的重要成分——乙酸
数据
乙酸
熔点:16.6℃
沸点:118 ℃
密度:1.05 g/cm
纯净的乙酸又称冰醋酸
1、关于乙酸的下列说法中不正确的是( D )
A 乙酸易溶于水和乙醇。
B 无水乙酸又称冰醋酸,它是纯净物。
C 乙酸是一种重要的有机酸,是有刺激性气味的液体。
D 在标准状况下醋酸是一种无色有强烈刺激性气味的液体
巩固练习
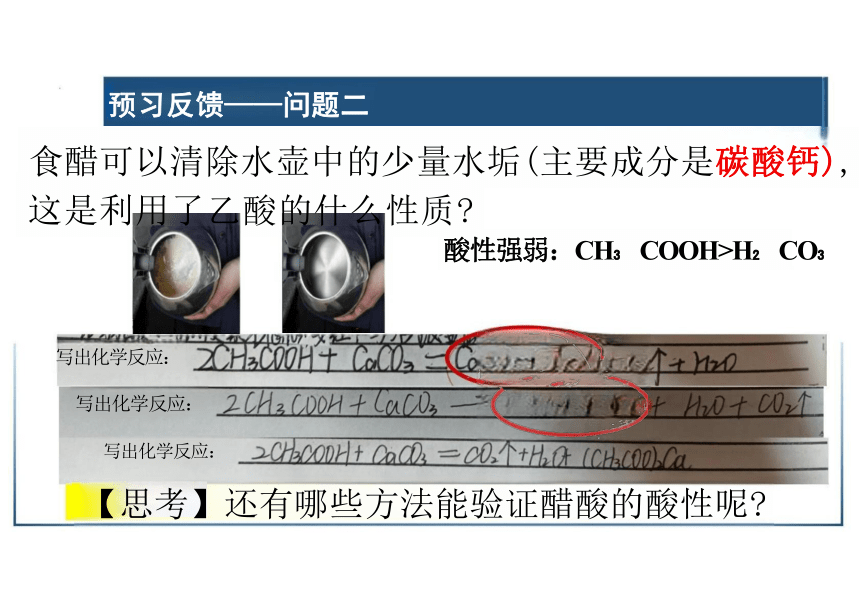
食醋可以清除水壶中的少量水垢(主要成分是碳酸钙),
这是利用了乙酸的什么性质
酸性强弱:CH COOH>H CO
写出化学反应:
写出化学反应:
写出化学反应:
预习反馈——问题二
【思考】还有哪些方法能验证醋酸的酸性呢
实验用品
醋酸、镁条、紫色石蕊溶液、碳酸盐
醋酸的酸性验证方案:
(1)与指示剂作用:使紫色石蕊变红
(2)活泼金属反应:有气泡产生,反应放热
(3)与碳酸盐反应:产生气体 (CO )
乙酸的酸性
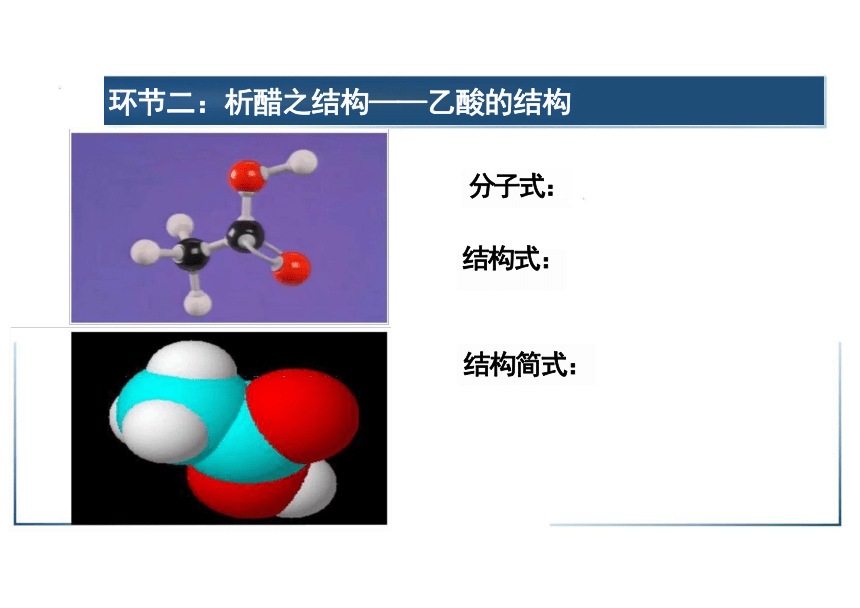
环节二:析醋之结构——乙酸的结构
分子式:
结构式:
结构简式:
环节二:析醋之结构—乙酸的结构
CH COOH 中哪个H 能电离呢
乙烷结构简式: CH ——CH
H 0
乙酸结构简式 :H- C-C-0-H 或 —COOH
官能团:决定醋酸化学性质的基团——羧基
环节三:探醋之辛酸——乙酸酸性的探究
1 . 弱 酸 性 :CH COOH —CH CO0-+H+
(1)使指示剂变色 使紫色石蕊试液变红
(2)与金属反应(Na) 2Na+2CH COOH→2CH COONa+H 个
(3)与碱性氧化物反应(CuO) CuO+2CH COOH→(CH CO0) Cu+H O
(4)与碱反应(NaOH) NaOH+CH COOH→CH COONa+H O
(5)与盐反应(Na CO )
Na CO +2CH COOH →2CH COONa+CO 个+H O
(6)与酸式盐反应(NaHCO )
NaHCO +CH COOH →CH COONa+CO 个+H O
乙酸的酸性
1.具有弱酸性 酸性:HCI> CH COOH >H CO
CH COOH— CH CO0-+H+
上好课
XUE KE wa 步 高
环节三:探醋之辛酸——乙酸酸性的探究
拿小本记下来
醋酸的生产工艺
酒醅(乙醇)
●醋酸发
酵
淀粉
●发酵 ●糖化
谷物(糯米)
●蒸煮
醋
·酯 化
决定香醋的质量
ch C-OH +HO-c H 二 CH C-o-C H +H O
实验用品:乙醇、冰醋酸、浓硫酸、乙酸、乙醇、
碎瓷片
【交流讨论】在实验仪器组装和实
验操作中有哪些注意事项
乙醇和乙酸反应装置图
环节四:品酯之醇香——乙酸的酯化反应
资料卡片
酯化酶 I
【c实n 】-OH +HO-C H; CH C- 、 +、H O
在一支试管中加入3 mL 乙醇,然后边振荡试管
边慢慢加入2 mL 浓 H SO 和2 mL 乙酸,
再加入几片碎瓷片。连接好装置,用酒精灯小
心加热,
将产生的蒸气经导管通到饱和Na CO 溶液的液
面上,观察现象。
乙醇和乙酸反应装置图
乙醇
H
酸
-C
乙
0
环节四:品酯之醇香——乙酸的酯化反应
资料卡片
浓硫酸
O
LI
酯化反应
实验交流
实验现象:液体分层,上层有无色油状液体 生成,有特殊香味
环节四:品酯之醇香——乙酸的酯化反应
酯一般密度比水小,难溶于水,易溶于乙醇、乙醚等有机溶剂。
酯是有芳香气味的液体,存在于各种水果和花草中。
酯类
酯类物质
乙酸乙酯
乙酸异戊酯
戊酸戊酯
1.药品的装入顺序如何 乙醇→浓硫酸 → (冷却后)乙酸 2.浓硫酸的作用是什么 催化剂、吸水剂 3.得到的反应产物主要杂质有哪些 乙酸、乙醇 A
4.用饱和Na CO 溶液接收的作用 导管不能
①中和乙酸②吸收乙醇 ③降低酯在水中的溶解度 饱 和Na Co 溶液
B
④提高水溶液的密度以加速乙酸乙酯与 水溶液的分层
【 拓 展 】碳酸钠溶液中滴入酚酞, 反应后分层明显,但震荡后红色 变浅,这是为何
物质 沸点/℃ 密度/(g/mL)
水溶性
乙酸 117.9 1.05
易溶
乙醇 78.5 0.7893
易溶
乙酸乙酯 77 0.90
微溶
环节四:品酯之醇香—乙酸的酯化反应
环节四:品酯之醇香——乙酸的酯化反应
浓硫酸
CH C-OH +HO一C H CH C-o-C H +H O
思考:乙醇和乙酸形成乙酸乙酯的断键方式
CH COOH+HSOC H 浓硫酸、H O+CH COSOC H
浓硫酸
CH CO0H+QC H △H SO+CH COOC H
思考:如何判断乙酸与乙醇反应,哪种物质提供—H, 哪种物质提供—OH
同位素示踪
环节四:品酯之醇香——乙酸的酯化反应
可能一
可能二
乙酸酯化反应机理
思考:如何判断乙酸与乙醇反应,哪种物质提供—H,哪种物质提供—OH
同位素示踪
CH COoH±H -QC H 浓硫酸 H O+CH COSOC H
可能二 CH Coof+ @C H ; H 四O+CH COOC H
浓硫酸
环节四:品酯之醇香——乙酸的酯化反应
酸脱羟基醇脱氢
取代反应
酯化反应
羧酸 + 醇 酯 水
举 例 乙酸 乙醇 乙酸乙酯
推广 某酸 某醇 某酸某酯
CH C- o -CH + H O
乙酸甲酯
H C-o- CH CH +H O
甲酸乙酯
—O—R
浓 H SO
CH COOH+HOCH
HCOOH+HOCH CH 浓H SQ
入
酸与醇反应生成酯和水的反应——酯化反应
酯基
1.加热蒸馏后,在饱和Na CO 溶液的液面上得到 无色油状液体,下列叙述正确的是( C )
A.浓硫酸只是乙酸与乙醇反应的催化剂 B.乙醇可以全部反应 C.反应前的混合液中应加入碎瓷片 D.导气管口应插入液面以下
a
b 饱和
Na CO 溶液
酯化反应
环节五:明醋之用途——幽幽醋香,无醋不在
乙酸用途
有机化工原料
除水垢
喷漆溶剂
醋酸纤维
合成纤维
香料
调味品
医药
结构
有机物
用途 性质
思维建模-课堂小结
关于乳酸的说法不正确的是 (A)
A.乳酸中不含羟基
B.乳酸中含有两种官能团
C.1mol乳酸与足量金属钠反应
可生成1molH
D.乳酸与氢氧化钠可以反应
模型应用一习题巩固
2.下列说法正确的是 ( D )
A. 乙酸中含有双键,因此属于不饱和烃
B. 在标准状况下醋酸是一种无色有强烈刺激性气味 的液体
C. 乙酸分子中含有两种官能团
D. 乙酸的结构简式可以写成CH COOH
巩固练习
3.乙酸和乙醇在浓硫酸的催化下发生酯化反应时,乙酸分子
中断键的位置是( B ),乙酸体现酸性时断键的位置是
(C )
巩固练习
B.b
D.d
A.a
C.c
4.食醋中含有乙酸,下列关于乙酸的说法正确的是(A )
A.乙酸是有刺激性气味的酸
B.乙酸不属于一元酸
C. 乙酸在常温下就很容易发生酯化反应
D.乙酸酸性较弱,能使紫色的石蕊溶液变为蓝色
巩固练习
舌尖上的有机物 ——乙酸
1、掌握乙酸物理性质
2、能认识乙酸弱酸性并书写相关反应
3、能书写乙酸分子式、结构式、结构简式、 官能团等。
4、能推理酯化反应的断键情况并书写方程式。
学习目标
学习反馈——问题一
总结香醋的酿造的酿造过程;
环节一:懂醋之文化——创设情境,引入新课
谷物(糯米) 淀粉 酒醅(乙醇) 醋
●蒸煮 ●发酵 ●醋酸发 ·酯化 ●糖化 酵
决定香醋的产量和质量
环节一:懂醋之文化——创设情境,引入新课
观察食用白醋,结合生活经验,总结乙酸有哪些物 理性质
作为常见调味品的食醋,其中含有3%~5%的乙酸, 乙酸又被称为醋酸
1.在洗澡水中加适量的醋,对毛孔起到缩小的作用。 可以使皮肤变得光滑细腻
2.白醋:甘油为5:1混合(即5滴白配1滴甘油),常 搽皮肤能使皮肤湿润,减少黑色素沉积。
3.民间偏方有熏蒸食醋一说,就是把醋放在容器里置 于火上,把醋烧开让它在室内挥发,杀灭房间的病 菌,来预防感冒。
醋中的重要成分——乙酸的物理性质
醋中的重要成分——乙酸
数据
乙酸
熔点:16.6℃
沸点:118 ℃
密度:1.05 g/cm
纯净的乙酸又称冰醋酸
1、关于乙酸的下列说法中不正确的是( D )
A 乙酸易溶于水和乙醇。
B 无水乙酸又称冰醋酸,它是纯净物。
C 乙酸是一种重要的有机酸,是有刺激性气味的液体。
D 在标准状况下醋酸是一种无色有强烈刺激性气味的液体
巩固练习
食醋可以清除水壶中的少量水垢(主要成分是碳酸钙),
这是利用了乙酸的什么性质
酸性强弱:CH COOH>H CO
写出化学反应:
写出化学反应:
写出化学反应:
预习反馈——问题二
【思考】还有哪些方法能验证醋酸的酸性呢
实验用品
醋酸、镁条、紫色石蕊溶液、碳酸盐
醋酸的酸性验证方案:
(1)与指示剂作用:使紫色石蕊变红
(2)活泼金属反应:有气泡产生,反应放热
(3)与碳酸盐反应:产生气体 (CO )
乙酸的酸性
环节二:析醋之结构——乙酸的结构
分子式:
结构式:
结构简式:
环节二:析醋之结构—乙酸的结构
CH COOH 中哪个H 能电离呢
乙烷结构简式: CH ——CH
H 0
乙酸结构简式 :H- C-C-0-H 或 —COOH
官能团:决定醋酸化学性质的基团——羧基
环节三:探醋之辛酸——乙酸酸性的探究
1 . 弱 酸 性 :CH COOH —CH CO0-+H+
(1)使指示剂变色 使紫色石蕊试液变红
(2)与金属反应(Na) 2Na+2CH COOH→2CH COONa+H 个
(3)与碱性氧化物反应(CuO) CuO+2CH COOH→(CH CO0) Cu+H O
(4)与碱反应(NaOH) NaOH+CH COOH→CH COONa+H O
(5)与盐反应(Na CO )
Na CO +2CH COOH →2CH COONa+CO 个+H O
(6)与酸式盐反应(NaHCO )
NaHCO +CH COOH →CH COONa+CO 个+H O
乙酸的酸性
1.具有弱酸性 酸性:HCI> CH COOH >H CO
CH COOH— CH CO0-+H+
上好课
XUE KE wa 步 高
环节三:探醋之辛酸——乙酸酸性的探究
拿小本记下来
醋酸的生产工艺
酒醅(乙醇)
●醋酸发
酵
淀粉
●发酵 ●糖化
谷物(糯米)
●蒸煮
醋
·酯 化
决定香醋的质量
ch C-OH +HO-c H 二 CH C-o-C H +H O
实验用品:乙醇、冰醋酸、浓硫酸、乙酸、乙醇、
碎瓷片
【交流讨论】在实验仪器组装和实
验操作中有哪些注意事项
乙醇和乙酸反应装置图
环节四:品酯之醇香——乙酸的酯化反应
资料卡片
酯化酶 I
【c实n 】-OH +HO-C H; CH C- 、 +、H O
在一支试管中加入3 mL 乙醇,然后边振荡试管
边慢慢加入2 mL 浓 H SO 和2 mL 乙酸,
再加入几片碎瓷片。连接好装置,用酒精灯小
心加热,
将产生的蒸气经导管通到饱和Na CO 溶液的液
面上,观察现象。
乙醇和乙酸反应装置图
乙醇
H
酸
-C
乙
0
环节四:品酯之醇香——乙酸的酯化反应
资料卡片
浓硫酸
O
LI
酯化反应
实验交流
实验现象:液体分层,上层有无色油状液体 生成,有特殊香味
环节四:品酯之醇香——乙酸的酯化反应
酯一般密度比水小,难溶于水,易溶于乙醇、乙醚等有机溶剂。
酯是有芳香气味的液体,存在于各种水果和花草中。
酯类
酯类物质
乙酸乙酯
乙酸异戊酯
戊酸戊酯
1.药品的装入顺序如何 乙醇→浓硫酸 → (冷却后)乙酸 2.浓硫酸的作用是什么 催化剂、吸水剂 3.得到的反应产物主要杂质有哪些 乙酸、乙醇 A
4.用饱和Na CO 溶液接收的作用 导管不能
①中和乙酸②吸收乙醇 ③降低酯在水中的溶解度 饱 和Na Co 溶液
B
④提高水溶液的密度以加速乙酸乙酯与 水溶液的分层
【 拓 展 】碳酸钠溶液中滴入酚酞, 反应后分层明显,但震荡后红色 变浅,这是为何
物质 沸点/℃ 密度/(g/mL)
水溶性
乙酸 117.9 1.05
易溶
乙醇 78.5 0.7893
易溶
乙酸乙酯 77 0.90
微溶
环节四:品酯之醇香—乙酸的酯化反应
环节四:品酯之醇香——乙酸的酯化反应
浓硫酸
CH C-OH +HO一C H CH C-o-C H +H O
思考:乙醇和乙酸形成乙酸乙酯的断键方式
CH COOH+HSOC H 浓硫酸、H O+CH COSOC H
浓硫酸
CH CO0H+QC H △H SO+CH COOC H
思考:如何判断乙酸与乙醇反应,哪种物质提供—H, 哪种物质提供—OH
同位素示踪
环节四:品酯之醇香——乙酸的酯化反应
可能一
可能二
乙酸酯化反应机理
思考:如何判断乙酸与乙醇反应,哪种物质提供—H,哪种物质提供—OH
同位素示踪
CH COoH±H -QC H 浓硫酸 H O+CH COSOC H
可能二 CH Coof+ @C H ; H 四O+CH COOC H
浓硫酸
环节四:品酯之醇香——乙酸的酯化反应
酸脱羟基醇脱氢
取代反应
酯化反应
羧酸 + 醇 酯 水
举 例 乙酸 乙醇 乙酸乙酯
推广 某酸 某醇 某酸某酯
CH C- o -CH + H O
乙酸甲酯
H C-o- CH CH +H O
甲酸乙酯
—O—R
浓 H SO
CH COOH+HOCH
HCOOH+HOCH CH 浓H SQ
入
酸与醇反应生成酯和水的反应——酯化反应
酯基
1.加热蒸馏后,在饱和Na CO 溶液的液面上得到 无色油状液体,下列叙述正确的是( C )
A.浓硫酸只是乙酸与乙醇反应的催化剂 B.乙醇可以全部反应 C.反应前的混合液中应加入碎瓷片 D.导气管口应插入液面以下
a
b 饱和
Na CO 溶液
酯化反应
环节五:明醋之用途——幽幽醋香,无醋不在
乙酸用途
有机化工原料
除水垢
喷漆溶剂
醋酸纤维
合成纤维
香料
调味品
医药
结构
有机物
用途 性质
思维建模-课堂小结
关于乳酸的说法不正确的是 (A)
A.乳酸中不含羟基
B.乳酸中含有两种官能团
C.1mol乳酸与足量金属钠反应
可生成1molH
D.乳酸与氢氧化钠可以反应
模型应用一习题巩固
2.下列说法正确的是 ( D )
A. 乙酸中含有双键,因此属于不饱和烃
B. 在标准状况下醋酸是一种无色有强烈刺激性气味 的液体
C. 乙酸分子中含有两种官能团
D. 乙酸的结构简式可以写成CH COOH
巩固练习
3.乙酸和乙醇在浓硫酸的催化下发生酯化反应时,乙酸分子
中断键的位置是( B ),乙酸体现酸性时断键的位置是
(C )
巩固练习
B.b
D.d
A.a
C.c
4.食醋中含有乙酸,下列关于乙酸的说法正确的是(A )
A.乙酸是有刺激性气味的酸
B.乙酸不属于一元酸
C. 乙酸在常温下就很容易发生酯化反应
D.乙酸酸性较弱,能使紫色的石蕊溶液变为蓝色
巩固练习
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
