7.3 乙酸高一下学期化学人教版(2019)必修二(共33张PPT)
文档属性
| 名称 | 7.3 乙酸高一下学期化学人教版(2019)必修二(共33张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-08-14 00:00:00 | ||
图片预览








文档简介
(共33张PPT)
人教版化学必修2
舌尖上的有机物 — —乙酸
核心素养发展目标
1.了解乙酸的物理性质和用途,培养科学态度与社会责任。
2. 掌握乙酸的组成、结构和化学性质,培养变化观念与平衡思想。
3.掌握酯化反应的原理、实质和实验操作,能依据给出的问题,设计 简单的实验方案,培养科学探究与创新意识。
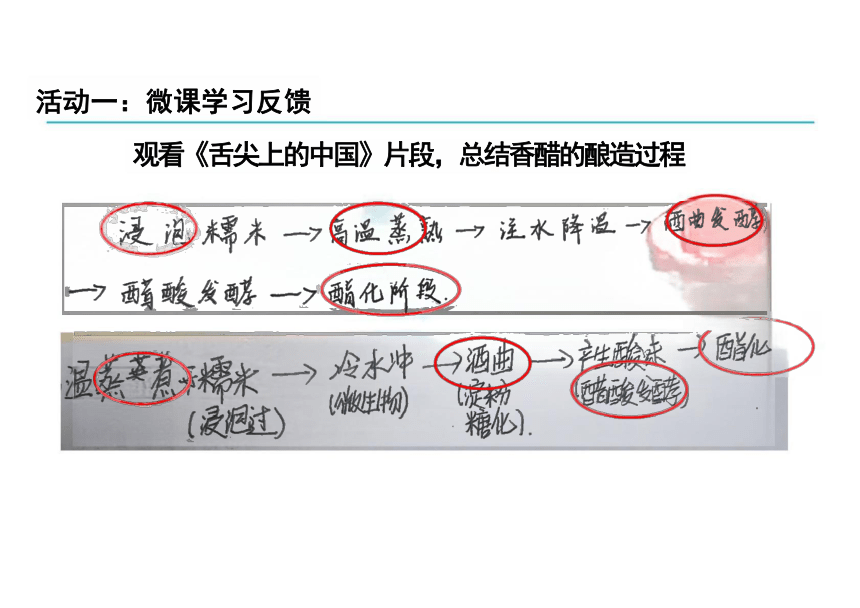
活动一:微课学习反馈
观看《舌尖上的中国》片段,总结香醋的酿造过程
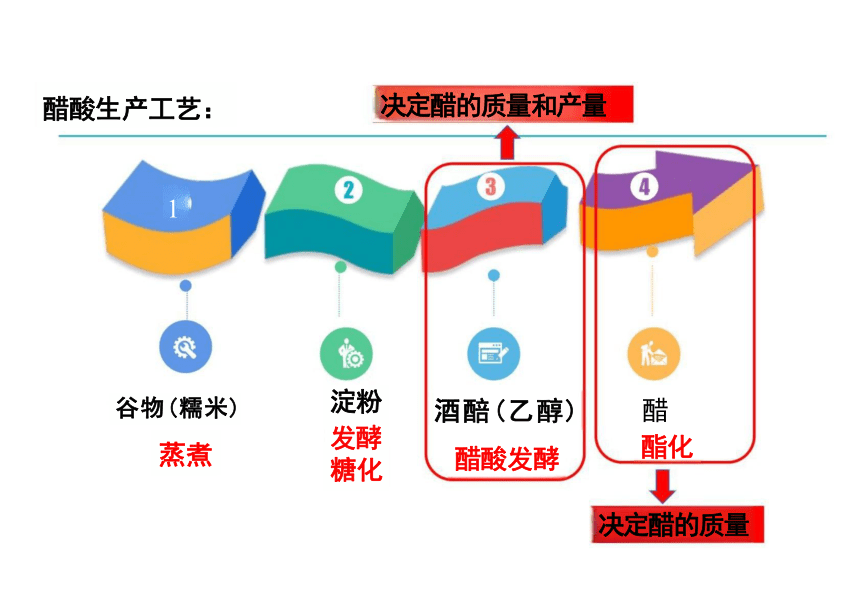
醋酸生产工艺:
1
谷物(糯米)
蒸煮
酒醅(乙醇)
醋酸发酵
决定醋的质量和产量
淀粉
发酵 糖化
决定醋的质量
醋
酯化
酉莒
醋的来历
活动二:观察思考
一、物理性质
乙酸(俗称醋酸)
颜色:无色透明
状态:液 体
气味:有强烈刺激性气味
沸点:118℃(易挥发)
熔点:16.6℃(无水乙酸又称为:冰醋酸) 溶解性:易溶于水、乙醇等溶剂
乙 酸
熔点:16.6 ℃ 沸点:118℃
密度:1.05 g/cm
数据
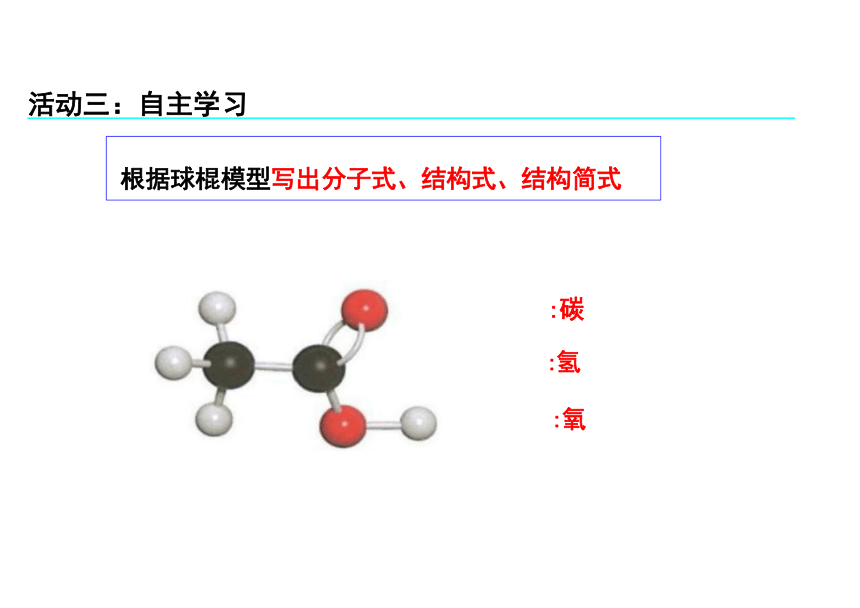
根据球棍模型写出分子式、结构式、结构简式
活动三:自主学习
:碳
:氢 :氧
H O
H-C-C-O-H
H
CH COOH
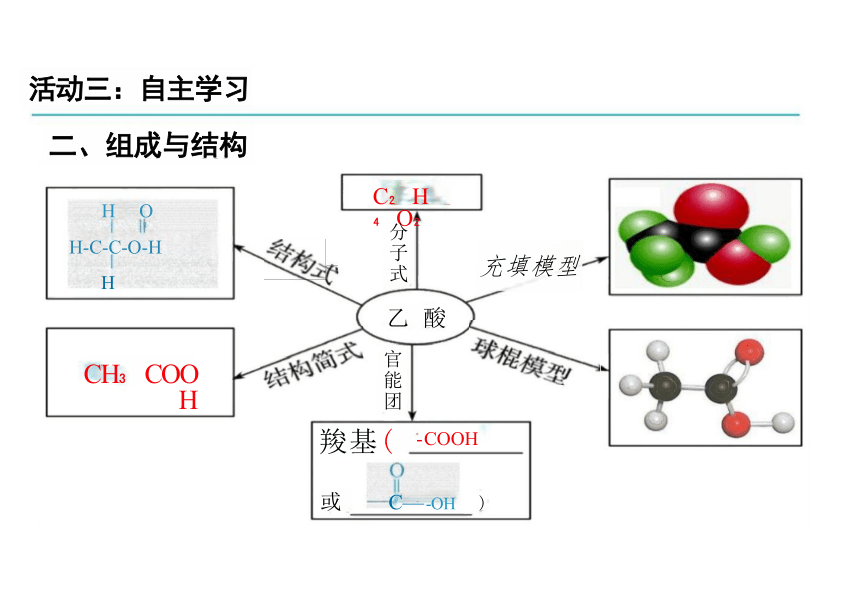
活动三:自主学习
二、组成与结构
羧基( -COOH
或 C— -OH )
充填模型
乙 酸
C H O
分子式
官能团
思 考 :食醋可以清除水壶中的少量水垢(主要成分是碳酸钙), 这是利用了乙酸的什么性质 请写出相关反应方程式。
2CH COOH+CaCO =(CH CO0) Ca+H O+CO 个 酸性:CH COOH>H CO
三、化学性质
1.酸性
活动四:认识乙酸的酸性
①与指示剂反应:使紫色石蕊变红
②与金属反应 (Na)2Na+2CH COOH==2CH COO N a+H 个
③与碱性氧化物反应(CuO)
2CH CO0H十CuO==(CH CO0) Cu+H O
④与碱反应(NaOH)
CH COOH+NaOH==CH COONa+H O
⑤与盐反应 (Na CO )
2CH COOH+Na CO ==2CH COONa+H O+CO 个
三 、乙酸的化学性质
1、酸性 :CH COOH是一种重要的有机酸,具有酸的通性。
电离方程式:CH COOH—CH CO0-+ H+ 一元弱酸
酸的通性
查阅资料,根据生活经验设计实验方案,比较乙 酸与碳酸、盐酸酸性强弱
课后思考
醋酸生产工艺:
①
谷物(糯米)
蒸煮
2
淀粉
发酵 糖化
酒醅(乙醇)
醋酸发酵
决定醋的质量
醋
酯化
酯化酶
CH COOH +C H OH— CH COOC H + H O
探究活动二:
实验用品:乙醇、冰醋酸、浓硫酸、碎瓷片
根据资料信息,阅读教材P80,查看实验装置,在实验 仪器组装和实验操作中有哪些注意事项
活动五:认识乙酸的酯化反应
实验交流
实验现象:(1)溶液分层
(2)上层有无色透明的油状液体产生
(3)并有特殊香味
活动五:认识乙酸的酯化反应
乙酸乙酯
乙酸异戊酯
酯类物质
戊酸戊酯
实验拓展
适当倾斜试管,往试管中加入石蕊指示剂, 但不振荡,观察现象。
活动五:认识乙酸的酯化反应
(1)为什么会出现这种现象
乙酸乙酯中溶有乙酸,乙酸显酸性
(2)如何得到较为纯净的乙酸乙酯
用饱和Na CO 除去
(3)饱和Na CO 溶液的作用是什么
①除去乙酸②溶解乙醇③降低乙酸乙酯的溶 解度,便于分层。
现象解释
探究活动三:
乙酸和乙醇可能是以怎样的方式相互结合形成乙酸乙 酯的 尝试通过球棍模型模拟酯化反应过程,分析酯化反应 断键和成键的方式。
微观结构分析
活动五:微观结构分析
可能二:
可能一:
乙酸乙酯(香味)
酯化反应的实质:酸脱羟基、醇脱氢(羟基上的)
酯化反应属于取代反应
通过同位素原子示踪法测知反应如下:
活动五:探究乙酸的酯化反应
酯化反应注意事项
药品顺序:乙醇 → 浓硫酸→ 乙酸
浓硫酸:催化剂、 吸水剂
碎瓷片防暴沸
小心加热:减少乙酸、 乙醇的挥发。
加 热 :加快反应速
率,蒸出乙酸乙酯, 提高反应物的转化率。
长导管冷凝、导 气作用
导管在饱和
Na CO 液面上:
防止倒吸
分离碳酸钠和乙 酸乙酯:分液
饱和Na CO 作用
①溶解乙醇;
②除去乙酸;
③降低乙酸乙酯的溶解 度,利于酯的析出
沸点:
乙酸乙酯(77.1)
乙醇(78.3 ℃)
乙酸(118℃)
X 酸+Y 醇→X 酸Y酯
(1) 乙 酸 + 甲醇 → 乙酸甲酯
CH COOH+CH OH 浓硫酸CH COOCH +H O
(2) 甲 酸 + 乙醇 → 甲酸乙酯
HCOOH+CH CH OH 浓硫酸、HCOOCH CH +H O
课堂训练
合成
纤维
乙酸 农药
喷漆
溶剂
染料
香料
医药
活动六:认识乙酸的用途
含有-COOH
H 0
决定
弱酸性
化学性质
酯化反应
H- C-C-O-H
l
课堂小结
结构特点
决定
名称 乙酸 水 乙醇
碳酸
分子结构 CH COOH H—OH C H OH
H CO
遇石蕊溶液 变红 不变红 不变红
变红
与 N a 反应 反应 反应
反应
与Na CO 溶液 反应 不反应
反应
与NaHCO 溶液 反应 不反应
不反应
羟基氢原子的活泼性强弱 CH CO0H>H CO >H O>C H OH
(补充1)乙酸、水、乙醇、碳酸的性质比较
2.物理性质酯一般密度比水小,难溶于水,易溶于乙醇、乙醚等有机溶剂,
低级酯(如乙酸乙酯)是具有一定的挥发性,有芳香气味。
3.用途(1)用作香料,如作饮料、糖果、化妆品等中的香料。
(2)用作有机溶剂,如作指甲油、胶水的溶剂。
4.酯的化学反应 RCOOH+R'OH (水解/取代反应)
酯酸或碱条件下,酯类水解生成相应的酸和醇。
补充2:酯
或 —COOR 酯基
1.官能团
O
CH CH CO0C H
丙酸乙酯
请说出下列酯的名称及水解产物:
CH CO0CH
乙酸甲酯
HCO0CH
甲酸甲酯
有机化合物类别 官能团 代表物
结构 名称 结构简式
名称
烃 烷烃 — — CH
甲烷
烯烃 C=C 碳碳双键 CH =CH
乙烯
炔烃 — C = C 一 碳碳三键 CH=CH
乙炔
芳香烃 — —
苯
补充3:官能团与有机物分类(书p81)
常见的有机化合物类别、官能团和代表物 苯环不是官能团
烃 的 衍 生 物 卤代烃 (X表示 卤素原子) 碳卤键 CH CH Br
溴乙烷
醇 —OH 羟基 CH CH OH
乙醇
醛 -H 醛基 CH —C—H
乙醛
羧酸 O OH 羧基 O CH —C—OH
乙酸
酯 O O—R 酯基 O C H 一 C H
乙酸乙酯
0 丨
课堂练习:
1、关于乙酸的下列说法中不正确的是( D )
A. 乙酸易溶于水和乙醇
B. 无水乙酸又称冰醋酸,它是纯净物
C. 乙酸是一种重要的有机酸,是有刺激性气味的液体
D. 乙酸分子里有四个氢原子,所以不是一元酸
A.1 mol柠檬酸可与4 mol NaOH发生中和反应
B.柠檬酸中能发生酯化反应的官能团有2种
C.1 mol柠檬酸与足量金属Na 反应生成1.5 mol H
D.柠檬酸与O 在Cu作催化剂、加热的条件下发生催化氧化反应
2.柠檬酸的结构简式如图,下列说法正确的是(B )
3.某有机物结构简式为CH =CHCOOH, 该有机物能发生的
反应类型是( D )
A. 加成反应
B. 取代反应
C.中 和 反 应
D. 以上反应均能发生
人教版化学必修2
舌尖上的有机物 — —乙酸
核心素养发展目标
1.了解乙酸的物理性质和用途,培养科学态度与社会责任。
2. 掌握乙酸的组成、结构和化学性质,培养变化观念与平衡思想。
3.掌握酯化反应的原理、实质和实验操作,能依据给出的问题,设计 简单的实验方案,培养科学探究与创新意识。
活动一:微课学习反馈
观看《舌尖上的中国》片段,总结香醋的酿造过程
醋酸生产工艺:
1
谷物(糯米)
蒸煮
酒醅(乙醇)
醋酸发酵
决定醋的质量和产量
淀粉
发酵 糖化
决定醋的质量
醋
酯化
酉莒
醋的来历
活动二:观察思考
一、物理性质
乙酸(俗称醋酸)
颜色:无色透明
状态:液 体
气味:有强烈刺激性气味
沸点:118℃(易挥发)
熔点:16.6℃(无水乙酸又称为:冰醋酸) 溶解性:易溶于水、乙醇等溶剂
乙 酸
熔点:16.6 ℃ 沸点:118℃
密度:1.05 g/cm
数据
根据球棍模型写出分子式、结构式、结构简式
活动三:自主学习
:碳
:氢 :氧
H O
H-C-C-O-H
H
CH COOH
活动三:自主学习
二、组成与结构
羧基( -COOH
或 C— -OH )
充填模型
乙 酸
C H O
分子式
官能团
思 考 :食醋可以清除水壶中的少量水垢(主要成分是碳酸钙), 这是利用了乙酸的什么性质 请写出相关反应方程式。
2CH COOH+CaCO =(CH CO0) Ca+H O+CO 个 酸性:CH COOH>H CO
三、化学性质
1.酸性
活动四:认识乙酸的酸性
①与指示剂反应:使紫色石蕊变红
②与金属反应 (Na)2Na+2CH COOH==2CH COO N a+H 个
③与碱性氧化物反应(CuO)
2CH CO0H十CuO==(CH CO0) Cu+H O
④与碱反应(NaOH)
CH COOH+NaOH==CH COONa+H O
⑤与盐反应 (Na CO )
2CH COOH+Na CO ==2CH COONa+H O+CO 个
三 、乙酸的化学性质
1、酸性 :CH COOH是一种重要的有机酸,具有酸的通性。
电离方程式:CH COOH—CH CO0-+ H+ 一元弱酸
酸的通性
查阅资料,根据生活经验设计实验方案,比较乙 酸与碳酸、盐酸酸性强弱
课后思考
醋酸生产工艺:
①
谷物(糯米)
蒸煮
2
淀粉
发酵 糖化
酒醅(乙醇)
醋酸发酵
决定醋的质量
醋
酯化
酯化酶
CH COOH +C H OH— CH COOC H + H O
探究活动二:
实验用品:乙醇、冰醋酸、浓硫酸、碎瓷片
根据资料信息,阅读教材P80,查看实验装置,在实验 仪器组装和实验操作中有哪些注意事项
活动五:认识乙酸的酯化反应
实验交流
实验现象:(1)溶液分层
(2)上层有无色透明的油状液体产生
(3)并有特殊香味
活动五:认识乙酸的酯化反应
乙酸乙酯
乙酸异戊酯
酯类物质
戊酸戊酯
实验拓展
适当倾斜试管,往试管中加入石蕊指示剂, 但不振荡,观察现象。
活动五:认识乙酸的酯化反应
(1)为什么会出现这种现象
乙酸乙酯中溶有乙酸,乙酸显酸性
(2)如何得到较为纯净的乙酸乙酯
用饱和Na CO 除去
(3)饱和Na CO 溶液的作用是什么
①除去乙酸②溶解乙醇③降低乙酸乙酯的溶 解度,便于分层。
现象解释
探究活动三:
乙酸和乙醇可能是以怎样的方式相互结合形成乙酸乙 酯的 尝试通过球棍模型模拟酯化反应过程,分析酯化反应 断键和成键的方式。
微观结构分析
活动五:微观结构分析
可能二:
可能一:
乙酸乙酯(香味)
酯化反应的实质:酸脱羟基、醇脱氢(羟基上的)
酯化反应属于取代反应
通过同位素原子示踪法测知反应如下:
活动五:探究乙酸的酯化反应
酯化反应注意事项
药品顺序:乙醇 → 浓硫酸→ 乙酸
浓硫酸:催化剂、 吸水剂
碎瓷片防暴沸
小心加热:减少乙酸、 乙醇的挥发。
加 热 :加快反应速
率,蒸出乙酸乙酯, 提高反应物的转化率。
长导管冷凝、导 气作用
导管在饱和
Na CO 液面上:
防止倒吸
分离碳酸钠和乙 酸乙酯:分液
饱和Na CO 作用
①溶解乙醇;
②除去乙酸;
③降低乙酸乙酯的溶解 度,利于酯的析出
沸点:
乙酸乙酯(77.1)
乙醇(78.3 ℃)
乙酸(118℃)
X 酸+Y 醇→X 酸Y酯
(1) 乙 酸 + 甲醇 → 乙酸甲酯
CH COOH+CH OH 浓硫酸CH COOCH +H O
(2) 甲 酸 + 乙醇 → 甲酸乙酯
HCOOH+CH CH OH 浓硫酸、HCOOCH CH +H O
课堂训练
合成
纤维
乙酸 农药
喷漆
溶剂
染料
香料
医药
活动六:认识乙酸的用途
含有-COOH
H 0
决定
弱酸性
化学性质
酯化反应
H- C-C-O-H
l
课堂小结
结构特点
决定
名称 乙酸 水 乙醇
碳酸
分子结构 CH COOH H—OH C H OH
H CO
遇石蕊溶液 变红 不变红 不变红
变红
与 N a 反应 反应 反应
反应
与Na CO 溶液 反应 不反应
反应
与NaHCO 溶液 反应 不反应
不反应
羟基氢原子的活泼性强弱 CH CO0H>H CO >H O>C H OH
(补充1)乙酸、水、乙醇、碳酸的性质比较
2.物理性质酯一般密度比水小,难溶于水,易溶于乙醇、乙醚等有机溶剂,
低级酯(如乙酸乙酯)是具有一定的挥发性,有芳香气味。
3.用途(1)用作香料,如作饮料、糖果、化妆品等中的香料。
(2)用作有机溶剂,如作指甲油、胶水的溶剂。
4.酯的化学反应 RCOOH+R'OH (水解/取代反应)
酯酸或碱条件下,酯类水解生成相应的酸和醇。
补充2:酯
或 —COOR 酯基
1.官能团
O
CH CH CO0C H
丙酸乙酯
请说出下列酯的名称及水解产物:
CH CO0CH
乙酸甲酯
HCO0CH
甲酸甲酯
有机化合物类别 官能团 代表物
结构 名称 结构简式
名称
烃 烷烃 — — CH
甲烷
烯烃 C=C 碳碳双键 CH =CH
乙烯
炔烃 — C = C 一 碳碳三键 CH=CH
乙炔
芳香烃 — —
苯
补充3:官能团与有机物分类(书p81)
常见的有机化合物类别、官能团和代表物 苯环不是官能团
烃 的 衍 生 物 卤代烃 (X表示 卤素原子) 碳卤键 CH CH Br
溴乙烷
醇 —OH 羟基 CH CH OH
乙醇
醛 -H 醛基 CH —C—H
乙醛
羧酸 O OH 羧基 O CH —C—OH
乙酸
酯 O O—R 酯基 O C H 一 C H
乙酸乙酯
0 丨
课堂练习:
1、关于乙酸的下列说法中不正确的是( D )
A. 乙酸易溶于水和乙醇
B. 无水乙酸又称冰醋酸,它是纯净物
C. 乙酸是一种重要的有机酸,是有刺激性气味的液体
D. 乙酸分子里有四个氢原子,所以不是一元酸
A.1 mol柠檬酸可与4 mol NaOH发生中和反应
B.柠檬酸中能发生酯化反应的官能团有2种
C.1 mol柠檬酸与足量金属Na 反应生成1.5 mol H
D.柠檬酸与O 在Cu作催化剂、加热的条件下发生催化氧化反应
2.柠檬酸的结构简式如图,下列说法正确的是(B )
3.某有机物结构简式为CH =CHCOOH, 该有机物能发生的
反应类型是( D )
A. 加成反应
B. 取代反应
C.中 和 反 应
D. 以上反应均能发生
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
