2015—2016山东省泰安市新城实验中学分层走班精品学案:酸的性质
文档属性
| 名称 | 2015—2016山东省泰安市新城实验中学分层走班精品学案:酸的性质 |

|
|
| 格式 | zip | ||
| 文件大小 | 114.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-01-14 00:00:00 | ||
图片预览




文档简介
常见的酸
考点梳理
一、酸的组成
例:(2014常德)物质分类是一种重要的化学思想。下列物质中属于酸的是( )
A. H2CO3 B. NaHCO3 C. P2O5 D. KOH
二、知道两种浓酸的性质:
浓盐酸:①挥发性;②腐蚀性
浓硫酸 :①吸水性(干燥剂);②脱水性;③腐蚀性
例1.(2013.泰安市)下列物质露置于空气中,没有发生化学变化而质量增大的是
A.浓硫酸 B.浓盐酸 C.生石灰 D.氢氧化钠
例2.(2014北京)下列物质必须密封保存的是( )
A.木炭 B.浓盐酸 C.石灰石 D.氯化钠
三、酸的化学性质
(一)能与酸反应的物质
(二)酸的通性(知道现象、会写化学方程式)
酸有相似的化学性质是因为酸在水中都能电离出H+,有不同的化学性质是因为能电离出的酸根离子不同。
1.酸溶液能使酸碱指示剂变色:使紫色石蕊溶液变红。
2.与活泼金属反应生成盐和氢气。(Mg、Fe、Zn) 放热
3.与金属氧化物反应生成盐和水。(Fe2O3 CuO)
4.与碱反应生成盐和水。[Fe(OH)3,Cu(OH)2] 放热
5.与某些盐反应生成新酸和新盐。(Na2CO3、CaCO3)
注意:AgNO3 与盐酸反应,BaCl2与硫酸反应。不是酸的通性
四、记忆以下知识:
有色溶液:含Cu2+溶液为蓝色溶液,含Fe3+溶液为黄色溶液,含Fe2+溶液为浅绿色溶液。
常用的沉淀:
既不溶于水也不溶于酸的沉淀:BaSO4、AgCl;
两种碳酸盐沉淀:BaCO3、CaCO3;
不溶性的碱:Cu(OH)2蓝色沉淀、Fe(OH)3红褐色沉淀、Mg(OH)2;
例.(2013邵阳市)如图两圆相交部分是五种物质中两两之间相互反应的示意图.下列对反应现象的说法中,错误的是( )www.21-cn-jy.com
A.a处形成浅绿色溶液 B.b处形成大量气泡
C.c处反应放热 D.d处溶液呈红色
考点练习
1、(2015益阳)2015年5月28日,广东省发布“输入性中东呼吸综合征”疑似病例后,许多中小学校为预防传染病的扩散,要求学生在饭前便后用84消毒液洗手。84消毒液的主要成分是次氯酸钠(NaClO),则NaClO属于 21·世纪*教育网
A.氧化物 B.酸 C.碱 D.盐
2. (2015泸州)化学上常对物质进行分类和研究,以下物质中属于酸的是( )
A.HNO3 B.MgO C.O2 D.NaCl
3.(2015?遵义)酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是( )21教育网
A.能使紫色石蕊试液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
4.(2014大庆)化学方程式是重要的“化学语言”,下列化学方程式与文字表述均正确的是( )
A.用氢氧化镁治疗胃酸过多症:
H2SO4+Mg(OH)2═MgSO4+2H2O
B.用稀盐酸除去铁锈:Fe2O3+4HCl═2FeCl2+2H2O
C.实验室制备CO2:CaCO3+2HCl═CaCl2+CO2↑+H2O
D.甲醇不充分燃烧:2CH3OH+3O22CO2+4H2O
5.如图是物质间发生化学反应的颜色变化,其中X是
A.稀盐酸B.稀硫酸C.硫酸钠溶液D.澄清石灰水
6.(2013临沂市)构建知识网络能帮助我们理解知识间的内在联系,请分析以下知识网络图,回答有关问题。21·cn·jy·com
(1)则①中填写 ,②中填写 。
(2)上图中“金属氧化物”若为氧化铁,请你写出稀盐酸与氧化铁反应的化学方程式 。【来源:21cnj*y.co*m】
7.(2014大庆)如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题:【版权所有:21教育】
(1)稀盐酸中阳离子的符号是 ;
(2)反应①中石蕊溶液变为
色;
(3)反应⑤的化学方程式为 ;
(4)图中只生成盐和水的反应有 (填序号);
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、Na2CO3)中的 .www-2-1-cnjy-com
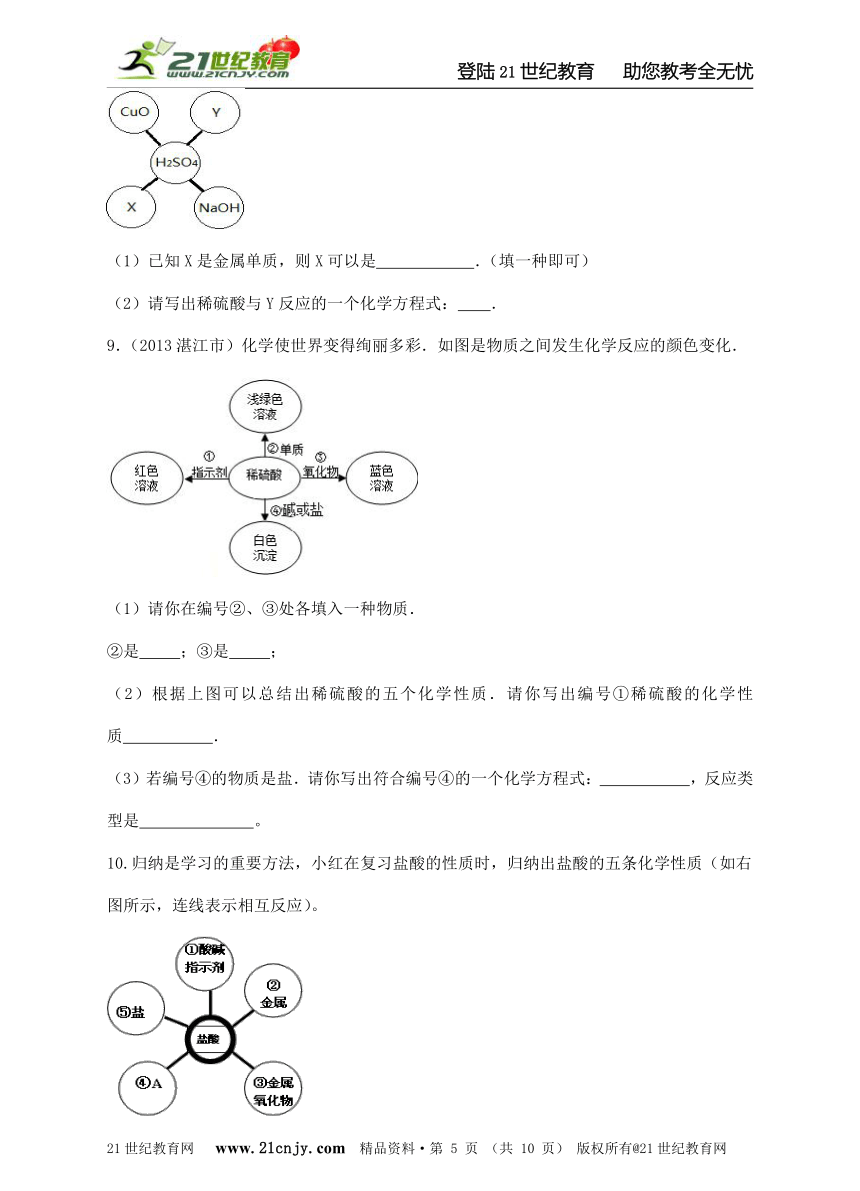
8.(2015?嘉兴)对知识的及时整理与归纳是学习科学的重要方法,某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“﹣”表示相连的两种物质间发生的反应,五个圈中的物质属于不同的类别).21*cnjy*com
(1)已知X是金属单质,则X可以是 .(填一种即可)
(2)请写出稀硫酸与Y反应的一个化学方程式: .
9.(2013湛江市)化学使世界变得绚丽多彩.如图是物质之间发生化学反应的颜色变化.
(1)请你在编号②、③处各填入一种物质.
②是 ;③是 ;
(2)根据上图可以总结出稀硫酸的五个化学性质.请你写出编号①稀硫酸的化学性质 .【来源:21·世纪·教育·网】
(3)若编号④的物质是盐.请你写出符合编号④的一个化学方程式: ,反应类型是 。
10.归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如右图所示,连线表示相互反应)。
(1)为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变___色;
(2)图中A所表示的物质类别是_____________;
(3)盐酸的性质③决定了盐酸可用于清除铁锈,该反应的化学方程式是_______ ______;
(4)为了验证性质⑤,可选用的物质是_ (填一种即可)
(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁
和锌与盐酸反应的快慢,需要控制不变(相同)的量
是__________(填序号);
A.两种金属的形状 B.盐酸的质量分数
C.反应容器的大小 D.温度
11. (2015·黄冈)构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会_______(填“偏大”、“偏小”、“无影响”)。
(2)图中①的现象是:_____________。
(3)写出一个符合图中③的化学方程式______________。
(4)图中性质④属于_________反应(填基本反应类型)。
(5)图中⑤的性质在工业上可用于__________(填用途)。
12.(2015?自贡)硫酸和盐酸时实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.2-1-c-n-j-y
(1)它们水溶液的pH都 7(填“>”、“=”或“<”).
(2)它们都能除铁锈,写出盐酸与铁锈的主要成分反应的化学方程式: .
(3)它们都能与碱反应生成盐和水,该类反应叫 反应.
(4)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是盛有 的试剂瓶.
(5)写出把硫酸转化为盐酸的化学方程式: .
13.(2013.广州市)硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应: 21*cnjy*com
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,属于酸的共同性质的是 (填编号)
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌
③除去NaCl中的少量NaOH
14.某班同学为验证酸的化学通性,做了五组实验.分析并回答问题.
(1)A组试管中都产生H2.若要制得较纯的H2,选稀硫酸而不选盐酸的原因是 。21cnjy.com
(2)B组试管中实验现象相同,该现象是 。
(3)写出C组任一试管中发生反应的化学方程式 。
(4)上述五组实验中没有体现酸的通性的是 。(填序号).
参考答案:
1、D 2、A 3、C 4、C 5、B
6、(1)金属;碱 (2) 6HCl+Fe2O3==2FeCl3+3H2O
7、(1)H+;(2)红;(3)Al2O3+6HCl=2AlCl3+3H2O;(4)③⑤;(5)Na2CO3.
8、(1)锌等;(2)BaCl2+H2SO4═BaSO4↓+2HCl(合理即可)
9、(1)②铁(或Fe);③氧化铜(或CuO)
(2)硫酸可使紫色石蕊试液变红
(3)BaCl2+H2SO4=BaSO4↓+2HCl(合理均可),复分解反应
10、?(1)红 (2)碱; (3)CaCO3+2HCl═CaCl2+H2O+CO2↑. (4)铁锈. (5)ABD21世纪教育网版权所有
11. (1)偏大 (2)石蕊变红 (3)HCl+AgNO3=AgCl↓+HNO3(合理即可) (4)复分解(5)盐酸除铁锈(合理即可)2·1·c·n·j·y
12. <;Fe2O3+6HCl=2FeCl3+3H2O;中和(或复分解);浓盐酸;H2SO4+BaCl2=2HCl+BaSO4↓
13、⑴ 吸水性 ⑵ ①Fe + H2SO4?= FeSO4?+ H2↑ ②Na2CO3?+ H2SO4 === Na2SO4?+ H2O + CO2↑ ③H2SO4?+ BaCl2?==== BaSO4?↓+ 2HCl; ①② ⑶ ②③【出处:21教育名师】
14. (1)盐酸具有挥发性,挥发出氯化氢气体,使制得的氢气中混有氯化氢气体;(2)红棕色固体逐渐减少,溶液变成黄色;(3)NaOH+HCl=NaCl+H2O或2NaOH+H2SO4=Na2SO4+2H2O;(4)D.21教育名师原创作品
考点梳理
一、酸的组成
例:(2014常德)物质分类是一种重要的化学思想。下列物质中属于酸的是( )
A. H2CO3 B. NaHCO3 C. P2O5 D. KOH
二、知道两种浓酸的性质:
浓盐酸:①挥发性;②腐蚀性
浓硫酸 :①吸水性(干燥剂);②脱水性;③腐蚀性
例1.(2013.泰安市)下列物质露置于空气中,没有发生化学变化而质量增大的是
A.浓硫酸 B.浓盐酸 C.生石灰 D.氢氧化钠
例2.(2014北京)下列物质必须密封保存的是( )
A.木炭 B.浓盐酸 C.石灰石 D.氯化钠
三、酸的化学性质
(一)能与酸反应的物质
(二)酸的通性(知道现象、会写化学方程式)
酸有相似的化学性质是因为酸在水中都能电离出H+,有不同的化学性质是因为能电离出的酸根离子不同。
1.酸溶液能使酸碱指示剂变色:使紫色石蕊溶液变红。
2.与活泼金属反应生成盐和氢气。(Mg、Fe、Zn) 放热
3.与金属氧化物反应生成盐和水。(Fe2O3 CuO)
4.与碱反应生成盐和水。[Fe(OH)3,Cu(OH)2] 放热
5.与某些盐反应生成新酸和新盐。(Na2CO3、CaCO3)
注意:AgNO3 与盐酸反应,BaCl2与硫酸反应。不是酸的通性
四、记忆以下知识:
有色溶液:含Cu2+溶液为蓝色溶液,含Fe3+溶液为黄色溶液,含Fe2+溶液为浅绿色溶液。
常用的沉淀:
既不溶于水也不溶于酸的沉淀:BaSO4、AgCl;
两种碳酸盐沉淀:BaCO3、CaCO3;
不溶性的碱:Cu(OH)2蓝色沉淀、Fe(OH)3红褐色沉淀、Mg(OH)2;
例.(2013邵阳市)如图两圆相交部分是五种物质中两两之间相互反应的示意图.下列对反应现象的说法中,错误的是( )www.21-cn-jy.com
A.a处形成浅绿色溶液 B.b处形成大量气泡
C.c处反应放热 D.d处溶液呈红色
考点练习
1、(2015益阳)2015年5月28日,广东省发布“输入性中东呼吸综合征”疑似病例后,许多中小学校为预防传染病的扩散,要求学生在饭前便后用84消毒液洗手。84消毒液的主要成分是次氯酸钠(NaClO),则NaClO属于 21·世纪*教育网
A.氧化物 B.酸 C.碱 D.盐
2. (2015泸州)化学上常对物质进行分类和研究,以下物质中属于酸的是( )
A.HNO3 B.MgO C.O2 D.NaCl
3.(2015?遵义)酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是( )21教育网
A.能使紫色石蕊试液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
4.(2014大庆)化学方程式是重要的“化学语言”,下列化学方程式与文字表述均正确的是( )
A.用氢氧化镁治疗胃酸过多症:
H2SO4+Mg(OH)2═MgSO4+2H2O
B.用稀盐酸除去铁锈:Fe2O3+4HCl═2FeCl2+2H2O
C.实验室制备CO2:CaCO3+2HCl═CaCl2+CO2↑+H2O
D.甲醇不充分燃烧:2CH3OH+3O22CO2+4H2O
5.如图是物质间发生化学反应的颜色变化,其中X是
A.稀盐酸B.稀硫酸C.硫酸钠溶液D.澄清石灰水
6.(2013临沂市)构建知识网络能帮助我们理解知识间的内在联系,请分析以下知识网络图,回答有关问题。21·cn·jy·com
(1)则①中填写 ,②中填写 。
(2)上图中“金属氧化物”若为氧化铁,请你写出稀盐酸与氧化铁反应的化学方程式 。【来源:21cnj*y.co*m】
7.(2014大庆)如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题:【版权所有:21教育】
(1)稀盐酸中阳离子的符号是 ;
(2)反应①中石蕊溶液变为
色;
(3)反应⑤的化学方程式为 ;
(4)图中只生成盐和水的反应有 (填序号);
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、Na2CO3)中的 .www-2-1-cnjy-com
8.(2015?嘉兴)对知识的及时整理与归纳是学习科学的重要方法,某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“﹣”表示相连的两种物质间发生的反应,五个圈中的物质属于不同的类别).21*cnjy*com
(1)已知X是金属单质,则X可以是 .(填一种即可)
(2)请写出稀硫酸与Y反应的一个化学方程式: .
9.(2013湛江市)化学使世界变得绚丽多彩.如图是物质之间发生化学反应的颜色变化.
(1)请你在编号②、③处各填入一种物质.
②是 ;③是 ;
(2)根据上图可以总结出稀硫酸的五个化学性质.请你写出编号①稀硫酸的化学性质 .【来源:21·世纪·教育·网】
(3)若编号④的物质是盐.请你写出符合编号④的一个化学方程式: ,反应类型是 。
10.归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如右图所示,连线表示相互反应)。
(1)为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变___色;
(2)图中A所表示的物质类别是_____________;
(3)盐酸的性质③决定了盐酸可用于清除铁锈,该反应的化学方程式是_______ ______;
(4)为了验证性质⑤,可选用的物质是_ (填一种即可)
(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁
和锌与盐酸反应的快慢,需要控制不变(相同)的量
是__________(填序号);
A.两种金属的形状 B.盐酸的质量分数
C.反应容器的大小 D.温度
11. (2015·黄冈)构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会_______(填“偏大”、“偏小”、“无影响”)。
(2)图中①的现象是:_____________。
(3)写出一个符合图中③的化学方程式______________。
(4)图中性质④属于_________反应(填基本反应类型)。
(5)图中⑤的性质在工业上可用于__________(填用途)。
12.(2015?自贡)硫酸和盐酸时实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.2-1-c-n-j-y
(1)它们水溶液的pH都 7(填“>”、“=”或“<”).
(2)它们都能除铁锈,写出盐酸与铁锈的主要成分反应的化学方程式: .
(3)它们都能与碱反应生成盐和水,该类反应叫 反应.
(4)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是盛有 的试剂瓶.
(5)写出把硫酸转化为盐酸的化学方程式: .
13.(2013.广州市)硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应: 21*cnjy*com
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,属于酸的共同性质的是 (填编号)
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌
③除去NaCl中的少量NaOH
14.某班同学为验证酸的化学通性,做了五组实验.分析并回答问题.
(1)A组试管中都产生H2.若要制得较纯的H2,选稀硫酸而不选盐酸的原因是 。21cnjy.com
(2)B组试管中实验现象相同,该现象是 。
(3)写出C组任一试管中发生反应的化学方程式 。
(4)上述五组实验中没有体现酸的通性的是 。(填序号).
参考答案:
1、D 2、A 3、C 4、C 5、B
6、(1)金属;碱 (2) 6HCl+Fe2O3==2FeCl3+3H2O
7、(1)H+;(2)红;(3)Al2O3+6HCl=2AlCl3+3H2O;(4)③⑤;(5)Na2CO3.
8、(1)锌等;(2)BaCl2+H2SO4═BaSO4↓+2HCl(合理即可)
9、(1)②铁(或Fe);③氧化铜(或CuO)
(2)硫酸可使紫色石蕊试液变红
(3)BaCl2+H2SO4=BaSO4↓+2HCl(合理均可),复分解反应
10、?(1)红 (2)碱; (3)CaCO3+2HCl═CaCl2+H2O+CO2↑. (4)铁锈. (5)ABD21世纪教育网版权所有
11. (1)偏大 (2)石蕊变红 (3)HCl+AgNO3=AgCl↓+HNO3(合理即可) (4)复分解(5)盐酸除铁锈(合理即可)2·1·c·n·j·y
12. <;Fe2O3+6HCl=2FeCl3+3H2O;中和(或复分解);浓盐酸;H2SO4+BaCl2=2HCl+BaSO4↓
13、⑴ 吸水性 ⑵ ①Fe + H2SO4?= FeSO4?+ H2↑ ②Na2CO3?+ H2SO4 === Na2SO4?+ H2O + CO2↑ ③H2SO4?+ BaCl2?==== BaSO4?↓+ 2HCl; ①② ⑶ ②③【出处:21教育名师】
14. (1)盐酸具有挥发性,挥发出氯化氢气体,使制得的氢气中混有氯化氢气体;(2)红棕色固体逐渐减少,溶液变成黄色;(3)NaOH+HCl=NaCl+H2O或2NaOH+H2SO4=Na2SO4+2H2O;(4)D.21教育名师原创作品
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
