【高中化学人教版(2019)选择性必修1同步练习】第三节金属的腐蚀与防护(含答案)
文档属性
| 名称 | 【高中化学人教版(2019)选择性必修1同步练习】第三节金属的腐蚀与防护(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-09-04 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
【高中化学人教版(2019)选择性必修1同步练习】
第三节金属的腐蚀与防护
一、单选题
1.下列反应与电化学反应原理无关的是
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.市售“暖贴”中含有铁粉、炭粉、木屑、少量氯化钠和水等,揉搓后释放热量
C.纯银器表面变黑
D.用电镀法将镍、铬等金属外衣“披”在塑料制品上
2.以下防腐措施中,属于电化学保护法的是( )
A.用氧化剂使金属表面生成致密稳定的氧化物保护膜
B.在金属中加入一些铬或者镍制成合金
C.在轮船的船壳水线以下部分,装上一锌锭
D.在金属表面喷漆
3.化学与生产、生活、科技密切相关。下列有关说法不正确的是( )
A.一次性保暖贴利用了铁被腐蚀时放热的原理
B.植树造林有利于实现“碳中和”,其捕获和储存大气中的CO2过程涉及了氧化还原反应
C.将桥墩钢铁与外接电源负极相连的方法,称为牺牲阳极的阴极保护法
D.“绿氢”燃料电池客车投入“冰丝带”:光伏电解水制氢可作为“绿氢”的主要来源
4.如图各烧杯中盛有海水,铁在其中会发生腐蚀。铁腐蚀的速率由快至慢的顺序为
A.②①③④ B.②①④③ C.④②①③ D.②④①③
5.关于下列装置的叙述正确的是
选项 A B C D
装置
叙述 用牺牲阳极保护法防止铁管道被腐蚀 在铁极附近放置一片湿润的淀粉―KI试纸,试纸变蓝 铅蓄电池充电时,阴极的质量减小 电子从Fe电极流出
A.A B.B C.C D.D
6.在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,厌氧细菌可促使土壤中的 与H2反应生成S2-,加速钢管的腐蚀,其反应原理如下图所示。
下列说法正确的是( )
A.正极的电极反应式为:2H2O+O2+4e-=4OH-
B.钢管腐蚀的直接产物中含有FeS、Fe(OH)2
C.在钢管表面镀锌或镀铜均可减缓钢管的腐蚀
D. 与H2的反应可表示为:4H2+ -8e- S2-+4H2O
二、多选题
7.陕西历史博物馆展出了许多鎏金工艺青铜器。鎏金是古代常用的镀金工艺,将金汞合金涂于器物表面,加热使汞挥发,便形成一层光亮的金镀层。下列关于青铜器鎏金工艺的说法正确的
鎏金铜沐缶
A.鎏金工艺的镀金过程是一种化学变化
B.鎏金除了改善外观,还可保护青铜器,使其不易生锈
C.若表面的金镀层破损,暴露出的青铜表面会更易生锈
D.青铜比纯铜硬度小
三、填空题
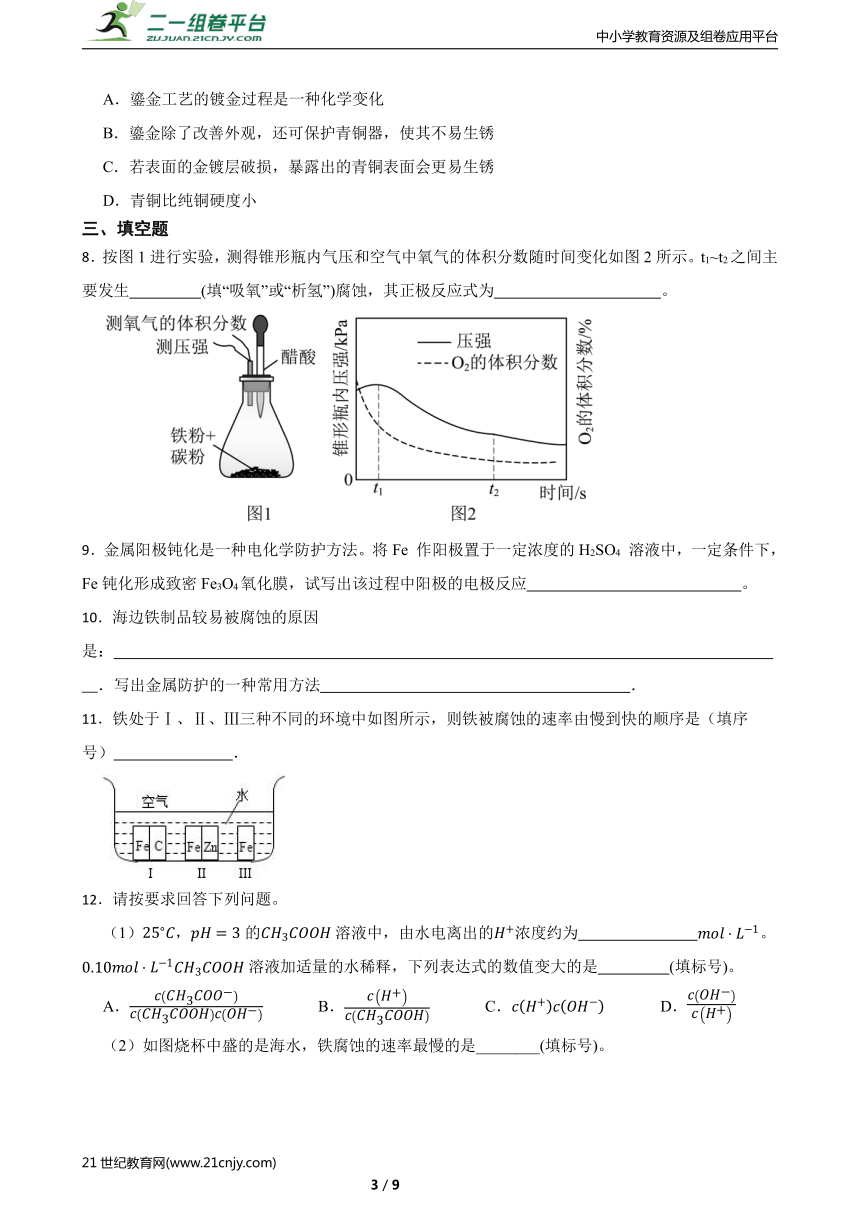
8.按图1进行实验,测得锥形瓶内气压和空气中氧气的体积分数随时间变化如图2所示。t1~t2之间主要发生 (填“吸氧”或“析氢”)腐蚀,其正极反应式为 。
9.金属阳极钝化是一种电化学防护方法。将Fe 作阳极置于一定浓度的H2SO4 溶液中,一定条件下,Fe钝化形成致密Fe3O4氧化膜,试写出该过程中阳极的电极反应 。
10.海边铁制品较易被腐蚀的原因是: .写出金属防护的一种常用方法 .
11.铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中如图所示,则铁被腐蚀的速率由慢到快的顺序是(填序号) .
12.请按要求回答下列问题。
(1),的溶液中,由水电离出的浓度约为 。溶液加适量的水稀释,下列表达式的数值变大的是 (填标号)。
A. B. C. D.
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是________(填标号)。
A. B. C. D.
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。
①甲装置中负极反应式为 。
②乙装置中石墨电极上生成的气体为 (填化学式)。
③丙装置中足量,工作一段时间后,溶液的 (填“变大”、“变小”或“不变”),反应的化学方程式为 ,若要将电解后的溶液复原,需加入一定量的 (填化学式)。
四、综合题
13.Ⅰ.完成下列问题
(1)理论上不能设计为原电池的化学反应是 。
a.
b.
c.
d.
(2)电池比能量高,可用于汽车、航天等领域。电池反应式为:,放电时,下列说法正确的是 。
a.电能转化成化学能 b.在正极发生氧化反应
c.正离子由负极移向正极 d.在负极失去电子
(3)下列关于金属腐蚀与防护的说法不正确的是 。
a.图①,放置于干燥空气中的铁钉不易生锈
b.图②,若断开电源,钢闸门将发生吸氧腐蚀
c.图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀
d.图③,若金属比活泼,可防止输水管腐蚀
Ⅱ.某实验小组为探究与能否发生氧化还原反应,设计如下双液原电池(盐桥中为饱和溶液的琼脂)。
(4)该装置石墨棒上发生的电极反应式为 ,盐桥中向 烧杯移动。(填“甲”或“乙”)
Ⅲ.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
根据要求回答相关问题:
(5)写出氢气所在电极的电极反应式 。
(6)石墨电极为 (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液, (填“铁极”或“石墨极”)区的溶液先变红。
(7)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将 (填“增大”“减小”或“不变”)。当甲装置消耗标准状况下时,丙装置中纯铜电极增重 g。
14.
(1)由氢气和氧气反应生成1mol水蒸气放热242kJ,写出该反应的热化学方程式: 。
已知断裂1molH2、1molO2的化学键分别需要消耗436kJ、496kJ的能量,则断裂1molH-O所需的能量为 kJ。
(2)已知:①CH4(g)+H2O(g) CO(g)+3H2(g)△H1=+205.9kJ mol-1
②CO(g)+H2O(g) CO2(g)+H2(g)△H2=-41.2kJ mol-1
则反应③:CH4(g)+CO2(g) 2CO(g)+2H2(g)△H3= kJ mol-1。
写出反应③的平衡常数表达式K= 。
(3)若将反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,则该电池正极的电极反应式为: 。
(4)如图所示,水槽中试管内有一枚铁钉,放置数天后观察,发现试管内液面上升,铁钉表面出现铁锈。该铁钉发生的电化学腐蚀类型为 腐蚀,其正极电极反应式为 。
五、解答题
15.某同学为了探究不同条件下铁钉的锈蚀情况,设计了如下实验:
(ⅰ)取三支试管,标记为I、II、III,I中盛有适量蒸馏水,II中盛有适量蒸馏水和植物油,III洁净干燥
(ⅱ)在三支试管中各放入一根无锈铁钉.并将II和III用软木塞塞紧,III中放入一小团棉花(如图所示).请回答:
(1)三支试管中铁钉锈蚀的速度从高到低依次排列为
由此可以得出铁钉锈蚀的条件有 和 .
若该同学将I放在每天阳光直晒的阳台上,与避光保存相比,哪种保存方法锈蚀更快?这说明锈蚀速度与什么因素有关?
若该同学将I中的液体换做食盐水,对锈蚀的速率有何影响?这说明锈蚀速率还和什么因素有关? .
六、实验探究题
16.如图所示套实验装置,分别回答下列问题:
(1)装置1为铁的吸氧腐蚀实验.一段时间后,向插入铁钉的玻璃筒内滴入KSCN溶液呈无色,再滴入氯水即可观察到铁钉附近的溶液变红色,表明铁被 ;向插入碳棒的玻璃筒内滴入酚酞试液,可观察到碳棒附近的溶液变红,该电极反应为 .
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 .
(3)装置3中甲烧杯盛放100mL 0.2mol L﹣1的NaCl溶液,乙烧杯盛放100mL 0.5mol L﹣1的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞试液,观察到石墨电极附近首先变红.
①电源的M端为 极,甲烧杯中铁电极的电极反应为 ;
②乙烧杯中电解反应的离子方程式为 ;
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64g,则甲烧杯中产生的气体在标准状况下为 mL.
答案解析部分
1.【答案】C
【知识点】金属的电化学腐蚀与防护
2.【答案】C
【知识点】金属的电化学腐蚀与防护
3.【答案】C
【知识点】氧化还原反应;金属的电化学腐蚀与防护
4.【答案】A
【知识点】金属的电化学腐蚀与防护
5.【答案】C
【知识点】金属的电化学腐蚀与防护;电解原理;电解池工作原理及应用
6.【答案】B
【知识点】金属的电化学腐蚀与防护
7.【答案】B,C
【知识点】金属的电化学腐蚀与防护;合金及其应用;原电池工作原理及应用
8.【答案】吸氧;O2+2H2O+4e-=4OH-
【知识点】铁的吸氧腐蚀
9.【答案】3Fe-8e-+4H2O=Fe3O4+8H+
【知识点】金属的电化学腐蚀与防护;电解池工作原理及应用
10.【答案】铁制品和海水构成原电池,铁制品中铁作负极易失电子发生电化学腐蚀,所以铁加速被腐蚀;刷油漆(涂油酯、电镀、包塑料膜)等
【知识点】金属的电化学腐蚀与防护
11.【答案】Ⅱ<Ⅲ<Ⅰ
【知识点】金属的电化学腐蚀与防护
12.【答案】(1);BD
(2)B
(3);;变小;;或
【知识点】金属的电化学腐蚀与防护
13.【答案】b;d;c;Fe3++e-=Fe2+;甲;H2-2e-+2OH-=2H2O;阳极;铁极;减小;32
【知识点】电极反应和电池反应方程式;金属的电化学腐蚀与防护;电解池工作原理及应用
14.【答案】(1)H2(g)+ O2(g)=H2O(g)△H=-242kJ mol-1;463
(2)+247.1; (或 )
(3)Fe3++e-=Fe2+
(4)吸氧;O2+4e-+2H2O=4OH-
【知识点】反应热和焓变;热化学方程式;化学平衡常数;原电池工作原理及应用;铁的吸氧腐蚀
15.【答案】(1)I>II>III;水;氧气;阳光直晒腐蚀快,温度越高金属腐蚀越快;腐蚀加快,加入电解质溶液可以加快金属的腐蚀
【知识点】金属的电化学腐蚀与防护
16.【答案】(1)氧化;O2+4e﹣+2H2O﹣═4OH﹣
(2)正;Cu+2Fe3+=Cu2++2Fe2+
(3)正;Fe﹣2e﹣═Fe2+;2Cu2++2H2O 2Cu+O2↑+4H+;224
【知识点】原电池工作原理及应用;电解池工作原理及应用;铁的吸氧腐蚀
21世纪教育网(www.21cnjy.com)
1 / 9
【高中化学人教版(2019)选择性必修1同步练习】
第三节金属的腐蚀与防护
一、单选题
1.下列反应与电化学反应原理无关的是
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.市售“暖贴”中含有铁粉、炭粉、木屑、少量氯化钠和水等,揉搓后释放热量
C.纯银器表面变黑
D.用电镀法将镍、铬等金属外衣“披”在塑料制品上
2.以下防腐措施中,属于电化学保护法的是( )
A.用氧化剂使金属表面生成致密稳定的氧化物保护膜
B.在金属中加入一些铬或者镍制成合金
C.在轮船的船壳水线以下部分,装上一锌锭
D.在金属表面喷漆
3.化学与生产、生活、科技密切相关。下列有关说法不正确的是( )
A.一次性保暖贴利用了铁被腐蚀时放热的原理
B.植树造林有利于实现“碳中和”,其捕获和储存大气中的CO2过程涉及了氧化还原反应
C.将桥墩钢铁与外接电源负极相连的方法,称为牺牲阳极的阴极保护法
D.“绿氢”燃料电池客车投入“冰丝带”:光伏电解水制氢可作为“绿氢”的主要来源
4.如图各烧杯中盛有海水,铁在其中会发生腐蚀。铁腐蚀的速率由快至慢的顺序为
A.②①③④ B.②①④③ C.④②①③ D.②④①③
5.关于下列装置的叙述正确的是
选项 A B C D
装置
叙述 用牺牲阳极保护法防止铁管道被腐蚀 在铁极附近放置一片湿润的淀粉―KI试纸,试纸变蓝 铅蓄电池充电时,阴极的质量减小 电子从Fe电极流出
A.A B.B C.C D.D
6.在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,厌氧细菌可促使土壤中的 与H2反应生成S2-,加速钢管的腐蚀,其反应原理如下图所示。
下列说法正确的是( )
A.正极的电极反应式为:2H2O+O2+4e-=4OH-
B.钢管腐蚀的直接产物中含有FeS、Fe(OH)2
C.在钢管表面镀锌或镀铜均可减缓钢管的腐蚀
D. 与H2的反应可表示为:4H2+ -8e- S2-+4H2O
二、多选题
7.陕西历史博物馆展出了许多鎏金工艺青铜器。鎏金是古代常用的镀金工艺,将金汞合金涂于器物表面,加热使汞挥发,便形成一层光亮的金镀层。下列关于青铜器鎏金工艺的说法正确的
鎏金铜沐缶
A.鎏金工艺的镀金过程是一种化学变化
B.鎏金除了改善外观,还可保护青铜器,使其不易生锈
C.若表面的金镀层破损,暴露出的青铜表面会更易生锈
D.青铜比纯铜硬度小
三、填空题
8.按图1进行实验,测得锥形瓶内气压和空气中氧气的体积分数随时间变化如图2所示。t1~t2之间主要发生 (填“吸氧”或“析氢”)腐蚀,其正极反应式为 。
9.金属阳极钝化是一种电化学防护方法。将Fe 作阳极置于一定浓度的H2SO4 溶液中,一定条件下,Fe钝化形成致密Fe3O4氧化膜,试写出该过程中阳极的电极反应 。
10.海边铁制品较易被腐蚀的原因是: .写出金属防护的一种常用方法 .
11.铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中如图所示,则铁被腐蚀的速率由慢到快的顺序是(填序号) .
12.请按要求回答下列问题。
(1),的溶液中,由水电离出的浓度约为 。溶液加适量的水稀释,下列表达式的数值变大的是 (填标号)。
A. B. C. D.
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是________(填标号)。
A. B. C. D.
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。
①甲装置中负极反应式为 。
②乙装置中石墨电极上生成的气体为 (填化学式)。
③丙装置中足量,工作一段时间后,溶液的 (填“变大”、“变小”或“不变”),反应的化学方程式为 ,若要将电解后的溶液复原,需加入一定量的 (填化学式)。
四、综合题
13.Ⅰ.完成下列问题
(1)理论上不能设计为原电池的化学反应是 。
a.
b.
c.
d.
(2)电池比能量高,可用于汽车、航天等领域。电池反应式为:,放电时,下列说法正确的是 。
a.电能转化成化学能 b.在正极发生氧化反应
c.正离子由负极移向正极 d.在负极失去电子
(3)下列关于金属腐蚀与防护的说法不正确的是 。
a.图①,放置于干燥空气中的铁钉不易生锈
b.图②,若断开电源,钢闸门将发生吸氧腐蚀
c.图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀
d.图③,若金属比活泼,可防止输水管腐蚀
Ⅱ.某实验小组为探究与能否发生氧化还原反应,设计如下双液原电池(盐桥中为饱和溶液的琼脂)。
(4)该装置石墨棒上发生的电极反应式为 ,盐桥中向 烧杯移动。(填“甲”或“乙”)
Ⅲ.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
根据要求回答相关问题:
(5)写出氢气所在电极的电极反应式 。
(6)石墨电极为 (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液, (填“铁极”或“石墨极”)区的溶液先变红。
(7)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将 (填“增大”“减小”或“不变”)。当甲装置消耗标准状况下时,丙装置中纯铜电极增重 g。
14.
(1)由氢气和氧气反应生成1mol水蒸气放热242kJ,写出该反应的热化学方程式: 。
已知断裂1molH2、1molO2的化学键分别需要消耗436kJ、496kJ的能量,则断裂1molH-O所需的能量为 kJ。
(2)已知:①CH4(g)+H2O(g) CO(g)+3H2(g)△H1=+205.9kJ mol-1
②CO(g)+H2O(g) CO2(g)+H2(g)△H2=-41.2kJ mol-1
则反应③:CH4(g)+CO2(g) 2CO(g)+2H2(g)△H3= kJ mol-1。
写出反应③的平衡常数表达式K= 。
(3)若将反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,则该电池正极的电极反应式为: 。
(4)如图所示,水槽中试管内有一枚铁钉,放置数天后观察,发现试管内液面上升,铁钉表面出现铁锈。该铁钉发生的电化学腐蚀类型为 腐蚀,其正极电极反应式为 。
五、解答题
15.某同学为了探究不同条件下铁钉的锈蚀情况,设计了如下实验:
(ⅰ)取三支试管,标记为I、II、III,I中盛有适量蒸馏水,II中盛有适量蒸馏水和植物油,III洁净干燥
(ⅱ)在三支试管中各放入一根无锈铁钉.并将II和III用软木塞塞紧,III中放入一小团棉花(如图所示).请回答:
(1)三支试管中铁钉锈蚀的速度从高到低依次排列为
由此可以得出铁钉锈蚀的条件有 和 .
若该同学将I放在每天阳光直晒的阳台上,与避光保存相比,哪种保存方法锈蚀更快?这说明锈蚀速度与什么因素有关?
若该同学将I中的液体换做食盐水,对锈蚀的速率有何影响?这说明锈蚀速率还和什么因素有关? .
六、实验探究题
16.如图所示套实验装置,分别回答下列问题:
(1)装置1为铁的吸氧腐蚀实验.一段时间后,向插入铁钉的玻璃筒内滴入KSCN溶液呈无色,再滴入氯水即可观察到铁钉附近的溶液变红色,表明铁被 ;向插入碳棒的玻璃筒内滴入酚酞试液,可观察到碳棒附近的溶液变红,该电极反应为 .
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 .
(3)装置3中甲烧杯盛放100mL 0.2mol L﹣1的NaCl溶液,乙烧杯盛放100mL 0.5mol L﹣1的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞试液,观察到石墨电极附近首先变红.
①电源的M端为 极,甲烧杯中铁电极的电极反应为 ;
②乙烧杯中电解反应的离子方程式为 ;
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64g,则甲烧杯中产生的气体在标准状况下为 mL.
答案解析部分
1.【答案】C
【知识点】金属的电化学腐蚀与防护
2.【答案】C
【知识点】金属的电化学腐蚀与防护
3.【答案】C
【知识点】氧化还原反应;金属的电化学腐蚀与防护
4.【答案】A
【知识点】金属的电化学腐蚀与防护
5.【答案】C
【知识点】金属的电化学腐蚀与防护;电解原理;电解池工作原理及应用
6.【答案】B
【知识点】金属的电化学腐蚀与防护
7.【答案】B,C
【知识点】金属的电化学腐蚀与防护;合金及其应用;原电池工作原理及应用
8.【答案】吸氧;O2+2H2O+4e-=4OH-
【知识点】铁的吸氧腐蚀
9.【答案】3Fe-8e-+4H2O=Fe3O4+8H+
【知识点】金属的电化学腐蚀与防护;电解池工作原理及应用
10.【答案】铁制品和海水构成原电池,铁制品中铁作负极易失电子发生电化学腐蚀,所以铁加速被腐蚀;刷油漆(涂油酯、电镀、包塑料膜)等
【知识点】金属的电化学腐蚀与防护
11.【答案】Ⅱ<Ⅲ<Ⅰ
【知识点】金属的电化学腐蚀与防护
12.【答案】(1);BD
(2)B
(3);;变小;;或
【知识点】金属的电化学腐蚀与防护
13.【答案】b;d;c;Fe3++e-=Fe2+;甲;H2-2e-+2OH-=2H2O;阳极;铁极;减小;32
【知识点】电极反应和电池反应方程式;金属的电化学腐蚀与防护;电解池工作原理及应用
14.【答案】(1)H2(g)+ O2(g)=H2O(g)△H=-242kJ mol-1;463
(2)+247.1; (或 )
(3)Fe3++e-=Fe2+
(4)吸氧;O2+4e-+2H2O=4OH-
【知识点】反应热和焓变;热化学方程式;化学平衡常数;原电池工作原理及应用;铁的吸氧腐蚀
15.【答案】(1)I>II>III;水;氧气;阳光直晒腐蚀快,温度越高金属腐蚀越快;腐蚀加快,加入电解质溶液可以加快金属的腐蚀
【知识点】金属的电化学腐蚀与防护
16.【答案】(1)氧化;O2+4e﹣+2H2O﹣═4OH﹣
(2)正;Cu+2Fe3+=Cu2++2Fe2+
(3)正;Fe﹣2e﹣═Fe2+;2Cu2++2H2O 2Cu+O2↑+4H+;224
【知识点】原电池工作原理及应用;电解池工作原理及应用;铁的吸氧腐蚀
21世纪教育网(www.21cnjy.com)
1 / 9
