1.1.2 物质的分类(胶体)课件(共19张PPT) 人教版(2019)必修一
文档属性
| 名称 | 1.1.2 物质的分类(胶体)课件(共19张PPT) 人教版(2019)必修一 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-09-14 00:00:00 | ||
图片预览




文档简介
(共19张PPT)
第一节 物质的分类及转化
氧化物
Na K
物质
纯净物
混合物
单质
金属
单质
非金属
单质
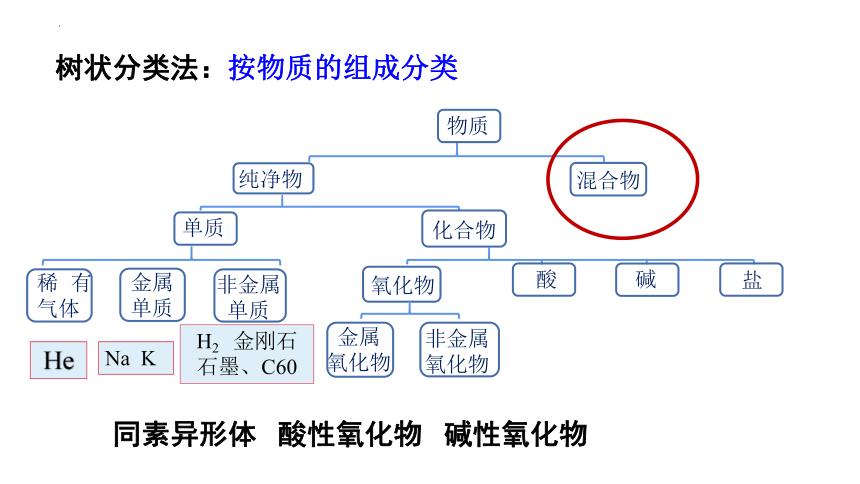
树状分类法:按物质的组成分类
金属
氧化物
非金属
氧化物
酸
碱
盐
H2 金刚石
石墨、C60
化合物
稀有气体
He
同素异形体 酸性氧化物 碱性氧化物
1、溶液、乳浊液和悬浊液都属于 (填写“物质类别”)
2、溶液由溶质和溶剂组成,乳浊液和悬浊液呢?
3、溶液、乳浊液和悬浊液的不同点是什么?
4、胶体是如何定义的?
5、根据分散剂的状体不同,可以将胶体分为哪几类?能举例其典型代表吗?
6、如何制得氢氧化铁胶体?
7、胶体的丁达尔现象是怎么产生的?
8、胶体能透过滤纸吗?
一、分散系
1、概念:
把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物,叫做分散系。
2、分散系组成
分散质:被分散的物质(可以是固体、液体、气体)。
分散剂:起容纳分散质作用的物质(可以是固体、液体、气体)。
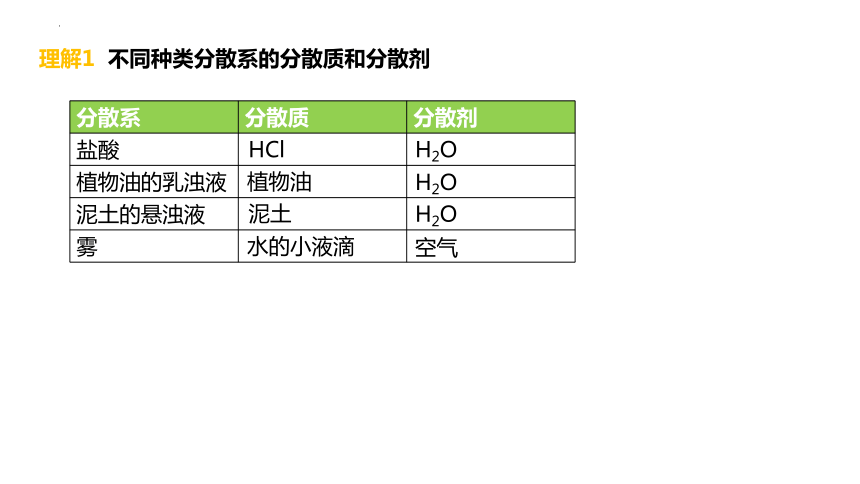
理解1 不同种类分散系的分散质和分散剂
分散系 分散质 分散剂
盐酸
植物油的乳浊液
泥土的悬浊液
雾
HCl
H2O
植物油
H2O
泥土
H2O
水的小液滴
空气
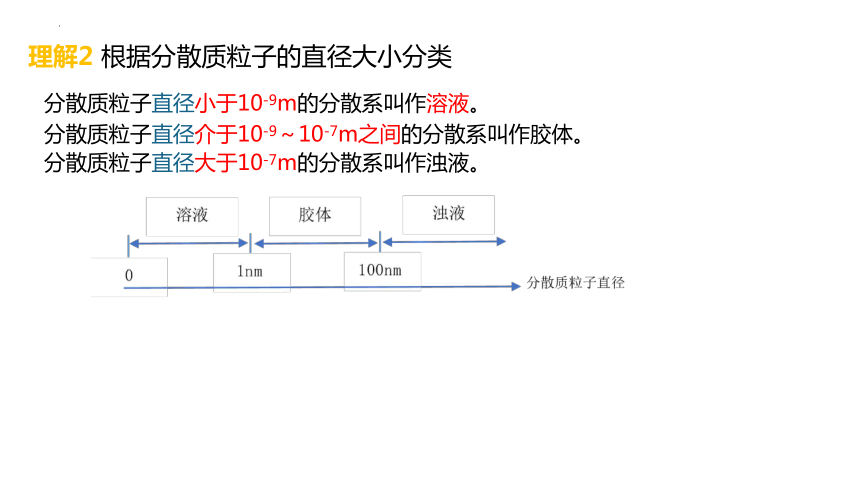
分散质粒子直径小于10-9m的分散系叫作溶液。
理解2 根据分散质粒子的直径大小分类
分散质粒子直径介于10-9~10-7m之间的分散系叫作胶体。
分散质粒子直径大于10-7m的分散系叫作浊液。
胶体及其分类
云 气溶胶
雾 气溶胶
有色玻璃 固溶胶
淀粉溶液 液溶胶
2.溶液和胶体的区分
操作 现象
用激光笔照射氢氧化铁胶体
用激光笔照射硫酸铜溶液
有光亮的通路
没有光亮的通路
当一束强光透过胶体时,在垂直于光线的方向可以看到一条光亮的通路
是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的丁达尔效应
丁达尔效应
区分溶液和胶体
3、胶体的制备和特征
(1) Fe(OH)3胶体的制备
①制备原理:_____________________________________
②制备操作
往烧杯中注入40 mL蒸馏水,将烧杯中的蒸馏水加
热至沸腾,向沸水中逐滴加入5~6滴FeCl3______溶液,
继续煮沸至溶液呈_______色,停止加热
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
饱和
红褐
新知讲解
探照灯
树林中的丁达尔效应
资料卡:滤纸的孔径是0.1-10微米。
问题:用滤纸可以分离胶体粒子和水吗?
大理石的硬度,
又有橡胶的弹性,
还有塑料的可塑性而且加热后不会软化?
浙江大学团队发明了一种新物质——弹性陶瓷塑料,首次在分子级别上实现有机化合物与无机离子化合物的结合,得到了一种性质完全不同于以往材料的新物质。功能之强大,可谓是一个“五边形”战士。
酸:阳离子全部是氢离子(H+)的化合物
碱:阴离子全部是氢氧根离子( OH- )的化合物
盐:由金属阳离子(或NH4+)和酸根离子构成的化合物
盐
正盐
碱式盐
酸式盐
不含H+和OH-的盐
含有H+的盐
含有OH-离子的盐
三、物质转化
新知讲解
1.基于物质类别认识物质性质
同类物质具有相似的化学性质
2.基于反应规律确定转化关系
酸碱盐的性质
化学性质 反应实例(写出化学方程式) 基本反应类型
酸的主要化学性质 与活泼金属反应 H2SO4+Mg=MgSO4+H2↑ 置换反应
与碱性氧化物反应 H2SO4+CuO=CuSO4+H2O 复分解反应
与碱反应 H2SO4+2NaOH=Na2SO4+2H2O 复分解反应
与某些盐反应 2HCl+CaCO3=CaCl2+H2O+CO2↑ 复分解反应
新知讲解
化学性质 反应实例(写出化学方程式) 基本反应类型
碱的主要化学性质 与酸反应 NaOH+HCl=NaCl+H2O 复分解反应
与酸性氧化物反应 2NaOH+CO2=Na2CO3+H2O 复分解反应
与某些盐反应 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 复分解反应
盐的主要化学性质 与较活泼金属反应 CuSO4+Zn=ZnSO4+Cu 置换反应
与某些酸反应 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 复分解反应
与某些碱反应 Na2SO4+Ba(OH)2=BaSO4↓+2NaOH 复分解反应
与某些盐反应 AgNO3+NaCl=AgCl↓+NaNO3 复分解反应
新知讲解
第一节 物质的分类及转化
氧化物
Na K
物质
纯净物
混合物
单质
金属
单质
非金属
单质
树状分类法:按物质的组成分类
金属
氧化物
非金属
氧化物
酸
碱
盐
H2 金刚石
石墨、C60
化合物
稀有气体
He
同素异形体 酸性氧化物 碱性氧化物
1、溶液、乳浊液和悬浊液都属于 (填写“物质类别”)
2、溶液由溶质和溶剂组成,乳浊液和悬浊液呢?
3、溶液、乳浊液和悬浊液的不同点是什么?
4、胶体是如何定义的?
5、根据分散剂的状体不同,可以将胶体分为哪几类?能举例其典型代表吗?
6、如何制得氢氧化铁胶体?
7、胶体的丁达尔现象是怎么产生的?
8、胶体能透过滤纸吗?
一、分散系
1、概念:
把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物,叫做分散系。
2、分散系组成
分散质:被分散的物质(可以是固体、液体、气体)。
分散剂:起容纳分散质作用的物质(可以是固体、液体、气体)。
理解1 不同种类分散系的分散质和分散剂
分散系 分散质 分散剂
盐酸
植物油的乳浊液
泥土的悬浊液
雾
HCl
H2O
植物油
H2O
泥土
H2O
水的小液滴
空气
分散质粒子直径小于10-9m的分散系叫作溶液。
理解2 根据分散质粒子的直径大小分类
分散质粒子直径介于10-9~10-7m之间的分散系叫作胶体。
分散质粒子直径大于10-7m的分散系叫作浊液。
胶体及其分类
云 气溶胶
雾 气溶胶
有色玻璃 固溶胶
淀粉溶液 液溶胶
2.溶液和胶体的区分
操作 现象
用激光笔照射氢氧化铁胶体
用激光笔照射硫酸铜溶液
有光亮的通路
没有光亮的通路
当一束强光透过胶体时,在垂直于光线的方向可以看到一条光亮的通路
是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的丁达尔效应
丁达尔效应
区分溶液和胶体
3、胶体的制备和特征
(1) Fe(OH)3胶体的制备
①制备原理:_____________________________________
②制备操作
往烧杯中注入40 mL蒸馏水,将烧杯中的蒸馏水加
热至沸腾,向沸水中逐滴加入5~6滴FeCl3______溶液,
继续煮沸至溶液呈_______色,停止加热
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
饱和
红褐
新知讲解
探照灯
树林中的丁达尔效应
资料卡:滤纸的孔径是0.1-10微米。
问题:用滤纸可以分离胶体粒子和水吗?
大理石的硬度,
又有橡胶的弹性,
还有塑料的可塑性而且加热后不会软化?
浙江大学团队发明了一种新物质——弹性陶瓷塑料,首次在分子级别上实现有机化合物与无机离子化合物的结合,得到了一种性质完全不同于以往材料的新物质。功能之强大,可谓是一个“五边形”战士。
酸:阳离子全部是氢离子(H+)的化合物
碱:阴离子全部是氢氧根离子( OH- )的化合物
盐:由金属阳离子(或NH4+)和酸根离子构成的化合物
盐
正盐
碱式盐
酸式盐
不含H+和OH-的盐
含有H+的盐
含有OH-离子的盐
三、物质转化
新知讲解
1.基于物质类别认识物质性质
同类物质具有相似的化学性质
2.基于反应规律确定转化关系
酸碱盐的性质
化学性质 反应实例(写出化学方程式) 基本反应类型
酸的主要化学性质 与活泼金属反应 H2SO4+Mg=MgSO4+H2↑ 置换反应
与碱性氧化物反应 H2SO4+CuO=CuSO4+H2O 复分解反应
与碱反应 H2SO4+2NaOH=Na2SO4+2H2O 复分解反应
与某些盐反应 2HCl+CaCO3=CaCl2+H2O+CO2↑ 复分解反应
新知讲解
化学性质 反应实例(写出化学方程式) 基本反应类型
碱的主要化学性质 与酸反应 NaOH+HCl=NaCl+H2O 复分解反应
与酸性氧化物反应 2NaOH+CO2=Na2CO3+H2O 复分解反应
与某些盐反应 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 复分解反应
盐的主要化学性质 与较活泼金属反应 CuSO4+Zn=ZnSO4+Cu 置换反应
与某些酸反应 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 复分解反应
与某些碱反应 Na2SO4+Ba(OH)2=BaSO4↓+2NaOH 复分解反应
与某些盐反应 AgNO3+NaCl=AgCl↓+NaNO3 复分解反应
新知讲解
