人教版(2019)选择性必修二 2.1.1共价键的极性 (共25张PPT)
文档属性
| 名称 | 人教版(2019)选择性必修二 2.1.1共价键的极性 (共25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-09-15 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
《第二章 分子结构与性质—共价键极性》
2022级高二·选择性必修2
共价键
极性共价键
非极性共价键
由不同原子形成的共价键,
电子对会发生偏移
由相同原子形成的共价键,电子对不发生偏移
H—Cl
δ+
δ-
氯化氢分子中的极性共价键
【任务一:键的极性】
Cl
Cl
氯气分子中的非极性共价键
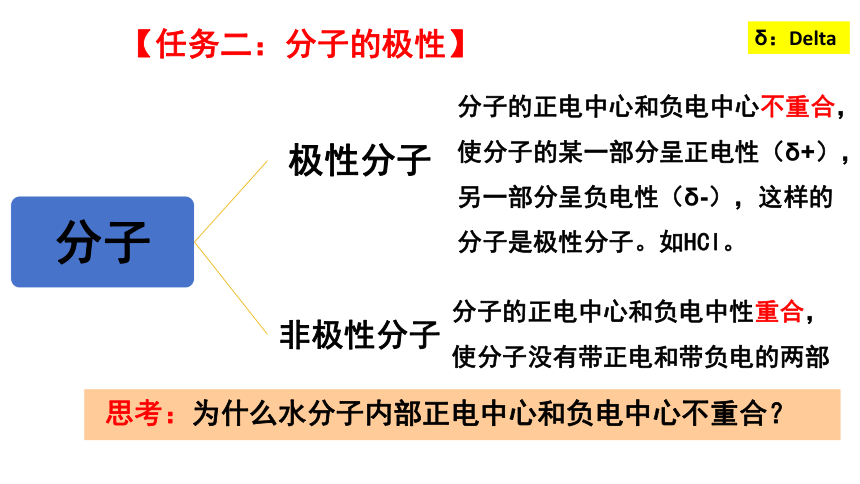
分子的正电中心和负电中心不重合,使分子的某一部分呈正电性(δ+),另一部分呈负电性(δ-),这样的分子是极性分子。如HCl。
分子的正电中心和负电中性重合,使分子没有带正电和带负电的两部
【任务二:分子的极性】
思考:为什么水分子内部正电中心和负电中心不重合?
δ:Delta
①若分子中共价键的极性的向量和等于0,则分子中没有带正电和带负电的两部分,为非极性分子,如BF3、CH4等。
从向量的角度理解分子的极性
实例
解释
3个F所带负电的负电中心与B的正电中心重合
极性的向量和等于0
4个H所带正电的正电中心与C的负电中心重合
极性的向量和等于0
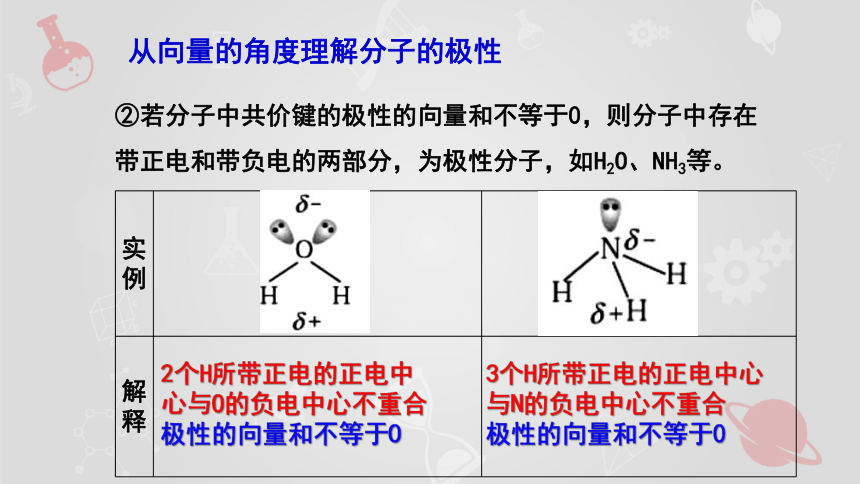
②若分子中共价键的极性的向量和不等于0,则分子中存在带正电和带负电的两部分,为极性分子,如H2O、NH3等。
实例
解释
2个H所带正电的正电中心与O的负电中心不重合
极性的向量和不等于0
3个H所带正电的正电中心与N的负电中心不重合
极性的向量和不等于0
从向量的角度理解分子的极性
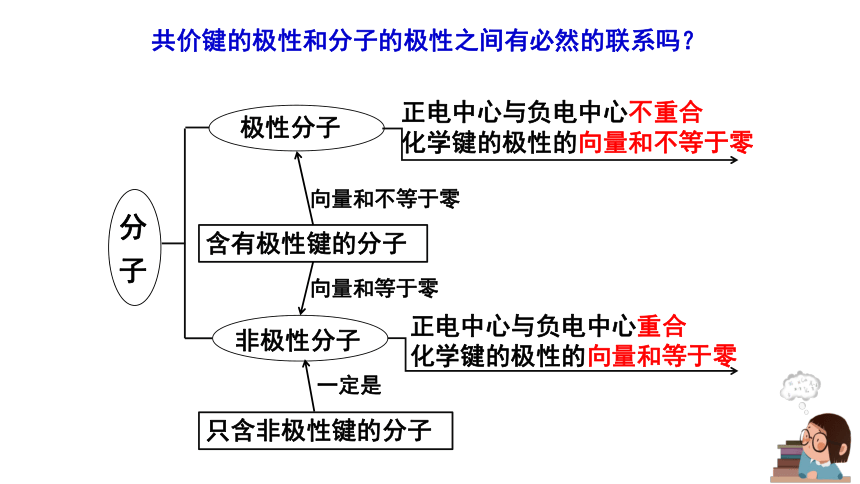
分 子
极性分子
非极性分子
正电中心与负电中心不重合
化学键的极性的向量和不等于零
正电中心与负电中心重合
化学键的极性的向量和等于零
只含非极性键的分子
含有极性键的分子
向量和不等于零
向量和等于零
一定是
共价键的极性和分子的极性之间有必然的联系吗?
是一种重要物质。大气高空的臭氧层;
保护了地球生物的生存;空气质量预报中臭氧含量是空气质量的重要指标;它还是有机合成的氧化剂、替代氯气的净水剂……
臭氧分子的空间结构与水分子的相似,
臭氧分子中的共价键是极性键,
臭氧分子有极性,但很微弱。
仅是水分子的极性的28%。
其中心氧原子是呈正电性的,
而端位的两个氧原子是呈电负性的。
臭氧是极性分子
【资料卡片】
常见的极性分子和非极性分子
如何判断分子的极性?
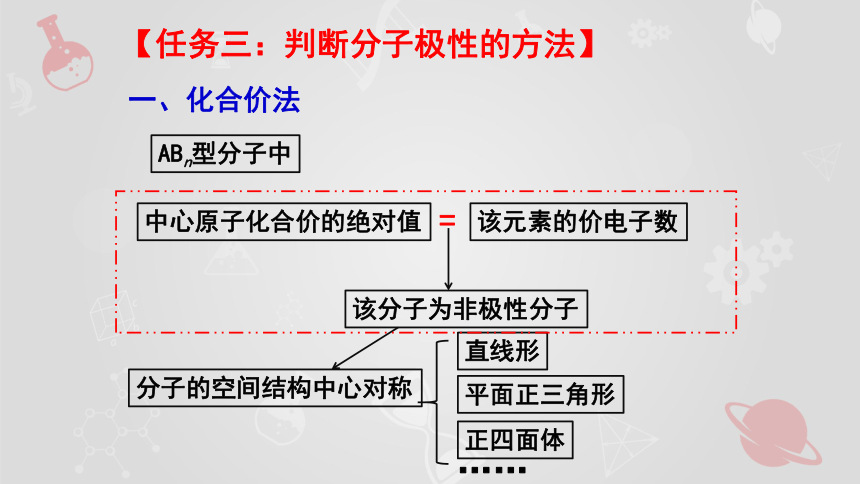
一、化合价法
ABn型分子中
中心原子化合价的绝对值
该元素的价电子数
=
该分子为非极性分子
分子的空间结构中心对称
直线形
平面正三角形
正四面体
……
【任务三:判断分子极性的方法】
ABn型分子中
中心原子化合价的绝对值
该元素的价电子数
≠
该分子为极性分子
分子的空间结构不中心对称
V形
三角锥形
四面体
……
【任务三:判断分子极性的方法】
一、化合价法
分子 BF3 CO2 PCl5 SO3 H2O NH3 SO2
化合价绝对值
价电子数
分子极性
3
3
4
4
5
5
6
6
2
6
3
5
4
6
非极性
非极性
非极性
非极性
极性
极性
极性
【任务三:判断分子极性的方法】
一、化合价法
二、根据分子的空间结构判断
分子类型 价电子对数 空间结构 分子极性 代表物
A2
AB
AB2
AB3
AB4
2+0
2+1
2+2
直线形
V形
V形
非极性分子
极性分子
极性分子
CO2、CS2
SO2、
H2O、H2S
3+0
3+1
平面三角形
三角锥
非极性分子
极性分子
BF3、AlCl3
NH3、PCl3
4+0
正四面体
非极性分子
CH4、CCl4
直线形
非极性分子
极性分子
O2、H2
HF、CO
【任务三:判断分子极性的方法】
含孤对电子对
根据图2-18,思考和回答下列问题:
(1)以下双原子分子中,哪些是极性分子,哪些是非极性分子 H2O2 、Cl2、HCl
(2)P4和C60是极性分子还是非极性分子
(3)以下化合物分子中,哪些是极性分子,哪些是非极性分子 CO2、HCN、H2O、NH3、BF3、CH4、CH3Cl
H2O2、 HCl是极性分子, Cl2 是非极性分子
HCN、H2O、NH3、CH3Cl是极性分子,
CO2、 BF3、CH4是非极性分子
P4和C60是非极性分子
【课堂练习】
①稀有气体分子是非极性分子,但不含共价键
②臭氧是极性分子,共价键为极性键
③H2O2是由极性键和非极性键构成的极性分子
【任务三:判断分子极性的方法】
科普小能手
表面活性剂
简要回答表面活性剂的去污原理
表面活性剂在水中会形成亲水基团向外,疏水基团向内的胶束,由于油渍等污垢是疏水的,会被包裹在胶束内腔,在摩擦力的作用下油渍脱离,达到去污目的。
【拓展延伸】
2Na+2H2O===2NaOH+H2↑
2Na+2CH3CH2OH 2CH3CH2ONa+H2↑
钠和水的反应
钠和乙醇的反应
为什么钠和水的反应比钠和乙醇的反应剧烈?
【思考交流】
H
O
H
C2H5
O
H
δ+
δ-
δ+
δ-
乙醇分子中的C2H5—是推电子基团,使得乙醇分子中的电子云向着远离乙基的方向偏移,羟基的极性比水分子中的小,因而钠和乙醇的反应不如钠和水的剧烈
【任务四:键的极性对化学性质的影响】
分子结构
化学键的极性
物质的化学性质
【任务四:键的极性对化学性质的影响】
CH3COOH
CH3COO- + H+
Ka =
c(CH3COO-) c(H+ )
c(CH3COOH)
pKa = -lgKa
pKa 越小,酸性越强
【任务四:键的极性对化学性质的影响】
分析表格中pKa数据的变化规律及原因
酸
性
增
强
【学生活动】
CH3
O
H
δ+
δ-
O
C
C2H5
O
H
δ+
δ-
O
C
H
O
H
δ+
δ-
O
C
【学生活动】
烃基是推电子基团,烃基越长,推电子效应越大,使羧基中的羟基的极性越小,羧酸的酸性越弱。
酸
性
增
强
分析表格中pKa数据的变化规律及原因
【学生活动】
CH2
O
H
δ+
δ-
O
C
Cl
CH3
O
H
δ+
δ-
O
C
【释疑解惑】
CH3
O
H
δ+
δ-
O
C
CH
O
H
δ+
δ-
O
C
Cl
Cl
CH3
O
H
δ+
δ-
O
C
C
O
H
δ+
δ-
O
C
Cl
Cl
Cl
酸
性
增
强
由于氯的电负性较大,极性:Cl3C— > Cl2CH— > ClCH2—
导致三氯乙酸中的羧基的极性最大,更易电离出氢离子
【释疑解惑】
《第二章 分子结构与性质—共价键极性》
2022级高二·选择性必修2
共价键
极性共价键
非极性共价键
由不同原子形成的共价键,
电子对会发生偏移
由相同原子形成的共价键,电子对不发生偏移
H—Cl
δ+
δ-
氯化氢分子中的极性共价键
【任务一:键的极性】
Cl
Cl
氯气分子中的非极性共价键
分子的正电中心和负电中心不重合,使分子的某一部分呈正电性(δ+),另一部分呈负电性(δ-),这样的分子是极性分子。如HCl。
分子的正电中心和负电中性重合,使分子没有带正电和带负电的两部
【任务二:分子的极性】
思考:为什么水分子内部正电中心和负电中心不重合?
δ:Delta
①若分子中共价键的极性的向量和等于0,则分子中没有带正电和带负电的两部分,为非极性分子,如BF3、CH4等。
从向量的角度理解分子的极性
实例
解释
3个F所带负电的负电中心与B的正电中心重合
极性的向量和等于0
4个H所带正电的正电中心与C的负电中心重合
极性的向量和等于0
②若分子中共价键的极性的向量和不等于0,则分子中存在带正电和带负电的两部分,为极性分子,如H2O、NH3等。
实例
解释
2个H所带正电的正电中心与O的负电中心不重合
极性的向量和不等于0
3个H所带正电的正电中心与N的负电中心不重合
极性的向量和不等于0
从向量的角度理解分子的极性
分 子
极性分子
非极性分子
正电中心与负电中心不重合
化学键的极性的向量和不等于零
正电中心与负电中心重合
化学键的极性的向量和等于零
只含非极性键的分子
含有极性键的分子
向量和不等于零
向量和等于零
一定是
共价键的极性和分子的极性之间有必然的联系吗?
是一种重要物质。大气高空的臭氧层;
保护了地球生物的生存;空气质量预报中臭氧含量是空气质量的重要指标;它还是有机合成的氧化剂、替代氯气的净水剂……
臭氧分子的空间结构与水分子的相似,
臭氧分子中的共价键是极性键,
臭氧分子有极性,但很微弱。
仅是水分子的极性的28%。
其中心氧原子是呈正电性的,
而端位的两个氧原子是呈电负性的。
臭氧是极性分子
【资料卡片】
常见的极性分子和非极性分子
如何判断分子的极性?
一、化合价法
ABn型分子中
中心原子化合价的绝对值
该元素的价电子数
=
该分子为非极性分子
分子的空间结构中心对称
直线形
平面正三角形
正四面体
……
【任务三:判断分子极性的方法】
ABn型分子中
中心原子化合价的绝对值
该元素的价电子数
≠
该分子为极性分子
分子的空间结构不中心对称
V形
三角锥形
四面体
……
【任务三:判断分子极性的方法】
一、化合价法
分子 BF3 CO2 PCl5 SO3 H2O NH3 SO2
化合价绝对值
价电子数
分子极性
3
3
4
4
5
5
6
6
2
6
3
5
4
6
非极性
非极性
非极性
非极性
极性
极性
极性
【任务三:判断分子极性的方法】
一、化合价法
二、根据分子的空间结构判断
分子类型 价电子对数 空间结构 分子极性 代表物
A2
AB
AB2
AB3
AB4
2+0
2+1
2+2
直线形
V形
V形
非极性分子
极性分子
极性分子
CO2、CS2
SO2、
H2O、H2S
3+0
3+1
平面三角形
三角锥
非极性分子
极性分子
BF3、AlCl3
NH3、PCl3
4+0
正四面体
非极性分子
CH4、CCl4
直线形
非极性分子
极性分子
O2、H2
HF、CO
【任务三:判断分子极性的方法】
含孤对电子对
根据图2-18,思考和回答下列问题:
(1)以下双原子分子中,哪些是极性分子,哪些是非极性分子 H2O2 、Cl2、HCl
(2)P4和C60是极性分子还是非极性分子
(3)以下化合物分子中,哪些是极性分子,哪些是非极性分子 CO2、HCN、H2O、NH3、BF3、CH4、CH3Cl
H2O2、 HCl是极性分子, Cl2 是非极性分子
HCN、H2O、NH3、CH3Cl是极性分子,
CO2、 BF3、CH4是非极性分子
P4和C60是非极性分子
【课堂练习】
①稀有气体分子是非极性分子,但不含共价键
②臭氧是极性分子,共价键为极性键
③H2O2是由极性键和非极性键构成的极性分子
【任务三:判断分子极性的方法】
科普小能手
表面活性剂
简要回答表面活性剂的去污原理
表面活性剂在水中会形成亲水基团向外,疏水基团向内的胶束,由于油渍等污垢是疏水的,会被包裹在胶束内腔,在摩擦力的作用下油渍脱离,达到去污目的。
【拓展延伸】
2Na+2H2O===2NaOH+H2↑
2Na+2CH3CH2OH 2CH3CH2ONa+H2↑
钠和水的反应
钠和乙醇的反应
为什么钠和水的反应比钠和乙醇的反应剧烈?
【思考交流】
H
O
H
C2H5
O
H
δ+
δ-
δ+
δ-
乙醇分子中的C2H5—是推电子基团,使得乙醇分子中的电子云向着远离乙基的方向偏移,羟基的极性比水分子中的小,因而钠和乙醇的反应不如钠和水的剧烈
【任务四:键的极性对化学性质的影响】
分子结构
化学键的极性
物质的化学性质
【任务四:键的极性对化学性质的影响】
CH3COOH
CH3COO- + H+
Ka =
c(CH3COO-) c(H+ )
c(CH3COOH)
pKa = -lgKa
pKa 越小,酸性越强
【任务四:键的极性对化学性质的影响】
分析表格中pKa数据的变化规律及原因
酸
性
增
强
【学生活动】
CH3
O
H
δ+
δ-
O
C
C2H5
O
H
δ+
δ-
O
C
H
O
H
δ+
δ-
O
C
【学生活动】
烃基是推电子基团,烃基越长,推电子效应越大,使羧基中的羟基的极性越小,羧酸的酸性越弱。
酸
性
增
强
分析表格中pKa数据的变化规律及原因
【学生活动】
CH2
O
H
δ+
δ-
O
C
Cl
CH3
O
H
δ+
δ-
O
C
【释疑解惑】
CH3
O
H
δ+
δ-
O
C
CH
O
H
δ+
δ-
O
C
Cl
Cl
CH3
O
H
δ+
δ-
O
C
C
O
H
δ+
δ-
O
C
Cl
Cl
Cl
酸
性
增
强
由于氯的电负性较大,极性:Cl3C— > Cl2CH— > ClCH2—
导致三氯乙酸中的羧基的极性最大,更易电离出氢离子
【释疑解惑】
