人教版(2019)选择性必修三 3.4 羧酸 (共34张PPT)
文档属性
| 名称 | 人教版(2019)选择性必修三 3.4 羧酸 (共34张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-09-18 00:00:00 | ||
图片预览










文档简介
(共34张PPT)
羧酸、酯
carboxylic acid and ester
人教版高中化学选择性必修3
羧 酸
1
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。故醋在古代又叫“苦酒”。
醋的来历?
酉
廿
一
日
第二十一日的酉时发现:
乙酸又名醋酸,它是食醋的主要成分,是日常生活中经常接触的一种有机酸。
自然界和日常生活中的有机酸
蚁酸(甲酸)
HCOOH
CH3COOH
醋酸(乙酸)
未成熟的梅子、李子、杏子等水果中,含有草酸、安息香酸等成分
草酸
(乙二酸)
安息香酸
(苯甲酸)
COOH
COOH
COOH
CH2COOH
CH(OH)COOH
苹果酸
乳酸
CH3CHCOOH
OH
柠檬酸
HO — C — COOH
CH2—COOH
CH2—COOH
羧酸的结构
由烃基(或氢原子)与羧基( )相连而构成的有机化合物。
-C-OH
O
羧酸:
羧酸衍生物:
羧酸分子中羧基上的羟基被其他原子或原子团取代后的生成物。
CH3-C-OCH2CH3
O
CH3-C-NH2
O
H-C-C-O-H
H O
H
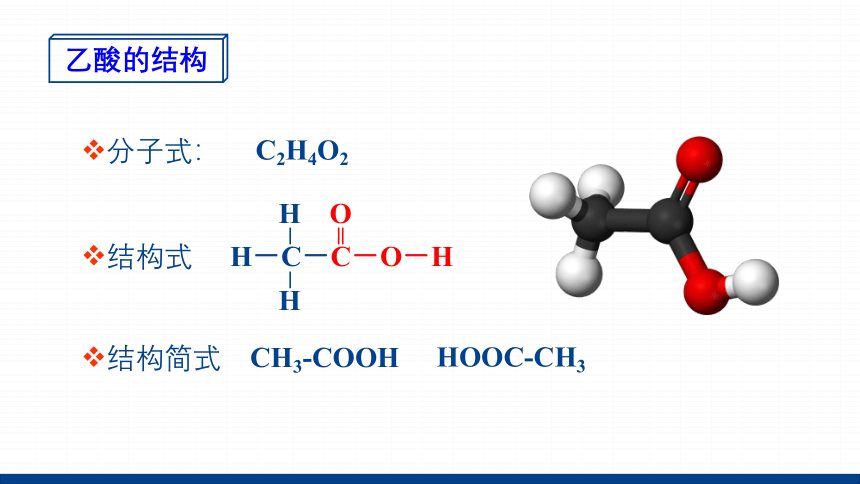
乙酸的结构
分子式:
C2H4O2
结构式
结构简式
CH3-COOH
HOOC-CH3
乙酸的物理性质
颜色、状态:
无色液体
气味:
有强烈刺激性气味
沸点:
117.9℃ (低,易挥发)
熔点:
16.6℃
溶解性:
易溶于水、乙醇等溶剂
在室温较低时,无水乙酸就会凝结成像冰一样的晶体,所以纯醋酸又称为冰醋酸
δ+
δ-
乙醛的化学性质
H-C-C-O-H
H O
H
δ+
羧酸的化学性质主要由羧基所决定,乙酸中的碳氧单键和氧氢键有较强的极性,在反应中都有断裂的可能。
化学性质
酸性
【练习】写出乙酸与CaCO3 、 NaHCO3反应方程式
羧酸具有使指示剂变色等酸的通性
2CH3COOH+CaCO3 →(CH3COO)2Ca+CO2↑+H2O
CH3COOH+NaHCO3 →CH3COONa+CO2↑+H2O
CH3COOH CH3COO – + H+
乙醇 水 苯酚 碳酸 乙酸
电离程度 不电离 微弱电离 部分电离 部分电离 部分电离
酸碱性 中性 中性 弱酸性 弱酸性 弱酸性
与Na 反应 反应 反应 反应 反应
与NaOH 不反应 不反应 反应 反应 反应
与Na2CO3 不反应 不反应 反应 反应 反应
与NaHCO3 不反应 不反应 不反应 不反应 反应
氢原子的活泼性
化学性质
酸性
越来越活泼
科学探究
探究乙酸、碳酸、苯酚酸性强弱
步骤要求:
﹙1﹚根据提供的仪器及药品,讨论并设计实验方案
﹙2﹚依据方案,连接实验装置。
﹙3﹚进行实验,探究乙酸、碳酸、苯酚的酸性强弱
﹙4﹚记录实验现象
﹙5﹚根据实验结果分析酸性强弱顺序
酸性 CH3COOH > H2CO3 > C6H5OH
实验方案:
仪器连接顺序:
A-D-E-B-C-F-G-H-I-J
实验现象:
碳酸钠试剂瓶中有气体产生。产生的气体通入苯酚钠溶液,溶液变浑浊。
结论:
【练习】下列物质不可以鉴别乙酸、乙醇、苯的
金属钠 B.溴水
C.碳酸钠溶液 D.紫色石蕊试液
B
化学性质
酸性
化学性质
酯化反应
+
CH3-C-O-H
O
H-O-CH2CH3
CH3-C-OCH2CH3
O
H2O
+
浓硫酸
△
乙酸
乙酸乙酯
乙醇
水
酸脱羟基醇脱氢
反应机理
18
18
可逆反应
反应特点
【练习】若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )
A 1种 B 2种 C 3 种 D 4种
C
CH3COOH和
【练习】写出 发生酯化反应的方程式。
2CH3COOH +
+ 2H2O
CH2OOCCH3
CH2OOCCH3
CH2OH
CH2OH
CH2OH
CH2OH
【练习】写出 发生酯化反应的方程式。
+ 2H2O
COOCH2CH3
COOCH2CH3
CH3CH2OH和
2CH3CH2OH +
COOH
COOH
COOH
COOH
【练习】写出HNO3和丙三醇发生酯化反应的方程式。
CH2OH
CH OH
CH2OH
+ 3HO-NO2
CH2O-NO2
CH O-NO2
CH2O-NO2
+ 3H2O
【练习】写出下列物质可以发生酯化成环的方程式
②
①
和
【练习】写出下列物质可以发生酯化成环的方程式
③
④
⑤
⑥
【练习】写出下列物质可以发生酯化成环的方程式
【练习】写出HOCHCOOH缩聚反应的方程式
-
CH3
n HOCHCOOH
-O-CH-C-
[
]n
-
-
O
+ (n-1)H2O
OH
H
-
CH3
-
CH3
【练习】写出HOCHCOOH缩聚反应的方程式
-
CH3
【练习】写出 缩聚反应的方程式
和
+ n
n
+ (2n-1)H2O
-O-CH2-CH2-O-C-C-
[
]n
-
-
-
-
O
O
H
OH
几种重要的羧酸
甲酸
推测
O
H—C—OH
羧基
既具有醛的性质
又具有羧酸的性质
醛基
无色、有刺激性气味的液体,
有腐蚀性,
能与水、乙醇等互溶。
推测可能发生的化学反应方程式
银镜反应
与新制Cu(OH)2
与金属钠反应
与碳酸钠反应
与碱反应
酯化反应
COOH
苯甲酸
无色晶体、易升华,微溶于水、易溶于乙醇。
可以用于合成香料、药物等,它的钠盐是常用的食品防腐剂。
草酸
(乙二酸)
COOH
COOH
无色晶体,可溶于水和乙醇。
化学分析中常用的还原剂,也是重要的化工原料。
2KMnO4 + 5H2C2O4 + 3H2SO4→ K2SO4+ 2MnSO4+ 10CO2↑+ 8H2O
H2C2O4 . 2H2O
羧酸、酯
carboxylic acid and ester
人教版高中化学选择性必修3
羧 酸
1
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。故醋在古代又叫“苦酒”。
醋的来历?
酉
廿
一
日
第二十一日的酉时发现:
乙酸又名醋酸,它是食醋的主要成分,是日常生活中经常接触的一种有机酸。
自然界和日常生活中的有机酸
蚁酸(甲酸)
HCOOH
CH3COOH
醋酸(乙酸)
未成熟的梅子、李子、杏子等水果中,含有草酸、安息香酸等成分
草酸
(乙二酸)
安息香酸
(苯甲酸)
COOH
COOH
COOH
CH2COOH
CH(OH)COOH
苹果酸
乳酸
CH3CHCOOH
OH
柠檬酸
HO — C — COOH
CH2—COOH
CH2—COOH
羧酸的结构
由烃基(或氢原子)与羧基( )相连而构成的有机化合物。
-C-OH
O
羧酸:
羧酸衍生物:
羧酸分子中羧基上的羟基被其他原子或原子团取代后的生成物。
CH3-C-OCH2CH3
O
CH3-C-NH2
O
H-C-C-O-H
H O
H
乙酸的结构
分子式:
C2H4O2
结构式
结构简式
CH3-COOH
HOOC-CH3
乙酸的物理性质
颜色、状态:
无色液体
气味:
有强烈刺激性气味
沸点:
117.9℃ (低,易挥发)
熔点:
16.6℃
溶解性:
易溶于水、乙醇等溶剂
在室温较低时,无水乙酸就会凝结成像冰一样的晶体,所以纯醋酸又称为冰醋酸
δ+
δ-
乙醛的化学性质
H-C-C-O-H
H O
H
δ+
羧酸的化学性质主要由羧基所决定,乙酸中的碳氧单键和氧氢键有较强的极性,在反应中都有断裂的可能。
化学性质
酸性
【练习】写出乙酸与CaCO3 、 NaHCO3反应方程式
羧酸具有使指示剂变色等酸的通性
2CH3COOH+CaCO3 →(CH3COO)2Ca+CO2↑+H2O
CH3COOH+NaHCO3 →CH3COONa+CO2↑+H2O
CH3COOH CH3COO – + H+
乙醇 水 苯酚 碳酸 乙酸
电离程度 不电离 微弱电离 部分电离 部分电离 部分电离
酸碱性 中性 中性 弱酸性 弱酸性 弱酸性
与Na 反应 反应 反应 反应 反应
与NaOH 不反应 不反应 反应 反应 反应
与Na2CO3 不反应 不反应 反应 反应 反应
与NaHCO3 不反应 不反应 不反应 不反应 反应
氢原子的活泼性
化学性质
酸性
越来越活泼
科学探究
探究乙酸、碳酸、苯酚酸性强弱
步骤要求:
﹙1﹚根据提供的仪器及药品,讨论并设计实验方案
﹙2﹚依据方案,连接实验装置。
﹙3﹚进行实验,探究乙酸、碳酸、苯酚的酸性强弱
﹙4﹚记录实验现象
﹙5﹚根据实验结果分析酸性强弱顺序
酸性 CH3COOH > H2CO3 > C6H5OH
实验方案:
仪器连接顺序:
A-D-E-B-C-F-G-H-I-J
实验现象:
碳酸钠试剂瓶中有气体产生。产生的气体通入苯酚钠溶液,溶液变浑浊。
结论:
【练习】下列物质不可以鉴别乙酸、乙醇、苯的
金属钠 B.溴水
C.碳酸钠溶液 D.紫色石蕊试液
B
化学性质
酸性
化学性质
酯化反应
+
CH3-C-O-H
O
H-O-CH2CH3
CH3-C-OCH2CH3
O
H2O
+
浓硫酸
△
乙酸
乙酸乙酯
乙醇
水
酸脱羟基醇脱氢
反应机理
18
18
可逆反应
反应特点
【练习】若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )
A 1种 B 2种 C 3 种 D 4种
C
CH3COOH和
【练习】写出 发生酯化反应的方程式。
2CH3COOH +
+ 2H2O
CH2OOCCH3
CH2OOCCH3
CH2OH
CH2OH
CH2OH
CH2OH
【练习】写出 发生酯化反应的方程式。
+ 2H2O
COOCH2CH3
COOCH2CH3
CH3CH2OH和
2CH3CH2OH +
COOH
COOH
COOH
COOH
【练习】写出HNO3和丙三醇发生酯化反应的方程式。
CH2OH
CH OH
CH2OH
+ 3HO-NO2
CH2O-NO2
CH O-NO2
CH2O-NO2
+ 3H2O
【练习】写出下列物质可以发生酯化成环的方程式
②
①
和
【练习】写出下列物质可以发生酯化成环的方程式
③
④
⑤
⑥
【练习】写出下列物质可以发生酯化成环的方程式
【练习】写出HOCHCOOH缩聚反应的方程式
-
CH3
n HOCHCOOH
-O-CH-C-
[
]n
-
-
O
+ (n-1)H2O
OH
H
-
CH3
-
CH3
【练习】写出HOCHCOOH缩聚反应的方程式
-
CH3
【练习】写出 缩聚反应的方程式
和
+ n
n
+ (2n-1)H2O
-O-CH2-CH2-O-C-C-
[
]n
-
-
-
-
O
O
H
OH
几种重要的羧酸
甲酸
推测
O
H—C—OH
羧基
既具有醛的性质
又具有羧酸的性质
醛基
无色、有刺激性气味的液体,
有腐蚀性,
能与水、乙醇等互溶。
推测可能发生的化学反应方程式
银镜反应
与新制Cu(OH)2
与金属钠反应
与碳酸钠反应
与碱反应
酯化反应
COOH
苯甲酸
无色晶体、易升华,微溶于水、易溶于乙醇。
可以用于合成香料、药物等,它的钠盐是常用的食品防腐剂。
草酸
(乙二酸)
COOH
COOH
无色晶体,可溶于水和乙醇。
化学分析中常用的还原剂,也是重要的化工原料。
2KMnO4 + 5H2C2O4 + 3H2SO4→ K2SO4+ 2MnSO4+ 10CO2↑+ 8H2O
H2C2O4 . 2H2O
