2.3物质的量 课件(共18张PPT)2024-2025学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 2.3物质的量 课件(共18张PPT)2024-2025学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 15.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-09-22 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
物质的量
(第一课时)
人教版必修一第二章第三节
知识
能力
素养
认识摩尔是物质的量的单位,了解阿伏伽德罗常数,知道摩尔质量的概念和表达式。
能运用物质的量、摩尔质量之间的关系进行简单计算。
通过“打包”模型的建构和摩尔质量的推导,发展证据推理与模型认知的核心素养,体会宏观与微观之间的内在联系。
学习目标
认识“集合体”
资料显示,营造这样的舞台效果大约需要采购22kg的干冰,你知道这些干冰中包含了多少个CO2分子吗?
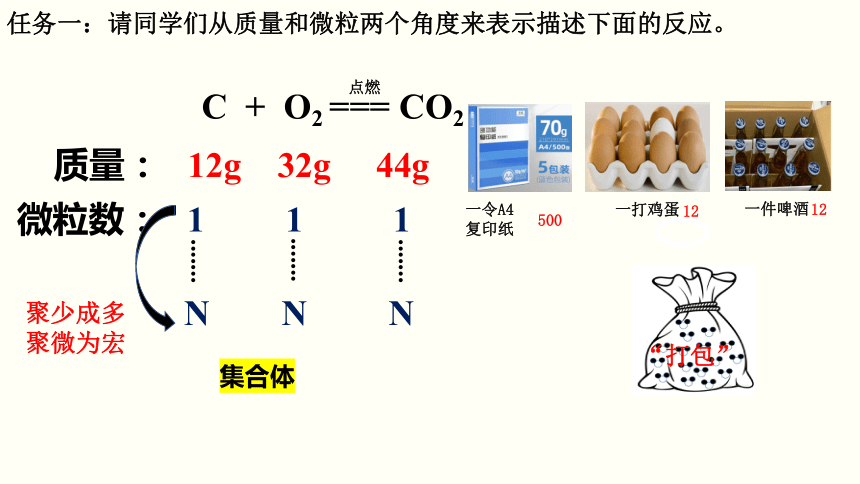
任务一:请同学们从质量和微粒两个角度来表示描述下面的反应。
C + O2 === CO2
点燃
质量: 12g 32g 44g
微粒数: 1 1 1
.......
.......
.......
N N N
聚少成多
聚微为宏
“打包”
一令A4
复印纸
一打鸡蛋
一件啤酒
500
12
12
集合体
2、符号:n
1、定义:表示含有一定数目微观粒子的集合体
3、单位:mol(摩尔)
一、物质的量
物质的量的是一个专有名词,在表述时不可增减,不可分割。
描述对象:微观粒子(分子、原子、离子、电子、质子、中子等),不能表示宏观物质。
物质的量表示的是很多个微粒的集合体,其数值可以是整数,也可以是小数。
在使用物质的量表示物质时,必须具体指明粒子的种类。
专有化
具体化
微观化
集体化
1mol氢( ) 1mol H2( )
0.5 molO2
注意事项
1mol H2O
1mol Zn
1mol Na+
1mol SO42-
1mol到底是多少粒子的“集合体”?
1mol H2O
1mol Zn
1mol Na+
1mol SO42-
6.02×10 个钠离子
6.02×10 个锌原子
6.02×10 个水分子
6.02×10 个硫酸根离子
1 mol任何粒子集体所含的粒子数≈6.02×10 个
1、定义:1 mol粒子集合体所含粒子数
【注意】阿伏加德罗常数是一个物理量,有单位,而不是纯数,不能误认为NA就是6.02×1023。
二、阿伏伽德罗常数
2、符号:NA
3、单位: mol-1
4、数值:6.02×1023 mol-1
阿莫迪欧·阿伏伽德罗
意大利化学家
(1776~1856)
6.02X1022个CH4,中有___ molCH4, 有___ molC, 有___ mol H;
含有1.204X 1023个H的H2SO4的物质的量是___ mol, 含有__ mol O.
2 molCO2是___ 个CO2, 10molCl- 是___ 个Cl-, a mol N2是___ 个N2.
课堂练习
n(物质的量)
N(粒子总数)
1mol
NA 个
2mol
2×NA 个
……
…
n mol
n×NA 个
N
NA
n=
思考交流
1 mol H2O
约有6.02×1023个水分子
1 mol Al
约有6.02×1023 个铝原子
1mol任何微观物质都约含6.02×1023个粒子,那么,这1mol物质的质量到底有多大?
???
粒子符号 物质的相对分子(原子)质量 每个粒子的质量(g/个) 1mol微粒含有的粒子数(个) 1mol物质的质量(g) 摩尔质量(g·mol-1)
C 1.993×10-23 12
Fe 9.302×10-23 56
H2SO4 1.628×10-22 98
H2O 2.990×10-23 18
Na+ 3.821×10-23 23
OH- 2.824×10-23 17
6.02x1023
6.02x1023
6.02x1023
6.02x1023
6.02x1023
6.02x1023
12
56
98
18
23
17
12
56
98
18
23
17
1mol任何微粒或物质的质量,当以g为单位时,在数值上等于该微粒的相对原子质量或相对分子质量.
发现规律
★对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的质量、物质的量改变而发生变化。
三、摩尔质量
密度: 单位体积的物质所具有的质量。
符号:ρ
单位: g/m3
m
V
ρ=
表达式:
单位物质的量的物质所具有的质量。
M
g/mol
表达式:
m
n
M=
摩尔质量:
符号:
单位:
?
?
注意
SO2的摩尔质量是____,2 mol SO2的质量是____g;
32 g SO2的物质的量是____mol,含有个____SO2.
NaOH的相对分子质量是____, 摩尔质量是____;
提高练习
小结
n
N
NA
m
M
物理量
符号
单位
物质的量
粒子数
阿伏伽德罗常数
质量
摩尔质量
mol
个
mol-1
g
g/mol
NA
N
=
M
m
=
n
16
学以致用
22kg干冰中有多少个CO2分子吗?
舞台上22kg干冰升华后变成CO2气体的体积为多少?
质量
(m)
物质的量
(n)
气体体积(V)
微粒个数
(N)
?
17
学以致用
22kg干冰中有多少个CO2分子吗?
舞台上22kg干冰升华后变成CO2气体的体积为多少?
质量
(m)
物质的量
(n)
气体体积(V)
微粒个数
(N)
?
【小结】
一、物质的量
二、阿伏伽德罗常数
三、摩尔质量
四、转化关系
概念:表示含有一定数目粒子的集合体,符号:n
单位:摩尔 ,符号:mol
符号:NA ,约为6.02×1023mol-1
关系:n=N/NA
概念:表示单位物质的量的物质所具有的质量,符号:M
关系:n=m/M
NA
N
=
M
m
=
n
物质的量
(第一课时)
人教版必修一第二章第三节
知识
能力
素养
认识摩尔是物质的量的单位,了解阿伏伽德罗常数,知道摩尔质量的概念和表达式。
能运用物质的量、摩尔质量之间的关系进行简单计算。
通过“打包”模型的建构和摩尔质量的推导,发展证据推理与模型认知的核心素养,体会宏观与微观之间的内在联系。
学习目标
认识“集合体”
资料显示,营造这样的舞台效果大约需要采购22kg的干冰,你知道这些干冰中包含了多少个CO2分子吗?
任务一:请同学们从质量和微粒两个角度来表示描述下面的反应。
C + O2 === CO2
点燃
质量: 12g 32g 44g
微粒数: 1 1 1
.......
.......
.......
N N N
聚少成多
聚微为宏
“打包”
一令A4
复印纸
一打鸡蛋
一件啤酒
500
12
12
集合体
2、符号:n
1、定义:表示含有一定数目微观粒子的集合体
3、单位:mol(摩尔)
一、物质的量
物质的量的是一个专有名词,在表述时不可增减,不可分割。
描述对象:微观粒子(分子、原子、离子、电子、质子、中子等),不能表示宏观物质。
物质的量表示的是很多个微粒的集合体,其数值可以是整数,也可以是小数。
在使用物质的量表示物质时,必须具体指明粒子的种类。
专有化
具体化
微观化
集体化
1mol氢( ) 1mol H2( )
0.5 molO2
注意事项
1mol H2O
1mol Zn
1mol Na+
1mol SO42-
1mol到底是多少粒子的“集合体”?
1mol H2O
1mol Zn
1mol Na+
1mol SO42-
6.02×10 个钠离子
6.02×10 个锌原子
6.02×10 个水分子
6.02×10 个硫酸根离子
1 mol任何粒子集体所含的粒子数≈6.02×10 个
1、定义:1 mol粒子集合体所含粒子数
【注意】阿伏加德罗常数是一个物理量,有单位,而不是纯数,不能误认为NA就是6.02×1023。
二、阿伏伽德罗常数
2、符号:NA
3、单位: mol-1
4、数值:6.02×1023 mol-1
阿莫迪欧·阿伏伽德罗
意大利化学家
(1776~1856)
6.02X1022个CH4,中有___ molCH4, 有___ molC, 有___ mol H;
含有1.204X 1023个H的H2SO4的物质的量是___ mol, 含有__ mol O.
2 molCO2是___ 个CO2, 10molCl- 是___ 个Cl-, a mol N2是___ 个N2.
课堂练习
n(物质的量)
N(粒子总数)
1mol
NA 个
2mol
2×NA 个
……
…
n mol
n×NA 个
N
NA
n=
思考交流
1 mol H2O
约有6.02×1023个水分子
1 mol Al
约有6.02×1023 个铝原子
1mol任何微观物质都约含6.02×1023个粒子,那么,这1mol物质的质量到底有多大?
???
粒子符号 物质的相对分子(原子)质量 每个粒子的质量(g/个) 1mol微粒含有的粒子数(个) 1mol物质的质量(g) 摩尔质量(g·mol-1)
C 1.993×10-23 12
Fe 9.302×10-23 56
H2SO4 1.628×10-22 98
H2O 2.990×10-23 18
Na+ 3.821×10-23 23
OH- 2.824×10-23 17
6.02x1023
6.02x1023
6.02x1023
6.02x1023
6.02x1023
6.02x1023
12
56
98
18
23
17
12
56
98
18
23
17
1mol任何微粒或物质的质量,当以g为单位时,在数值上等于该微粒的相对原子质量或相对分子质量.
发现规律
★对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的质量、物质的量改变而发生变化。
三、摩尔质量
密度: 单位体积的物质所具有的质量。
符号:ρ
单位: g/m3
m
V
ρ=
表达式:
单位物质的量的物质所具有的质量。
M
g/mol
表达式:
m
n
M=
摩尔质量:
符号:
单位:
?
?
注意
SO2的摩尔质量是____,2 mol SO2的质量是____g;
32 g SO2的物质的量是____mol,含有个____SO2.
NaOH的相对分子质量是____, 摩尔质量是____;
提高练习
小结
n
N
NA
m
M
物理量
符号
单位
物质的量
粒子数
阿伏伽德罗常数
质量
摩尔质量
mol
个
mol-1
g
g/mol
NA
N
=
M
m
=
n
16
学以致用
22kg干冰中有多少个CO2分子吗?
舞台上22kg干冰升华后变成CO2气体的体积为多少?
质量
(m)
物质的量
(n)
气体体积(V)
微粒个数
(N)
?
17
学以致用
22kg干冰中有多少个CO2分子吗?
舞台上22kg干冰升华后变成CO2气体的体积为多少?
质量
(m)
物质的量
(n)
气体体积(V)
微粒个数
(N)
?
【小结】
一、物质的量
二、阿伏伽德罗常数
三、摩尔质量
四、转化关系
概念:表示含有一定数目粒子的集合体,符号:n
单位:摩尔 ,符号:mol
符号:NA ,约为6.02×1023mol-1
关系:n=N/NA
概念:表示单位物质的量的物质所具有的质量,符号:M
关系:n=m/M
NA
N
=
M
m
=
n
