1.1.1有机化合物的分类方法 有机化合物的共价键 课件(共22张PPT)人教版选择性必修3
文档属性
| 名称 | 1.1.1有机化合物的分类方法 有机化合物的共价键 课件(共22张PPT)人教版选择性必修3 |
|
|
| 格式 | pptx | ||
| 文件大小 | 6.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-09-24 00:00:00 | ||
图片预览



文档简介
(共22张PPT)
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
第一课时
一、有机化合物的分类方法
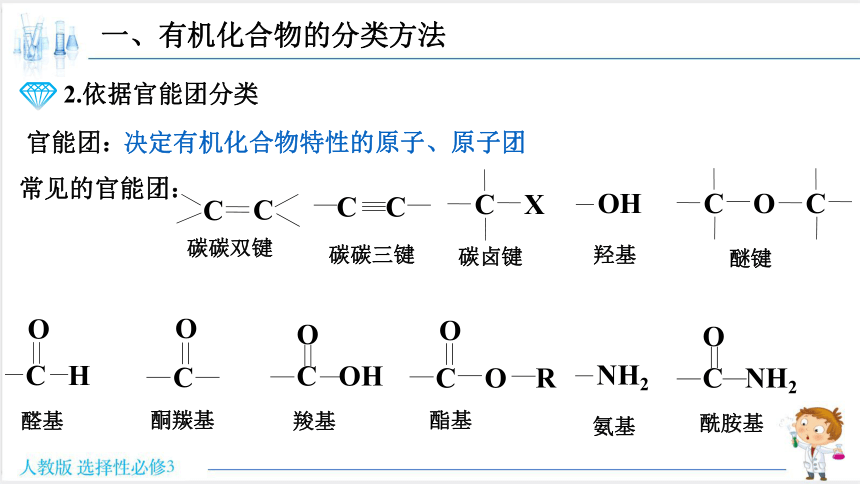
1.依据碳骨架分类
有机化合物
链状化合物
环状化合物
脂肪烃
脂肪烃衍生物
如丁烷CH3CH2CH2CH3
如溴乙烷CH3CH2Br
脂环化合物
芳香烃化合物
脂环烃
脂环烃衍生物
芳香烃
芳香族衍生物
如环己烷
如环己醇
OH
如苯
如溴苯
Br
一、有机化合物的分类方法
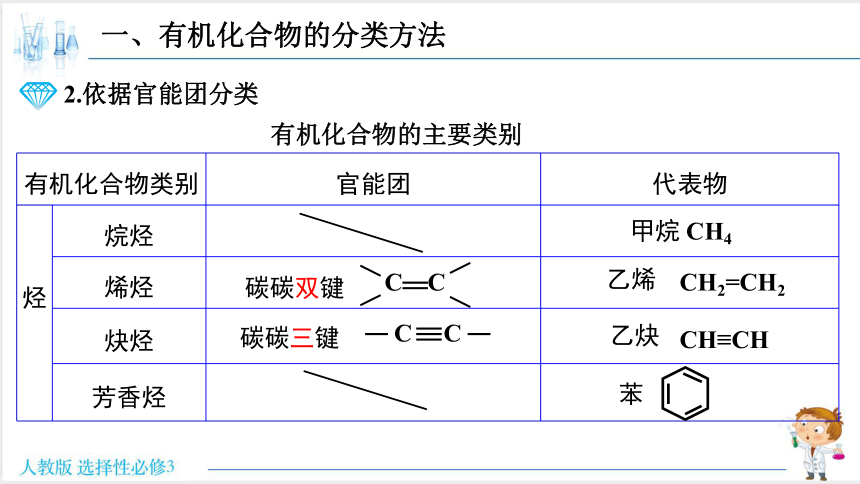
2.依据官能团分类
官能团:
决定有机化合物特性的原子、原子团
碳碳双键
碳碳三键
碳卤键
羟基
醛基
酮羰基
羧基
酯基
C C
OH
C H
O
C
O
C OH
O
常见的官能团:
C
C
C X
C O R
O
氨基
NH2
酰胺基
C NH2
O
醚键
C O
C
一、有机化合物的分类方法
2.依据官能团分类
有机化合物
烃
烃的衍生物
只含碳、氢元素的有机物
烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物
烷烃
烯烃
炔烃
芳香烃
卤代烃
醇
酚
醚
醛
酮
羧酸
羧酸
酯
胺
酰胺
一、有机化合物的分类方法
有机化合物类别 官能团 代表物
烃 烷烃
烯烃
炔烃
芳香烃
CH2=CH2
CH≡CH
C C
C C
甲烷 CH4
碳碳双键
乙烯
碳碳三键
苯
2.依据官能团分类
有机化合物的主要类别
乙炔
一、有机化合物的分类方法
有机化合物类别 官能团 代表物
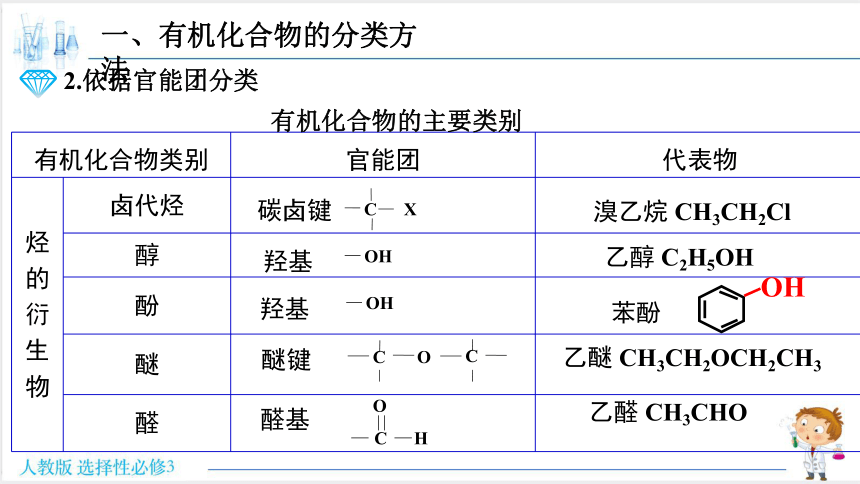
烃 的 衍 生 物 卤代烃
醇
酚
醚
醛
OH
2.依据官能团分类
有机化合物的主要类别
碳卤键
羟基
羟基
醚键
醛基
C X
OH
C H
O
OH
C O
C
溴乙烷 CH3CH2Cl
乙醇 C2H5OH
苯酚
乙醚 CH3CH2OCH2CH3
乙醛 CH3CHO
一、有机化合物的分类方法
有机化合物类别 官能团 代表物
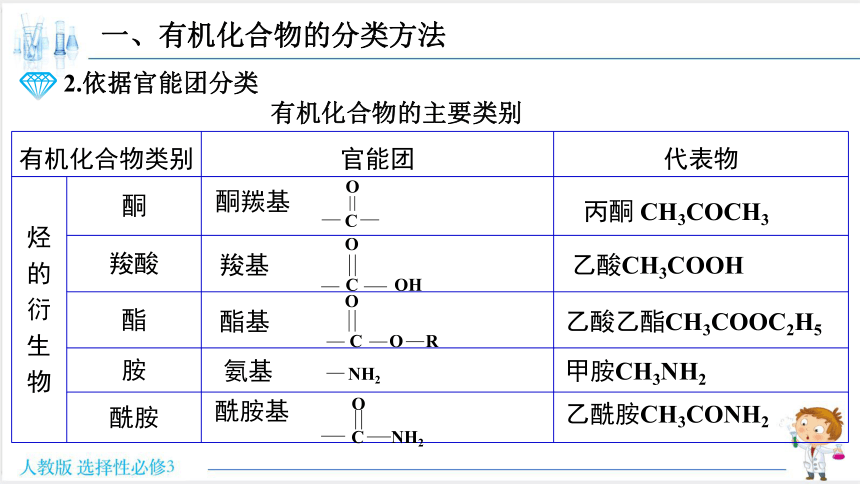
烃 的 衍 生 物 酮
羧酸
酯
胺
酰胺
2.依据官能团分类
有机化合物的主要类别
丙酮 CH3COCH3
乙酸CH3COOH
乙酸乙酯CH3COOC2H5
甲胺CH3NH2
乙酰胺CH3CONH2
酮羰基
羧基
酯基
氨基
酰胺基
C
O
C OH
O
C O R
O
NH2
C NH2
O
一、有机化合物的分类方法
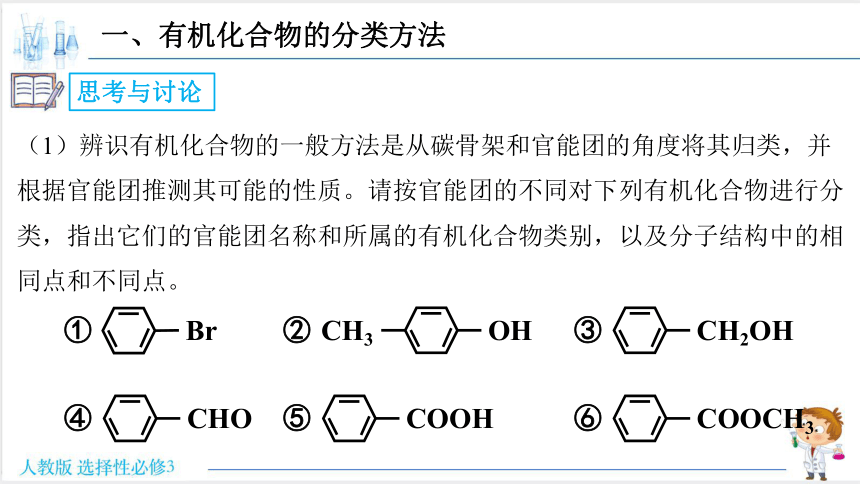
(1)辨识有机化合物的一般方法是从碳骨架和官能团的角度将其归类,并根据官能团推测其可能的性质。请按官能团的不同对下列有机化合物进行分类,指出它们的官能团名称和所属的有机化合物类别,以及分子结构中的相同点和不同点。
Br
①
②
OH
CH3
③
CH2OH
④
CHO
⑤
COOH
⑥
COOCH3
思考与讨论
一、有机化合物的分类方法
(2)有机化合物的官能团决定其化学性质。丙烯酸(CH2=CHCOOH)是重要的有机合成原料,请指出其分子中官能团的名称,并根据乙烯和乙酸的官能团及性质,推测丙烯酸可能具有的化学性质。
思考与讨论
课堂检测
CH4 CH3Cl CH3OH HCHO HCOOH HCOOCH3
1.按照官能团对下列各物质分类
HCHO HCOOCH2CH3 CH2=CH-COOH
烷烃
卤代烃
醇
醛
羧酸
酯
醛
酯
羧酸
酚
芳香烃
羧酸
C2H5
COOH
OH
HO
二、有机化合物中的共价键
在有机化合物的分子中,碳原子通过共用电子对与其它原子形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大影响。
1.共价键的类型
σ键和π键
(1)σ键
甲烷分子中的C—H和乙烷分子中的C—C都是σ键。
在甲烷分子中,氢原子的1s轨道与碳原子的一个sp3杂化轨道沿着两个原子核间的键轴,以“头碰头”的形式相互重叠,形成σ键。
通过σ键连接的原子或原子团可绕键轴旋转而不会导致化学键的破坏。
甲烷分子中的σ键
二、有机化合物中的共价键
1.共价键的类型
(2)π键
在乙烯分子中,两个碳原子均以sp2杂化轨道与氢原子的1s轨道及另一个碳原子的sp2杂化轨道进行重叠,形成4个C—H σ键与一个C—C σ键;两个碳原子未参与杂化的p轨道以“肩并肩”的形式从侧面重叠,形成了π键。
π键的轨道重叠程度比σ键的小,所以不如σ键牢固,比较容易断裂而发生化学反应。通过π键连接的原子或原子团不能绕键轴旋转。
σ键
π键
乙烯分子中的σ键和π键
二、有机化合物中的共价键
一般情况下,有机化合物中的单键是σ键,双键中含有一个σ键和一个π键,三键中含有一个σ键和两个π键。
共价键类型与反应类型密切相关。例如,甲烷分子中含有C—H σ键,能发生取代反应;乙烯和乙炔分子的双键和三键中含有π键,它们都能发生加成反应。
二、有机化合物中的共价键
思考与讨论
请从化学键和官能团的角度分析下列反应中有机化合物的变化。
(1)CH4+Cl2 CH3Cl+HCl
光
(2)CH2=CH2+Br2 CH2Br—CH2Br
课堂检测
下列反应中,官能团和化学键是如何变化的?
(4)乙酸与乙醇反应,生成乙酸乙酯。
(1)一氯甲烷与氯气反应,生成二氯甲烷。
(2)乙烯与水反应,生成乙醇。
(3)乙醇与氧气反应,生成乙醛。
浓硫酸
二、有机化合物中的共价键
由于不同的成键原子间电负性的差异,共用电子对会发生偏移。偏移的程度越大,共价键极性越强,在反应中越容易发生断裂。因此有机化合物的官能团及其邻近的化学键往往是发生化学反应的活性部位。
2.共价键的极性和有机反应
二、有机化合物中的共价键
实验1-1
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
二、有机化合物中的共价键
实验1-1
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度
剧烈程度:H2O>CH3CH2OH
受乙基的影响,乙醇分子中氢氧键的极性比水分子氢氧键的极性弱,乙醇比水更难电离出氢离子
2Na+2H2O=2NaOH+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
二、有机化合物中的共价键
为什么乙醇与钠能发生反应放出氢气?
原因在于乙醇分子中的氢氧键极性较强,能够发生断裂
同样条件下,为什么乙醇与钠的反应没有水与钠的反应剧烈?
这是由于乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱。
基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
二、有机化合物中的共价键
由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,在乙醇与氢溴酸的反应中,碳氧键发生了断裂。
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。相对无机反应,有机反应一般反应速率较小,副反应较多,产物比较复杂。
H—C—C—O—H+H—Br
H
H
H
H
△
H—C—C—Br+H2O
H
H
H
H
有机化合物的分类方法
依据碳骨架分类
依据官能团分类
有机化合物中的共价键
共价键的类型
共价键的极性和有机反应
σ键和π键
共价键的极性越强,在反应中越易发生断裂
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
第一课时
一、有机化合物的分类方法
1.依据碳骨架分类
有机化合物
链状化合物
环状化合物
脂肪烃
脂肪烃衍生物
如丁烷CH3CH2CH2CH3
如溴乙烷CH3CH2Br
脂环化合物
芳香烃化合物
脂环烃
脂环烃衍生物
芳香烃
芳香族衍生物
如环己烷
如环己醇
OH
如苯
如溴苯
Br
一、有机化合物的分类方法
2.依据官能团分类
官能团:
决定有机化合物特性的原子、原子团
碳碳双键
碳碳三键
碳卤键
羟基
醛基
酮羰基
羧基
酯基
C C
OH
C H
O
C
O
C OH
O
常见的官能团:
C
C
C X
C O R
O
氨基
NH2
酰胺基
C NH2
O
醚键
C O
C
一、有机化合物的分类方法
2.依据官能团分类
有机化合物
烃
烃的衍生物
只含碳、氢元素的有机物
烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物
烷烃
烯烃
炔烃
芳香烃
卤代烃
醇
酚
醚
醛
酮
羧酸
羧酸
酯
胺
酰胺
一、有机化合物的分类方法
有机化合物类别 官能团 代表物
烃 烷烃
烯烃
炔烃
芳香烃
CH2=CH2
CH≡CH
C C
C C
甲烷 CH4
碳碳双键
乙烯
碳碳三键
苯
2.依据官能团分类
有机化合物的主要类别
乙炔
一、有机化合物的分类方法
有机化合物类别 官能团 代表物
烃 的 衍 生 物 卤代烃
醇
酚
醚
醛
OH
2.依据官能团分类
有机化合物的主要类别
碳卤键
羟基
羟基
醚键
醛基
C X
OH
C H
O
OH
C O
C
溴乙烷 CH3CH2Cl
乙醇 C2H5OH
苯酚
乙醚 CH3CH2OCH2CH3
乙醛 CH3CHO
一、有机化合物的分类方法
有机化合物类别 官能团 代表物
烃 的 衍 生 物 酮
羧酸
酯
胺
酰胺
2.依据官能团分类
有机化合物的主要类别
丙酮 CH3COCH3
乙酸CH3COOH
乙酸乙酯CH3COOC2H5
甲胺CH3NH2
乙酰胺CH3CONH2
酮羰基
羧基
酯基
氨基
酰胺基
C
O
C OH
O
C O R
O
NH2
C NH2
O
一、有机化合物的分类方法
(1)辨识有机化合物的一般方法是从碳骨架和官能团的角度将其归类,并根据官能团推测其可能的性质。请按官能团的不同对下列有机化合物进行分类,指出它们的官能团名称和所属的有机化合物类别,以及分子结构中的相同点和不同点。
Br
①
②
OH
CH3
③
CH2OH
④
CHO
⑤
COOH
⑥
COOCH3
思考与讨论
一、有机化合物的分类方法
(2)有机化合物的官能团决定其化学性质。丙烯酸(CH2=CHCOOH)是重要的有机合成原料,请指出其分子中官能团的名称,并根据乙烯和乙酸的官能团及性质,推测丙烯酸可能具有的化学性质。
思考与讨论
课堂检测
CH4 CH3Cl CH3OH HCHO HCOOH HCOOCH3
1.按照官能团对下列各物质分类
HCHO HCOOCH2CH3 CH2=CH-COOH
烷烃
卤代烃
醇
醛
羧酸
酯
醛
酯
羧酸
酚
芳香烃
羧酸
C2H5
COOH
OH
HO
二、有机化合物中的共价键
在有机化合物的分子中,碳原子通过共用电子对与其它原子形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大影响。
1.共价键的类型
σ键和π键
(1)σ键
甲烷分子中的C—H和乙烷分子中的C—C都是σ键。
在甲烷分子中,氢原子的1s轨道与碳原子的一个sp3杂化轨道沿着两个原子核间的键轴,以“头碰头”的形式相互重叠,形成σ键。
通过σ键连接的原子或原子团可绕键轴旋转而不会导致化学键的破坏。
甲烷分子中的σ键
二、有机化合物中的共价键
1.共价键的类型
(2)π键
在乙烯分子中,两个碳原子均以sp2杂化轨道与氢原子的1s轨道及另一个碳原子的sp2杂化轨道进行重叠,形成4个C—H σ键与一个C—C σ键;两个碳原子未参与杂化的p轨道以“肩并肩”的形式从侧面重叠,形成了π键。
π键的轨道重叠程度比σ键的小,所以不如σ键牢固,比较容易断裂而发生化学反应。通过π键连接的原子或原子团不能绕键轴旋转。
σ键
π键
乙烯分子中的σ键和π键
二、有机化合物中的共价键
一般情况下,有机化合物中的单键是σ键,双键中含有一个σ键和一个π键,三键中含有一个σ键和两个π键。
共价键类型与反应类型密切相关。例如,甲烷分子中含有C—H σ键,能发生取代反应;乙烯和乙炔分子的双键和三键中含有π键,它们都能发生加成反应。
二、有机化合物中的共价键
思考与讨论
请从化学键和官能团的角度分析下列反应中有机化合物的变化。
(1)CH4+Cl2 CH3Cl+HCl
光
(2)CH2=CH2+Br2 CH2Br—CH2Br
课堂检测
下列反应中,官能团和化学键是如何变化的?
(4)乙酸与乙醇反应,生成乙酸乙酯。
(1)一氯甲烷与氯气反应,生成二氯甲烷。
(2)乙烯与水反应,生成乙醇。
(3)乙醇与氧气反应,生成乙醛。
浓硫酸
二、有机化合物中的共价键
由于不同的成键原子间电负性的差异,共用电子对会发生偏移。偏移的程度越大,共价键极性越强,在反应中越容易发生断裂。因此有机化合物的官能团及其邻近的化学键往往是发生化学反应的活性部位。
2.共价键的极性和有机反应
二、有机化合物中的共价键
实验1-1
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
二、有机化合物中的共价键
实验1-1
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度
剧烈程度:H2O>CH3CH2OH
受乙基的影响,乙醇分子中氢氧键的极性比水分子氢氧键的极性弱,乙醇比水更难电离出氢离子
2Na+2H2O=2NaOH+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
二、有机化合物中的共价键
为什么乙醇与钠能发生反应放出氢气?
原因在于乙醇分子中的氢氧键极性较强,能够发生断裂
同样条件下,为什么乙醇与钠的反应没有水与钠的反应剧烈?
这是由于乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱。
基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
二、有机化合物中的共价键
由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,在乙醇与氢溴酸的反应中,碳氧键发生了断裂。
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。相对无机反应,有机反应一般反应速率较小,副反应较多,产物比较复杂。
H—C—C—O—H+H—Br
H
H
H
H
△
H—C—C—Br+H2O
H
H
H
H
有机化合物的分类方法
依据碳骨架分类
依据官能团分类
有机化合物中的共价键
共价键的类型
共价键的极性和有机反应
σ键和π键
共价键的极性越强,在反应中越易发生断裂
