华师版科学九年级上册 第2章 酸与碱(含答案)
文档属性
| 名称 | 华师版科学九年级上册 第2章 酸与碱(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-09-25 00:00:00 | ||
图片预览


文档简介
第2章 酸与碱
班级 学号 姓名 得分
本卷可能用到的相对原子质量:
H—1 C—12 O—16 S—32 Ca—40 Cu—64
一、选择题(每小题只有一个正确答案,每题2分,共46分)
1.下列所示为人体部分体液的pH,其中酸性最强的是( )
A.胃液(0.8~1.5) B.唾液(6.6~7.1)
C.胆汁(6.8~7.4) D.血液(7.35~7.45)
2.下列有关硫酸的叙述中不正确的是( )
A.硫酸溶液中 可以大量共存
B.硫酸和盐酸溶液中都含有 H ,因此它们的化学性质相似
C.在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中,并不断搅拌
D.稀硫酸滴加到氢氧化钡溶液中,出现白色沉淀,即可说明反应已经发生
3.一些食物的近似pH如下,其中呈碱性的是( )
选项 A B C D
食物 苹果汁 西红柿汁 菠菜汁 鸡蛋清
pH 2.9~3.3 4.0~4.4 5.1~5.7 7.6~8.0
4. SO2 是一种有刺激性气味的气体,能溶于水形成亚硫酸。小明设计如图实验验证“SO2 的水溶液呈酸性”。他先向甲装置中通入 ,发现干燥的纸花不变色,然后滴入水,纸花变红。下列说法不正确的是( )
A.闻到刺激性气味,说明分子在不断运动
B.用乙装置吸收多余的SO2,应将b、c相连
C.实验证明水、SO2 都不能使紫色石蕊变红色
D.烧杯中反应为
5.利用如图所示探究物质的性质实验,点滴板①②③处是无色透明溶液。分别滴加稀盐酸,下列叙述错误的是( )
A.镁条迅速反应,铜片没有现象,则可判断镁和铜的金属活动性
B.①处有白色沉淀,则①处可能为硝酸银溶液
C.②处没有现象,则②处没有化学反应发生
D.③处有气泡,则③处可能是碳酸钠溶液
6.有一包粉末由氧化铁、氧化铜和二氧化硅三种氧化物组成,向该混合物样品中滴加过量稀盐酸,充分反应后,过滤,得到滤液和滤渣(二氧化硅是非金属氧化物,不与稀硫酸、稀盐酸等酸溶液反应)。下列有关说法正确的是( )
A.滤液中含有两种阳离子
B.滤渣中只有二氧化硅
C.在三种氧化物中,所含元素的化合价最高是+3价
D.由于铜不与稀盐酸反应,则氧化铜也不与稀盐酸反应
7.食醋里通常含有3%~5%的醋酸 食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列说法不正确的是 ( )
A.产生的气体是二氧化碳 B.加水稀释食醋,溶液pH变小
C.鸡蛋壳中含有碳酸盐 D.不宜用铝制容器盛装食醋
8.归纳总结稀硫酸的化学性质,并用“H2SO +X→盐+Y”进行整理,下列观点错误的是( )
选项 X的物质类别 观点描述
A 金属 若X为 Cu,则反应能够发生
B 金属氧化物 若X为MgO,则Y为H2O
C 碱 若 X 为 NaOH,则盐为 Na2SO
D 盐 若X为 BaCl2,则生成白色沉淀
9.下列实验中不宜使用稀盐酸的是( )
A.除去熟石灰中的石灰石 B.除去铜粉中混有的铁粉
C.除去氯化钠溶液中的碳酸钠 D.清洗铁丝表面的锈迹
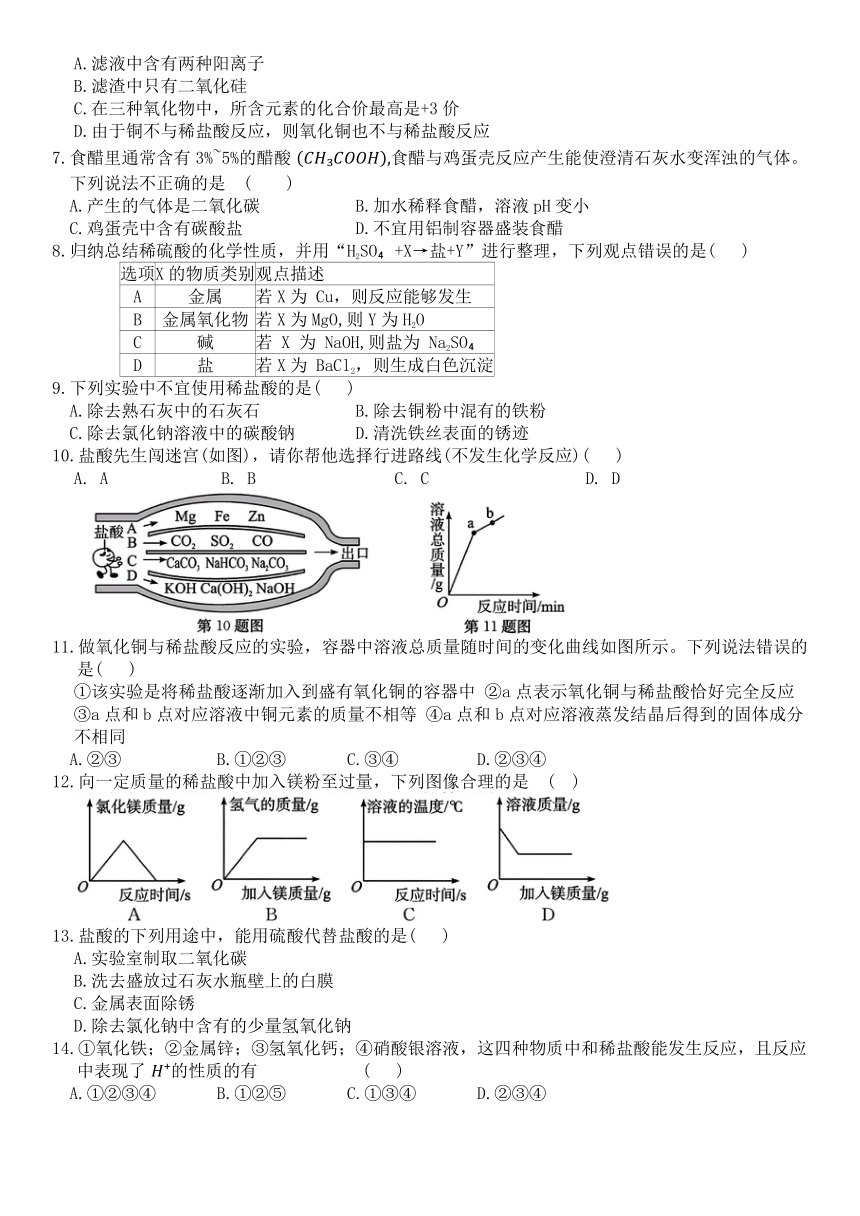
10.盐酸先生闯迷宫(如图),请你帮他选择行进路线(不发生化学反应)( )
A. A B. B C. C D. D
11.做氧化铜与稀盐酸反应的实验,容器中溶液总质量随时间的变化曲线如图所示。下列说法错误的是( )
①该实验是将稀盐酸逐渐加入到盛有氧化铜的容器中 ②a点表示氧化铜与稀盐酸恰好完全反应 ③a点和b点对应溶液中铜元素的质量不相等 ④a点和b点对应溶液蒸发结晶后得到的固体成分不相同
A.②③ B.①②③ C.③④ D.②③④
12.向一定质量的稀盐酸中加入镁粉至过量,下列图像合理的是 ( )
13.盐酸的下列用途中,能用硫酸代替盐酸的是( )
A.实验室制取二氧化碳
B.洗去盛放过石灰水瓶壁上的白膜
C.金属表面除锈
D.除去氯化钠中含有的少量氢氧化钠
14.①氧化铁;②金属锌;③氢氧化钙;④硝酸银溶液,这四种物质中和稀盐酸能发生反应,且反应中表现了 的性质的有 ( )
A.①②③④ B.①②⑤ C.①③④ D.②③④
15.小明在学习“重要的酸”知识后,结合常见酸(HCl、H2SO )的性质与变化绘制出如图所示图像。图中“ ”两端的物质都能够反应,其中酸碱中和反应生成盐和水,则其他连线的产物也都是盐和水的是( )
A. A B. B C. C D. D
16.如图表示化学反应中溶液的颜色变化。下列叙述错误的是 ( )
A.若X 是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
17.市场上的“问题藕”切开有一股难闻的酸味,估计含有硫酸或盐酸中的一种。管理人员榨取其液汁进行实验。有关说法正确的是 ( )
A.加入紫色石蕊试液,变成蓝色
B.用pH试纸测试,在9~10之间
C.选择碳酸钠溶液进行鉴别,若产生气泡,则证明含有硫酸
D.选择氯化钡溶液进行鉴别,若无明显现象,则证明含有盐酸
18.向盛有一定质量表面被氧化的镁条的烧杯中,慢慢加入一定浓度的盐酸。下列能正确反映其对应变化关系的是( )
19.下列关于硫酸的认识,正确的是( )
A.组成:硫酸溶液中H 和SOR 的数目相同
B.性质:能与CO2、SO 等非金属氧化物反应
C.用途:可用于实验室制备( 等硫酸盐
D.生产:含硫酸废水用 CaCl2 处理后直接排放
20.向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是( )
21.下列各种污垢或附着物,不宜用稀盐酸清洗的是( )
①玻璃水槽内的黄色铁锈斑 ②久置的石灰水的试剂瓶内壁的白色固体 ③不锈钢茶杯内的茶垢 ④厨房中的油污 ⑤置换反应后铁片表面附着的铜
A.①③⑤ B.②③⑤
C.③④⑤ D.①②
22.向稀硫酸中加入下列物质,可能使溶液的pH没有明显改变的是( )
A.加入 CaO B.加入 溶液
C.加入NaOH溶液 D.加入 溶液
23.向一定量稀硫酸中加入一定量铜粉,无气泡冒出;用导管向稀硫酸中通入空气并加热,铜粉逐渐减少,溶液由无色变为蓝色。测得溶液质量与实验时间的关系如图。下列说法错误的是( )
A. ab段说明 Cu不能转换出硫酸中的氢
B.从b点到c点,溶液的pH逐渐增大
C.从c点到d 点,溶液中的溶质只可能有一种
D. bc 段发生的反应为
二、填空题(每空1分,共25分)
24.某学习小组用黑枸杞提取液做了以下实验:
实验一:室温时,将蒸馏水和不同pH的硫酸、氢氧化钠溶液,放入14支试管中,分别向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
pH 1 2 3 4 5 6 7 8 9 10 11 12 13 14
颜色 粉红 粉红 粉红 浅紫 浅紫 紫 紫 蓝 蓝 深蓝 深蓝 灰绿 黄 黄棕
实验二:室温时,向试管中分别加入相同体积的4种物质,各滴加3滴黑枸杞提取液。实验结果如下:
物质 稀盐酸 牛奶 蒸馏水 炉具清洁剂
颜色 粉红 紫 紫 黄
回答下列问题:
(1)炉具清洁剂的pH为 。
(2)根据实验现象,不能确定牛奶呈中性的理由是 。
(3)小苏打溶液的pH为8.3,向小苏打溶液中滴加 3 滴黑枸杞提取液,再滴入pH为2的稀盐酸至过量,观察到的实验现象为 。
25.稀盐酸是实验室常用的试剂,有关稀盐酸的性质实验如下:
(1)若需检验某盐酸样品中是否含有硫酸,应选用的试剂是 。
(2)向放有锌粒的试管中滴加稀盐酸,有气泡产生,该反应的基本类型是 。
(3)向滴有酚酞的氢氧化钠溶液中滴加稀盐酸至过量,观察到的现象是 ,反应的化学方程式是 。
(4)镓( Ga)是一种活泼金属,能与稀盐酸反应。反应中,反应物 Ga与生成物 H2 的量关系如图所示,请写出该反应的化学方程式: 。
26.某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图。
(1)编号①反应的指示剂是 ;编号②反应的金属单质是 。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是 反应。
(3)请你写出符合编号③反应的化学方程式: 。
(4)假设编号④反应的盐是 AgNO ,则编号④对应方框中的现象是 。
27.如图是盐酸与不同类别物质之间反应的知识网络。
(1)实验室常用M与稀盐酸反应制取CO2,其主要成分化学式为 。
(2)写出金属铁与盐酸反应的化学方程式: 。
(3)用盐酸除铁锈(主要成分 Fe2O )的化学方程式是 。
(4)讨论:醋酸和盐酸具有相似的化学性质,下列说法正确的是 (填字母)。
A.能使无色酚酞试液变红色
B.能与氢氧化钠溶液发生反应
C.能与活泼金属发生反应
(5)反思:盐酸、硫酸、食醋具有相似化学性质的原因是它们水溶液中都含有 离子。
(6)氢氧化铝用以治疗胃酸过多,写出此反应的化学方程式: ,除了氢氧化铝外,下列物质也可用于治疗胃酸的是 (填字母)。
A.氢氧化钙 B.氢氧化钠 C.氢氧化镁
28.(1)MgCl2 溶液中含有少量 HCl,为除去少量 HCl可加入过量的 (多选,填字母)。
A. Mg B. MgO
(2)要将含有盐酸的氯化钙中和到中性,并得到较为纯净的氯化钙溶液,若用酚酞作指示剂,加入的试剂可以是 ;在不用指示剂的情况下,加入的试剂可以是 [均填“NaOH” ”或“NaCl”]。
(3)烧水的铝壶中常结有一层水垢(该水垢的主要成分是( 用适量稀盐酸可以除去它,反应的化学方程式是 ,若盐酸的用量过多,会产生的不良后果用化学方程式可表示为 。
三、实验探究题(每空2分,22分)
29.为了验证“酸的化学性质”,在实验室进行如图所示实验,请回答:
(1)图1中,1孔的现象是 ,4孔的现象是 。
(2)写出图2中发生中和反应的化学方程式: 。
(3)写出C试管中的现象: 。
(4)要全面验证酸的化学性质,D试管中能与酸反应的固体单质是 (写1种)。
(5)实验完成后,将A、B、C、D与第(2)问中选择物质相对应四支试管中的废液倒入废液缸内,测得 写出废液中所含全部溶质的化学式: (溶质不计指示剂与气体)。
30.如图所示,是为了验证稀硫酸化学性质所做的三个实验,回答下列问题:
(1)A实验最终能观察到的现象是 。
(2)B实验能体现出稀硫酸具有的化学性质是 。
(3)C实验中发生反应的化学方程式为 。
(4)(2分)若要证明C实验所加的 过量,小明的实验的操作及现象:取C中的上层清液少量于试管中,滴加 溶液,如果产生白色沉淀,则证明C实验所加溶液过量。你认为该同学的做法对吗 。如果不对,你的操作及现象是 °
四、分析计算题(7分)
31.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应),求:
序号 加入稀盐酸的质量/g 剩余固体质量/g
第一次 10 5.5
第二次 10 3.0
第三次 10 1.2
第四次 10 n
(1)样品中碳酸钙的质量分数是多少
(2)上表中n的数值为 。
(3)求反应生成的氯化钙的质量。
第2章 酸与碱
1. A 2. A 3. D 4. C 5. C 6. B 7. B 8. A 9. A 10. B11. C 12. B 13. C 14. B 15. C 16. C 17. D 18. C 19. C20. D 21. C 22. B 23. C
24.(1)13 (2)牛奶滴加黑枸杞提取液后为紫色,而紫色对应的pH分别为6和7 (3)有气泡生成、溶液颜色由蓝色变为粉红色
25.(1)硝酸钡溶液 (2)置换反应 (3)溶液由红色变为无色 HCl+NaOH——NaCl+H2O
(4)2Ga+6HCl——2GaCl +3H2↑
26.(1)紫色石蕊试液 铁 (2)置换 +3H2O (4)产生白色沉淀
27.(1)CaCO (2) Fe+2HCl══FeCl2+H2↑
、
(5)氢
28.(1)ABC (2) Ca(OH)2 CaCO
(3)CaCO +2HCl═CaCl2+H2O+CO2↑ 2Al+6HCl——2AlCl +3H2↑
29.(1)紫色石蕊试液变红色 无色酚酞试液不变色
(2)2NaOH+
(3)黑色粉末逐渐溶解,溶液变为蓝色
(4) Zn(或 Fe等,合理即可)
(5)H2SO 、Na2SO 、CuSO 、ZnSO
30.(1)溶液变蓝 (2)能与金属氧化物和活泼金属反应
(4)不对 取C中的上层清液少量于试管中,向其中加入硫酸钠(硫酸与可溶性硫酸盐即可)溶液,有白色沉淀生成
31.(1)8g石灰石样品中含有1.2g杂质,样品中碳酸钙的质量分数为
(2)1、2 [解析:第3次加入10g稀盐酸,充分反应后,碳酸钙完全反应,第4次加入 10g稀盐酸,剩余固体为杂质、质量不变,故n=1.2。]
(3)设完全反应后最终生成氯化钙的质量为心则
100 111
8g--1.2g x
x=7.548g
班级 学号 姓名 得分
本卷可能用到的相对原子质量:
H—1 C—12 O—16 S—32 Ca—40 Cu—64
一、选择题(每小题只有一个正确答案,每题2分,共46分)
1.下列所示为人体部分体液的pH,其中酸性最强的是( )
A.胃液(0.8~1.5) B.唾液(6.6~7.1)
C.胆汁(6.8~7.4) D.血液(7.35~7.45)
2.下列有关硫酸的叙述中不正确的是( )
A.硫酸溶液中 可以大量共存
B.硫酸和盐酸溶液中都含有 H ,因此它们的化学性质相似
C.在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中,并不断搅拌
D.稀硫酸滴加到氢氧化钡溶液中,出现白色沉淀,即可说明反应已经发生
3.一些食物的近似pH如下,其中呈碱性的是( )
选项 A B C D
食物 苹果汁 西红柿汁 菠菜汁 鸡蛋清
pH 2.9~3.3 4.0~4.4 5.1~5.7 7.6~8.0
4. SO2 是一种有刺激性气味的气体,能溶于水形成亚硫酸。小明设计如图实验验证“SO2 的水溶液呈酸性”。他先向甲装置中通入 ,发现干燥的纸花不变色,然后滴入水,纸花变红。下列说法不正确的是( )
A.闻到刺激性气味,说明分子在不断运动
B.用乙装置吸收多余的SO2,应将b、c相连
C.实验证明水、SO2 都不能使紫色石蕊变红色
D.烧杯中反应为
5.利用如图所示探究物质的性质实验,点滴板①②③处是无色透明溶液。分别滴加稀盐酸,下列叙述错误的是( )
A.镁条迅速反应,铜片没有现象,则可判断镁和铜的金属活动性
B.①处有白色沉淀,则①处可能为硝酸银溶液
C.②处没有现象,则②处没有化学反应发生
D.③处有气泡,则③处可能是碳酸钠溶液
6.有一包粉末由氧化铁、氧化铜和二氧化硅三种氧化物组成,向该混合物样品中滴加过量稀盐酸,充分反应后,过滤,得到滤液和滤渣(二氧化硅是非金属氧化物,不与稀硫酸、稀盐酸等酸溶液反应)。下列有关说法正确的是( )
A.滤液中含有两种阳离子
B.滤渣中只有二氧化硅
C.在三种氧化物中,所含元素的化合价最高是+3价
D.由于铜不与稀盐酸反应,则氧化铜也不与稀盐酸反应
7.食醋里通常含有3%~5%的醋酸 食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列说法不正确的是 ( )
A.产生的气体是二氧化碳 B.加水稀释食醋,溶液pH变小
C.鸡蛋壳中含有碳酸盐 D.不宜用铝制容器盛装食醋
8.归纳总结稀硫酸的化学性质,并用“H2SO +X→盐+Y”进行整理,下列观点错误的是( )
选项 X的物质类别 观点描述
A 金属 若X为 Cu,则反应能够发生
B 金属氧化物 若X为MgO,则Y为H2O
C 碱 若 X 为 NaOH,则盐为 Na2SO
D 盐 若X为 BaCl2,则生成白色沉淀
9.下列实验中不宜使用稀盐酸的是( )
A.除去熟石灰中的石灰石 B.除去铜粉中混有的铁粉
C.除去氯化钠溶液中的碳酸钠 D.清洗铁丝表面的锈迹
10.盐酸先生闯迷宫(如图),请你帮他选择行进路线(不发生化学反应)( )
A. A B. B C. C D. D
11.做氧化铜与稀盐酸反应的实验,容器中溶液总质量随时间的变化曲线如图所示。下列说法错误的是( )
①该实验是将稀盐酸逐渐加入到盛有氧化铜的容器中 ②a点表示氧化铜与稀盐酸恰好完全反应 ③a点和b点对应溶液中铜元素的质量不相等 ④a点和b点对应溶液蒸发结晶后得到的固体成分不相同
A.②③ B.①②③ C.③④ D.②③④
12.向一定质量的稀盐酸中加入镁粉至过量,下列图像合理的是 ( )
13.盐酸的下列用途中,能用硫酸代替盐酸的是( )
A.实验室制取二氧化碳
B.洗去盛放过石灰水瓶壁上的白膜
C.金属表面除锈
D.除去氯化钠中含有的少量氢氧化钠
14.①氧化铁;②金属锌;③氢氧化钙;④硝酸银溶液,这四种物质中和稀盐酸能发生反应,且反应中表现了 的性质的有 ( )
A.①②③④ B.①②⑤ C.①③④ D.②③④
15.小明在学习“重要的酸”知识后,结合常见酸(HCl、H2SO )的性质与变化绘制出如图所示图像。图中“ ”两端的物质都能够反应,其中酸碱中和反应生成盐和水,则其他连线的产物也都是盐和水的是( )
A. A B. B C. C D. D
16.如图表示化学反应中溶液的颜色变化。下列叙述错误的是 ( )
A.若X 是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
17.市场上的“问题藕”切开有一股难闻的酸味,估计含有硫酸或盐酸中的一种。管理人员榨取其液汁进行实验。有关说法正确的是 ( )
A.加入紫色石蕊试液,变成蓝色
B.用pH试纸测试,在9~10之间
C.选择碳酸钠溶液进行鉴别,若产生气泡,则证明含有硫酸
D.选择氯化钡溶液进行鉴别,若无明显现象,则证明含有盐酸
18.向盛有一定质量表面被氧化的镁条的烧杯中,慢慢加入一定浓度的盐酸。下列能正确反映其对应变化关系的是( )
19.下列关于硫酸的认识,正确的是( )
A.组成:硫酸溶液中H 和SOR 的数目相同
B.性质:能与CO2、SO 等非金属氧化物反应
C.用途:可用于实验室制备( 等硫酸盐
D.生产:含硫酸废水用 CaCl2 处理后直接排放
20.向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是( )
21.下列各种污垢或附着物,不宜用稀盐酸清洗的是( )
①玻璃水槽内的黄色铁锈斑 ②久置的石灰水的试剂瓶内壁的白色固体 ③不锈钢茶杯内的茶垢 ④厨房中的油污 ⑤置换反应后铁片表面附着的铜
A.①③⑤ B.②③⑤
C.③④⑤ D.①②
22.向稀硫酸中加入下列物质,可能使溶液的pH没有明显改变的是( )
A.加入 CaO B.加入 溶液
C.加入NaOH溶液 D.加入 溶液
23.向一定量稀硫酸中加入一定量铜粉,无气泡冒出;用导管向稀硫酸中通入空气并加热,铜粉逐渐减少,溶液由无色变为蓝色。测得溶液质量与实验时间的关系如图。下列说法错误的是( )
A. ab段说明 Cu不能转换出硫酸中的氢
B.从b点到c点,溶液的pH逐渐增大
C.从c点到d 点,溶液中的溶质只可能有一种
D. bc 段发生的反应为
二、填空题(每空1分,共25分)
24.某学习小组用黑枸杞提取液做了以下实验:
实验一:室温时,将蒸馏水和不同pH的硫酸、氢氧化钠溶液,放入14支试管中,分别向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
pH 1 2 3 4 5 6 7 8 9 10 11 12 13 14
颜色 粉红 粉红 粉红 浅紫 浅紫 紫 紫 蓝 蓝 深蓝 深蓝 灰绿 黄 黄棕
实验二:室温时,向试管中分别加入相同体积的4种物质,各滴加3滴黑枸杞提取液。实验结果如下:
物质 稀盐酸 牛奶 蒸馏水 炉具清洁剂
颜色 粉红 紫 紫 黄
回答下列问题:
(1)炉具清洁剂的pH为 。
(2)根据实验现象,不能确定牛奶呈中性的理由是 。
(3)小苏打溶液的pH为8.3,向小苏打溶液中滴加 3 滴黑枸杞提取液,再滴入pH为2的稀盐酸至过量,观察到的实验现象为 。
25.稀盐酸是实验室常用的试剂,有关稀盐酸的性质实验如下:
(1)若需检验某盐酸样品中是否含有硫酸,应选用的试剂是 。
(2)向放有锌粒的试管中滴加稀盐酸,有气泡产生,该反应的基本类型是 。
(3)向滴有酚酞的氢氧化钠溶液中滴加稀盐酸至过量,观察到的现象是 ,反应的化学方程式是 。
(4)镓( Ga)是一种活泼金属,能与稀盐酸反应。反应中,反应物 Ga与生成物 H2 的量关系如图所示,请写出该反应的化学方程式: 。
26.某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图。
(1)编号①反应的指示剂是 ;编号②反应的金属单质是 。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是 反应。
(3)请你写出符合编号③反应的化学方程式: 。
(4)假设编号④反应的盐是 AgNO ,则编号④对应方框中的现象是 。
27.如图是盐酸与不同类别物质之间反应的知识网络。
(1)实验室常用M与稀盐酸反应制取CO2,其主要成分化学式为 。
(2)写出金属铁与盐酸反应的化学方程式: 。
(3)用盐酸除铁锈(主要成分 Fe2O )的化学方程式是 。
(4)讨论:醋酸和盐酸具有相似的化学性质,下列说法正确的是 (填字母)。
A.能使无色酚酞试液变红色
B.能与氢氧化钠溶液发生反应
C.能与活泼金属发生反应
(5)反思:盐酸、硫酸、食醋具有相似化学性质的原因是它们水溶液中都含有 离子。
(6)氢氧化铝用以治疗胃酸过多,写出此反应的化学方程式: ,除了氢氧化铝外,下列物质也可用于治疗胃酸的是 (填字母)。
A.氢氧化钙 B.氢氧化钠 C.氢氧化镁
28.(1)MgCl2 溶液中含有少量 HCl,为除去少量 HCl可加入过量的 (多选,填字母)。
A. Mg B. MgO
(2)要将含有盐酸的氯化钙中和到中性,并得到较为纯净的氯化钙溶液,若用酚酞作指示剂,加入的试剂可以是 ;在不用指示剂的情况下,加入的试剂可以是 [均填“NaOH” ”或“NaCl”]。
(3)烧水的铝壶中常结有一层水垢(该水垢的主要成分是( 用适量稀盐酸可以除去它,反应的化学方程式是 ,若盐酸的用量过多,会产生的不良后果用化学方程式可表示为 。
三、实验探究题(每空2分,22分)
29.为了验证“酸的化学性质”,在实验室进行如图所示实验,请回答:
(1)图1中,1孔的现象是 ,4孔的现象是 。
(2)写出图2中发生中和反应的化学方程式: 。
(3)写出C试管中的现象: 。
(4)要全面验证酸的化学性质,D试管中能与酸反应的固体单质是 (写1种)。
(5)实验完成后,将A、B、C、D与第(2)问中选择物质相对应四支试管中的废液倒入废液缸内,测得 写出废液中所含全部溶质的化学式: (溶质不计指示剂与气体)。
30.如图所示,是为了验证稀硫酸化学性质所做的三个实验,回答下列问题:
(1)A实验最终能观察到的现象是 。
(2)B实验能体现出稀硫酸具有的化学性质是 。
(3)C实验中发生反应的化学方程式为 。
(4)(2分)若要证明C实验所加的 过量,小明的实验的操作及现象:取C中的上层清液少量于试管中,滴加 溶液,如果产生白色沉淀,则证明C实验所加溶液过量。你认为该同学的做法对吗 。如果不对,你的操作及现象是 °
四、分析计算题(7分)
31.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应),求:
序号 加入稀盐酸的质量/g 剩余固体质量/g
第一次 10 5.5
第二次 10 3.0
第三次 10 1.2
第四次 10 n
(1)样品中碳酸钙的质量分数是多少
(2)上表中n的数值为 。
(3)求反应生成的氯化钙的质量。
第2章 酸与碱
1. A 2. A 3. D 4. C 5. C 6. B 7. B 8. A 9. A 10. B11. C 12. B 13. C 14. B 15. C 16. C 17. D 18. C 19. C20. D 21. C 22. B 23. C
24.(1)13 (2)牛奶滴加黑枸杞提取液后为紫色,而紫色对应的pH分别为6和7 (3)有气泡生成、溶液颜色由蓝色变为粉红色
25.(1)硝酸钡溶液 (2)置换反应 (3)溶液由红色变为无色 HCl+NaOH——NaCl+H2O
(4)2Ga+6HCl——2GaCl +3H2↑
26.(1)紫色石蕊试液 铁 (2)置换 +3H2O (4)产生白色沉淀
27.(1)CaCO (2) Fe+2HCl══FeCl2+H2↑
、
(5)氢
28.(1)ABC (2) Ca(OH)2 CaCO
(3)CaCO +2HCl═CaCl2+H2O+CO2↑ 2Al+6HCl——2AlCl +3H2↑
29.(1)紫色石蕊试液变红色 无色酚酞试液不变色
(2)2NaOH+
(3)黑色粉末逐渐溶解,溶液变为蓝色
(4) Zn(或 Fe等,合理即可)
(5)H2SO 、Na2SO 、CuSO 、ZnSO
30.(1)溶液变蓝 (2)能与金属氧化物和活泼金属反应
(4)不对 取C中的上层清液少量于试管中,向其中加入硫酸钠(硫酸与可溶性硫酸盐即可)溶液,有白色沉淀生成
31.(1)8g石灰石样品中含有1.2g杂质,样品中碳酸钙的质量分数为
(2)1、2 [解析:第3次加入10g稀盐酸,充分反应后,碳酸钙完全反应,第4次加入 10g稀盐酸,剩余固体为杂质、质量不变,故n=1.2。]
(3)设完全反应后最终生成氯化钙的质量为心则
100 111
8g--1.2g x
x=7.548g
