1.4常见的碱
图片预览











文档简介
课件33张PPT。常见的碱 你已经知道哪些碱?了解它们的性质吗?它们在生产、生活中有哪些应用?讨论:1、石灰浆的主要成分是什么?手接触石灰浆时间久了手会怎么样?知道是什么原因吗?
2、你知道什么是烧碱吗?为什么这种物质叫做烧碱?而且有人把这种物质叫做火碱。
3、你见过氨水吗?它有些什么性质?二、常见的碱 氢氧化钠俗称烧碱、火碱或苛性钠,是一种重要的碱。石灰水和氨水都呈碱性,这是因为石灰水中含有碱——氢氧化钙,氧氧化钙俗称消石灰或熟石灰。氨水(NH3的水溶液)也是碱。碱有哪些重要的性质呢?氢氧化钠的用途氢氧化钠的化学性质氢氧化钠的物理性质 1、氢氧化钠氢氧化钠物理性质物理性质 纯净的氢氧化钠是白色固体,极易溶于水,溶解时放出大量的热,易潮解,水溶液有涩味和滑腻感。氢氧化钠有强烈的腐蚀性俗名:苛性钠、火碱、烧碱在使用氢氧化钠时必须十分小心,防止皮肤、衣服被它腐蚀氢氧化钠有强烈的腐蚀性
俗名:苛性钠、火碱、烧碱
课堂练习一:氢氧化钠是 _ 色_ 体。_ 溶于水,溶解时放出____。
固体氢氧化钠在空气中易__水分,而__,所以它可以做为某些气体的___ 。 ?
氢氧化钠有强烈的__性,所以它又叫__、__、__ 。 白 大量热吸收干燥剂 腐蚀烧碱潮解火碱苛性钠固 易化学性质石蕊试液变蓝、酚酞试液变红1:与酸碱指示剂反应实验化学性质CO2+2NaOH=Na2CO3+H2O
SO2+2NaOH=Na2SO3+H2O
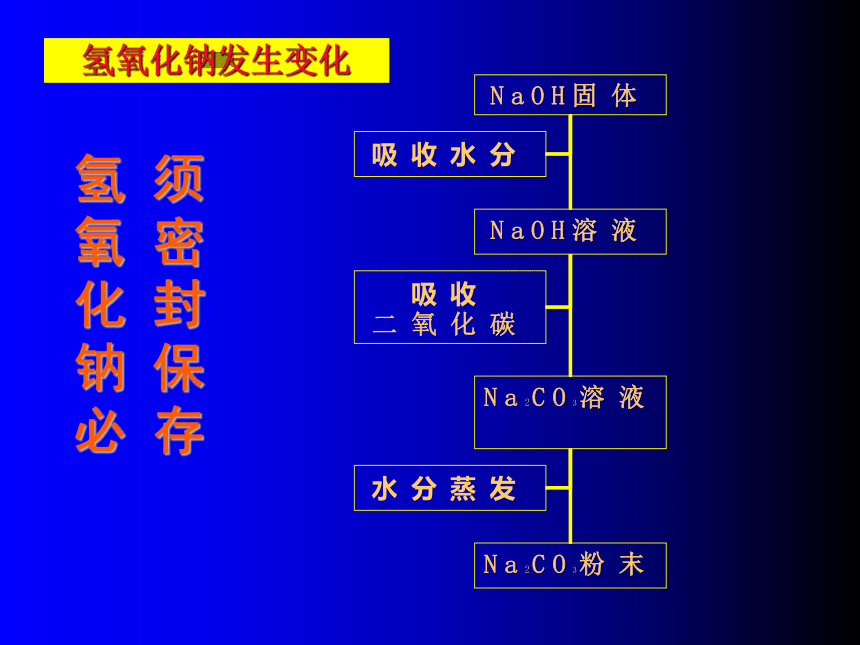
SO3+2NaOH=Na2SO4+H2O 2.与非金属氧化物反应1 .与酸碱指示剂反应氢氧化钠必须密封保存氢氧化钠发生变化化学性质NaOH+HCl=NaCl+H2O
2NaOH+H2SO4=Na2SO4+2H2O3:与酸反应(中和反应)2:与非金属氧化物反应1:与酸碱指示剂反应氢氧化钠是一种碱性干燥剂干燥范围:碱性气体 (NH3)
中性气体 (H2、O2、N2等)注意;不能干燥酸性气体
(HCl、CO2、SO2、H2S等)
化学性质3:与酸反应(中和反应)4:与盐的反应 2:与非金属氧化物反应1:与酸碱指示剂反应与盐的反应制取不溶性碱的方法课堂练习二CA1:下列气体中,可以用氢氧化钠干燥的是( ) (A)H2 (B)SO2 (C)CO2 (D)HCl
2:用天平称量固体氢氧化钠时,应把氢氧化钠直接放在
(A)天平的托盘上 (B)滤纸上
(C)小烧杯内 (D)试管中
3:下列物质暴露在空气中,质量增加且变质的是
(A)浓硫酸 (B)火碱 (C)水 (D)浓盐酸
4:按下列要求各写一个化学方程式
(1) NaOH → Cu(OH)2
(2) NaOH → Na2CO3
NaOH → NaCl
课堂练习二B课堂练习二5:盛有盐酸、水、氢氧化钠的三瓶无色液体,请选用一种试剂将它们区别开 。化学性质1、与酸碱指示剂反应氢氧化钠的用途氢氧化钠自制叶脉书签氢氧化钙氢氧化钙的物理性质 纯净的氢氧化钙是白色固体, 微溶于水氢氧化钙的溶解性生石灰与水反应制取: 氧化钙与水作用CaO + H2O === Ca(OH)22、与非金属氧化物反应 氢氧化钙的化学性质1、 与酸碱指示剂反应 氢氧化钙的用途4、与盐的反应 3、与酸反应碱相似的化学性质:1、能与酸碱指示剂作用2、能与某些非金属氧化物反应 3、能与酸作用4、能与某些盐作用碱溶液的导电性碱性溶液:都含有相同的氢氧根离子例如:KOH 、Ba (OH )2
NH3?H2O 等。溶液的导电性实验酸具有相似化学性质的原因:酸在水溶液中能解离出H+和酸根离子。
酸 H+ + 酸根离子碱具有相似化学性质的原因:碱在水溶液中能解离出OH—和金属离子。
碱 OH— + 金属离子练习:1用化学方程式解释下列现象:(1)氢氧化钠溶液长期放置在空气中后滴入氢氧化钙溶液会产生白色沉淀.(2)在生石灰中加入水会放出大量的热,在所得溶液中滴入酚酞,溶液变红色.(3)在KOH溶液中滴入几滴酚酞,溶液会变红色,滴入几滴稀硫酸.红色渐渐消失.2、如何区别氢氧化钠溶液、氢氧化钙溶液和稀盐酸。3、如何检验氢氧化钠变质,写出实验步骤、现象,化学方程式。4、有一部分变质的NaOH固体8.26g溶于水后加入足量的澄清的石灰水,生成白色沉淀,将沉淀洗涤,灼烧,称量为0.56g
(1)求NaOH变质后的生成物的质量;(2)求变质的NaOH的质量
(3)求变质的NaOH 占原固体物质总质量的质量分数。答案:(1)1.06g (2)0.8g(3)10%你能得出答案吗?1.碱溶液有相似的化学性质的原因是碱溶液中都含有( )
A.氢离子
B.氢氧根离子
C.金属离子
D.酸根离子B酸具有相似性的本质原因是
A.使指示剂变色
B.分子中具有酸根
C.酸分子在溶液中的水分子作用下解离出共同的氢离子
D.具有腐蚀性
2、你知道什么是烧碱吗?为什么这种物质叫做烧碱?而且有人把这种物质叫做火碱。
3、你见过氨水吗?它有些什么性质?二、常见的碱 氢氧化钠俗称烧碱、火碱或苛性钠,是一种重要的碱。石灰水和氨水都呈碱性,这是因为石灰水中含有碱——氢氧化钙,氧氧化钙俗称消石灰或熟石灰。氨水(NH3的水溶液)也是碱。碱有哪些重要的性质呢?氢氧化钠的用途氢氧化钠的化学性质氢氧化钠的物理性质 1、氢氧化钠氢氧化钠物理性质物理性质 纯净的氢氧化钠是白色固体,极易溶于水,溶解时放出大量的热,易潮解,水溶液有涩味和滑腻感。氢氧化钠有强烈的腐蚀性俗名:苛性钠、火碱、烧碱在使用氢氧化钠时必须十分小心,防止皮肤、衣服被它腐蚀氢氧化钠有强烈的腐蚀性
俗名:苛性钠、火碱、烧碱
课堂练习一:氢氧化钠是 _ 色_ 体。_ 溶于水,溶解时放出____。
固体氢氧化钠在空气中易__水分,而__,所以它可以做为某些气体的___ 。 ?
氢氧化钠有强烈的__性,所以它又叫__、__、__ 。 白 大量热吸收干燥剂 腐蚀烧碱潮解火碱苛性钠固 易化学性质石蕊试液变蓝、酚酞试液变红1:与酸碱指示剂反应实验化学性质CO2+2NaOH=Na2CO3+H2O
SO2+2NaOH=Na2SO3+H2O
SO3+2NaOH=Na2SO4+H2O 2.与非金属氧化物反应1 .与酸碱指示剂反应氢氧化钠必须密封保存氢氧化钠发生变化化学性质NaOH+HCl=NaCl+H2O
2NaOH+H2SO4=Na2SO4+2H2O3:与酸反应(中和反应)2:与非金属氧化物反应1:与酸碱指示剂反应氢氧化钠是一种碱性干燥剂干燥范围:碱性气体 (NH3)
中性气体 (H2、O2、N2等)注意;不能干燥酸性气体
(HCl、CO2、SO2、H2S等)
化学性质3:与酸反应(中和反应)4:与盐的反应 2:与非金属氧化物反应1:与酸碱指示剂反应与盐的反应制取不溶性碱的方法课堂练习二CA1:下列气体中,可以用氢氧化钠干燥的是( ) (A)H2 (B)SO2 (C)CO2 (D)HCl
2:用天平称量固体氢氧化钠时,应把氢氧化钠直接放在
(A)天平的托盘上 (B)滤纸上
(C)小烧杯内 (D)试管中
3:下列物质暴露在空气中,质量增加且变质的是
(A)浓硫酸 (B)火碱 (C)水 (D)浓盐酸
4:按下列要求各写一个化学方程式
(1) NaOH → Cu(OH)2
(2) NaOH → Na2CO3
NaOH → NaCl
课堂练习二B课堂练习二5:盛有盐酸、水、氢氧化钠的三瓶无色液体,请选用一种试剂将它们区别开 。化学性质1、与酸碱指示剂反应氢氧化钠的用途氢氧化钠自制叶脉书签氢氧化钙氢氧化钙的物理性质 纯净的氢氧化钙是白色固体, 微溶于水氢氧化钙的溶解性生石灰与水反应制取: 氧化钙与水作用CaO + H2O === Ca(OH)22、与非金属氧化物反应 氢氧化钙的化学性质1、 与酸碱指示剂反应 氢氧化钙的用途4、与盐的反应 3、与酸反应碱相似的化学性质:1、能与酸碱指示剂作用2、能与某些非金属氧化物反应 3、能与酸作用4、能与某些盐作用碱溶液的导电性碱性溶液:都含有相同的氢氧根离子例如:KOH 、Ba (OH )2
NH3?H2O 等。溶液的导电性实验酸具有相似化学性质的原因:酸在水溶液中能解离出H+和酸根离子。
酸 H+ + 酸根离子碱具有相似化学性质的原因:碱在水溶液中能解离出OH—和金属离子。
碱 OH— + 金属离子练习:1用化学方程式解释下列现象:(1)氢氧化钠溶液长期放置在空气中后滴入氢氧化钙溶液会产生白色沉淀.(2)在生石灰中加入水会放出大量的热,在所得溶液中滴入酚酞,溶液变红色.(3)在KOH溶液中滴入几滴酚酞,溶液会变红色,滴入几滴稀硫酸.红色渐渐消失.2、如何区别氢氧化钠溶液、氢氧化钙溶液和稀盐酸。3、如何检验氢氧化钠变质,写出实验步骤、现象,化学方程式。4、有一部分变质的NaOH固体8.26g溶于水后加入足量的澄清的石灰水,生成白色沉淀,将沉淀洗涤,灼烧,称量为0.56g
(1)求NaOH变质后的生成物的质量;(2)求变质的NaOH的质量
(3)求变质的NaOH 占原固体物质总质量的质量分数。答案:(1)1.06g (2)0.8g(3)10%你能得出答案吗?1.碱溶液有相似的化学性质的原因是碱溶液中都含有( )
A.氢离子
B.氢氧根离子
C.金属离子
D.酸根离子B酸具有相似性的本质原因是
A.使指示剂变色
B.分子中具有酸根
C.酸分子在溶液中的水分子作用下解离出共同的氢离子
D.具有腐蚀性
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
