第3节 沉淀溶解平衡--2025年高考化学选择性必修第一册(鲁科版)(共76张PPT)
文档属性
| 名称 | 第3节 沉淀溶解平衡--2025年高考化学选择性必修第一册(鲁科版)(共76张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-06 00:00:00 | ||
图片预览








文档简介
(共76张PPT)
第3章 物质在水溶液中的行为
2025年高考化学一轮复习
选择性必修第一册鲁科版
第3节 沉淀溶解平衡
课时1 沉淀溶解平衡与溶度积
题型觉醒
题型一 沉淀溶解平衡及其影响因素
1.已知时,的溶度积 ,则下列说法正确的是
( )
D
A.向饱和水溶液中加入盐酸, 变大
B.溶液与溶液混合后的溶液中,一定有
C.温度一定时,当溶液中时,此溶液中必有 沉淀析出
D.时, 在水中的溶解度大于在饱和食盐水中的溶解度
【解析】 A(×) 是一种平衡常数,只受温度影响,与溶液浓度无关。
B(×)溶液与溶液混合后的溶液中,和 大小不能确定,这取
决于与 的相对多少。
C(×)温度一定时,当溶液中时,此溶液中 达到沉淀溶解平
衡,但不一定有沉淀析出,如 的饱和溶液。
D(√)
第一步:外 界条件变化 第二步:判断 、 的变化 第三步:平衡移 动方向 第四步:结果分析
不变、 , 逆向(生成 的方向)移动 、 (平衡移动是有限
的,不能抵消条件的改变)
故 在水中的溶解度大于在饱和食盐水中的溶解度。
2.(2024四川阆中东风中学期中)把足量熟石灰放入蒸馏水中,一段时间后达到平衡:
。下列叙述正确的是( )
D
A.给溶液加热,溶液的 升高
B.恒温下向溶液中加入,溶液的 升高
C.向溶液中加入溶液, 固体增多
D.向溶液中加入少量的固体, 固体增多
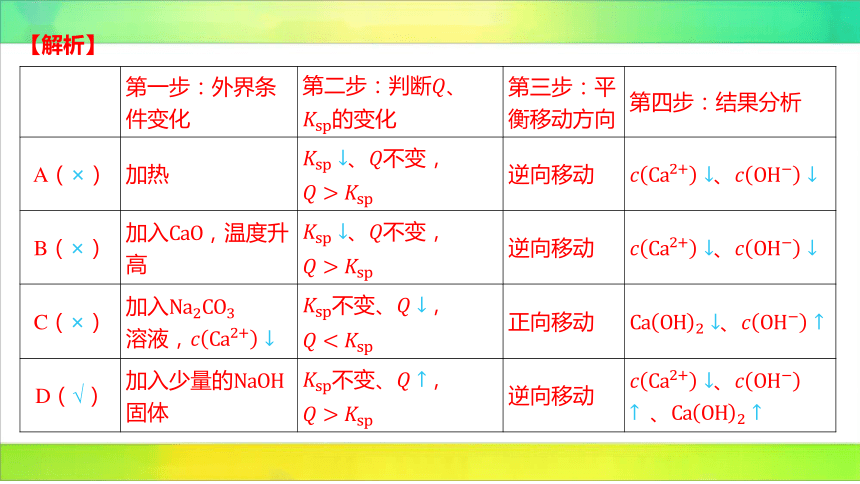
【解析】
第一步:外界条 件变化 第二步:判断 、 的变化 第三步:平 衡移动方向 第四步:结果分析
A(×) 加热 、 不变, 逆向移动 、
B(×) 加入 ,温度升 高 、 不变, 逆向移动 、
C(×) 加入 溶液, 不变、 , 正向移动 、
D(√) 加入少量的 固体 不变、, 逆向移动 、
、
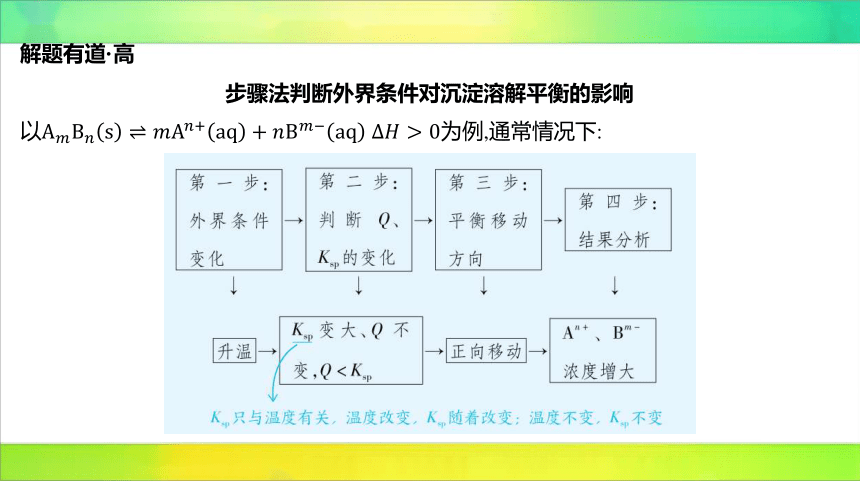
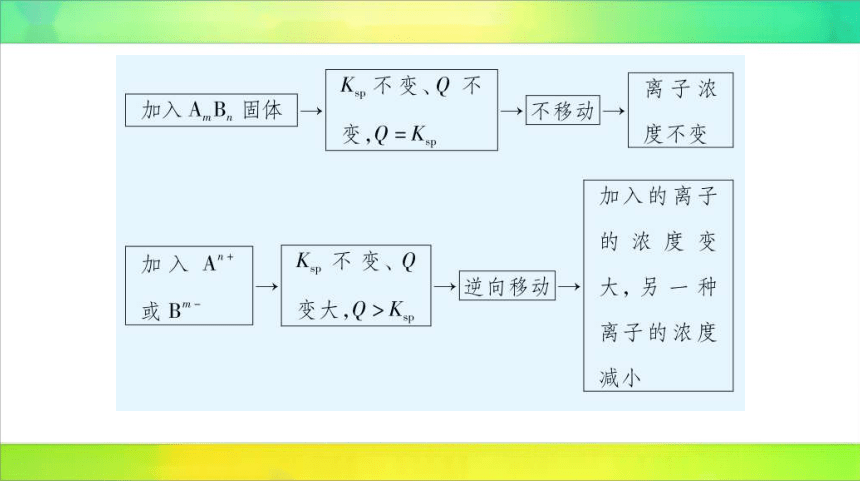
解题有道·高
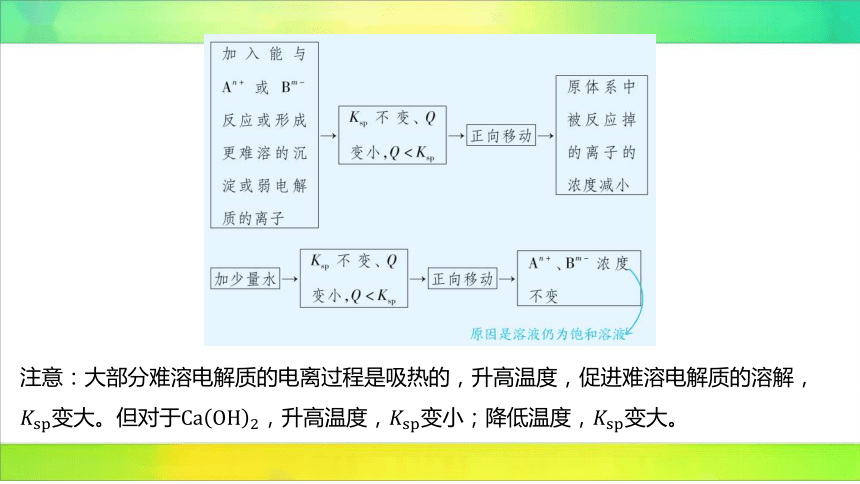
步骤法判断外界条件对沉淀溶解平衡的影响
以 为例,通常情况下:
注意:大部分难溶电解质的电离过程是吸热的,升高温度,促进难溶电解质的溶解,
变大。但对于,升高温度,变小;降低温度, 变大。
题型二 沉淀的溶解、生成与转化
3.已知某温度下, ,
,下列叙述正确的是( )
D
A.饱和溶液与饱和溶液相比,前者的 大
B.向溶液中加入等体积的 溶液,则
有 沉淀生成
C.若向溶液中加入等体积的 溶液,则
完全沉淀[提示:沉淀完全的
D.将溶液逐滴滴入和 的混
合溶液中,则先产生 沉淀
【解析】 A(×)饱和溶液中 ,
,饱和 溶液中
, ,显然后者
的 大。
B(×)混合后, (【提醒】两种溶液等体积
混合,离子浓度减半),
,则没有 沉淀生成。
C(×)完全沉淀,则 ,此时
,故应向 溶液
中加入等体积的 溶液的浓度至少是
。
D(√)饱和溶液中比饱和溶液中小,故在同浓度的 和
混合溶液中滴入溶液,先生成 沉淀。
4.(2024河北正定中学月考)下列说法不正确的是( )
B
A.固体在溶液中存在平衡: ,该固体可溶
于 溶液
B.向沉淀上滴加溶液沉淀变为黑色,可推知同温下
C.向悬浊液中滴加 溶液,白色沉淀变成黑色,反应的离子方程式为
D.向浓度均为的、混合溶液中滴加滴
溶液,振荡沉淀呈黄色,说明
【解析】 A(√)是强酸弱碱盐,水解使溶液显酸性,将加入
溶液中,水解出的与溶解生成的反应,使 溶解平衡
正向移动,从而使 固体逐渐溶解。
B(×)向沉淀上滴加溶液,沉淀变黑色说明溶度积较大的与 溶液反
应生成溶度积较小的,即 。
C(√)向悬浊液中加入溶液,白色沉淀变成黑色说明溶解度大的与
溶液反应生成溶解度小的 ,反应的离子方程式为
。
D(√)向等浓度的和溶液中加入溶液,先生成黄色沉淀,可知 的溶
度积大于 。
有“化”好说
组成类型相似,且含相同离子的难溶电解质沉淀时,不一定是 小的先沉淀。如向含
、、的混合液中加入时,确定哪种卤化银先沉淀要看、、 的浓
度大小。
题型三 溶度积的应用
5.(2023浙江金华模拟)在时,下列几种难溶电解质的溶度积常数 如表所示,
下列说法不正确的是( )
(白) (白) (白) (浅黄) (黑)
A
A.由溶度积常数可判断在相同条件下物质的溶解性大小
B.重晶石的主要成分是 ,工业上常用饱和碳酸钠溶液反复浸泡重晶石,将难处理
的转化为较易处理的
C.向的悬浊液中滴加饱和溶液可以得到浅黄色 悬浊液
D.在含银工业废水的处理中,相同浓度的溶液比溶液沉淀效果好,而且
溶液可以沉淀多种重金属离子
【解析】 A(×)对于结构相似的物质,溶度积常数越小,溶解度越小。
B(√)由表格中数据可知,反应 的平衡常
数, 浓度较大
时,,反应正向进行,可生成沉淀(【提醒】当类型相同的难溶物的 相
差不大时,通过控制条件也能使小的难溶物转化为 大的难溶物),故工业上常用
饱和碳酸钠溶液反复浸泡重晶石,将难处理的转化为较易处理的 。
C(√)一般来说,溶解能力相对较强的沉淀容易转化为溶解能力相对较弱的沉淀,由
表格中数据可知的溶度积比小,即溶解度:,故向 的悬浊液
中滴加的饱和溶液可以得到浅黄色 悬浊液。
D(√)由表格中数据可知的溶度积远小于 ,则在含银工业废水的处理中,相
同浓度的溶液比溶液沉淀效果好,而且多种金属的硫化物均为难溶物,
溶液可以沉淀多种重金属离子。
能力觉醒
6.(2023福建宁德名校联考)对 悬浊液进行下列操作,达到平衡后(选项C、D均
指恢复至原温度,不考虑体积变化),和 均保持不变的是( )
B
A.适当升温 B.加少量水
C.加入少量浓硫酸 D.加入少量氯化钡固体
【解析】 溶解平衡是吸热反应。
第一步:外界条 件变化 第二步:判断 、 的变化 第三步:平衡移 动方向 第四步:结果分析
A (×) 升高温度 、 不变, 正向移动 、
B (√) 加少量水, 、 不变、 , 正向移动 不变、
不变(得到的仍为
饱和溶液)
第一步:外界条 件变化 第二步:判断 、 的变化 第三步:平衡移 动方向 第四步:结果分析
C (×) 加入少量浓硫 酸, 不变、 , 逆向移动
D (×) 加入少量氯化钡 固体, 不变、 , 逆向移动 续表
7.(2023上海虹口区模拟)某兴趣小组对氢氧化镁的溶解进行如图探究实验。下列说法
错误的是( )
A
A.:① ③
B.③中存在:
C.③中液体又变红的原因:沉淀溶解平衡正向移动
D.①、③中存在沉淀溶解平衡:
【解析】 A(×)方法一 ①中含有氢氧化镁,③中除了氢氧化镁还有氯化镁,同温度
下相同,③中大,则:③ ①。
方法二 ③中除了氢氧化镁还有氯化镁,相当于增大 。
第一步:外 界条件变化 第二步:判断、 的变化 第三步:平 衡移动方向 第四步:结果分析
不变、 , 逆向移动 、(平衡移动是有限的,
不能抵消条件的改变)
故:③ ①。
B(√)③中除了有还有,完全电离, 存在溶解平衡,也
能产生,则 。
C(√)
第一步:外界条件变化 第二步:判断 、 的变化 第三步:平 衡移动方向 第四步:结果
分析
加入几滴浓盐酸,与 电离出的 反应, ,溶液褪色 不变、 , 正向移动 电离出 ,
液体又变红
D(√)根据上述分析知,①、③中存在沉淀溶解平衡
。
8.(2024浙江金华十校期末)时,金属离子初始浓度为 时,发生相应
变化的 如下表所示:
开始沉淀 完全沉淀(离子浓度等于 ) 开始溶解 完全溶解
7.0 9.0 13.5
1.9 3.2 14
6.3 8.0 10.5 12.6
下列做法正确的是( )
B
A.悬浊液中,
B.加入可能实现向 的转化
C.若初始浓度为,则开始溶解的
D.分离、:加碱至 ,搅拌后过滤,固体、滤液分别加酸至强酸性
【解析】 A(×)悬浊液中存在 ,该沉淀
溶解平衡微弱,故比较离子浓度要考虑水的电离,则 。
B(√)根据表中数据,当金属离子浓度相等时,开始沉淀的, 开始
沉淀的,说明比更难溶, 悬浊液中存在
,加入,与 结合生成更难溶的
,促进平衡向右进行,可能实现向 转化。
C(×)开始生成时,发生反应 ,则
越大、越小,即开始沉淀的减小; 开始溶解时,发生反应
, 对该反应无影响,即不会影响
开始溶解的 。
D(×)根据表中数据,加碱至,以的形式存在, 完全溶
解,为絮状沉淀,不易用过滤方法从溶液中分离出来,同时根据表中 、
开始沉淀时的 ,不需要加酸至强酸性。
9.(2024福建厦门一中期中)常温下,将 粉
末置于盛有 蒸馏水的烧杯中,然后向烧杯中加入
固体(忽略溶液体积的变化)并充分搅拌,该过程
中几种离子的浓度变化曲线如图所示,下列说法不正确的
是( )
C
A.反应 的
B.相同温度下,在水中和在溶液中的 不变
C.曲线代表 浓度变化
D.锅炉水垢中的可先用溶液处理,使转化为 后,再用酸除去
【解析】 开始时溶液中存在沉淀溶解平衡:
,
;
当加入的 固体使溶液中
时( 点)开始发生沉淀
的转化,此时溶液中存在、 的溶解平衡,故
;继续加入固体,
与结合生成沉淀,减小, 平衡右
移,增大,故曲线代表浓度变化,曲线代表 浓度变化。
A(√)反应
的 。
B(√) 只与温度有关,而与溶剂无关,故相同温度
下,在水中和在溶液中的 不变。
C(×)曲线代表 浓度变化。
D(√)锅炉水垢中的 微溶于水,不溶于酸,可根据
沉淀溶解平衡,先用溶液处理,使 转化为
,弃去沉淀转化后的溶液,再向沉淀中加入盐酸,
发生反应: ,达到
除去锅炉水垢的目的。
素养觉醒
10.(传统文化)沈括《梦溪笔谈》记载“石穴中水,所滴皆为钟乳”,下列条件不利于
碳酸钙析出的是( )
A
A.减小 B.水分蒸发 C. 压强减小 D.温度升高
【解析】 钟乳石的主要成分为碳酸钙,它的形成涉及石灰岩中不溶性碳酸
钙转化为可溶性的碳酸氢钙: 和碳酸钙沉淀的析出:
。
A(√) 减小,碳酸钙沉淀的析出反应平衡逆向移动,不利于碳酸钙的析出,符
合题意。
B(×)水分蒸发,碳酸钙沉淀的析出反应平衡正向移动,有利于碳酸钙的析出,不符
合题意。
C(×)压强减小,则其溶解度降低,溶液中 的浓度减小,碳酸钙沉淀的析出反
应平衡正向移动,有利于碳酸钙的析出,不符合题意。
D(×)碳酸钙沉淀的析出为分解反应,此过程吸热,温度升高,平衡正向移动,有利
于碳酸钙的析出,不符合题意。
11.(生活情境)(2024四川成都七中期中)牙釉质的主要成分为羟基磷酸钙
,在牙齿表面存在平衡:
,
已知的 。下列说法错误的是( )
C
A.残留在牙齿上的糖会发酵产生 ,使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质
B.按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀牙齿
C.用含 的溶液漱口,可使平衡左移,保护牙齿
D.含氟牙膏使转化为更难溶的 ,促进牙齿表面矿物质的沉积,
修复牙釉质
【解析】 A(√)
第一步:外界条件变化 第二步:判断 、 的变化 第三步:平 衡移动方向 第四步:结果分析
残留在牙齿上的糖会发酵产 生 ,中和溶解平衡生成的 , 不变、 , 正向移动 促进
溶解,破坏牙釉质
B(√)由A项分析可知,按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀
牙齿。
C(×)碱性太强,具有强腐蚀性,不能用含 的溶液漱口,否则将腐蚀口腔
等组织。
D(√),含氟牙膏使 转化为更难溶
的 ,促进牙齿表面矿物质的沉积,修复牙釉质。
第3章 物质在水溶液中的行为
2025年高考化学一轮复习
选择性必修第一册鲁科版
第3节 沉淀溶解平衡
课时2 相关计算及图像分析
题型觉醒
题型一 的相关计算
1.(2023重庆万州二中月考)已知室温时 ,
。下列关于和 两种悬浊液的说法错误的
是( )
B
A.和两种悬浊液中前者的 较小
B.分别滴加稀硫酸,与 的溶度积常数均增大
C.分别加入的溶液,和 均减小
D.和共存的饱和溶液中, 的值约为97.4
【解析】 A(√) 悬浊液中
, 悬浊液中,
,故
,因此和 两种悬浊液
中前者的 较小。
B(×)溶度积常数只与温度有关,温度不变,溶度积常数不变。
C(√)加入溶液,浓度增大,、 沉淀溶解平衡均逆向移动,
和 均减小。
D(√) 。
题型二 沉淀溶解平衡曲线
2.(2023辽宁重点高中期末)在时,
(砖红色)在水溶液中的沉淀溶解平衡曲线如图
所示。又知 的
。下列说法正
确的是( )
B
A.时,的为
B.时,点和点时的 相等
C.时,向饱和溶液中加入 能使
溶液由点变为 点
D.时,向悬浊液中加入 固体,可
生成白色沉淀
【解析】
A(×)根据题图知,达到沉淀溶解平衡时, 、
,故
。
B(√)溶度积只受温度影响,温度不变,溶度积不变。
C(×)饱和溶液中加入,增大、减小,能使溶液由 点
变为 点。
D(×)固体的量没有给出,不能确定此时 ,不能确定
此时是否有白色沉淀生成。
3.(2024天津耀华中学期末)室温时, 、
和 在水中达到沉淀溶解平衡时的
关系如图所示, 表示
、、; 可
认为 沉淀完全]。下列叙述正确的是( )
C
A.由点可求得
B.时的溶解度为
C.浓度均为的和 可通过分步沉淀进行分离
D.、混合溶液中 时二者不会同时沉淀
【解析】
A(×)根据题图知,点时 处于沉淀溶解平衡状态,
、
,故
。
B(×)根据题图知,时,即,故
的溶解度为 。
C(√)由题图可知,当(即)时, ,
而当(即)时,, 才开始沉淀,故当
完全沉淀时,尚未开始沉淀,可通过调节溶液的方法分步沉淀和 。
D(×)由题图可知,沉淀完全时,, 刚要开始沉淀,此时
,而,则、 会
同时沉淀。
4.(2024广东深圳中学期中)工业废水中含重
金属离子,可通过化学沉淀法将其除去,
时,与 在水中的沉淀溶解平衡曲线如
图所示(表示和 )。下列说法不
正确的是( )
D
A.点对应的 溶液为过饱和溶液
B.时,
C.向含沉淀的悬浊液中加入 固体可实
现点到 点的变化
D.向、浓度均为 的工业废水中通入气体,首先沉淀的是
【解析】
A(√)点在的沉淀区,对应 的过饱和溶液。
B(√)时,取点数据计算, 、
,
。
C(√)
第一步:外界条件变 化 第二步:判断、 的变 化 第三步:平衡 移动方向 第四步:结果分析
加入固体, 不变、, 逆向移动 、
温度不变时, 不变,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变
化,不会出现在曲线以外,减小、 增大,即横轴增大、纵轴减小。
D(×)取 点数据计算,
,、 的
浓度均为时,开始生成 沉淀时,
,开始生成 沉淀时,
,生成沉淀时所需
小,故向、浓度均为工业废水中通入,先生成 沉淀。
题型三 沉淀滴定曲线
5.已知时,、、的 分别为
、、
,用标准溶液滴定
卤素离子,以滴入 标准溶液的体积为横轴,
为纵轴,
就可绘得滴定曲线。现以 溶
液分别滴定、、 ,
绘得滴定曲线如图,下列有关说法正确的是 ( )
A.、、分别表示、、
B.、、分别表示、、
C.、、分别表示、、
D.用滴定法测定试样中,可用 作
指示剂
√
【解析】 A(×)B(×)C(√)
D(×)若溶液中同时存在和,当 时,
加入,先沉淀的是 ,测得的结果不准确。
能力觉醒
6.(2023河南焦作第一高级中学期末)已知 ,
, 。某溶液中含有
、和,浓度均为,向该溶液中逐滴加入 的
溶液时,三种阳离子产生沉淀的先后顺序为( )
A
A.、、 B.、、
C.、、 D.、、
【解析】 根据溶度积的定义可知,三种离子沉淀时分别有
,
,,溶液中、、 的浓度均为
,则向该溶液中逐滴加入溶液产生沉淀时,所需 分别为
、 、
,所以这三种离子产生沉淀的先后顺序为 、
、 。
7.(2023广东广州广雅中学期中)时, 在不
同浓度盐酸中的最大溶解量(单位: )如图所示。
下列叙述正确的是( )
B
A.盐酸浓度越大, 越大
B. 能与一定浓度的盐酸反应
C.、两点对应的溶液中 相等
D.向含的溶液中加入过量浓盐酸,可将 完全转化为
【解析】 A(×) 只受温度影响,温度不变,
不变。
B(√)时,增大盐酸浓度, 的
溶解平衡逆向移动, 的溶解量减少,而当
时, 的溶解度随盐酸浓度的
增大而显著增大,则 能与一定浓度的盐酸反应。
C(×)、两点的溶解量相等,但点时与发生了反应,故、 两点对
应的溶液中 不相等。
D(×)存在溶解平衡,且能与盐酸反应,故向含 的溶液中加入过量
浓盐酸,不能将完全转化为 。
8.(大招39)(2023广东惠州四校联考) 可用于人
工降雨。 溶于水,溶液中离子浓度与温度的关系如
图所示,已知:, 。
下列说法正确的是( )
B
A.
B.的溶度积
C.时,粉末溶于饱和 溶液中
D.在点饱和溶液中加粉末,点移动到 点
【解析】
A(×)碘化银的沉淀溶解平衡是吸热反应,
则升高温度,增大,而题图中 点对
应的、较点的小,即 点对应的
较点的小,故 。
B(√)根据A项分析知, ,又
只受温度影响,在相同温度下,曲线
上的各点溶度积相同,故
。
C(×) 在溶液中存在沉淀溶解平衡:
, 溶液中存在大
量,抑制溶解, 减小,由题图
知,点为时 的饱和溶液,此时
,故
粉末溶于饱和 溶液中
。
D(×)温度不变时, 不变,无论改变哪种
离子的浓度,另一种离子的浓度只能在曲线上
变化,不会出现在曲线以外。在点饱和 溶
液中加粉末, 的沉淀溶解平衡逆向
移动,增大、减小,减小、
增大,点沿曲线向 点方向移动。
9.(2024云南师范大学附中期中)已知:常温下,
,
;
。常温下,向
溶液中逐滴滴加
溶液,溶液与加入 溶液
C
A.,
B.若,则反应终点可能为 点
C.、、三点中,由水电离出的与之和最大的为 点
D.相同条件下,若用等浓度、等体积的溶液代替上述 溶液,则反应终点
由点向 点方向移动
的体积 的关系如图所示。下列说法错误的是( )
【解析】
. .
.
A(√) 点为反应终点,则
,此时存在 的沉
淀溶解平
衡,该点, ,即
。
B(√) 减小,达到反应终点需要的
溶液的体积减小,而反应终点时 不变
(【提醒】反应终点时的取决于 ,
与起始时的无关),即 不变,反应终点
可能为 点。
C(×)点溶液中溶质为和 ,
水解促进水的电离; 点溶液中溶质为
;点溶液中溶质为和, 水
解促进水的电离,故点由水电离出的 与
之和最小。
D(√) ,达到反应终点时,
,相同条件下,若用等浓度、等
体积的溶液代替 溶液,反应终
点时,消耗 溶液的体积相等,但,,故反应终点由点向 点方向移动。
10.(大招39)(2023山东枣庄第一中学期末)已知:
,(代表、 、
)。时, ,
, 。在
、、 的饱和溶液中阳离子和阴离子的浓度关系如
图所示。下列说法正确的是( )
D
A.时,在的饱和溶液中加入少量,和 都减小
B.图中曲线代表,且点
C.时,增大点阴离子的浓度,则点沿方向向 点移动
D.时,的平衡常数
【解析】
A(×)
第一步:外界条 件变化 第二步:判断、 的变化 第三步:平 衡移动方向 第四步:结果分析
加入少量 , 不变、 , 逆向移动 ( 平衡移动是有限
的,不能抵消条件的改变)、
B(×)曲线代表,点 。
C(×)根据A项分析知,增大点的阴离子浓度,即 增大,沉淀溶解平衡逆向移
动,减小、增大,则增大、减小,故点沿方向向 点的斜下方
移动。
D(√) 。
11.(大招39)(2024广东五校联考)常温
下,用 溶液滴定
溶液,
作指示剂,测得溶液中
、 随
加入 溶液体积的变化关系如图所示。
C
A.为防止指示剂失效,溶液应维持
B.该温度下,的溶度积常数
C.时,(已知 )
D.相同实验条件下,若改为溶液,则滴定终点 向左平移
已知:;常温下,在时易形成沉淀 。下列
说法错误的是( )
【解析】
A(√)在时易形成沉淀 而失去作为指示剂的作用,故为防止指示剂
失效,溶液应维持 。
B(√)点时溶液中 ,则该温度下
。
C(×)(溶液)时,溶液过量 ,
, ,
。
D(√)若改为溶液,则达到滴定终点时消耗 溶液的体积减
小,滴定终点 向左平移。
12.(大招39)(2024重庆西南大学附中月考)某元素 的
氢氧化物 在水中的溶解反应为
、
。, 与
的关系如图所示,为或 的浓度。下列说
法正确的是( )
B
A.曲线①代表与 的关系
B.的为
C.当溶液达到15.0时, 才开始溶解
D.向的溶液中加入 溶液至,
体系中元素主要以 的形式存在
【解析】
A(×)曲线②代表与 的关系。
B(√)曲线①代表与 的关系,
时, ,即
, ,
则 。
C(×)由题图可知,小于8.0时, 溶解得
到,约大于12.5时, 溶解得到 。
D(×)由题图可知,时, 、
都很小,体系中元素主要以 的
形式存在。
13.(2023江苏南京中华中学月考)铁的化合物有广泛用途,如三草酸合铁(Ⅲ)酸钾
晶体是一种光敏材料,也可作催化剂,碳酸亚铁 可作补
血剂等,以废铁屑(含及少量和 )为原料制备以上物质的流程如下:
已知:①, ,
, ;
②某离子浓度小于等于 时认为该离子沉淀完全;
③ 为可溶于水、难溶于乙醇的翠绿色晶体。
回答下列问题:
(1) 滤液Ⅰ中含有、,检验 所用的试剂为____________(填化学式)。
【解析】 废铁屑含、、 ,滤液Ⅰ是废铁屑与盐酸反应后的混合液,故
滤液Ⅰ中含、。检验可选用试剂,与 反应生成蓝色沉淀。
(2) 室温下,若滤液Ⅰ中为 ,要保证滤液Ⅰ中不出现沉淀,则滤
液Ⅰ中应大于____ 。
0.1
【解析】 滤液Ⅰ中主要含,若较大,则会生成 沉淀,要保证滤液Ⅰ中无沉
淀,则 ,即
,则 。
(3) 将滤液Ⅱ与饱和 溶液混合,发生反应的离子方程式为
____________________________________________________________________________
___________________________________________________________________________;
已知饱和溶液的大于11,是否能用饱和溶液代替饱和 溶液来
制备 ?____(填“是”或“否”)。
(或、)
否
【解析】 向滤液Ⅰ中加入足量,与反应生成,滤液Ⅱ为 溶液,其与饱
和溶液混合后,与反应得到 ,离子方程式为
(或 、
)。溶液中,饱和 溶
液的, ,则
,故若用饱和 溶液代替饱
和溶液来制备,会生成少量,导致得到的 不纯。
(4) 滤液Ⅰ与足量空气发生反应的离子方程式为_________________________________;
甲同学认为该步反应用稀 代替空气效果更好,乙同学不同意甲的观点,其理由是
_____________________________________________________________。
是分解的催化剂,会消耗大量的,导致生产成本过高
【解析】 滤液Ⅰ中通入足量空气的目的是将氧化成 ,离子方程式为
;溶液中的能催化分解,若用稀 代
替空气,会消耗大量的 ,使生产成本过高。
(5) 获得翠绿色晶体的“一系列操作”包含__________________________(填操作名
称);用乙醇洗涤晶体而不用水洗涤的目的为________________________________。
蒸发浓缩、冷却结晶、过滤
减少晶体溶解损失,使晶体易干燥
【解析】 获得翠绿色晶体的“一系列操作”包含蒸发浓缩、冷却结晶、过滤;用乙醇洗
涤晶体而不用水洗涤的目的是减少晶体溶解损失,使晶体易干燥。
第3章 物质在水溶液中的行为
2025年高考化学一轮复习
选择性必修第一册鲁科版
第3节 沉淀溶解平衡
课时1 沉淀溶解平衡与溶度积
题型觉醒
题型一 沉淀溶解平衡及其影响因素
1.已知时,的溶度积 ,则下列说法正确的是
( )
D
A.向饱和水溶液中加入盐酸, 变大
B.溶液与溶液混合后的溶液中,一定有
C.温度一定时,当溶液中时,此溶液中必有 沉淀析出
D.时, 在水中的溶解度大于在饱和食盐水中的溶解度
【解析】 A(×) 是一种平衡常数,只受温度影响,与溶液浓度无关。
B(×)溶液与溶液混合后的溶液中,和 大小不能确定,这取
决于与 的相对多少。
C(×)温度一定时,当溶液中时,此溶液中 达到沉淀溶解平
衡,但不一定有沉淀析出,如 的饱和溶液。
D(√)
第一步:外 界条件变化 第二步:判断 、 的变化 第三步:平衡移 动方向 第四步:结果分析
不变、 , 逆向(生成 的方向)移动 、 (平衡移动是有限
的,不能抵消条件的改变)
故 在水中的溶解度大于在饱和食盐水中的溶解度。
2.(2024四川阆中东风中学期中)把足量熟石灰放入蒸馏水中,一段时间后达到平衡:
。下列叙述正确的是( )
D
A.给溶液加热,溶液的 升高
B.恒温下向溶液中加入,溶液的 升高
C.向溶液中加入溶液, 固体增多
D.向溶液中加入少量的固体, 固体增多
【解析】
第一步:外界条 件变化 第二步:判断 、 的变化 第三步:平 衡移动方向 第四步:结果分析
A(×) 加热 、 不变, 逆向移动 、
B(×) 加入 ,温度升 高 、 不变, 逆向移动 、
C(×) 加入 溶液, 不变、 , 正向移动 、
D(√) 加入少量的 固体 不变、, 逆向移动 、
、
解题有道·高
步骤法判断外界条件对沉淀溶解平衡的影响
以 为例,通常情况下:
注意:大部分难溶电解质的电离过程是吸热的,升高温度,促进难溶电解质的溶解,
变大。但对于,升高温度,变小;降低温度, 变大。
题型二 沉淀的溶解、生成与转化
3.已知某温度下, ,
,下列叙述正确的是( )
D
A.饱和溶液与饱和溶液相比,前者的 大
B.向溶液中加入等体积的 溶液,则
有 沉淀生成
C.若向溶液中加入等体积的 溶液,则
完全沉淀[提示:沉淀完全的
D.将溶液逐滴滴入和 的混
合溶液中,则先产生 沉淀
【解析】 A(×)饱和溶液中 ,
,饱和 溶液中
, ,显然后者
的 大。
B(×)混合后, (【提醒】两种溶液等体积
混合,离子浓度减半),
,则没有 沉淀生成。
C(×)完全沉淀,则 ,此时
,故应向 溶液
中加入等体积的 溶液的浓度至少是
。
D(√)饱和溶液中比饱和溶液中小,故在同浓度的 和
混合溶液中滴入溶液,先生成 沉淀。
4.(2024河北正定中学月考)下列说法不正确的是( )
B
A.固体在溶液中存在平衡: ,该固体可溶
于 溶液
B.向沉淀上滴加溶液沉淀变为黑色,可推知同温下
C.向悬浊液中滴加 溶液,白色沉淀变成黑色,反应的离子方程式为
D.向浓度均为的、混合溶液中滴加滴
溶液,振荡沉淀呈黄色,说明
【解析】 A(√)是强酸弱碱盐,水解使溶液显酸性,将加入
溶液中,水解出的与溶解生成的反应,使 溶解平衡
正向移动,从而使 固体逐渐溶解。
B(×)向沉淀上滴加溶液,沉淀变黑色说明溶度积较大的与 溶液反
应生成溶度积较小的,即 。
C(√)向悬浊液中加入溶液,白色沉淀变成黑色说明溶解度大的与
溶液反应生成溶解度小的 ,反应的离子方程式为
。
D(√)向等浓度的和溶液中加入溶液,先生成黄色沉淀,可知 的溶
度积大于 。
有“化”好说
组成类型相似,且含相同离子的难溶电解质沉淀时,不一定是 小的先沉淀。如向含
、、的混合液中加入时,确定哪种卤化银先沉淀要看、、 的浓
度大小。
题型三 溶度积的应用
5.(2023浙江金华模拟)在时,下列几种难溶电解质的溶度积常数 如表所示,
下列说法不正确的是( )
(白) (白) (白) (浅黄) (黑)
A
A.由溶度积常数可判断在相同条件下物质的溶解性大小
B.重晶石的主要成分是 ,工业上常用饱和碳酸钠溶液反复浸泡重晶石,将难处理
的转化为较易处理的
C.向的悬浊液中滴加饱和溶液可以得到浅黄色 悬浊液
D.在含银工业废水的处理中,相同浓度的溶液比溶液沉淀效果好,而且
溶液可以沉淀多种重金属离子
【解析】 A(×)对于结构相似的物质,溶度积常数越小,溶解度越小。
B(√)由表格中数据可知,反应 的平衡常
数, 浓度较大
时,,反应正向进行,可生成沉淀(【提醒】当类型相同的难溶物的 相
差不大时,通过控制条件也能使小的难溶物转化为 大的难溶物),故工业上常用
饱和碳酸钠溶液反复浸泡重晶石,将难处理的转化为较易处理的 。
C(√)一般来说,溶解能力相对较强的沉淀容易转化为溶解能力相对较弱的沉淀,由
表格中数据可知的溶度积比小,即溶解度:,故向 的悬浊液
中滴加的饱和溶液可以得到浅黄色 悬浊液。
D(√)由表格中数据可知的溶度积远小于 ,则在含银工业废水的处理中,相
同浓度的溶液比溶液沉淀效果好,而且多种金属的硫化物均为难溶物,
溶液可以沉淀多种重金属离子。
能力觉醒
6.(2023福建宁德名校联考)对 悬浊液进行下列操作,达到平衡后(选项C、D均
指恢复至原温度,不考虑体积变化),和 均保持不变的是( )
B
A.适当升温 B.加少量水
C.加入少量浓硫酸 D.加入少量氯化钡固体
【解析】 溶解平衡是吸热反应。
第一步:外界条 件变化 第二步:判断 、 的变化 第三步:平衡移 动方向 第四步:结果分析
A (×) 升高温度 、 不变, 正向移动 、
B (√) 加少量水, 、 不变、 , 正向移动 不变、
不变(得到的仍为
饱和溶液)
第一步:外界条 件变化 第二步:判断 、 的变化 第三步:平衡移 动方向 第四步:结果分析
C (×) 加入少量浓硫 酸, 不变、 , 逆向移动
D (×) 加入少量氯化钡 固体, 不变、 , 逆向移动 续表
7.(2023上海虹口区模拟)某兴趣小组对氢氧化镁的溶解进行如图探究实验。下列说法
错误的是( )
A
A.:① ③
B.③中存在:
C.③中液体又变红的原因:沉淀溶解平衡正向移动
D.①、③中存在沉淀溶解平衡:
【解析】 A(×)方法一 ①中含有氢氧化镁,③中除了氢氧化镁还有氯化镁,同温度
下相同,③中大,则:③ ①。
方法二 ③中除了氢氧化镁还有氯化镁,相当于增大 。
第一步:外 界条件变化 第二步:判断、 的变化 第三步:平 衡移动方向 第四步:结果分析
不变、 , 逆向移动 、(平衡移动是有限的,
不能抵消条件的改变)
故:③ ①。
B(√)③中除了有还有,完全电离, 存在溶解平衡,也
能产生,则 。
C(√)
第一步:外界条件变化 第二步:判断 、 的变化 第三步:平 衡移动方向 第四步:结果
分析
加入几滴浓盐酸,与 电离出的 反应, ,溶液褪色 不变、 , 正向移动 电离出 ,
液体又变红
D(√)根据上述分析知,①、③中存在沉淀溶解平衡
。
8.(2024浙江金华十校期末)时,金属离子初始浓度为 时,发生相应
变化的 如下表所示:
开始沉淀 完全沉淀(离子浓度等于 ) 开始溶解 完全溶解
7.0 9.0 13.5
1.9 3.2 14
6.3 8.0 10.5 12.6
下列做法正确的是( )
B
A.悬浊液中,
B.加入可能实现向 的转化
C.若初始浓度为,则开始溶解的
D.分离、:加碱至 ,搅拌后过滤,固体、滤液分别加酸至强酸性
【解析】 A(×)悬浊液中存在 ,该沉淀
溶解平衡微弱,故比较离子浓度要考虑水的电离,则 。
B(√)根据表中数据,当金属离子浓度相等时,开始沉淀的, 开始
沉淀的,说明比更难溶, 悬浊液中存在
,加入,与 结合生成更难溶的
,促进平衡向右进行,可能实现向 转化。
C(×)开始生成时,发生反应 ,则
越大、越小,即开始沉淀的减小; 开始溶解时,发生反应
, 对该反应无影响,即不会影响
开始溶解的 。
D(×)根据表中数据,加碱至,以的形式存在, 完全溶
解,为絮状沉淀,不易用过滤方法从溶液中分离出来,同时根据表中 、
开始沉淀时的 ,不需要加酸至强酸性。
9.(2024福建厦门一中期中)常温下,将 粉
末置于盛有 蒸馏水的烧杯中,然后向烧杯中加入
固体(忽略溶液体积的变化)并充分搅拌,该过程
中几种离子的浓度变化曲线如图所示,下列说法不正确的
是( )
C
A.反应 的
B.相同温度下,在水中和在溶液中的 不变
C.曲线代表 浓度变化
D.锅炉水垢中的可先用溶液处理,使转化为 后,再用酸除去
【解析】 开始时溶液中存在沉淀溶解平衡:
,
;
当加入的 固体使溶液中
时( 点)开始发生沉淀
的转化,此时溶液中存在、 的溶解平衡,故
;继续加入固体,
与结合生成沉淀,减小, 平衡右
移,增大,故曲线代表浓度变化,曲线代表 浓度变化。
A(√)反应
的 。
B(√) 只与温度有关,而与溶剂无关,故相同温度
下,在水中和在溶液中的 不变。
C(×)曲线代表 浓度变化。
D(√)锅炉水垢中的 微溶于水,不溶于酸,可根据
沉淀溶解平衡,先用溶液处理,使 转化为
,弃去沉淀转化后的溶液,再向沉淀中加入盐酸,
发生反应: ,达到
除去锅炉水垢的目的。
素养觉醒
10.(传统文化)沈括《梦溪笔谈》记载“石穴中水,所滴皆为钟乳”,下列条件不利于
碳酸钙析出的是( )
A
A.减小 B.水分蒸发 C. 压强减小 D.温度升高
【解析】 钟乳石的主要成分为碳酸钙,它的形成涉及石灰岩中不溶性碳酸
钙转化为可溶性的碳酸氢钙: 和碳酸钙沉淀的析出:
。
A(√) 减小,碳酸钙沉淀的析出反应平衡逆向移动,不利于碳酸钙的析出,符
合题意。
B(×)水分蒸发,碳酸钙沉淀的析出反应平衡正向移动,有利于碳酸钙的析出,不符
合题意。
C(×)压强减小,则其溶解度降低,溶液中 的浓度减小,碳酸钙沉淀的析出反
应平衡正向移动,有利于碳酸钙的析出,不符合题意。
D(×)碳酸钙沉淀的析出为分解反应,此过程吸热,温度升高,平衡正向移动,有利
于碳酸钙的析出,不符合题意。
11.(生活情境)(2024四川成都七中期中)牙釉质的主要成分为羟基磷酸钙
,在牙齿表面存在平衡:
,
已知的 。下列说法错误的是( )
C
A.残留在牙齿上的糖会发酵产生 ,使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质
B.按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀牙齿
C.用含 的溶液漱口,可使平衡左移,保护牙齿
D.含氟牙膏使转化为更难溶的 ,促进牙齿表面矿物质的沉积,
修复牙釉质
【解析】 A(√)
第一步:外界条件变化 第二步:判断 、 的变化 第三步:平 衡移动方向 第四步:结果分析
残留在牙齿上的糖会发酵产 生 ,中和溶解平衡生成的 , 不变、 , 正向移动 促进
溶解,破坏牙釉质
B(√)由A项分析可知,按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀
牙齿。
C(×)碱性太强,具有强腐蚀性,不能用含 的溶液漱口,否则将腐蚀口腔
等组织。
D(√),含氟牙膏使 转化为更难溶
的 ,促进牙齿表面矿物质的沉积,修复牙釉质。
第3章 物质在水溶液中的行为
2025年高考化学一轮复习
选择性必修第一册鲁科版
第3节 沉淀溶解平衡
课时2 相关计算及图像分析
题型觉醒
题型一 的相关计算
1.(2023重庆万州二中月考)已知室温时 ,
。下列关于和 两种悬浊液的说法错误的
是( )
B
A.和两种悬浊液中前者的 较小
B.分别滴加稀硫酸,与 的溶度积常数均增大
C.分别加入的溶液,和 均减小
D.和共存的饱和溶液中, 的值约为97.4
【解析】 A(√) 悬浊液中
, 悬浊液中,
,故
,因此和 两种悬浊液
中前者的 较小。
B(×)溶度积常数只与温度有关,温度不变,溶度积常数不变。
C(√)加入溶液,浓度增大,、 沉淀溶解平衡均逆向移动,
和 均减小。
D(√) 。
题型二 沉淀溶解平衡曲线
2.(2023辽宁重点高中期末)在时,
(砖红色)在水溶液中的沉淀溶解平衡曲线如图
所示。又知 的
。下列说法正
确的是( )
B
A.时,的为
B.时,点和点时的 相等
C.时,向饱和溶液中加入 能使
溶液由点变为 点
D.时,向悬浊液中加入 固体,可
生成白色沉淀
【解析】
A(×)根据题图知,达到沉淀溶解平衡时, 、
,故
。
B(√)溶度积只受温度影响,温度不变,溶度积不变。
C(×)饱和溶液中加入,增大、减小,能使溶液由 点
变为 点。
D(×)固体的量没有给出,不能确定此时 ,不能确定
此时是否有白色沉淀生成。
3.(2024天津耀华中学期末)室温时, 、
和 在水中达到沉淀溶解平衡时的
关系如图所示, 表示
、、; 可
认为 沉淀完全]。下列叙述正确的是( )
C
A.由点可求得
B.时的溶解度为
C.浓度均为的和 可通过分步沉淀进行分离
D.、混合溶液中 时二者不会同时沉淀
【解析】
A(×)根据题图知,点时 处于沉淀溶解平衡状态,
、
,故
。
B(×)根据题图知,时,即,故
的溶解度为 。
C(√)由题图可知,当(即)时, ,
而当(即)时,, 才开始沉淀,故当
完全沉淀时,尚未开始沉淀,可通过调节溶液的方法分步沉淀和 。
D(×)由题图可知,沉淀完全时,, 刚要开始沉淀,此时
,而,则、 会
同时沉淀。
4.(2024广东深圳中学期中)工业废水中含重
金属离子,可通过化学沉淀法将其除去,
时,与 在水中的沉淀溶解平衡曲线如
图所示(表示和 )。下列说法不
正确的是( )
D
A.点对应的 溶液为过饱和溶液
B.时,
C.向含沉淀的悬浊液中加入 固体可实
现点到 点的变化
D.向、浓度均为 的工业废水中通入气体,首先沉淀的是
【解析】
A(√)点在的沉淀区,对应 的过饱和溶液。
B(√)时,取点数据计算, 、
,
。
C(√)
第一步:外界条件变 化 第二步:判断、 的变 化 第三步:平衡 移动方向 第四步:结果分析
加入固体, 不变、, 逆向移动 、
温度不变时, 不变,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变
化,不会出现在曲线以外,减小、 增大,即横轴增大、纵轴减小。
D(×)取 点数据计算,
,、 的
浓度均为时,开始生成 沉淀时,
,开始生成 沉淀时,
,生成沉淀时所需
小,故向、浓度均为工业废水中通入,先生成 沉淀。
题型三 沉淀滴定曲线
5.已知时,、、的 分别为
、、
,用标准溶液滴定
卤素离子,以滴入 标准溶液的体积为横轴,
为纵轴,
就可绘得滴定曲线。现以 溶
液分别滴定、、 ,
绘得滴定曲线如图,下列有关说法正确的是 ( )
A.、、分别表示、、
B.、、分别表示、、
C.、、分别表示、、
D.用滴定法测定试样中,可用 作
指示剂
√
【解析】 A(×)B(×)C(√)
D(×)若溶液中同时存在和,当 时,
加入,先沉淀的是 ,测得的结果不准确。
能力觉醒
6.(2023河南焦作第一高级中学期末)已知 ,
, 。某溶液中含有
、和,浓度均为,向该溶液中逐滴加入 的
溶液时,三种阳离子产生沉淀的先后顺序为( )
A
A.、、 B.、、
C.、、 D.、、
【解析】 根据溶度积的定义可知,三种离子沉淀时分别有
,
,,溶液中、、 的浓度均为
,则向该溶液中逐滴加入溶液产生沉淀时,所需 分别为
、 、
,所以这三种离子产生沉淀的先后顺序为 、
、 。
7.(2023广东广州广雅中学期中)时, 在不
同浓度盐酸中的最大溶解量(单位: )如图所示。
下列叙述正确的是( )
B
A.盐酸浓度越大, 越大
B. 能与一定浓度的盐酸反应
C.、两点对应的溶液中 相等
D.向含的溶液中加入过量浓盐酸,可将 完全转化为
【解析】 A(×) 只受温度影响,温度不变,
不变。
B(√)时,增大盐酸浓度, 的
溶解平衡逆向移动, 的溶解量减少,而当
时, 的溶解度随盐酸浓度的
增大而显著增大,则 能与一定浓度的盐酸反应。
C(×)、两点的溶解量相等,但点时与发生了反应,故、 两点对
应的溶液中 不相等。
D(×)存在溶解平衡,且能与盐酸反应,故向含 的溶液中加入过量
浓盐酸,不能将完全转化为 。
8.(大招39)(2023广东惠州四校联考) 可用于人
工降雨。 溶于水,溶液中离子浓度与温度的关系如
图所示,已知:, 。
下列说法正确的是( )
B
A.
B.的溶度积
C.时,粉末溶于饱和 溶液中
D.在点饱和溶液中加粉末,点移动到 点
【解析】
A(×)碘化银的沉淀溶解平衡是吸热反应,
则升高温度,增大,而题图中 点对
应的、较点的小,即 点对应的
较点的小,故 。
B(√)根据A项分析知, ,又
只受温度影响,在相同温度下,曲线
上的各点溶度积相同,故
。
C(×) 在溶液中存在沉淀溶解平衡:
, 溶液中存在大
量,抑制溶解, 减小,由题图
知,点为时 的饱和溶液,此时
,故
粉末溶于饱和 溶液中
。
D(×)温度不变时, 不变,无论改变哪种
离子的浓度,另一种离子的浓度只能在曲线上
变化,不会出现在曲线以外。在点饱和 溶
液中加粉末, 的沉淀溶解平衡逆向
移动,增大、减小,减小、
增大,点沿曲线向 点方向移动。
9.(2024云南师范大学附中期中)已知:常温下,
,
;
。常温下,向
溶液中逐滴滴加
溶液,溶液与加入 溶液
C
A.,
B.若,则反应终点可能为 点
C.、、三点中,由水电离出的与之和最大的为 点
D.相同条件下,若用等浓度、等体积的溶液代替上述 溶液,则反应终点
由点向 点方向移动
的体积 的关系如图所示。下列说法错误的是( )
【解析】
. .
.
A(√) 点为反应终点,则
,此时存在 的沉
淀溶解平
衡,该点, ,即
。
B(√) 减小,达到反应终点需要的
溶液的体积减小,而反应终点时 不变
(【提醒】反应终点时的取决于 ,
与起始时的无关),即 不变,反应终点
可能为 点。
C(×)点溶液中溶质为和 ,
水解促进水的电离; 点溶液中溶质为
;点溶液中溶质为和, 水
解促进水的电离,故点由水电离出的 与
之和最小。
D(√) ,达到反应终点时,
,相同条件下,若用等浓度、等
体积的溶液代替 溶液,反应终
点时,消耗 溶液的体积相等,但,,故反应终点由点向 点方向移动。
10.(大招39)(2023山东枣庄第一中学期末)已知:
,(代表、 、
)。时, ,
, 。在
、、 的饱和溶液中阳离子和阴离子的浓度关系如
图所示。下列说法正确的是( )
D
A.时,在的饱和溶液中加入少量,和 都减小
B.图中曲线代表,且点
C.时,增大点阴离子的浓度,则点沿方向向 点移动
D.时,的平衡常数
【解析】
A(×)
第一步:外界条 件变化 第二步:判断、 的变化 第三步:平 衡移动方向 第四步:结果分析
加入少量 , 不变、 , 逆向移动 ( 平衡移动是有限
的,不能抵消条件的改变)、
B(×)曲线代表,点 。
C(×)根据A项分析知,增大点的阴离子浓度,即 增大,沉淀溶解平衡逆向移
动,减小、增大,则增大、减小,故点沿方向向 点的斜下方
移动。
D(√) 。
11.(大招39)(2024广东五校联考)常温
下,用 溶液滴定
溶液,
作指示剂,测得溶液中
、 随
加入 溶液体积的变化关系如图所示。
C
A.为防止指示剂失效,溶液应维持
B.该温度下,的溶度积常数
C.时,(已知 )
D.相同实验条件下,若改为溶液,则滴定终点 向左平移
已知:;常温下,在时易形成沉淀 。下列
说法错误的是( )
【解析】
A(√)在时易形成沉淀 而失去作为指示剂的作用,故为防止指示剂
失效,溶液应维持 。
B(√)点时溶液中 ,则该温度下
。
C(×)(溶液)时,溶液过量 ,
, ,
。
D(√)若改为溶液,则达到滴定终点时消耗 溶液的体积减
小,滴定终点 向左平移。
12.(大招39)(2024重庆西南大学附中月考)某元素 的
氢氧化物 在水中的溶解反应为
、
。, 与
的关系如图所示,为或 的浓度。下列说
法正确的是( )
B
A.曲线①代表与 的关系
B.的为
C.当溶液达到15.0时, 才开始溶解
D.向的溶液中加入 溶液至,
体系中元素主要以 的形式存在
【解析】
A(×)曲线②代表与 的关系。
B(√)曲线①代表与 的关系,
时, ,即
, ,
则 。
C(×)由题图可知,小于8.0时, 溶解得
到,约大于12.5时, 溶解得到 。
D(×)由题图可知,时, 、
都很小,体系中元素主要以 的
形式存在。
13.(2023江苏南京中华中学月考)铁的化合物有广泛用途,如三草酸合铁(Ⅲ)酸钾
晶体是一种光敏材料,也可作催化剂,碳酸亚铁 可作补
血剂等,以废铁屑(含及少量和 )为原料制备以上物质的流程如下:
已知:①, ,
, ;
②某离子浓度小于等于 时认为该离子沉淀完全;
③ 为可溶于水、难溶于乙醇的翠绿色晶体。
回答下列问题:
(1) 滤液Ⅰ中含有、,检验 所用的试剂为____________(填化学式)。
【解析】 废铁屑含、、 ,滤液Ⅰ是废铁屑与盐酸反应后的混合液,故
滤液Ⅰ中含、。检验可选用试剂,与 反应生成蓝色沉淀。
(2) 室温下,若滤液Ⅰ中为 ,要保证滤液Ⅰ中不出现沉淀,则滤
液Ⅰ中应大于____ 。
0.1
【解析】 滤液Ⅰ中主要含,若较大,则会生成 沉淀,要保证滤液Ⅰ中无沉
淀,则 ,即
,则 。
(3) 将滤液Ⅱ与饱和 溶液混合,发生反应的离子方程式为
____________________________________________________________________________
___________________________________________________________________________;
已知饱和溶液的大于11,是否能用饱和溶液代替饱和 溶液来
制备 ?____(填“是”或“否”)。
(或、)
否
【解析】 向滤液Ⅰ中加入足量,与反应生成,滤液Ⅱ为 溶液,其与饱
和溶液混合后,与反应得到 ,离子方程式为
(或 、
)。溶液中,饱和 溶
液的, ,则
,故若用饱和 溶液代替饱
和溶液来制备,会生成少量,导致得到的 不纯。
(4) 滤液Ⅰ与足量空气发生反应的离子方程式为_________________________________;
甲同学认为该步反应用稀 代替空气效果更好,乙同学不同意甲的观点,其理由是
_____________________________________________________________。
是分解的催化剂,会消耗大量的,导致生产成本过高
【解析】 滤液Ⅰ中通入足量空气的目的是将氧化成 ,离子方程式为
;溶液中的能催化分解,若用稀 代
替空气,会消耗大量的 ,使生产成本过高。
(5) 获得翠绿色晶体的“一系列操作”包含__________________________(填操作名
称);用乙醇洗涤晶体而不用水洗涤的目的为________________________________。
蒸发浓缩、冷却结晶、过滤
减少晶体溶解损失,使晶体易干燥
【解析】 获得翠绿色晶体的“一系列操作”包含蒸发浓缩、冷却结晶、过滤;用乙醇洗
涤晶体而不用水洗涤的目的是减少晶体溶解损失,使晶体易干燥。
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
