江西宜春2015-2016学年第一学期高一化学第一章从实验学化学第二节化学计量在实验中的应用——物质的量教学课件(共22张PPT)
文档属性
| 名称 | 江西宜春2015-2016学年第一学期高一化学第一章从实验学化学第二节化学计量在实验中的应用——物质的量教学课件(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 976.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-02-16 00:00:00 | ||
图片预览






文档简介
课件22张PPT。第一章 从实验学化学第二节 化学计量在实验中的应用
(物质的量)
物质的量的概念1物质的量与微粒数的换算2摩尔质量的概念3物质的量与物质的质量的换算4 1月29日下午,一对夫妇抬着一大袋一角
硬币,在武汉市东西湖吴家山工贸家电买了台
热水器。他们原本想将这些硬币拿到银行换成
整钞,再到卖场购买热水器,但没有哪家银行
愿意兑换,只好抬着硬币到卖场来试试。该卖
场决定收下这些硬币,并立即组织6名售货员
进行清点:一角的硬币共5300枚。据了解,这
些硬币约有10公斤。顾客称,他从福建来到武
汉,这些硬币是老板付给他的部分工资。
新闻10Kg硬币
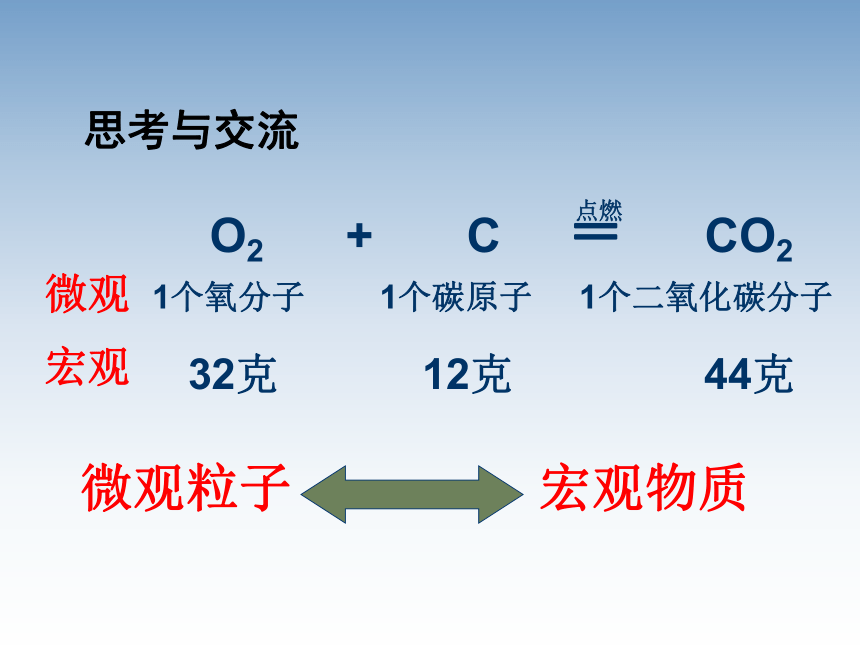
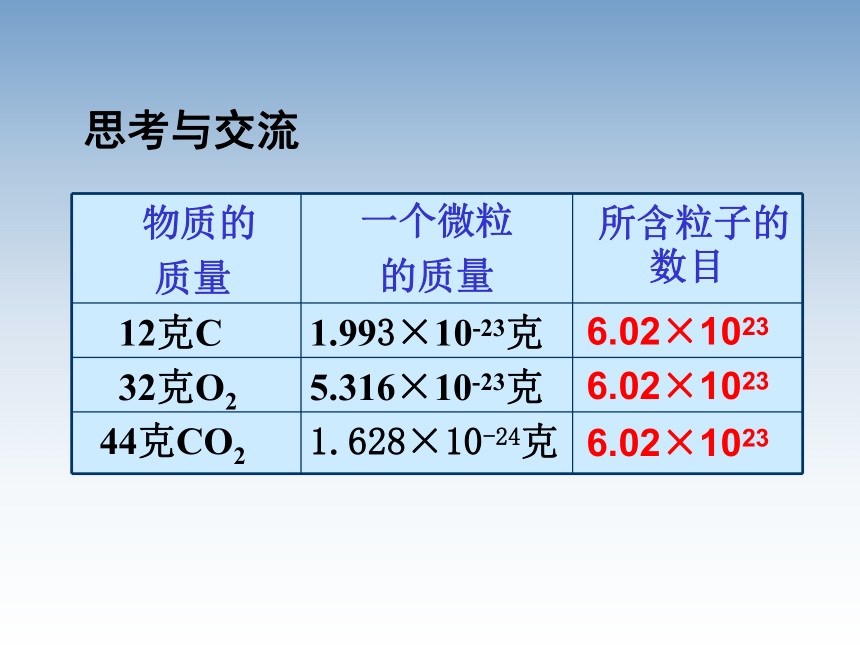
总数 ?1份=X g=一定数目的硬币约27枚50 g =我们如何计算硬币的数量? 信息:一滴水大约是0.05g,含有的水分子数让10亿人去数,每人每分钟数100个,日夜不停的数,需要3万年才能数完。如何计算一滴水分子的数目?1个氧分子 1个碳原子 1个二氧化碳分子 32克 12克 44克微观粒子 宏观物质微观宏观思考与交流6.02×1023 6.02×1023 6.02×1023 思考与交流一、物质的量1、定义:物质的量表示含有一定数目粒子
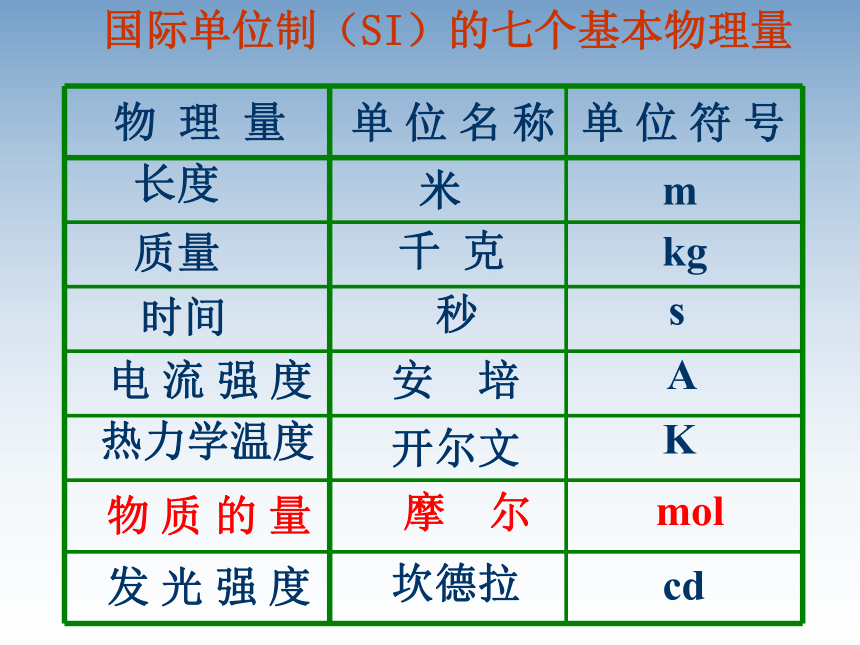
的集体。 符号——n2、物质的量的单位:摩尔 符号——mol物 理 量单 位 名 称单 位 符 号长度质量时间电 流 强 度热力学温度发 光 强 度米千 克秒安 培开尔文坎德拉摩 尔mkgsAKcdmol 国际单位制(SI)的七个基本物理量物 质 的 量一、物质的量1、定义:物质的量表示含有一定数目粒子
的集体。 符号——n2、物质的量的单位:摩尔 符号——mol 0.012Kg 12C中所含的碳原
子数,约为6.02×1023。 3、1mol的规定:阿伏加德罗常数:
0.012kg12C含有的原子数.
把1mol任何粒子的粒子数叫做阿伏加德罗常数,符号为NA,单位为mol—1◆ 0.5molO中约含有氧原子的个数是 。4NA 或2.408×10240.5NA或3.01×1023NA的应用◆ 1.806×1024个N2的物质的是 。◆ 2 molH2中约含 个
氢原子。 3mol1、物质的量既表示一定物质的质量,
又表示一定微粒的数量。
2、1mol的苹果的说法是对的吗?
3、1mol氧气中含有6.02×1023 个氧分子。正误判断错错错5、摩尔的使用范围:仅指微观粒子
(一般用化学符号表示)
微观粒子包括:
原子、分子、离子、质子、中子、电子。
如:1 molFe、1molSO42—、2molH2O等。一、物质的量O2 + C = CO2点燃1个氧分子 1个碳原子 1个二氧化碳分子 32克 12克 44克微观从宏观质 量角度探索发现扩大6.02
×1023倍6.02×1023 6.02×1023 6.02×1023从物质的
量角度 1molO2 1mol C 1mol CO21mol的几种物质1mol粒子的质量以克为单位数值上等于
该粒子的相对分子质量。奥妙被发现二、摩尔质量将单位物质的量的物质所具有的质量叫做摩尔
质量,符号为M,常用单位是克/摩 或 g/mol如:M(Mg)=24g/molM(SO2)= 64 g/mol物质的摩尔质量(M)、质量(m)和物质的量(n)之间的关系:关于摩尔质量的计算n= mM物质的量摩尔质量物质的质量公式变形:例题例1、求下列物质的物质的量:90 g H2O解:=5 mol例2、1.5mol Na2CO3的质量是多少?解:m(Na2CO3)= n(Na2CO3)×M(Na2CO3)=1.5mol×106g/mol=159g变式训练:例3、求24.5 g H2SO4的硫酸分子数为多少?思路:1、根据质量求出硫酸的物质的量
2、根据物质的量计算硫酸的分子数。解:N(H2SO4)=n(H2SO4)× NA
= 0.25 mol ×6.02×1023mol—1
= 1.505×1023n(H2SO4)==0.25molNnm÷NA×M×NA÷M联系宏观和微观物质的桥梁小结谢谢大家!
(物质的量)
物质的量的概念1物质的量与微粒数的换算2摩尔质量的概念3物质的量与物质的质量的换算4 1月29日下午,一对夫妇抬着一大袋一角
硬币,在武汉市东西湖吴家山工贸家电买了台
热水器。他们原本想将这些硬币拿到银行换成
整钞,再到卖场购买热水器,但没有哪家银行
愿意兑换,只好抬着硬币到卖场来试试。该卖
场决定收下这些硬币,并立即组织6名售货员
进行清点:一角的硬币共5300枚。据了解,这
些硬币约有10公斤。顾客称,他从福建来到武
汉,这些硬币是老板付给他的部分工资。
新闻10Kg硬币
总数 ?1份=X g=一定数目的硬币约27枚50 g =我们如何计算硬币的数量? 信息:一滴水大约是0.05g,含有的水分子数让10亿人去数,每人每分钟数100个,日夜不停的数,需要3万年才能数完。如何计算一滴水分子的数目?1个氧分子 1个碳原子 1个二氧化碳分子 32克 12克 44克微观粒子 宏观物质微观宏观思考与交流6.02×1023 6.02×1023 6.02×1023 思考与交流一、物质的量1、定义:物质的量表示含有一定数目粒子
的集体。 符号——n2、物质的量的单位:摩尔 符号——mol物 理 量单 位 名 称单 位 符 号长度质量时间电 流 强 度热力学温度发 光 强 度米千 克秒安 培开尔文坎德拉摩 尔mkgsAKcdmol 国际单位制(SI)的七个基本物理量物 质 的 量一、物质的量1、定义:物质的量表示含有一定数目粒子
的集体。 符号——n2、物质的量的单位:摩尔 符号——mol 0.012Kg 12C中所含的碳原
子数,约为6.02×1023。 3、1mol的规定:阿伏加德罗常数:
0.012kg12C含有的原子数.
把1mol任何粒子的粒子数叫做阿伏加德罗常数,符号为NA,单位为mol—1◆ 0.5molO中约含有氧原子的个数是 。4NA 或2.408×10240.5NA或3.01×1023NA的应用◆ 1.806×1024个N2的物质的是 。◆ 2 molH2中约含 个
氢原子。 3mol1、物质的量既表示一定物质的质量,
又表示一定微粒的数量。
2、1mol的苹果的说法是对的吗?
3、1mol氧气中含有6.02×1023 个氧分子。正误判断错错错5、摩尔的使用范围:仅指微观粒子
(一般用化学符号表示)
微观粒子包括:
原子、分子、离子、质子、中子、电子。
如:1 molFe、1molSO42—、2molH2O等。一、物质的量O2 + C = CO2点燃1个氧分子 1个碳原子 1个二氧化碳分子 32克 12克 44克微观从宏观质 量角度探索发现扩大6.02
×1023倍6.02×1023 6.02×1023 6.02×1023从物质的
量角度 1molO2 1mol C 1mol CO21mol的几种物质1mol粒子的质量以克为单位数值上等于
该粒子的相对分子质量。奥妙被发现二、摩尔质量将单位物质的量的物质所具有的质量叫做摩尔
质量,符号为M,常用单位是克/摩 或 g/mol如:M(Mg)=24g/molM(SO2)= 64 g/mol物质的摩尔质量(M)、质量(m)和物质的量(n)之间的关系:关于摩尔质量的计算n= mM物质的量摩尔质量物质的质量公式变形:例题例1、求下列物质的物质的量:90 g H2O解:=5 mol例2、1.5mol Na2CO3的质量是多少?解:m(Na2CO3)= n(Na2CO3)×M(Na2CO3)=1.5mol×106g/mol=159g变式训练:例3、求24.5 g H2SO4的硫酸分子数为多少?思路:1、根据质量求出硫酸的物质的量
2、根据物质的量计算硫酸的分子数。解:N(H2SO4)=n(H2SO4)× NA
= 0.25 mol ×6.02×1023mol—1
= 1.505×1023n(H2SO4)==0.25molNnm÷NA×M×NA÷M联系宏观和微观物质的桥梁小结谢谢大家!
