沪教版九年级全册《第4章燃烧 燃料》2015年单元检测卷(江苏省盐城市射阳县特庸中学)
文档属性
| 名称 | 沪教版九年级全册《第4章燃烧 燃料》2015年单元检测卷(江苏省盐城市射阳县特庸中学) |

|
|
| 格式 | zip | ||
| 文件大小 | 208.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-02-18 00:00:00 | ||
图片预览




文档简介
沪教版九年级全册《第4章 燃烧 燃料》2015年单元检测卷(江苏省盐城市射阳县特庸中学)
一、选择题(本大题15小题,每小题2分,共30分)
1.下列化学式中,书写错误的是( )
A.氧化钙OCa B.氧化镁 MgO
C.三氯化铁 FeCl3 D.三氧化硫SO3
2.关于原子的说法不正确的是( )
A.是构成物质的一种粒子 B.是化学变化中的最小粒子
C.在化学反应中可以再分 D.是由原子核和核外电子构成
3.下列符号中,既能表示氢元素,又能表示氢原子的是( )
A.2H B.2H+ C.2H2 D.H
4.《物质构成的奥秘》告诉我们:元素的种类、化学性质分别与下列粒子数密切相关的是( )
A.质子数、中子数 B.质子数、最外层电子数
C.中子数、最外层电子数 D.最外层电子数、质子数
5.“乐百氏”矿泉水标签上印有水质成分如 ( http: / / www.21cnjy.com )下(mg/L):硒:0.013;锶:0.0596;锌:0.00162;钠:18.4;钙:4.69.这里的硒、锶、锌、钠、钙是指( )
A.元素 B.原子 C.单质 D.分子
6.以下对O2、CO2、SO2、MnO2四种物质组成的说法中,正确的是( )
A.都含有氧分子 B.都含有2个氧原子
C.都含有氧元素 D.都是氧化物
7.葡萄糖(C6H12O6)是一种重要营养物质,下列关于葡萄糖的说法,正确的是( )
A.葡萄糖由6种碳元素、12种氢元素和6种氧元素组成
B.葡萄糖由6个碳原子、12个氢原子和6个氧原子构成
C.每个葡萄糖分子中所含原子个数为24
D.每个葡萄糖分子中碳、氢、氧原子个数比为6:1:8
8.已知某物质的化学式为RNO3,相对分子质量是85,则R元素的相对原子质量是( )
A.55 B.55g C.23 D.23g
9.按氯元素化合价由低至高的排列顺序,在HCl、X、HClO、KClO3中,X代表的是( )
A.NaCl B.KClO C.Cl2 D.ClO2
10.要使Fe3O4和Fe2O3中所含铁元素质量相等,则Fe3O4与Fe2O3质量比为( )
A.2:3 B.4:5 C.29:30 D.3:2
11.H2O与H2O2的化学性质不同的原因是( )
A.它们的元素组成不同 B.它们在常温下状态不同
C.它们的分子构成不同 D.H2O2有氧气而H2O中没有
12.元素X的原子最外层有3个电子,元素Y的原子最外层有6个电子,则这两种元素组成的化合物的化学式可能是( )
A.XY3 B.X2Y C.X2Y3 D.X3Y2
13.质子数相同的两种不同粒子可能是①同一 ( http: / / www.21cnjy.com )元素的原子或离子②两个不同的分子③一种原子和一种分子④两种不同的离子⑤一种离子和一种分子( )
A.①③ B.①②③④ C.①③④⑤ D.①②③④⑤
14.X2+的离子核外有28有电子,其相对原子质量为65,X原子核内中子数与质子数之差为( )
A.9 B.5 C.2 D.0
15.元素的原子最外层电子得到或失去后,一定不会改变的是( )
①元素种类②化学性质③相对原子质量④微粒电性⑤原子核⑥电子层数⑦最外层电子数⑧核外电子总数.
A.②③⑤ B.②④⑥⑧ C.②⑤ D.①③⑤
二、填空题(每空1分,共40分.)
16.标出下列划线元素的化合价
KClO3Cl2SO42﹣NH4NO3.
17.用化学符号表示
①硫离子__________
②2个氧分子__________
③+2价的锌元素__________
④4个亚铁离子__________
⑤2个碳酸根离子__________
⑥氧化铁中铁元素的化合价为+3价__________
⑦2SO2前“2”的意义__________;后“2”的意义__________
⑧氯离子的结构示意图__________.
18.根据名称写出下列物质的化学式
氧化钠__________氯化钡__________硫酸铝__________
氢氧化钙__________碳酸钠__________硝酸铵__________.
19.N2、Cl2、H2、HCl、CH4各 ( http: / / www.21cnjy.com )一个分子,按质量由小到大的排列顺序是__________;若取等质量的上述各气体,则分子数目由少到多的排列顺序是__________.
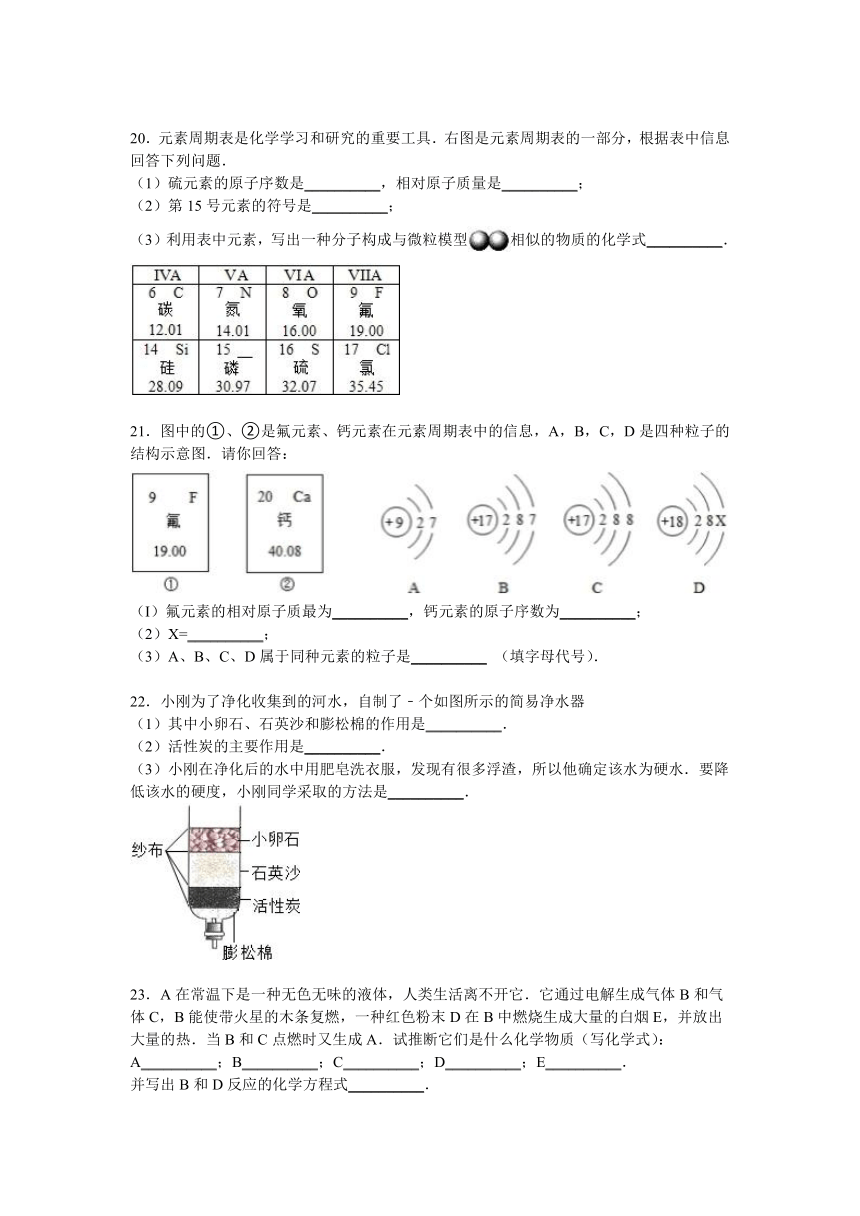
20.元素周期表是化学学习和研究的重要工具.右图是元素周期表的一部分,根据表中信息回答下列问题.
(1)硫元素的原子序数是__________,相对原子质量是__________;
(2)第15号元素的符号是__________;
(3)利用表中元素,写出一种分子构成与微粒模型相似的物质的化学式__________.
( http: / / www.21cnjy.com )
21.图中的①、②是氟元素、钙元素在元素周期表中的信息,A,B,C,D是四种粒子的结构示意图.请你回答:
( http: / / www.21cnjy.com )
(I)氟元素的相对原子质最为__________,钙元素的原子序数为__________;
(2)X=__________;
(3)A、B、C、D属于同种元素的粒子是__________ (填字母代号).
22.小刚为了净化收集到的河水,自制了﹣个如图所示的简易净水器
(1)其中小卵石、石英沙和膨松棉的作用是__________.
(2)活性炭的主要作用是__________.
(3)小刚在净化后的水中用肥皂洗衣服,发现有很多浮渣,所以他确定该水为硬水.要降低该水的硬度,小刚同学采取的方法是__________.
( http: / / www.21cnjy.com )
23.A在常温下是一种无色 ( http: / / www.21cnjy.com )无味的液体,人类生活离不开它.它通过电解生成气体B和气体C,B能使带火星的木条复燃,一种红色粉末D在B中燃烧生成大量的白烟E,并放出大量的热.当B和C点燃时又生成A.试推断它们是什么化学物质(写化学式):
A__________;B__________;C__________;D__________;E__________.
并写出B和D反应的化学方程式__________.
四、计算题:(共4分)
24.烟草中含有对健康危害(尼古丁),其化学式为C10H14N2,试计算:
(1)尼古丁的相对分子质量;
(2)尼古丁中各元素的质量比;
(3)尼古丁中氮元素的质量分数;
(4)与8.1克尼古丁所含氮元素相等CO(NH2)2的质量是多少?
沪教版九年级全册《第4章 燃烧 燃料》2015年单元检测卷(江苏省盐城市射阳县特庸中学)
一、选择题(本大题15小题,每小题2分,共30分)
1.下列化学式中,书写错误的是( )
A.氧化钙OCa B.氧化镁 MgO
C.三氯化铁 FeCl3 D.三氧化硫SO3
【考点】化学式的书写及意义.
【专题】化学用语和质量守恒定律.
【分析】化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.
【解答】解:A、氧化钙的化学式为;CaO,故选项书写错误.
B、氧化镁中镁元素显+2价,氧元素显﹣2价,其化学式为MgO,故选项书写正确.
C、三氯化铁中铁元素显+3价,氯元素显﹣1价,其化学式为FeCl3,故选项书写正确.
D、三氧化硫的化学式为SO3,故选项书写正确.
故选A.
【点评】本题难度不大,掌握化合物化学式 ( http: / / www.21cnjy.com )的书写一般规律(金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)是正确解答此类题的关键.
2.关于原子的说法不正确的是( )
A.是构成物质的一种粒子 B.是化学变化中的最小粒子
C.在化学反应中可以再分 D.是由原子核和核外电子构成
【考点】原子的定义与构成.
【专题】物质的微观构成与物质的宏观组成.
【分析】A、原子是构成物质的一种粒子;
B、原子是化学变化中的最小粒子;
C、在化学变化中,原子不能再分;
D、原子由原子核和核外电子构成.
【解答】解:A、原子是构成物质的一种粒子,故A正确;
B、原子是化学变化中的最小粒子,故B正确;
C、在化学变化中,原子不能再分,故C错误;
D、原子由原子核和核外电子构成,故D正确.
故选:C.
【点评】了解物质的组成和物质的构成;了解在化学变化中,原子不能再分.
3.下列符号中,既能表示氢元素,又能表示氢原子的是( )
A.2H B.2H+ C.2H2 D.H
【考点】化学符号及其周围数字的意义.
【专题】课本知识同类信息.
【分析】元素符号表示一种元素,还表示这种元素的一个原子.分为宏观和微观两个意义:
(1)宏观意义:①表示一种(元素种类)元素.②表示物质.(固体的金属、非金属、稀有气体的单质.)
(2)微观意义:表示这种元素的(一种同位素)一个原子.元素符号前加系数时,只表示原子个数.
【解答】解:A、表示两个氢原子,不能表示氢元素,故错误;
B、表示两个氢离子,不符合题意,故错误;
C、表示两个氢分子,不能表示氢元素、氢原子,故错误;
D、元素符号H可表示:①氢元素,②一个氢原子;故正确;
故选D.
【点评】了解元素的符号和意义,知道其有宏观意义和微观意义,是解答本题的关键.
4.《物质构成的奥秘》告诉我们:元素的种类、化学性质分别与下列粒子数密切相关的是( )
A.质子数、中子数 B.质子数、最外层电子数
C.中子数、最外层电子数 D.最外层电子数、质子数
【考点】元素的概念;核外电子在化学反应中的作用.
【专题】课本知识同类信息.
【分析】根据不同种元素最本质的区别是质子数不同,元素的化学性质由最外层电子数决定,进行分析解答本题.
【解答】解:不同种元素最本质的区别是质子数不同,元素的种类由质子数决定,元素的化学性质由最外层电子数决定,原子的质量主要集中在原子核上,
故选:B.
【点评】本题考查学生根据不同种元素最本质的区别是质子数不同,元素的化学性质由最外层电子数决定解题的能力.
5.“乐百氏”矿泉水标签上印有水质 ( http: / / www.21cnjy.com )成分如下(mg/L):硒:0.013;锶:0.0596;锌:0.00162;钠:18.4;钙:4.69.这里的硒、锶、锌、钠、钙是指( )
A.元素 B.原子 C.单质 D.分子
【考点】元素的概念.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据已有的知识进行分析解答,物质是由元素组成的.
【解答】解:物质是由元素组成的,这里的硒、锶、锌、钠、钙是指元素,观察选项,故选A.
【点评】本题考查了物质组成的知识,完成此题,可以依据已有的知识进行.
6.以下对O2、CO2、SO2、MnO2四种物质组成的说法中,正确的是( )
A.都含有氧分子 B.都含有2个氧原子
C.都含有氧元素 D.都是氧化物
【考点】分子、原子、离子、元素与物质之间的关系;从组成上识别氧化物.
【专题】物质的微观构成与物质的宏观组成.
【分析】A、氧气是由氧分子构成的,含有氧分子的物质为氧气或空气,化合物中都不含氧分子.
B、根据O2、CO2、SO2、MnO2四种物质的组成进行分析判断.
C、根据O2、CO2、SO2、MnO2四种物质元素组成进行分析判断.
D、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
【解答】解:A、氧气是由氧分子构成的,CO2、SO2、MnO2分别是由二氧化碳分子、二氧化硫分子、二氧化锰分子构成的,故选项说法错误.
B、由O2、CO2、SO2、MnO ( http: / / www.21cnjy.com )2四种物质的化学式可知,它们的一个分子中均含有2个氧原子,而不是四种物质中都含有2个氧原子,故选项说法错误.
C、由O2、CO2、SO2、MnO2四种物质的化学式可知,四种物质中均含有氧元素,故选项说法正确.
D、O2是由一种元素组成的纯净物,属于单质,故选项错误.
故选:C.
【点评】本题难度不大,主要考查了构成物质的宏观组成与微观粒子方面的知识,掌握常见物质的粒子宏观组成与微观构成是正确解答本题的关键.
7.葡萄糖(C6H12O6)是一种重要营养物质,下列关于葡萄糖的说法,正确的是( )
A.葡萄糖由6种碳元素、12种氢元素和6种氧元素组成
B.葡萄糖由6个碳原子、12个氢原子和6个氧原子构成
C.每个葡萄糖分子中所含原子个数为24
D.每个葡萄糖分子中碳、氢、氧原子个数比为6:1:8
【考点】化学式的书写及意义.
【分析】化学式的意义有:①表示一种物质,②表 ( http: / / www.21cnjy.com )示该物质的元素组成,③表示该物质的一个分子,④表示该分子的原子构成,⑤该物质中各元素的质量比,⑥该物质中各元素的原子个数比,⑦该物质的相对分子质量等.
【解答】解:A、元素只讲种类,不讲个数,因此A选项错误;
B、未指明在1个葡萄糖分子中,因此B选项错误;
D、葡萄糖分子中碳、氢、氧的原子个数比为1:2:1,不是6:1:8,因此D选项错误.
只有C选项是正确的.
故选C.
【点评】本题主要考查化学式的意义,难度稍大.
8.已知某物质的化学式为RNO3,相对分子质量是85,则R元素的相对原子质量是( )
A.55 B.55g C.23 D.23g
【考点】有关化学式的计算和推断;相对分子质量的概念及其计算.
【专题】化学式的计算.
【分析】该题考察的是利用相 ( http: / / www.21cnjy.com )对分子质量的基本计算公式,来求未知元素的相对原子质量.虽然该题很简单但却要学生掌握相对分子质量的基本计算公式,且还要求学生会数学基本运算.
【解答】解:设R的相对原子质量为X
则:X+14+16×3=85
X=23
故选C.
【点评】在简单的题目中提高了学生的基本计算能力,也加强了学生们对相对分子质量的理解.
9.按氯元素化合价由低至高的排列顺序,在HCl、X、HClO、KClO3中,X代表的是( )
A.NaCl B.KClO C.Cl2 D.ClO2
【考点】有关元素化合价的计算.
【专题】化学式的计算.
【分析】根据在化合物中正 ( http: / / www.21cnjy.com )负化合价代数和为零,分别计算出HCl、HClO、KClO3中氯元素的化合价,按照低至高的排列顺序,在计算出选项中氯元素的化合价,看哪个选项符号条件,进行分析解答本题.
【解答】解:根据在化合物中正负化合价代数和为零,可知:
HCl中Cl的化合价为:(+1)+a=0,则a=﹣1,
HClO中Cl的化合价为:(+1)+b+(﹣2)=0,则b=+1,
KClO3中Cl的化合价为:(+1)+c+(﹣2)×3=0,则c=+5,
选项中氯元素的化合价为:
NaCl中Cl的化合价为:(+1)+e=0,则e=﹣1;
KClO中Cl的化合价为:(+1)+f+(﹣2)=0,则f=+1;
单质中元素的化合价为零,因此Cl2中Cl的化合价为0;
ClO2中Cl的化合价为:g+(﹣2)×2=0,则g=+4;
在HCl、X、HClO、KClO3中,氯元素化合价由低至高的排列顺序,由计算可知X代表的是Cl2,故选C.
【点评】本题考查学生根据在化合物中正负化合价代数和为零进行分析解题的能力.
10.要使Fe3O4和Fe2O3中所含铁元素质量相等,则Fe3O4与Fe2O3质量比为( )
A.2:3 B.4:5 C.29:30 D.3:2
【考点】化合物中某元素的质量计算.
【专题】化学式的计算.
【分析】利用一定质量的化合物中元素的质 ( http: / / www.21cnjy.com )量为化合物的质量与化合物中质量分数的乘积,根据两物质的化学式,可通过两物质中铁元素质量相等建立等式,计算出两物质的质量比.
【解答】解:假设Fe3O4与Fe2O3的质量分别为x、y,则
x××100%=y××100%
x:y=29:30.
故选C.
或者
根据Fe3O4和Fe2O3中铁元素质量相等,所以对应铁原子也相等,即Fe3O4和Fe2O3的分子个数比为2:3,也就是两者存在2Fe3O4和3Fe2O3的比例关系.则两物质的质量比为==
即选C
【点评】利用化合物中组成元素的质量分数 ( http: / / www.21cnjy.com ),可由一定质量的化合物计算该化合物中所含元素的质量;利用两物质中共同元素的质量关系,可计算两化合物的质量关系.
11.H2O与H2O2的化学性质不同的原因是( )
A.它们的元素组成不同 B.它们在常温下状态不同
C.它们的分子构成不同 D.H2O2有氧气而H2O中没有
【考点】分子的定义与分子的特性.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据分子的定义及特性回答:分子是保持物质化学性质的一种微粒,同种分子性质相同,不同种分子性质不同.
【解答】解:A、H2O与H2O2的组成元素相同,都是由氢、氧两元素组成的.说法错误.
B、H2O与H2O2的状态在常温下都是液态,说法错误.
C、H2O与H2O2的分子构成不同 ( http: / / www.21cnjy.com ),一个水分子是由两个氢原子和一个氧原子构成,一个双氧水分子是由两个氢原子和两个氧原子构成,不同种分子性质不同.
D、H2O2和H2O中都没有氧气,双氧水中有双氧水分子,水中含有水分子,故说法错误.
故选C
【点评】记住分子的定义及特性,分子不同,化学性质不同.
12.元素X的原子最外层有3个电子,元素Y的原子最外层有6个电子,则这两种元素组成的化合物的化学式可能是( )
A.XY3 B.X2Y C.X2Y3 D.X3Y2
【考点】化学式的书写及意义.
【专题】化学用语和质量守恒定律.
【分析】根据化合价表示原子之间互相化合的 ( http: / / www.21cnjy.com )数目和元素最外层电子数进行分析解答本题;化合价的数值等于离子所带电荷的数值,且符号一致,利用最外层电子数推断元素的化合价,再根据元素化合价判断它们形成化合物的化学式.
【解答】解:元素X的原子最外层有3个 ( http: / / www.21cnjy.com )电子,在化学反应中容易失去3个电子,从而带上3个单位的正电荷,故X元素的化合价为+3价;元素Y的原子最外层有6个电子,在化学反应中容易得到2个电子,从而带上2个单位的负电荷,故Y元素的化合价为﹣2价;根据化合物中正负化合价的代数和为0,它们形成化合物的化学式为X2Y3.
故选:C.
【点评】本题难度不是很大,考查学生根据化合价表示原子之间互相化合的数目、利用化合价原则来书写化学式等进行解题的能力.
13.质子数相同的两种不同粒子可能是① ( http: / / www.21cnjy.com )同一元素的原子或离子②两个不同的分子③一种原子和一种分子④两种不同的离子⑤一种离子和一种分子( )
A.①③ B.①②③④ C.①③④⑤ D.①②③④⑤
【考点】分子、原子、离子、元素与物质之间的关系;原子的定义与构成;原子结构示意图与离子结构示意图.
【专题】物质的微观构成与物质的宏观组成.
【分析】构成物质的粒子包括分子、原子和离子,质子数相同的粒子可能是同种元素的原子和离子;也可能的分子和原子,分子和离子等.
【解答】解:
①同一元素的原子或离子,如钠离子和钠原子都是11个质子;故说法正确;
②两个不同的分子,如水分子和氨分子,都是10个质子;正确;
③一种原子和一种分子,如氖原子和水分子,都是10个质子,正确;
④两种不同的离子,如铁离子和亚铁离子,都是26个质子,正确;
⑤一种离子和一种分子,如磷离子和一氧化氮分子,都是15个质子,正确.
故选D
【点评】质子数相同的原子属于同一种元素,不同的粒子的质子数可能相同,但不一定是同种元素.
14.X2+的离子核外有28有电子,其相对原子质量为65,X原子核内中子数与质子数之差为( )
A.9 B.5 C.2 D.0
【考点】原子的有关数量计算;原子的定义与构成.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据X2+的离子核外有 ( http: / / www.21cnjy.com )28有电子,可求得其核外电子数,因为质子数等于核外电子数,所以可知质子数,再根据相对原子质量等于质子数加中子数,可对所求进行分析探讨.
【解答】解:因为X2+的离子核外有28 ( http: / / www.21cnjy.com )有电子,所以原子有30个电子,则核内质子数是30个,所以中子数是65﹣30=35,所以中子数与质子数之差是35﹣30=5.
故选B
【点评】相对原子质量、质子数(或核电荷数或 ( http: / / www.21cnjy.com )电子数)、中子数三者中,若知其中两项,便可求第三项.中子数的求法通常是用相对原子质量减去质子数来计算的.
15.元素的原子最外层电子得到或失去后,一定不会改变的是( )
①元素种类②化学性质③相对原子质量④微粒电性⑤原子核⑥电子层数⑦最外层电子数⑧核外电子总数.
A.②③⑤ B.②④⑥⑧ C.②⑤ D.①③⑤
【考点】原子的定义与构成;核外电子在化学反应中的作用;原子结构示意图与离子结构示意图;元素的简单分类.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据原子失去或得到电 ( http: / / www.21cnjy.com )子后,发生变化的是最外层电子数即核外电子数,电子层数发生了变化,化学性质发生了变化,电性发生了变化,而原子核没有变,决定元素种类的质子数没有变,决定相对原子质量的质子数与中子数没有变,进行解答.
【解答】解:
根据原子失去或得到电子后, ( http: / / www.21cnjy.com )原子核没有变,决定元素种类的质子数没有变,决定相对原子质量的质子数与中子数没有变,因此元素的原子最外层电子得到或失去后,一定不会改变的是①元素种类,③相对原子质量,⑤原子核;
故选D.
【点评】本题考查学生对原子的得失电子后“变与不变”性质的理解与掌握,并能在解题中灵活应用.
二、填空题(每空1分,共40分.)
16.标出下列划线元素的化合价
KClO3Cl2SO42﹣NH4NO3.
【考点】有关元素化合价的计算.
【专题】化学式的计算.
【分析】根据单质中元素的化合价为0、在 ( http: / / www.21cnjy.com )化合物中正负化合价代数和为零、原子团中元素的化合价代数和等于原子团的化合价,结合各化学式进行解答本题.
【解答】解:钾元素显+1价,氧元素显﹣2 ( http: / / www.21cnjy.com )价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)×3=0,解得x=+5;
根据单质中元素的化合价为零,Cl2属于单质,故氯元素的化合价为0;
硫酸根离子带两个单位的负电荷,硫酸根显﹣2价 ( http: / / www.21cnjy.com ),氧元素显﹣2价,设硫酸根中硫元素的化合价是y,由原子团中元素的化合价代数和等于原子团的化合价,可得:y+(﹣2)×4=﹣2,则y=+6价.
铵根显+1价,氢元素显+1价,设铵根 ( http: / / www.21cnjy.com )中氮元素的化合价是z,由原子团中元素的化合价代数和等于原子团的化合价,可得:z+(+1)×4=+1,则z=﹣3价.
硝酸根显﹣1价,氧元素显﹣2价,设硝酸 ( http: / / www.21cnjy.com )根中氮元素的化合价是m,由原子团中元素的化合价代数和等于原子团的化合价,可得:m+(﹣2)×3=﹣1,则m=+5价.
故答案为:;;;;.
【点评】本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.
17.用化学符号表示
①硫离子S2﹣
②2个氧分子2O2
③+2价的锌元素
④4个亚铁离子4Fe2+
⑤2个碳酸根离子2CO32﹣
⑥氧化铁中铁元素的化合价为+3价2O3
⑦2SO2前“2”的意义2个二氧化硫分子;后“2”的意义每个二氧化硫分子中含有2个氧原子
⑧氯离子的结构示意图.
【考点】化学符号及其周围数字的意义;原子结构示意图与离子结构示意图.
【专题】结合课本知识的信息;化学用语和质量守恒定律.
【分析】利用元素符号和相应的数字可以书写各种微观粒子.
【解答】解:①硫离子可以表示为S2﹣:
②2个氧分子可以表示为2O2:
③+2价的锌元素可以表示为:
④4个亚铁离子可以表示为4Fe2+:
⑤2个碳酸根离子可以表示为2CO32﹣:
⑥氧化铁中铁元素的化合价为+3价,可以表示为2O3:
⑦2SO2前“2”的意义是2个二氧化硫分子;后“2”的意义是每个二氧化硫分子中含有2个氧原子;
⑧氯离子的结构示意图可以表示为:.
故填:S2﹣:2O2::4Fe2+:2CO32﹣:2O3:2个二氧化硫分子;每个二氧化硫分子中含有2个氧原子;.
【点评】本题主要考查书写化学符号的能力,书写时要注意规范性和准确性.
18.根据名称写出下列物质的化学式
氧化钠Na2O氯化钡BaCl2硫酸铝Al2(SO4)3
氢氧化钙Ca(OH)2碳酸钠Na2CO3硝酸铵NH4NO3.
【考点】化学式的书写及意义.
【专题】化学用语和质量守恒定律.
【分析】根据单质和化合物(先读后写,后读 ( http: / / www.21cnjy.com )先写;金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)化学式的书写方法进行分析判断即可.
【解答】解:氧化钠中,钠元素的化合价是+1,氧元素的化合价是﹣2,化学式是Na2O.故填:Na2O.
氯化钡中,钡元素的化合价是+2,氯元素的化合价是﹣1,化学式是BaCl2.故填:BaCl2.
硫酸铝中,铝元素的化合价是+3,硫酸根的化合价是﹣2,化学式是Al2(SO4)3.故填:Al2(SO4)3.
氢氧化钙中钙元素显+2价,氢氧根显﹣1价,其化学式为Ca(OH)2.故填:Ca(OH)2;
碳酸钠中,钠元素的化合价是+1,碳酸根的化合价是﹣2,化学式是Na2CO3.故填:Na2CO3.
硝酸铵中,铵根离子(NH4)的化合价是+1,硝酸根(NO3)的化合价是﹣1,化学式是NH4NO3.故填:NH4NO3.
【点评】本题难度不大,考查化合物化学式的书写方法,掌握化合物化学式的书写方法是正确解答此类题的关键.
19.N2、Cl2、H2、HCl、 ( http: / / www.21cnjy.com )CH4各一个分子,按质量由小到大的排列顺序是Cl2、HCl、N2、CH4、H2;若取等质量的上述各气体,则分子数目由少到多的排列顺序是H2、CH4、N2、HCl、Cl2.
【考点】相对分子质量的概念及其计算.
【专题】化学式的计算;化学用语和质量守恒定律;有关化学式的计算.
【分析】分子个数相同时,相对分子质量大的其分子质量大;分子质量相等时,相对分子质量大的分子个数少,据此据此分析解答.
【解答】解:H2、CH4、Cl2、N ( http: / / www.21cnjy.com )2各1个分子,相对分子质量大的分子质量大,H2的相对分子质量为:1×2=2,CH4的相对分子质量为:12+1×4=16,Cl2的相对分子质量为:35.5×2=71,N2的相对分子质量为:14×2=28;HCl的相对分子质量为:35.5+1=36.5;
由于71>36.5>28>16>2,其质量由大到小的顺序是:Cl2、HCl、N2、CH4、H2;
取上述气体质量相等时,相对分子质量大的分子个数少,其分子个数由多到少的顺序为:H2、CH4、N2、HCl、Cl2.
故答案为:Cl2、HCl、N2、CH4、H2;H2、CH4、N2、HCl、Cl2.
【点评】本题主要考查学生对分子个数相同 ( http: / / www.21cnjy.com )时分子质量的大小的比较和分子质量相等时分子个数的比较.解题的关键是要知道分子个数相同时,相对分子质量大的分子质量大;分子质量相等时,相对分子质量大的分子个数少.
20.元素周期表是化学学习和研究的重要工具.右图是元素周期表的一部分,根据表中信息回答下列问题.
(1)硫元素的原子序数是16,相对原子质量是32.07;
(2)第15号元素的符号是P;
(3)利用表中元素,写出一种分子构成与微粒模型相似的物质的化学式N2(或 O2或 Cl2).
( http: / / www.21cnjy.com )
【考点】元素周期表的特点及其应用.
【专题】课本知识同类信息;压轴实验题.
【分析】(1)(2)根据元素周期表中所提供的信息进行解答;
(3)根据微粒模型可推断该分子由两个原子组成,从表中选出元素组成相似的物质,写出化学式即可.
【解答】解:(1)从元素周期表可查得硫元素的原子序数是 16,相对原子质量是32.07;故答案为:16; 32.07;
(2)第15号元素为磷,元素符号为:P;故答案为:P;
(3)根据微粒模型可推断该分子由两个原子组成,从表中选出元素组成相似的物质如:N2 (或 O2 或 Cl2);
故答案为:N2 (或 O2 或 Cl2).
【点评】本题考查了元素周期表中看图回答最简单的元素名称、符号、原子序数、相对原子质量,学生必须掌握的知识.
21.图中的①、②是氟元素、钙元素在元素周期表中的信息,A,B,C,D是四种粒子的结构示意图.请你回答:
( http: / / www.21cnjy.com )
(I)氟元素的相对原子质最为19.00,钙元素的原子序数为20;
(2)X=8;
(3)A、B、C、D属于同种元素的粒子是BC (填字母代号).
【考点】元素周期表的特点及其应用;原子结构示意图与离子结构示意图.
【专题】化学用语和质量守恒定律.
【分析】(1)根据图中元素周 ( http: / / www.21cnjy.com )期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析解答即可.
(2)根据原子中核电荷数=核内质子数,进行分析解答.
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答.
【解答】解;(1)根据元素周期表中的一格中获取的信息,可知氟元素的相对原子质量为19.00,钙元素的原子序数为20.
(2)原子中核电荷数=核内质子数,18=2+8+X,X=8.
(3)根据决定元素种类的是核电荷数(即核内质子数),因为B、C的核内质子数相同,所以B、C属于同种元素的粒子.
故答案为:(1)19.00;20;(2)8;(3)BC.
【点评】本题难度不大,灵活运用元素周期表中元素的信息、明确粒子中核内质子数和核外电子数之间的关系、掌握元素的特征等是即可正确决定本题.
22.小刚为了净化收集到的河水,自制了﹣个如图所示的简易净水器
(1)其中小卵石、石英沙和膨松棉的作用是过滤.
(2)活性炭的主要作用是吸附.
(3)小刚在净化后的水中用肥皂洗衣服,发现有很多浮渣,所以他确定该水为硬水.要降低该水的硬度,小刚同学采取的方法是煮沸.
( http: / / www.21cnjy.com )
【考点】水的净化;硬水与软水;碳单质的物理性质及用途.
【专题】物质的性质与用途;物质的分离和提纯;空气与水.
【分析】小卵石、石英沙和膨松棉可以滤去不溶于水的物质;活性炭具有吸附作用,可以吸附水中的色素和异味;加热煮沸可以降低水的硬度.
【解答】解:
(1)小卵石、石英沙和膨松棉的作用是过滤掉水中的固体不溶物.故填:过滤.
(2)活性炭的主要作用是吸附水中的色素和异味.故填:吸附.
(3)加热煮沸可以使水中的钙离子和镁离子以沉淀的形式析出,从而降低水的硬度.故填:煮沸.
【点评】解答本题要掌握活性炭的吸附质,加热煮沸可以把水中的镁离子和钙离子以沉淀的形式析出,从而降低水的硬度.
23.A在常温下是一种无色 ( http: / / www.21cnjy.com )无味的液体,人类生活离不开它.它通过电解生成气体B和气体C,B能使带火星的木条复燃,一种红色粉末D在B中燃烧生成大量的白烟E,并放出大量的热.当B和C点燃时又生成A.试推断它们是什么化学物质(写化学式):
AH2O;BO2;CH2;DP;EP2O5.
并写出B和D反应的化学方程式5O2+4P2P2O5.
【考点】物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
【专题】常见物质的推断题.
【分析】根据A在常温下是一种无色无味的液体 ( http: / / www.21cnjy.com ),推测A为水,它通过电解生成气体B和气体C,B能使带火星的木条复燃,因此B是氧气,C是氢气;一种红色粉末D在B氧气中燃烧生成大量的白烟E,因此D是红磷,E是五氧化二磷,带入验证符合即可.
【解答】解:由题意可知:A在常温下是一种无色无味的液体﹣﹣﹣水,它通过电解生成气体B和气体C,B能使带火星的木条复燃,因此B是氧气,C是氢气,A是水;一种红色粉末D在B﹣氧气中燃烧生成大量的白烟E,因此D是红磷,E是五氧化二磷,因此:A为 H2O;B为 O2;C为 H2;D为 P;E为 P2O5.B和D为磷和氧气的反应,故反应的化学方程式为:5O2+4P2P2O5.
故答案为:H2O;O2; H2; P; P2O5;5O2+4P2P2O5
【点评】本题是对常见物质的推断,难度不大,根据题目中的现象结合物质的性质进行分析得出结论即可.
四、计算题:(共4分)
24.烟草中含有对健康危害(尼古丁),其化学式为C10H14N2,试计算:
(1)尼古丁的相对分子质量;
(2)尼古丁中各元素的质量比;
(3)尼古丁中氮元素的质量分数;
(4)与8.1克尼古丁所含氮元素相等CO(NH2)2的质量是多少?
【考点】相对分子质量的概念及其计算;元素质量比的计算;元素的质量分数计算;化合物中某元素的质量计算.
【专题】化学式的计算.
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=×100%,进行分析解答.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
【解答】解:(1)尼古丁的相对分子质量是12×10+1×14+14×2=162.
(2)尼古丁中碳、氢、氮三种元素的质量比=(12×10):(1×14):(14×2)=60:7:14.
(3)尼古丁中氮元素的质量分数为100%≈17.3%.
(4)设与8.1克尼古丁所含氮元素相等CO(NH2)2的质量是x,
则8.1g×17.3%=x×100%,x=3g.
故答案为:(1)162;(2)60:7:14;(3)17.3%;(4)3g.
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.
一、选择题(本大题15小题,每小题2分,共30分)
1.下列化学式中,书写错误的是( )
A.氧化钙OCa B.氧化镁 MgO
C.三氯化铁 FeCl3 D.三氧化硫SO3
2.关于原子的说法不正确的是( )
A.是构成物质的一种粒子 B.是化学变化中的最小粒子
C.在化学反应中可以再分 D.是由原子核和核外电子构成
3.下列符号中,既能表示氢元素,又能表示氢原子的是( )
A.2H B.2H+ C.2H2 D.H
4.《物质构成的奥秘》告诉我们:元素的种类、化学性质分别与下列粒子数密切相关的是( )
A.质子数、中子数 B.质子数、最外层电子数
C.中子数、最外层电子数 D.最外层电子数、质子数
5.“乐百氏”矿泉水标签上印有水质成分如 ( http: / / www.21cnjy.com )下(mg/L):硒:0.013;锶:0.0596;锌:0.00162;钠:18.4;钙:4.69.这里的硒、锶、锌、钠、钙是指( )
A.元素 B.原子 C.单质 D.分子
6.以下对O2、CO2、SO2、MnO2四种物质组成的说法中,正确的是( )
A.都含有氧分子 B.都含有2个氧原子
C.都含有氧元素 D.都是氧化物
7.葡萄糖(C6H12O6)是一种重要营养物质,下列关于葡萄糖的说法,正确的是( )
A.葡萄糖由6种碳元素、12种氢元素和6种氧元素组成
B.葡萄糖由6个碳原子、12个氢原子和6个氧原子构成
C.每个葡萄糖分子中所含原子个数为24
D.每个葡萄糖分子中碳、氢、氧原子个数比为6:1:8
8.已知某物质的化学式为RNO3,相对分子质量是85,则R元素的相对原子质量是( )
A.55 B.55g C.23 D.23g
9.按氯元素化合价由低至高的排列顺序,在HCl、X、HClO、KClO3中,X代表的是( )
A.NaCl B.KClO C.Cl2 D.ClO2
10.要使Fe3O4和Fe2O3中所含铁元素质量相等,则Fe3O4与Fe2O3质量比为( )
A.2:3 B.4:5 C.29:30 D.3:2
11.H2O与H2O2的化学性质不同的原因是( )
A.它们的元素组成不同 B.它们在常温下状态不同
C.它们的分子构成不同 D.H2O2有氧气而H2O中没有
12.元素X的原子最外层有3个电子,元素Y的原子最外层有6个电子,则这两种元素组成的化合物的化学式可能是( )
A.XY3 B.X2Y C.X2Y3 D.X3Y2
13.质子数相同的两种不同粒子可能是①同一 ( http: / / www.21cnjy.com )元素的原子或离子②两个不同的分子③一种原子和一种分子④两种不同的离子⑤一种离子和一种分子( )
A.①③ B.①②③④ C.①③④⑤ D.①②③④⑤
14.X2+的离子核外有28有电子,其相对原子质量为65,X原子核内中子数与质子数之差为( )
A.9 B.5 C.2 D.0
15.元素的原子最外层电子得到或失去后,一定不会改变的是( )
①元素种类②化学性质③相对原子质量④微粒电性⑤原子核⑥电子层数⑦最外层电子数⑧核外电子总数.
A.②③⑤ B.②④⑥⑧ C.②⑤ D.①③⑤
二、填空题(每空1分,共40分.)
16.标出下列划线元素的化合价
KClO3Cl2SO42﹣NH4NO3.
17.用化学符号表示
①硫离子__________
②2个氧分子__________
③+2价的锌元素__________
④4个亚铁离子__________
⑤2个碳酸根离子__________
⑥氧化铁中铁元素的化合价为+3价__________
⑦2SO2前“2”的意义__________;后“2”的意义__________
⑧氯离子的结构示意图__________.
18.根据名称写出下列物质的化学式
氧化钠__________氯化钡__________硫酸铝__________
氢氧化钙__________碳酸钠__________硝酸铵__________.
19.N2、Cl2、H2、HCl、CH4各 ( http: / / www.21cnjy.com )一个分子,按质量由小到大的排列顺序是__________;若取等质量的上述各气体,则分子数目由少到多的排列顺序是__________.
20.元素周期表是化学学习和研究的重要工具.右图是元素周期表的一部分,根据表中信息回答下列问题.
(1)硫元素的原子序数是__________,相对原子质量是__________;
(2)第15号元素的符号是__________;
(3)利用表中元素,写出一种分子构成与微粒模型相似的物质的化学式__________.
( http: / / www.21cnjy.com )
21.图中的①、②是氟元素、钙元素在元素周期表中的信息,A,B,C,D是四种粒子的结构示意图.请你回答:
( http: / / www.21cnjy.com )
(I)氟元素的相对原子质最为__________,钙元素的原子序数为__________;
(2)X=__________;
(3)A、B、C、D属于同种元素的粒子是__________ (填字母代号).
22.小刚为了净化收集到的河水,自制了﹣个如图所示的简易净水器
(1)其中小卵石、石英沙和膨松棉的作用是__________.
(2)活性炭的主要作用是__________.
(3)小刚在净化后的水中用肥皂洗衣服,发现有很多浮渣,所以他确定该水为硬水.要降低该水的硬度,小刚同学采取的方法是__________.
( http: / / www.21cnjy.com )
23.A在常温下是一种无色 ( http: / / www.21cnjy.com )无味的液体,人类生活离不开它.它通过电解生成气体B和气体C,B能使带火星的木条复燃,一种红色粉末D在B中燃烧生成大量的白烟E,并放出大量的热.当B和C点燃时又生成A.试推断它们是什么化学物质(写化学式):
A__________;B__________;C__________;D__________;E__________.
并写出B和D反应的化学方程式__________.
四、计算题:(共4分)
24.烟草中含有对健康危害(尼古丁),其化学式为C10H14N2,试计算:
(1)尼古丁的相对分子质量;
(2)尼古丁中各元素的质量比;
(3)尼古丁中氮元素的质量分数;
(4)与8.1克尼古丁所含氮元素相等CO(NH2)2的质量是多少?
沪教版九年级全册《第4章 燃烧 燃料》2015年单元检测卷(江苏省盐城市射阳县特庸中学)
一、选择题(本大题15小题,每小题2分,共30分)
1.下列化学式中,书写错误的是( )
A.氧化钙OCa B.氧化镁 MgO
C.三氯化铁 FeCl3 D.三氧化硫SO3
【考点】化学式的书写及意义.
【专题】化学用语和质量守恒定律.
【分析】化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.
【解答】解:A、氧化钙的化学式为;CaO,故选项书写错误.
B、氧化镁中镁元素显+2价,氧元素显﹣2价,其化学式为MgO,故选项书写正确.
C、三氯化铁中铁元素显+3价,氯元素显﹣1价,其化学式为FeCl3,故选项书写正确.
D、三氧化硫的化学式为SO3,故选项书写正确.
故选A.
【点评】本题难度不大,掌握化合物化学式 ( http: / / www.21cnjy.com )的书写一般规律(金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)是正确解答此类题的关键.
2.关于原子的说法不正确的是( )
A.是构成物质的一种粒子 B.是化学变化中的最小粒子
C.在化学反应中可以再分 D.是由原子核和核外电子构成
【考点】原子的定义与构成.
【专题】物质的微观构成与物质的宏观组成.
【分析】A、原子是构成物质的一种粒子;
B、原子是化学变化中的最小粒子;
C、在化学变化中,原子不能再分;
D、原子由原子核和核外电子构成.
【解答】解:A、原子是构成物质的一种粒子,故A正确;
B、原子是化学变化中的最小粒子,故B正确;
C、在化学变化中,原子不能再分,故C错误;
D、原子由原子核和核外电子构成,故D正确.
故选:C.
【点评】了解物质的组成和物质的构成;了解在化学变化中,原子不能再分.
3.下列符号中,既能表示氢元素,又能表示氢原子的是( )
A.2H B.2H+ C.2H2 D.H
【考点】化学符号及其周围数字的意义.
【专题】课本知识同类信息.
【分析】元素符号表示一种元素,还表示这种元素的一个原子.分为宏观和微观两个意义:
(1)宏观意义:①表示一种(元素种类)元素.②表示物质.(固体的金属、非金属、稀有气体的单质.)
(2)微观意义:表示这种元素的(一种同位素)一个原子.元素符号前加系数时,只表示原子个数.
【解答】解:A、表示两个氢原子,不能表示氢元素,故错误;
B、表示两个氢离子,不符合题意,故错误;
C、表示两个氢分子,不能表示氢元素、氢原子,故错误;
D、元素符号H可表示:①氢元素,②一个氢原子;故正确;
故选D.
【点评】了解元素的符号和意义,知道其有宏观意义和微观意义,是解答本题的关键.
4.《物质构成的奥秘》告诉我们:元素的种类、化学性质分别与下列粒子数密切相关的是( )
A.质子数、中子数 B.质子数、最外层电子数
C.中子数、最外层电子数 D.最外层电子数、质子数
【考点】元素的概念;核外电子在化学反应中的作用.
【专题】课本知识同类信息.
【分析】根据不同种元素最本质的区别是质子数不同,元素的化学性质由最外层电子数决定,进行分析解答本题.
【解答】解:不同种元素最本质的区别是质子数不同,元素的种类由质子数决定,元素的化学性质由最外层电子数决定,原子的质量主要集中在原子核上,
故选:B.
【点评】本题考查学生根据不同种元素最本质的区别是质子数不同,元素的化学性质由最外层电子数决定解题的能力.
5.“乐百氏”矿泉水标签上印有水质 ( http: / / www.21cnjy.com )成分如下(mg/L):硒:0.013;锶:0.0596;锌:0.00162;钠:18.4;钙:4.69.这里的硒、锶、锌、钠、钙是指( )
A.元素 B.原子 C.单质 D.分子
【考点】元素的概念.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据已有的知识进行分析解答,物质是由元素组成的.
【解答】解:物质是由元素组成的,这里的硒、锶、锌、钠、钙是指元素,观察选项,故选A.
【点评】本题考查了物质组成的知识,完成此题,可以依据已有的知识进行.
6.以下对O2、CO2、SO2、MnO2四种物质组成的说法中,正确的是( )
A.都含有氧分子 B.都含有2个氧原子
C.都含有氧元素 D.都是氧化物
【考点】分子、原子、离子、元素与物质之间的关系;从组成上识别氧化物.
【专题】物质的微观构成与物质的宏观组成.
【分析】A、氧气是由氧分子构成的,含有氧分子的物质为氧气或空气,化合物中都不含氧分子.
B、根据O2、CO2、SO2、MnO2四种物质的组成进行分析判断.
C、根据O2、CO2、SO2、MnO2四种物质元素组成进行分析判断.
D、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
【解答】解:A、氧气是由氧分子构成的,CO2、SO2、MnO2分别是由二氧化碳分子、二氧化硫分子、二氧化锰分子构成的,故选项说法错误.
B、由O2、CO2、SO2、MnO ( http: / / www.21cnjy.com )2四种物质的化学式可知,它们的一个分子中均含有2个氧原子,而不是四种物质中都含有2个氧原子,故选项说法错误.
C、由O2、CO2、SO2、MnO2四种物质的化学式可知,四种物质中均含有氧元素,故选项说法正确.
D、O2是由一种元素组成的纯净物,属于单质,故选项错误.
故选:C.
【点评】本题难度不大,主要考查了构成物质的宏观组成与微观粒子方面的知识,掌握常见物质的粒子宏观组成与微观构成是正确解答本题的关键.
7.葡萄糖(C6H12O6)是一种重要营养物质,下列关于葡萄糖的说法,正确的是( )
A.葡萄糖由6种碳元素、12种氢元素和6种氧元素组成
B.葡萄糖由6个碳原子、12个氢原子和6个氧原子构成
C.每个葡萄糖分子中所含原子个数为24
D.每个葡萄糖分子中碳、氢、氧原子个数比为6:1:8
【考点】化学式的书写及意义.
【分析】化学式的意义有:①表示一种物质,②表 ( http: / / www.21cnjy.com )示该物质的元素组成,③表示该物质的一个分子,④表示该分子的原子构成,⑤该物质中各元素的质量比,⑥该物质中各元素的原子个数比,⑦该物质的相对分子质量等.
【解答】解:A、元素只讲种类,不讲个数,因此A选项错误;
B、未指明在1个葡萄糖分子中,因此B选项错误;
D、葡萄糖分子中碳、氢、氧的原子个数比为1:2:1,不是6:1:8,因此D选项错误.
只有C选项是正确的.
故选C.
【点评】本题主要考查化学式的意义,难度稍大.
8.已知某物质的化学式为RNO3,相对分子质量是85,则R元素的相对原子质量是( )
A.55 B.55g C.23 D.23g
【考点】有关化学式的计算和推断;相对分子质量的概念及其计算.
【专题】化学式的计算.
【分析】该题考察的是利用相 ( http: / / www.21cnjy.com )对分子质量的基本计算公式,来求未知元素的相对原子质量.虽然该题很简单但却要学生掌握相对分子质量的基本计算公式,且还要求学生会数学基本运算.
【解答】解:设R的相对原子质量为X
则:X+14+16×3=85
X=23
故选C.
【点评】在简单的题目中提高了学生的基本计算能力,也加强了学生们对相对分子质量的理解.
9.按氯元素化合价由低至高的排列顺序,在HCl、X、HClO、KClO3中,X代表的是( )
A.NaCl B.KClO C.Cl2 D.ClO2
【考点】有关元素化合价的计算.
【专题】化学式的计算.
【分析】根据在化合物中正 ( http: / / www.21cnjy.com )负化合价代数和为零,分别计算出HCl、HClO、KClO3中氯元素的化合价,按照低至高的排列顺序,在计算出选项中氯元素的化合价,看哪个选项符号条件,进行分析解答本题.
【解答】解:根据在化合物中正负化合价代数和为零,可知:
HCl中Cl的化合价为:(+1)+a=0,则a=﹣1,
HClO中Cl的化合价为:(+1)+b+(﹣2)=0,则b=+1,
KClO3中Cl的化合价为:(+1)+c+(﹣2)×3=0,则c=+5,
选项中氯元素的化合价为:
NaCl中Cl的化合价为:(+1)+e=0,则e=﹣1;
KClO中Cl的化合价为:(+1)+f+(﹣2)=0,则f=+1;
单质中元素的化合价为零,因此Cl2中Cl的化合价为0;
ClO2中Cl的化合价为:g+(﹣2)×2=0,则g=+4;
在HCl、X、HClO、KClO3中,氯元素化合价由低至高的排列顺序,由计算可知X代表的是Cl2,故选C.
【点评】本题考查学生根据在化合物中正负化合价代数和为零进行分析解题的能力.
10.要使Fe3O4和Fe2O3中所含铁元素质量相等,则Fe3O4与Fe2O3质量比为( )
A.2:3 B.4:5 C.29:30 D.3:2
【考点】化合物中某元素的质量计算.
【专题】化学式的计算.
【分析】利用一定质量的化合物中元素的质 ( http: / / www.21cnjy.com )量为化合物的质量与化合物中质量分数的乘积,根据两物质的化学式,可通过两物质中铁元素质量相等建立等式,计算出两物质的质量比.
【解答】解:假设Fe3O4与Fe2O3的质量分别为x、y,则
x××100%=y××100%
x:y=29:30.
故选C.
或者
根据Fe3O4和Fe2O3中铁元素质量相等,所以对应铁原子也相等,即Fe3O4和Fe2O3的分子个数比为2:3,也就是两者存在2Fe3O4和3Fe2O3的比例关系.则两物质的质量比为==
即选C
【点评】利用化合物中组成元素的质量分数 ( http: / / www.21cnjy.com ),可由一定质量的化合物计算该化合物中所含元素的质量;利用两物质中共同元素的质量关系,可计算两化合物的质量关系.
11.H2O与H2O2的化学性质不同的原因是( )
A.它们的元素组成不同 B.它们在常温下状态不同
C.它们的分子构成不同 D.H2O2有氧气而H2O中没有
【考点】分子的定义与分子的特性.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据分子的定义及特性回答:分子是保持物质化学性质的一种微粒,同种分子性质相同,不同种分子性质不同.
【解答】解:A、H2O与H2O2的组成元素相同,都是由氢、氧两元素组成的.说法错误.
B、H2O与H2O2的状态在常温下都是液态,说法错误.
C、H2O与H2O2的分子构成不同 ( http: / / www.21cnjy.com ),一个水分子是由两个氢原子和一个氧原子构成,一个双氧水分子是由两个氢原子和两个氧原子构成,不同种分子性质不同.
D、H2O2和H2O中都没有氧气,双氧水中有双氧水分子,水中含有水分子,故说法错误.
故选C
【点评】记住分子的定义及特性,分子不同,化学性质不同.
12.元素X的原子最外层有3个电子,元素Y的原子最外层有6个电子,则这两种元素组成的化合物的化学式可能是( )
A.XY3 B.X2Y C.X2Y3 D.X3Y2
【考点】化学式的书写及意义.
【专题】化学用语和质量守恒定律.
【分析】根据化合价表示原子之间互相化合的 ( http: / / www.21cnjy.com )数目和元素最外层电子数进行分析解答本题;化合价的数值等于离子所带电荷的数值,且符号一致,利用最外层电子数推断元素的化合价,再根据元素化合价判断它们形成化合物的化学式.
【解答】解:元素X的原子最外层有3个 ( http: / / www.21cnjy.com )电子,在化学反应中容易失去3个电子,从而带上3个单位的正电荷,故X元素的化合价为+3价;元素Y的原子最外层有6个电子,在化学反应中容易得到2个电子,从而带上2个单位的负电荷,故Y元素的化合价为﹣2价;根据化合物中正负化合价的代数和为0,它们形成化合物的化学式为X2Y3.
故选:C.
【点评】本题难度不是很大,考查学生根据化合价表示原子之间互相化合的数目、利用化合价原则来书写化学式等进行解题的能力.
13.质子数相同的两种不同粒子可能是① ( http: / / www.21cnjy.com )同一元素的原子或离子②两个不同的分子③一种原子和一种分子④两种不同的离子⑤一种离子和一种分子( )
A.①③ B.①②③④ C.①③④⑤ D.①②③④⑤
【考点】分子、原子、离子、元素与物质之间的关系;原子的定义与构成;原子结构示意图与离子结构示意图.
【专题】物质的微观构成与物质的宏观组成.
【分析】构成物质的粒子包括分子、原子和离子,质子数相同的粒子可能是同种元素的原子和离子;也可能的分子和原子,分子和离子等.
【解答】解:
①同一元素的原子或离子,如钠离子和钠原子都是11个质子;故说法正确;
②两个不同的分子,如水分子和氨分子,都是10个质子;正确;
③一种原子和一种分子,如氖原子和水分子,都是10个质子,正确;
④两种不同的离子,如铁离子和亚铁离子,都是26个质子,正确;
⑤一种离子和一种分子,如磷离子和一氧化氮分子,都是15个质子,正确.
故选D
【点评】质子数相同的原子属于同一种元素,不同的粒子的质子数可能相同,但不一定是同种元素.
14.X2+的离子核外有28有电子,其相对原子质量为65,X原子核内中子数与质子数之差为( )
A.9 B.5 C.2 D.0
【考点】原子的有关数量计算;原子的定义与构成.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据X2+的离子核外有 ( http: / / www.21cnjy.com )28有电子,可求得其核外电子数,因为质子数等于核外电子数,所以可知质子数,再根据相对原子质量等于质子数加中子数,可对所求进行分析探讨.
【解答】解:因为X2+的离子核外有28 ( http: / / www.21cnjy.com )有电子,所以原子有30个电子,则核内质子数是30个,所以中子数是65﹣30=35,所以中子数与质子数之差是35﹣30=5.
故选B
【点评】相对原子质量、质子数(或核电荷数或 ( http: / / www.21cnjy.com )电子数)、中子数三者中,若知其中两项,便可求第三项.中子数的求法通常是用相对原子质量减去质子数来计算的.
15.元素的原子最外层电子得到或失去后,一定不会改变的是( )
①元素种类②化学性质③相对原子质量④微粒电性⑤原子核⑥电子层数⑦最外层电子数⑧核外电子总数.
A.②③⑤ B.②④⑥⑧ C.②⑤ D.①③⑤
【考点】原子的定义与构成;核外电子在化学反应中的作用;原子结构示意图与离子结构示意图;元素的简单分类.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据原子失去或得到电 ( http: / / www.21cnjy.com )子后,发生变化的是最外层电子数即核外电子数,电子层数发生了变化,化学性质发生了变化,电性发生了变化,而原子核没有变,决定元素种类的质子数没有变,决定相对原子质量的质子数与中子数没有变,进行解答.
【解答】解:
根据原子失去或得到电子后, ( http: / / www.21cnjy.com )原子核没有变,决定元素种类的质子数没有变,决定相对原子质量的质子数与中子数没有变,因此元素的原子最外层电子得到或失去后,一定不会改变的是①元素种类,③相对原子质量,⑤原子核;
故选D.
【点评】本题考查学生对原子的得失电子后“变与不变”性质的理解与掌握,并能在解题中灵活应用.
二、填空题(每空1分,共40分.)
16.标出下列划线元素的化合价
KClO3Cl2SO42﹣NH4NO3.
【考点】有关元素化合价的计算.
【专题】化学式的计算.
【分析】根据单质中元素的化合价为0、在 ( http: / / www.21cnjy.com )化合物中正负化合价代数和为零、原子团中元素的化合价代数和等于原子团的化合价,结合各化学式进行解答本题.
【解答】解:钾元素显+1价,氧元素显﹣2 ( http: / / www.21cnjy.com )价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)×3=0,解得x=+5;
根据单质中元素的化合价为零,Cl2属于单质,故氯元素的化合价为0;
硫酸根离子带两个单位的负电荷,硫酸根显﹣2价 ( http: / / www.21cnjy.com ),氧元素显﹣2价,设硫酸根中硫元素的化合价是y,由原子团中元素的化合价代数和等于原子团的化合价,可得:y+(﹣2)×4=﹣2,则y=+6价.
铵根显+1价,氢元素显+1价,设铵根 ( http: / / www.21cnjy.com )中氮元素的化合价是z,由原子团中元素的化合价代数和等于原子团的化合价,可得:z+(+1)×4=+1,则z=﹣3价.
硝酸根显﹣1价,氧元素显﹣2价,设硝酸 ( http: / / www.21cnjy.com )根中氮元素的化合价是m,由原子团中元素的化合价代数和等于原子团的化合价,可得:m+(﹣2)×3=﹣1,则m=+5价.
故答案为:;;;;.
【点评】本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.
17.用化学符号表示
①硫离子S2﹣
②2个氧分子2O2
③+2价的锌元素
④4个亚铁离子4Fe2+
⑤2个碳酸根离子2CO32﹣
⑥氧化铁中铁元素的化合价为+3价2O3
⑦2SO2前“2”的意义2个二氧化硫分子;后“2”的意义每个二氧化硫分子中含有2个氧原子
⑧氯离子的结构示意图.
【考点】化学符号及其周围数字的意义;原子结构示意图与离子结构示意图.
【专题】结合课本知识的信息;化学用语和质量守恒定律.
【分析】利用元素符号和相应的数字可以书写各种微观粒子.
【解答】解:①硫离子可以表示为S2﹣:
②2个氧分子可以表示为2O2:
③+2价的锌元素可以表示为:
④4个亚铁离子可以表示为4Fe2+:
⑤2个碳酸根离子可以表示为2CO32﹣:
⑥氧化铁中铁元素的化合价为+3价,可以表示为2O3:
⑦2SO2前“2”的意义是2个二氧化硫分子;后“2”的意义是每个二氧化硫分子中含有2个氧原子;
⑧氯离子的结构示意图可以表示为:.
故填:S2﹣:2O2::4Fe2+:2CO32﹣:2O3:2个二氧化硫分子;每个二氧化硫分子中含有2个氧原子;.
【点评】本题主要考查书写化学符号的能力,书写时要注意规范性和准确性.
18.根据名称写出下列物质的化学式
氧化钠Na2O氯化钡BaCl2硫酸铝Al2(SO4)3
氢氧化钙Ca(OH)2碳酸钠Na2CO3硝酸铵NH4NO3.
【考点】化学式的书写及意义.
【专题】化学用语和质量守恒定律.
【分析】根据单质和化合物(先读后写,后读 ( http: / / www.21cnjy.com )先写;金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)化学式的书写方法进行分析判断即可.
【解答】解:氧化钠中,钠元素的化合价是+1,氧元素的化合价是﹣2,化学式是Na2O.故填:Na2O.
氯化钡中,钡元素的化合价是+2,氯元素的化合价是﹣1,化学式是BaCl2.故填:BaCl2.
硫酸铝中,铝元素的化合价是+3,硫酸根的化合价是﹣2,化学式是Al2(SO4)3.故填:Al2(SO4)3.
氢氧化钙中钙元素显+2价,氢氧根显﹣1价,其化学式为Ca(OH)2.故填:Ca(OH)2;
碳酸钠中,钠元素的化合价是+1,碳酸根的化合价是﹣2,化学式是Na2CO3.故填:Na2CO3.
硝酸铵中,铵根离子(NH4)的化合价是+1,硝酸根(NO3)的化合价是﹣1,化学式是NH4NO3.故填:NH4NO3.
【点评】本题难度不大,考查化合物化学式的书写方法,掌握化合物化学式的书写方法是正确解答此类题的关键.
19.N2、Cl2、H2、HCl、 ( http: / / www.21cnjy.com )CH4各一个分子,按质量由小到大的排列顺序是Cl2、HCl、N2、CH4、H2;若取等质量的上述各气体,则分子数目由少到多的排列顺序是H2、CH4、N2、HCl、Cl2.
【考点】相对分子质量的概念及其计算.
【专题】化学式的计算;化学用语和质量守恒定律;有关化学式的计算.
【分析】分子个数相同时,相对分子质量大的其分子质量大;分子质量相等时,相对分子质量大的分子个数少,据此据此分析解答.
【解答】解:H2、CH4、Cl2、N ( http: / / www.21cnjy.com )2各1个分子,相对分子质量大的分子质量大,H2的相对分子质量为:1×2=2,CH4的相对分子质量为:12+1×4=16,Cl2的相对分子质量为:35.5×2=71,N2的相对分子质量为:14×2=28;HCl的相对分子质量为:35.5+1=36.5;
由于71>36.5>28>16>2,其质量由大到小的顺序是:Cl2、HCl、N2、CH4、H2;
取上述气体质量相等时,相对分子质量大的分子个数少,其分子个数由多到少的顺序为:H2、CH4、N2、HCl、Cl2.
故答案为:Cl2、HCl、N2、CH4、H2;H2、CH4、N2、HCl、Cl2.
【点评】本题主要考查学生对分子个数相同 ( http: / / www.21cnjy.com )时分子质量的大小的比较和分子质量相等时分子个数的比较.解题的关键是要知道分子个数相同时,相对分子质量大的分子质量大;分子质量相等时,相对分子质量大的分子个数少.
20.元素周期表是化学学习和研究的重要工具.右图是元素周期表的一部分,根据表中信息回答下列问题.
(1)硫元素的原子序数是16,相对原子质量是32.07;
(2)第15号元素的符号是P;
(3)利用表中元素,写出一种分子构成与微粒模型相似的物质的化学式N2(或 O2或 Cl2).
( http: / / www.21cnjy.com )
【考点】元素周期表的特点及其应用.
【专题】课本知识同类信息;压轴实验题.
【分析】(1)(2)根据元素周期表中所提供的信息进行解答;
(3)根据微粒模型可推断该分子由两个原子组成,从表中选出元素组成相似的物质,写出化学式即可.
【解答】解:(1)从元素周期表可查得硫元素的原子序数是 16,相对原子质量是32.07;故答案为:16; 32.07;
(2)第15号元素为磷,元素符号为:P;故答案为:P;
(3)根据微粒模型可推断该分子由两个原子组成,从表中选出元素组成相似的物质如:N2 (或 O2 或 Cl2);
故答案为:N2 (或 O2 或 Cl2).
【点评】本题考查了元素周期表中看图回答最简单的元素名称、符号、原子序数、相对原子质量,学生必须掌握的知识.
21.图中的①、②是氟元素、钙元素在元素周期表中的信息,A,B,C,D是四种粒子的结构示意图.请你回答:
( http: / / www.21cnjy.com )
(I)氟元素的相对原子质最为19.00,钙元素的原子序数为20;
(2)X=8;
(3)A、B、C、D属于同种元素的粒子是BC (填字母代号).
【考点】元素周期表的特点及其应用;原子结构示意图与离子结构示意图.
【专题】化学用语和质量守恒定律.
【分析】(1)根据图中元素周 ( http: / / www.21cnjy.com )期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析解答即可.
(2)根据原子中核电荷数=核内质子数,进行分析解答.
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答.
【解答】解;(1)根据元素周期表中的一格中获取的信息,可知氟元素的相对原子质量为19.00,钙元素的原子序数为20.
(2)原子中核电荷数=核内质子数,18=2+8+X,X=8.
(3)根据决定元素种类的是核电荷数(即核内质子数),因为B、C的核内质子数相同,所以B、C属于同种元素的粒子.
故答案为:(1)19.00;20;(2)8;(3)BC.
【点评】本题难度不大,灵活运用元素周期表中元素的信息、明确粒子中核内质子数和核外电子数之间的关系、掌握元素的特征等是即可正确决定本题.
22.小刚为了净化收集到的河水,自制了﹣个如图所示的简易净水器
(1)其中小卵石、石英沙和膨松棉的作用是过滤.
(2)活性炭的主要作用是吸附.
(3)小刚在净化后的水中用肥皂洗衣服,发现有很多浮渣,所以他确定该水为硬水.要降低该水的硬度,小刚同学采取的方法是煮沸.
( http: / / www.21cnjy.com )
【考点】水的净化;硬水与软水;碳单质的物理性质及用途.
【专题】物质的性质与用途;物质的分离和提纯;空气与水.
【分析】小卵石、石英沙和膨松棉可以滤去不溶于水的物质;活性炭具有吸附作用,可以吸附水中的色素和异味;加热煮沸可以降低水的硬度.
【解答】解:
(1)小卵石、石英沙和膨松棉的作用是过滤掉水中的固体不溶物.故填:过滤.
(2)活性炭的主要作用是吸附水中的色素和异味.故填:吸附.
(3)加热煮沸可以使水中的钙离子和镁离子以沉淀的形式析出,从而降低水的硬度.故填:煮沸.
【点评】解答本题要掌握活性炭的吸附质,加热煮沸可以把水中的镁离子和钙离子以沉淀的形式析出,从而降低水的硬度.
23.A在常温下是一种无色 ( http: / / www.21cnjy.com )无味的液体,人类生活离不开它.它通过电解生成气体B和气体C,B能使带火星的木条复燃,一种红色粉末D在B中燃烧生成大量的白烟E,并放出大量的热.当B和C点燃时又生成A.试推断它们是什么化学物质(写化学式):
AH2O;BO2;CH2;DP;EP2O5.
并写出B和D反应的化学方程式5O2+4P2P2O5.
【考点】物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
【专题】常见物质的推断题.
【分析】根据A在常温下是一种无色无味的液体 ( http: / / www.21cnjy.com ),推测A为水,它通过电解生成气体B和气体C,B能使带火星的木条复燃,因此B是氧气,C是氢气;一种红色粉末D在B氧气中燃烧生成大量的白烟E,因此D是红磷,E是五氧化二磷,带入验证符合即可.
【解答】解:由题意可知:A在常温下是一种无色无味的液体﹣﹣﹣水,它通过电解生成气体B和气体C,B能使带火星的木条复燃,因此B是氧气,C是氢气,A是水;一种红色粉末D在B﹣氧气中燃烧生成大量的白烟E,因此D是红磷,E是五氧化二磷,因此:A为 H2O;B为 O2;C为 H2;D为 P;E为 P2O5.B和D为磷和氧气的反应,故反应的化学方程式为:5O2+4P2P2O5.
故答案为:H2O;O2; H2; P; P2O5;5O2+4P2P2O5
【点评】本题是对常见物质的推断,难度不大,根据题目中的现象结合物质的性质进行分析得出结论即可.
四、计算题:(共4分)
24.烟草中含有对健康危害(尼古丁),其化学式为C10H14N2,试计算:
(1)尼古丁的相对分子质量;
(2)尼古丁中各元素的质量比;
(3)尼古丁中氮元素的质量分数;
(4)与8.1克尼古丁所含氮元素相等CO(NH2)2的质量是多少?
【考点】相对分子质量的概念及其计算;元素质量比的计算;元素的质量分数计算;化合物中某元素的质量计算.
【专题】化学式的计算.
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=×100%,进行分析解答.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
【解答】解:(1)尼古丁的相对分子质量是12×10+1×14+14×2=162.
(2)尼古丁中碳、氢、氮三种元素的质量比=(12×10):(1×14):(14×2)=60:7:14.
(3)尼古丁中氮元素的质量分数为100%≈17.3%.
(4)设与8.1克尼古丁所含氮元素相等CO(NH2)2的质量是x,
则8.1g×17.3%=x×100%,x=3g.
故答案为:(1)162;(2)60:7:14;(3)17.3%;(4)3g.
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
