第五章合成高分子同步练习 2024-2025学年高二化学人教版(2019)选择性必修3(含答案)
文档属性
| 名称 | 第五章合成高分子同步练习 2024-2025学年高二化学人教版(2019)选择性必修3(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-13 21:16:38 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
第五章合成高分子
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列关于高分子材料的说法正确的是
A.酚醛树脂()可由苯酚和甲醛通过加聚反应制得
B.聚乙烯由线型结构转变为网状结构()能够增加材料的强度
C.天然橡胶的主要成分聚异戊二烯,其结构简式为
D.涤纶()是由苯甲酸和乙醇通过缩聚反应制得
2.劳动成就梦想,创造美好生活。下列对相关劳动实践项目的原因解释错误的是
选项 劳动实践项目 原因解释
A 环保:宣传使用聚乳酸制造的包装材料 聚乳酸在自然界可生物降解
B 兴趣:新榨果汁提取液可使酸性溶液褪色 果汁中含有还原性物质,能氧化,使其褪色
C 帮厨:帮食堂师傅准备午餐——煎鸡蛋 加热使蛋白质变性
D 探究:用柠檬酸除去水垢 柠檬酸酸性强于碳酸
A.A B.B C.C D.D
3.下列方程式书写正确的是
A.尿素与甲醛制备线型脲醛树脂:
B.水杨酸与过量的碳酸钠溶液反应:++CO2+H2O
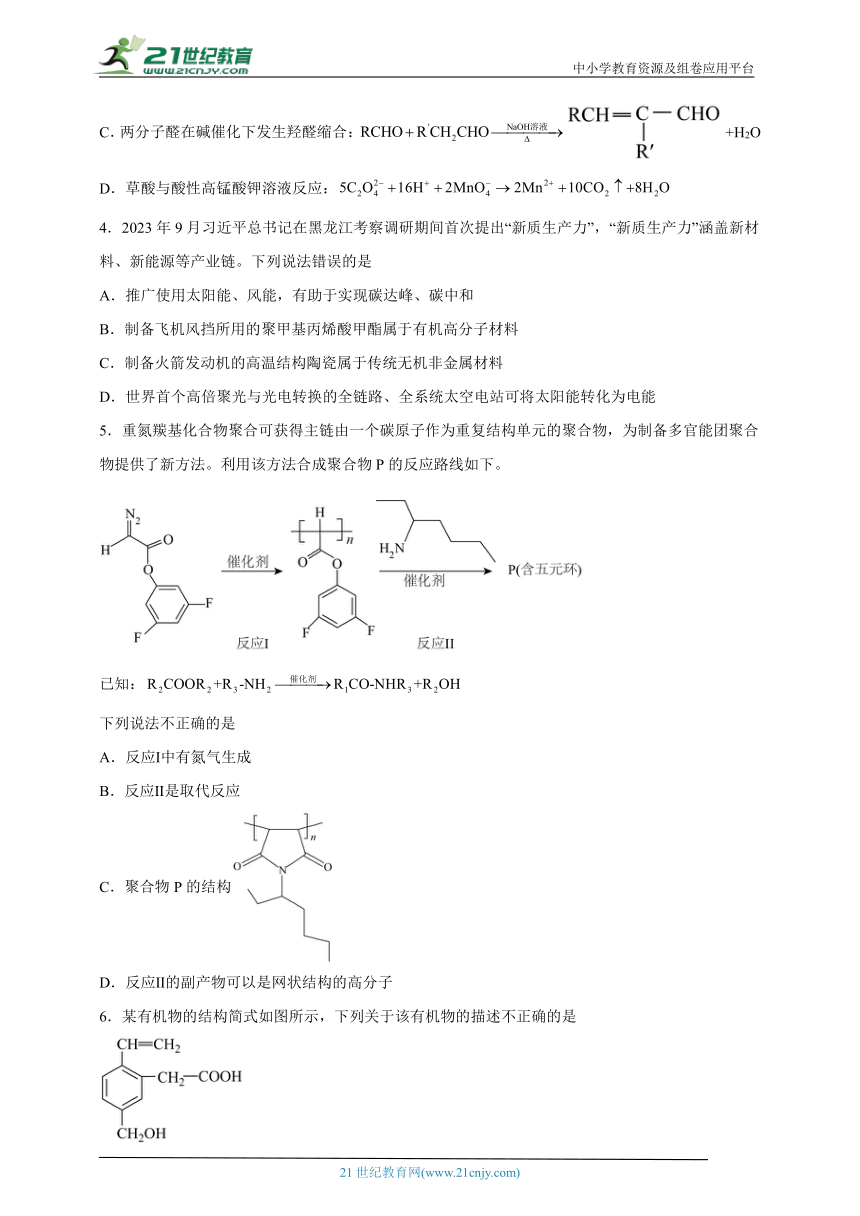
C.两分子醛在碱催化下发生羟醛缩合:+H2O
D.草酸与酸性高锰酸钾溶液反应:
4.2023年9月习近平总书记在黑龙江考察调研期间首次提出“新质生产力”,“新质生产力”涵盖新材料、新能源等产业链。下列说法错误的是
A.推广使用太阳能、风能,有助于实现碳达峰、碳中和
B.制备飞机风挡所用的聚甲基丙烯酸甲酯属于有机高分子材料
C.制备火箭发动机的高温结构陶瓷属于传统无机非金属材料
D.世界首个高倍聚光与光电转换的全链路、全系统太空电站可将太阳能转化为电能
5.重氮羰基化合物聚合可获得主链由一个碳原子作为重复结构单元的聚合物,为制备多官能团聚合物提供了新方法。利用该方法合成聚合物P的反应路线如下。
已知:
下列说法不正确的是
A.反应Ⅰ中有氮气生成
B.反应Ⅱ是取代反应
C.聚合物P的结构
D.反应Ⅱ的副产物可以是网状结构的高分子
6.某有机物的结构简式如图所示,下列关于该有机物的描述不正确的是
A.该有机物中有3种官能团
B.该有机物可以发生加成反应、取代反应、氧化反应
C.该物质可发生加聚反应
D.标准状况下,1mol该物质与足量的钠反应生成11.2L的氢气
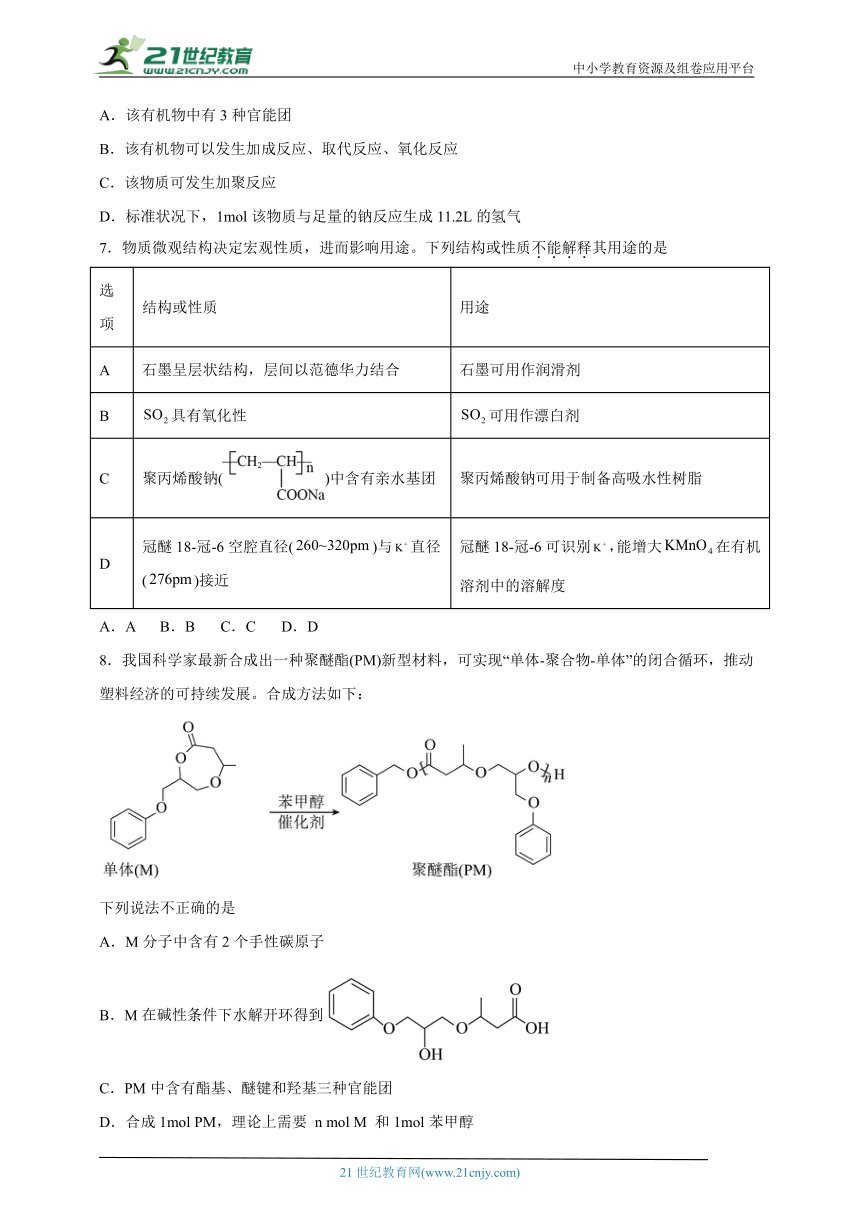
7.物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
选项 结构或性质 用途
A 石墨呈层状结构,层间以范德华力结合 石墨可用作润滑剂
B 具有氧化性 可用作漂白剂
C 聚丙烯酸钠()中含有亲水基团 聚丙烯酸钠可用于制备高吸水性树脂
D 冠醚18-冠-6空腔直径()与直径()接近 冠醚18-冠-6可识别,能增大在有机溶剂中的溶解度
A.A B.B C.C D.D
8.我国科学家最新合成出一种聚醚酯(PM)新型材料,可实现“单体-聚合物-单体”的闭合循环,推动塑料经济的可持续发展。合成方法如下:
下列说法不正确的是
A.M分子中含有2个手性碳原子
B.M在碱性条件下水解开环得到
C.PM中含有酯基、醚键和羟基三种官能团
D.合成1mol PM,理论上需要 n mol M 和1mol苯甲醇
9.下列关于有机化合物的说法正确的是
A.用系统命名法命名有机物:3,3-二甲基-4-乙基戊烷
B.高聚物的单体是
C.可以利用质谱法鉴别二甲醚和乙醇
D.有机物不存在顺反异构现象
10.环氧化物、CO2或环状酸酐在催化剂作用下开环共聚可制备脂肪族聚碳酸酯或聚酯。某聚碳酸酯的结构如下所示:
下列有关说法错误的是
A.该聚合物具有可降解性
B.合成该聚合物的一种单体是
C.合成该聚合物的反应类型为缩聚反应
D.利用上述反应原理,可用环氧乙烷()实现二氧化碳的固定
11.化学与生活、生产密切相关,下列说法正确的是
A.煤炭燃烧过程中添加“固硫”装置,可减少二氧化碳的排放
B.用“人工肾”进行血液透析救治患者,利用了胶体的性质
C.华为手机mate60使用的麒麟9000s芯片,其主要成分是二氧化硅
D.速滑竞赛服使用的聚氨酯材料属于天然有机高分子材料
12.化学与科技、生产、生活等方面密切相关,下列说法不正确的是
A.超导陶瓷在某一临界温度下电阻为零,具有超导性,可应用于磁悬浮技术
B.人民币票面使用含的油墨,验证真伪时利用了的磁性
C.将阿司匹林与高分子连接制成长效缓释药物,可减少用药次数
D.中国制造的乒乓球在巴黎奥运会中大放异彩,其主要成分为新型无机非金属材料
13.二甘醇可用作气体脱水剂、纺织品的润滑剂等。其结构如图所示,下列说法错误的是
A.能发生取代反应 B.分子中含有2种官能团
C.难溶于水 D.能与乙二酸发生缩聚反应
14.化学在社会、生活和科技进步方面发挥着重要的作用。下列说法错误的是
A.制造国产涡扇航空发动机的钛合金属于金属材料
B.桑蚕丝与涤纶都属于化学纤维
C.制造速滑服使用的聚乙烯属于有机高分子材料
D.淀粉在人体内水解可以为人体提供能量
15.控制NiOOH活性位点实现环己醇制备环己酮、己二酸的原理如图所示。下列叙述错误的是
A.环己醇中羟基上的H与NiOOH中的O能形成氢键
B.环己醇断裂H—O健和H—C键形成C=O键
C.环己酮和己二酸在核磁共振氢谱上都有3组峰且峰面积比为1∶2∶2
D.己二酸和己二胺发生加聚反应合成尼龙-66
二、填空题
16.有机高分子
高分子的相对分子质量比一般有机化合物大得多,通常在 以上。合成高分子的基本方法包括 反应和 反应,前者一般是含有 单体发生的聚合反应,后者一般是含有 的单体之间发生的聚合反应。
17.将化石燃料充分利用,并且实现“碳中和”是一项极具挑战的课题。下图①为自然界的碳循环过程,图②为石油化工重要产品乙烯的用途。
(1)图①植物中的纤维素在动物体内彻底水解,最终可得到 (填化学式)。
(2)畜禽养殖及水稻种植是CH4的主要排放源,捕捉CH4进行有效转化是“碳中和”的重要部分。若用硫与CH4在一定条件下生成乙烯,化学方程式为 。
(3)乙烯是重要的化工原料。将乙烯通入溴的CCl4溶液,现象为 ,反应类型为 ,产物名称为 。
(4)图②中聚氯乙烯的链节是 。
(5)环氧乙烷是重要的有机合成中间体。以乙烯为原料,用银作催化剂一步生成环氧乙烷的化学方程式为 。
18.填空
(1)按要求完成下列问题:
①甲基的电子式___________。
②写出制备TNT的化学反应方程式___________。
③反式2一丁烯的结构简式___________
(2)下列括号内的物质为杂质,将除去下列各组混合物中杂质所需的试剂填写在横线上:
①乙酸乙酯(乙醇)________;②甲苯(溴)________;
(3)下列卤代烃既能发生消去反应生成烯烃,又能发生水解反应生成醇的是
(4)实验室用纯溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作进行提纯:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗正确的操作顺序是 。
(5)某高聚物的结构式如图:其单体的名称为
(6)某有机物的结构简式为据此填写下列空格。
①该物质苯环上一氯代物有________种;
②1mol该物质和溴水混合,消耗Br2的物质的量为________mol;
③1mol该物质和H2加成需H2________mol;
(7)与等物质的量的Br2发生加成反应,生成的产物是
19.回答下列问题:
(1)现有下列6种有机物A.苯 B.乙烯 C.乙烷 D.乙醇 E.乙酸 F.油酸。
常温下能与溴水反应的有(填编号) 。
(2)下列各组物质:
A.金刚石与石墨; B.淀粉与纤维素; C.乙烯与聚乙烯; D.甲烷与戊烷;
E.CH3CH2CH(CH3)2与C(CH3)4 F. H2O与D2O G.葡萄糖与果糖
H.蔗糖与麦芽糖 I.甘氨酸与丙氨酸 J.乙醇与甘油
其中互为同分异构体的是 (填编号)。
(3)A.玻璃钢 B.明矾 C.隔热陶瓷瓦 D.氯丁橡胶
E.在合成树脂中加入碳纤维的材料 F.合成纤维
其中属于复合材料的是 (填编号)。
20.书写下列有机反应的方程式。
(1)与酯化成环 ;
(2)在氢氧化钠的乙醇溶液中加热 ;
(3)发生加聚反应 ;
(4)和缩聚 ;
(5)苯酚和乙醛的缩聚 ;
(6)与足量氢氧化钠溶液 。
21.按要求完成以下内容。
(1)肉桂醛是重要的医药原料,也是重要的香料,其结构简式如图一所示,以肉桂醛为原料合成的肉桂醛二乙缩醛的结构如图二所示:
肉桂醛是否存在顺反结构 (填写“是”或“否”),肉桂醛二乙缩醛的分子式为 。
(2)物质M结构如图, 具有的官能团除碳卤键外还有 (填名称)。
(3)正丙醇催化氧化的化学方程式为 。
(4)某高分子化合物的部分结构如图所示,合成此高聚物单体除CH2=CH-CH=CH2外,还有 、 。
(5)某烃A经红外光谱分析,含有-CH3、-CH2-和-CH-三种基团,质谱分析得出最大质荷比为86。则烃A的分子式为 ,符合题意的结构有 种。若烃A的核磁共振氢谱中吸收峰面积之比为6∶4∶3∶1,则烃A的系统名称为 ,它的一氯代物有 种。
22.完成下列填空:
I.下列 7 组物质或粒子:①淀粉和纤维素 ②16O 和18O ③氰酸铵(NH4CNO)与尿素[CO(NH2)2] ④C60和金刚石 ⑤CH3CH2CH3 和(CH3)2CHCH3 ⑥和⑦和
(1)互为同素异形体的是 (填编号,下同);
(2)互为同位素的是 ;
(3)互为同系物的是 ;
(4)互为同分异构体的是 。
II. 用系统命名法给下列有机物命名:
(1)
(2)(CH3)3COH
III.根据题目要求写出相应的化学方程式或结构简式。
(1)对苯二甲酸与乙二醇反应生成聚酯的方程式
(2)2-甲基-2-氯丙烷水解反应方程式
(3)某高聚物的结构简式如下:
则形成该高分子化合物的单体的结构简式分别为
23.工程塑料ABS树脂(结构简式如下),合成时用了三种单体(已知单体A中含有氰根,单体 S中含有苯环)
(1)书写三种单体的结构简式:A B S
(2)A、B和S三种单体,碳氢比(C:H)值最小的单体是 。
(3)经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比是 (用a、b、c表示)。
24.回答下列问题。
(1)将物质进行分类:①和②乙醇与二甲醚③D2O与H2O④和⑤和,用序号回答下列问题:
A互为同分异构体的是 ;B属于同一种化合物的是 ;C互为同系物的是 。
(2)分子中含有22个共价键的链状烷烃有多种同分异构体,写出其中含有三个甲基且等效氢有3种的结构简式:
(3)有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似。写出乙硅烷在空气中自燃的化学方程式: 。
(4)若、C2H4、C2H2、C6H6四种烃各为1g,在足量中燃烧,消耗最多的是: 。
(5)写出CH3—CH=CH—CH3发生加聚反应的化学方程式: 。
25.有机物具有广泛的用途。现有下列有机物:①乙烯 ②1,3-丁二烯 ③甲醛 ④油脂请将相应的序号填入空格内。
(1)能用于制备肥皂的是 ;
(2)能用于制备聚乙烯塑料的是 ;
(3)能用于制备顺丁橡胶的是 ;
(4)能用于制备酚醛树脂的是 ;
(5)为室内主要污染物的有毒的是 。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B B C C C D B B D C
题号 11 12 13 14 15
答案 B D C B D
1.B
【详解】
A.酚醛树脂是苯酚和甲醛通过缩聚反应制得的。方程式如下:n+nHCHO+nH2O,故A错误;
B.线型结构的高分子之间通过分子间作用力结合,强度小,聚乙烯由线型结构转变为网状结构时作用力增强,材料的强度增大,故B正确;
C.聚异戊二烯由异戊二烯()加聚获得,结构简式为,故C错误;
D.从涤纶()聚合物结构简式可以看出涤纶是由对苯二甲酸和乙二醇通过缩聚反应制得,故D错误;
故答案选B。
2.B
【详解】A.聚乳酸含酯基,能水解,聚乳酸在自然界可生物降解,A正确;
B.果汁中的还原性物质被酸性高锰酸钾溶液氧化,B错误;
C.鸡蛋主要成分是蛋白质,帮食堂师傅煎鸡蛋准备午餐,加热使蛋白质变性,C正确;
D.水垢的主要成分有碳酸钙,用白醋清洗水壶中的水垢,醋酸与碳酸钙反应生成二氧化碳,醋酸的酸性比碳酸强,强酸能制弱酸,D正确;
答案选B。
3.C
【详解】
A.尿素和甲醛制备线型脲醛树脂时,两者按物质的量之比为1∶2反应,生成(n-1)个水,化学方程式为+(n-1)H2O,A错误;
B.水杨酸与过量的碳酸钠溶液反应的化学方程式为2+→+,B错误;
C.两分子醛在碱催化下发生羟醛缩合,,然后再转化为RCH=CR -CHO,化学方程式为RCH=CR -CHO+H2O,C正确;
D.草酸与酸性高锰酸钾溶液反应的化学方程式为,D错误;
故答案为:C。
4.C
【详解】A.推广使用太阳能、风能,可以减少化石燃料的燃烧,有助于实现碳达峰、碳中和,A正确;
B.聚甲基丙烯酸甲酯为合成有机高分子材料,B正确;
C.高温结构陶瓷性能优良,属于新型无机非金属材料,C错误;
D.高倍聚光与光电转换的全链路、全系统太空电站可将太阳能转化为电能,实现太阳能与电能的转化,D正确;
故选C。
5.C
【分析】
根据反应①前后两个物质的结构简式,结合质量守恒,可以推出反应①的反应方程式为:n +nN2↑,根据反应②前后两个物质的结构简式,可以推出反应②的反应方程式为:n +n/2→+n,据此作答;
【详解】
A.根据分析,反应①的反应方程式为:n +nN2↑,反应①中有氮气生成,A正确;
B.根据分析,反应②的反应方程式为n +n/2→+n,是取代反应,B正确;
C.聚合物P为,C错误;
D.反应②的副产物也是聚合物,是网状结构的高分子,D正确;
故选C。
6.D
【详解】A.该有机物的官能团有碳碳双键、羟基、羧基3种官能团,A正确;
B.该物质含有碳碳双键,可以发生加成反应,含有羧基、羟基可以发生取代反应,羟基可以发生催化氧化反应,该物质还可以发生燃烧的氧化反应或是被酸性高锰酸钾氧化, B正确;
C.该物质含有碳碳双键,可以发生加聚反应,C正确;
D.含有羟基、羧基,都可以与钠反应生成氢气,则1mol该物质与足量的钠反应可以生成1mol氢气,标准状况下氢气的体积为11.2L ,D不正确;
故选D。
7.B
【详解】A. 石墨呈层状结构,层间以范德华力结合,该作用力较小,层与层容易滑动,石墨可用作润滑剂,A正确;
B. 具有漂白性,可用作漂白剂,B错误;
C. 聚丙烯酸钠()中含有亲水基团-COO-,聚丙烯酸钠可用于制备高吸水性树脂,C正确;
D. 冠醚18-冠-6空腔直径()与直径()接近,可识别,使K+存在于其空腔中,进而能增大在有机溶剂中的溶解度,D正确;
故选B。
8.B
【详解】
A.手性碳原子是指与四个各不相同原子或基团相连的碳原子,M分子中含有2个手性碳原子,位置为,A正确;
B.M中含有酯基,在酸性条件下水解开环得到,碱性条件下水解会生成相应的羧酸盐,B错误;
C.PM中含有酯基、醚键和羟基三种官能团,C正确;
D.由PM的结构简式可知,理论上,合成1mol PM需要消耗n mol M和1mol苯甲醇,D正确;
故选B。
9.D
【详解】
A. 的主链含有6个碳原子,名称为3,3,4-三甲基己烷,故A错误;
B. 高聚物的单体是,故B错误;
C.二甲醚和乙醇互为同分异构体,相对分子质量相等,无法用质谱法鉴别,故C错误;
D. 有机物CH3CH=CH2的碳碳双键一端的碳原子上连接有2个相同的基团,不存在顺反异构现象,故D正确;
故选D。
10.C
【详解】A.该聚合物为聚碳酸酯,酯类可以水解,所以该聚合物具有可降解性,故A正确;
B.环氧化物、CO2或环状酸酐在催化剂作用下开环共聚可制备脂肪族聚碳酸酯或聚酯,所以合成该聚合物的一种单体是环状酸酐,故B正确;
C.该聚合物是环氧化物、CO2、环状酸酐在催化剂作用下开环共聚制备的,所以合成该聚合物的反应类型为加聚反应,故C错误;
D.环氧乙烷()属于环氧化物,由题干可知:环氧化物、CO2或环状酸酐在催化剂作用下开环共聚,即环氧乙烷()可与二氧化碳发生开环加聚反应,实现二氧化碳的固定,故D正确;
故答案为:C。
11.B
【详解】A.煤炭燃烧过程中添加“固硫”装置,不减少二氧化碳的排放,A错误;
B.血液是胶体,而胶体不会通过半透膜,血液透析就是利用了该原理,B正确;
C.芯片主要成分是硅单质,C错误;
D.聚氨酯材料属于人工合成的有机高分子材料,D错误;
故选B。
12.D
【详解】A.超导陶瓷是一种特殊的材料,当温度降低到某一临界温度以下时,其电阻会降为零,表现出超导性。这种特性使得超导陶瓷在电力、交通、医疗等领域具有广泛的应用潜力。特别是在磁悬浮技术中,超导陶瓷的零电阻特性使得电流可以无损耗地流动,从而提高了磁悬浮系统的效率和稳定性,A正确;
B.是一种具有磁性的物质,因此被广泛应用于货币防伪技术中。在人民币的印刷过程中,通过使用含有的油墨,可以在票面上印制特定的磁性编码。这些磁性编码无法通过肉眼直接观察到,但可以通过专门的磁码识读器进行辨识,B正确;
C.缓释指慢慢释放药物,使其在血液中分解并逐渐发挥作用。这种技术可让药物效果长时间持续,从而有效减少服用药物的次数,C正确;
D.2014年7月1日起,新规定开始使用 高分子聚合物为原料的 新塑料球,其主要成分属于有机高分子材料,D错误;
故选D。
13.C
【详解】A.分子中含有羟基,能发生酯化反应,酯化反应是取代反应,故A正确;
B.分子中含有羟基和醚键两种官能团,故B正确;
C.分子中有2个羟基,能与水分子形成分子间氢键,易溶于水,故C错误;
D.分子中有2个羟基,能与乙二酸发生缩聚反应,故D正确;
答案选C。
14.B
【详解】A.合金和纯金属都属于金属材料,钛合金属于金属材料,A正确;
B.桑蚕丝属于蛋白质为天然纤维,B错误;
C.聚乙烯属于有机合成高分子材料,C正确;
D.淀粉在人体内水解生成葡萄糖,可以为人体提供能量,D正确;
答案选B。
15.D
【详解】A. 根据氢键形成的原理可知,环己醇中羟基上的H与NiOOH中的O能形成氢键,A正确;
B. 根据环己醇制备环己酮、己二酸的原理可知,环己醇断裂H—O键和H—C键形成了C=O键,B正确;
C. 根据环己酮、己二酸的结构可知,环己酮和己二酸在核磁共振氢谱上都有3组峰,且峰面积之比均为1:2:2,C正确;
D. 己二酸中的羧基和己二胺中的氨基会发生脱水反应,因此己二酸和己二胺发生了缩聚反应合成尼龙-66,D错误。
答案为:D。
16. 104 加成聚合 缩合聚合 双键的烯类 两个(或两个以上)官能团
【解析】略
17.(1)C6H12O6
(2)2S+2CH4CH2=CH2+2H2S
(3) 橙色褪去 加成反应 1,2-二溴乙烷
(4)
(5)2
【详解】(1)纤维素在动物体内彻底水解,最终可得到葡萄糖,化学式为C6H12O6,故答案为:C6H12O6。
(2)硫与CH4在一定条件下生成乙烯,化学方程式为2S+2CH4CH2=CH2+2H2S,故答案为:2S+2CH4CH2=CH2+2H2S。
(3)乙烯通入溴的CCl4溶液中,橙色褪去,发生加成反应CH2=CH2+Br2→BrCH2CH2Br,生成1,2-二溴乙烷,故答案为:橙色褪去;加成反应;1,2-二溴乙烷。
(4)氯乙烯CH2=CHCl发生加聚反应生成聚氯乙烯,则聚氯乙烯的链节为,故答案为:。
(5)在银的催化作用下,乙烯与氧气反应生成环氧乙烷,其化学方程式为2 ,故答案为: 。
18.(1)①;②;③
(2)①饱和碳酸钠溶液(或水);②NaOH溶液
(3)②④⑥
(4)②④②③①
(5)2-甲基-1,3-戊二烯和乙烯
(6)① 4 ② 2 ③ 5
(7)或
【详解】试题分析:(1)①电子式是把最外层电子用黑点标注在元素符合周围的式子,则甲基的电子式为;
②把浓H2SO4,浓HNO3和甲苯混合加热制备TNT,是苯环上氢原子被硝基取代生成三硝基甲苯,然后依据原子守恒配平化学方程式为;
③含有碳碳双键的烯烃有顺反异构,反式2一丁烯的结构简式为。
(2)①乙酸乙酯难溶于水,而乙醇与水互溶,所以除杂用饱和碳酸钠溶液或水;
②甲苯与NaOH溶液不反应且不溶于水,溴与NaOH溶液反应生成NaBr、NaBrO和水,所以除杂用NaOH溶液。
(3)卤代烃发生消去反应的条件是:①卤代烃含有的碳原子数大于等于2;②与卤素原子相连碳原子的相邻碳上有氢原子。①⑤中与卤素原子相连碳原子上的邻位碳上无氢原子,③中只有一个碳原子,没有邻位碳,②④⑥符合要求,答案选②④⑥。
(4)实验室用纯溴和苯反应制取的溴苯中含有溴、溴苯、HBr和水,先水洗除去溶于水的HBr,然后再用10%NaOH溶液洗除去Br2,再用水洗除去NaOH溶液,用干燥剂干燥除去水,最后蒸馏除去苯,正确的操作顺序是②④②③①。
(5)该高聚物的链接主链上有6个碳,说明是烯烃发生加聚反应生成的,主链碳上含有碳碳双键,截取双键两侧的2个碳原子,得到的单体为CH2=C(CH3)CH=CHCH3和CH2=CH2,对于有机物分子CH2=C(CH3)CH= CHCH3,选取含最多碳原子的链为主碳链,主链上有五个碳原子,从离碳碳双键最近的一端起编号,写出名称为2-甲基-1,3-戊二烯,同理另一种分子叫乙烯。
(6)有机物的结构简式为,含有两个碳碳双键和一个苯环。
①该物质苯环上有4种氢原子,其一氯代物有4种。
②该物质含有两个碳碳双键,则1mol该物质和溴水混合,消耗Br2的物质的量为2mol。
③该物质含有一个苯环和2个碳碳双键,则1mol该物质和H2加成需5mol氢气。
(7)属于共轭二烯烃,与等物质的量的Br2能发生1,2或1,4加成反应,生成的产物是或。
考点:考查电子式的书写,化学方程式的书写,物质的命名方法,消去反应的条件,有机物的提纯等知识。
19.(1)BF
(2)EGH
(3)ACE
【解析】(1)
乙烯和油酸结构中含有碳碳双键,能与溴水发生加成反应,故选BF;
(2)
分子式相同,结构不同的有机物互称同分异构体,其中E的分子式都为C5H12,互为同分异构体;葡萄糖和果糖分子式都为C6H12O6,结构不同,属于同分异构体;蔗糖和麦芽糖的分子式都为C12H22O11,结构不同,属于同分异构体,故选EGH;
(3)
玻璃钢是玻璃纤维与合成材料复合而成的一种特殊材料,属于复合材料,隔热陶瓷瓦是由纤维和陶瓷复合而成的复合材料,在合成树脂中加入碳纤维的材料形成复合材料,故选ACE。
20.(1)++2H2O
(2)+3NaOH+NaCl+3H2O
(3)n
(4)n+nHO-[-OC-CONHCH2CH2N2-]n-H+(2n-1)H2O
(5)n +nCH3CHO +nH2O
(6)+2nNaOH+n+nCH3OH
【详解】(1)
与 发生酯化反应得到,化学方程式为:++2H2O。
(2)
在氢氧化钠的乙醇溶液中加热发生消去和中和反应生成,化学方程式为:+3NaOH+NaCl+3H2O。
(3)
发生加聚反应生成,化学方程式为:n。
(4)
和发生缩聚反应生成HO-[-OC-CONHCH2CH2N2-]n-H,化学方程式为:n+nHO-[-OC-CONHCH2CH2N2-]n-H+(2n-1)H2O。
(5)
苯酚和乙醛的缩聚方程式为:n +nCH3CHO +nH2O。
(6)
与足量氢氧化钠溶液发生水解反应,方程式为:+2nNaOH+n+nCH3OH。
21.(1) 是 C13H18O2
(2)氨基、酮羰基
(3)2CH3CH2CH2OH+O22CH3CH2CHO+2H2O
(4) CH2=CHCN CH2=CH-CH3
(5) C6H14 2 3-甲基戊烷 4
【详解】(1)肉桂醛含碳碳双键,当相同的-H基团在同侧时为顺式结构,在异侧时为反式结构,根据肉桂醛二乙缩醛的分子式为C13H18O2;
(2)物质M结构如图,c具有的官能团除碳卤键外还有氨基、酮羰基;
(3)正丙醇催化氧化生成正丙醛,反应的化学方程式为2CH3CH2CH2OH+O22CH3CH2CHO+2H2O;
(4)主链只有C,应为加聚反应产物,添键断键法可知单体为CH2=CH-CH=CH2外,还有CH2=CHCN、CH2=CH-CH3;
(5)
烃A符合通式CnH2n+2,最大质荷比为86即相对分子质量为86,则12n+2n+2=86,解得n=6,则烃A的分子式为C6H14,含有-CH3、-CH2-和-CH-三种基团,结构有、共2种;核磁共振氢谱中吸收峰面积之比为6∶4∶3∶1,则烃A的系统名称为3-甲基戊烷,有4种氢,它的一氯代物有4种。
22. ④ ② ⑤ ③ 2,4-二甲基-3-乙基-3-己烯 2-甲基-2-丙醇 C(CH3)3Cl+NaOHC(CH3)3OH+NaCl CH2=CH—CH=CH2、 、NCCH=CH2
【详解】I(1)同种元素的不同单质互为同素异形体,C60和金刚石互为同素异形体,故答案为:④;
(2)同一原子的不同核素互为同位素,16O 和18O互为同位素,答案为:②;
(3)结构相似,相差n个—CH2的物质互为同系物,CH3CH2CH3 和(CH3)2CHCH3互为同系物,答案为:⑤;
(4)分子式相同,结构不同的物质互为同分异构体,氰酸铵(NH4CNO)与尿素[CO(NH2)2] 互为同分异构体,答案为:③;
II (1)选支链最多的最长碳链为主链,双键碳距两端等近时,从右边编号离甲基最近,故该物质命名为:2,4-二甲基-3-乙基-3-己烯;
(2)最长碳链是 3 个碳,官能团和取代基位置从哪端编号都一样,命名为:2-甲基-2-丙醇;
III(1)对苯二甲酸与乙二醇反应生成聚酯的方程式为:;
(2)卤代烃在氢氧化钠的水溶液中加热可发生水解反应,故2-甲基-2-氯丙烷水解反应方程式为:C(CH3)3Cl+NaOHC(CH3)3OH+NaCl;
(3) 从虚线处断开,把主链上的碳碳单键变成双键, 碳碳双键变成单键,就得到单体;故形成该高分子化合物的单体的结构简式分别为:CH2=CH—CH=CH2、 、NCCH=CH2。
23.(1) CH2=CHCN
(2)1,3-丁二烯
(3)
【详解】(1)该高聚物的形成过程属于加聚反应,加聚反应是由不饱和单体(如碳碳双键,碳碳三键以及碳氧双键等)聚合高分子的反应,其产物只有一种高分子化合物,凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换,直接合成该高聚物的物质为:CH2=CHCN、、;
(2)A、B和S三种单体,碳氢比(C:H)值分别是、、,所以最小的单体是,即1,3-丁二烯;
(3)若高聚物组成为CaHbNc,而三种单体中只有A的分子中含有一个氮原子,则高聚物中N原子个数必须等于单体A的个数,则根据高聚物CaHbNc可知CH2=CHCN为c个,因A、S中C和H的比值为1:1,碳氢个数的不同则是由单体B造成的,B分子中碳、氢原子的个数之差为2,因而高聚物中碳氢原子个数之差除以2,即是B分子的个数,因此可知A和B的物质的量之比为=。
24.(1) ①② ③⑤ ④
(2)
(3)
(4)
(5)
【详解】(1)①和分子式相同,结构不同,互为同分异构体;②乙醇与二甲醚分子式相同,结构不同,互为同分异构体;③D2O与H2O同种元素组成的相同的物质;④和结构相似,组成上相差1个CH2原子团,互为同系物;⑤和分子式相同,结构相同,属于同种物质;
(2)烷烃通式:,含共价键数目:,分子中含有22个共价键的链状烷烃碳原子个数:,分子式:,含有三个甲基且等效氢有3种说明结构对称,符合要求结构简式:;
(3)类比甲烷,乙硅烷燃烧化学方程式:;
(4)等质量的不同烃分别在氧气中完全燃烧,消耗氧气的量与烃的含碳量有关,烃的含碳量越小,消耗氧气的量越多,则消耗最多的是;
(5)
CH3—CH=CH—CH3发生加聚反应的化学方程式:。
25.(1)④
(2)①
(3)②
(4)③
(5)③
【详解】(1)肥皂的主要成分为高级脂肪酸盐,则油脂在碱性溶液中水解可制备肥皂,故答案为:④;
(2)乙烯中含双键,可发生加聚反应可制备聚乙烯塑料,故答案为:①;
(3)1,3-丁二烯中含双键,可发生加聚反应制备顺丁橡胶,故答案为:②;
(4)酚醛树脂为缩聚产物,苯酚与甲醛发生缩聚反应制备酚醛树脂,故答案为:③;
(5)为室内主要污染物的有毒的是甲醛,故答案为:③。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
第五章合成高分子
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列关于高分子材料的说法正确的是
A.酚醛树脂()可由苯酚和甲醛通过加聚反应制得
B.聚乙烯由线型结构转变为网状结构()能够增加材料的强度
C.天然橡胶的主要成分聚异戊二烯,其结构简式为
D.涤纶()是由苯甲酸和乙醇通过缩聚反应制得
2.劳动成就梦想,创造美好生活。下列对相关劳动实践项目的原因解释错误的是
选项 劳动实践项目 原因解释
A 环保:宣传使用聚乳酸制造的包装材料 聚乳酸在自然界可生物降解
B 兴趣:新榨果汁提取液可使酸性溶液褪色 果汁中含有还原性物质,能氧化,使其褪色
C 帮厨:帮食堂师傅准备午餐——煎鸡蛋 加热使蛋白质变性
D 探究:用柠檬酸除去水垢 柠檬酸酸性强于碳酸
A.A B.B C.C D.D
3.下列方程式书写正确的是
A.尿素与甲醛制备线型脲醛树脂:
B.水杨酸与过量的碳酸钠溶液反应:++CO2+H2O
C.两分子醛在碱催化下发生羟醛缩合:+H2O
D.草酸与酸性高锰酸钾溶液反应:
4.2023年9月习近平总书记在黑龙江考察调研期间首次提出“新质生产力”,“新质生产力”涵盖新材料、新能源等产业链。下列说法错误的是
A.推广使用太阳能、风能,有助于实现碳达峰、碳中和
B.制备飞机风挡所用的聚甲基丙烯酸甲酯属于有机高分子材料
C.制备火箭发动机的高温结构陶瓷属于传统无机非金属材料
D.世界首个高倍聚光与光电转换的全链路、全系统太空电站可将太阳能转化为电能
5.重氮羰基化合物聚合可获得主链由一个碳原子作为重复结构单元的聚合物,为制备多官能团聚合物提供了新方法。利用该方法合成聚合物P的反应路线如下。
已知:
下列说法不正确的是
A.反应Ⅰ中有氮气生成
B.反应Ⅱ是取代反应
C.聚合物P的结构
D.反应Ⅱ的副产物可以是网状结构的高分子
6.某有机物的结构简式如图所示,下列关于该有机物的描述不正确的是
A.该有机物中有3种官能团
B.该有机物可以发生加成反应、取代反应、氧化反应
C.该物质可发生加聚反应
D.标准状况下,1mol该物质与足量的钠反应生成11.2L的氢气
7.物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
选项 结构或性质 用途
A 石墨呈层状结构,层间以范德华力结合 石墨可用作润滑剂
B 具有氧化性 可用作漂白剂
C 聚丙烯酸钠()中含有亲水基团 聚丙烯酸钠可用于制备高吸水性树脂
D 冠醚18-冠-6空腔直径()与直径()接近 冠醚18-冠-6可识别,能增大在有机溶剂中的溶解度
A.A B.B C.C D.D
8.我国科学家最新合成出一种聚醚酯(PM)新型材料,可实现“单体-聚合物-单体”的闭合循环,推动塑料经济的可持续发展。合成方法如下:
下列说法不正确的是
A.M分子中含有2个手性碳原子
B.M在碱性条件下水解开环得到
C.PM中含有酯基、醚键和羟基三种官能团
D.合成1mol PM,理论上需要 n mol M 和1mol苯甲醇
9.下列关于有机化合物的说法正确的是
A.用系统命名法命名有机物:3,3-二甲基-4-乙基戊烷
B.高聚物的单体是
C.可以利用质谱法鉴别二甲醚和乙醇
D.有机物不存在顺反异构现象
10.环氧化物、CO2或环状酸酐在催化剂作用下开环共聚可制备脂肪族聚碳酸酯或聚酯。某聚碳酸酯的结构如下所示:
下列有关说法错误的是
A.该聚合物具有可降解性
B.合成该聚合物的一种单体是
C.合成该聚合物的反应类型为缩聚反应
D.利用上述反应原理,可用环氧乙烷()实现二氧化碳的固定
11.化学与生活、生产密切相关,下列说法正确的是
A.煤炭燃烧过程中添加“固硫”装置,可减少二氧化碳的排放
B.用“人工肾”进行血液透析救治患者,利用了胶体的性质
C.华为手机mate60使用的麒麟9000s芯片,其主要成分是二氧化硅
D.速滑竞赛服使用的聚氨酯材料属于天然有机高分子材料
12.化学与科技、生产、生活等方面密切相关,下列说法不正确的是
A.超导陶瓷在某一临界温度下电阻为零,具有超导性,可应用于磁悬浮技术
B.人民币票面使用含的油墨,验证真伪时利用了的磁性
C.将阿司匹林与高分子连接制成长效缓释药物,可减少用药次数
D.中国制造的乒乓球在巴黎奥运会中大放异彩,其主要成分为新型无机非金属材料
13.二甘醇可用作气体脱水剂、纺织品的润滑剂等。其结构如图所示,下列说法错误的是
A.能发生取代反应 B.分子中含有2种官能团
C.难溶于水 D.能与乙二酸发生缩聚反应
14.化学在社会、生活和科技进步方面发挥着重要的作用。下列说法错误的是
A.制造国产涡扇航空发动机的钛合金属于金属材料
B.桑蚕丝与涤纶都属于化学纤维
C.制造速滑服使用的聚乙烯属于有机高分子材料
D.淀粉在人体内水解可以为人体提供能量
15.控制NiOOH活性位点实现环己醇制备环己酮、己二酸的原理如图所示。下列叙述错误的是
A.环己醇中羟基上的H与NiOOH中的O能形成氢键
B.环己醇断裂H—O健和H—C键形成C=O键
C.环己酮和己二酸在核磁共振氢谱上都有3组峰且峰面积比为1∶2∶2
D.己二酸和己二胺发生加聚反应合成尼龙-66
二、填空题
16.有机高分子
高分子的相对分子质量比一般有机化合物大得多,通常在 以上。合成高分子的基本方法包括 反应和 反应,前者一般是含有 单体发生的聚合反应,后者一般是含有 的单体之间发生的聚合反应。
17.将化石燃料充分利用,并且实现“碳中和”是一项极具挑战的课题。下图①为自然界的碳循环过程,图②为石油化工重要产品乙烯的用途。
(1)图①植物中的纤维素在动物体内彻底水解,最终可得到 (填化学式)。
(2)畜禽养殖及水稻种植是CH4的主要排放源,捕捉CH4进行有效转化是“碳中和”的重要部分。若用硫与CH4在一定条件下生成乙烯,化学方程式为 。
(3)乙烯是重要的化工原料。将乙烯通入溴的CCl4溶液,现象为 ,反应类型为 ,产物名称为 。
(4)图②中聚氯乙烯的链节是 。
(5)环氧乙烷是重要的有机合成中间体。以乙烯为原料,用银作催化剂一步生成环氧乙烷的化学方程式为 。
18.填空
(1)按要求完成下列问题:
①甲基的电子式___________。
②写出制备TNT的化学反应方程式___________。
③反式2一丁烯的结构简式___________
(2)下列括号内的物质为杂质,将除去下列各组混合物中杂质所需的试剂填写在横线上:
①乙酸乙酯(乙醇)________;②甲苯(溴)________;
(3)下列卤代烃既能发生消去反应生成烯烃,又能发生水解反应生成醇的是
(4)实验室用纯溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作进行提纯:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗正确的操作顺序是 。
(5)某高聚物的结构式如图:其单体的名称为
(6)某有机物的结构简式为据此填写下列空格。
①该物质苯环上一氯代物有________种;
②1mol该物质和溴水混合,消耗Br2的物质的量为________mol;
③1mol该物质和H2加成需H2________mol;
(7)与等物质的量的Br2发生加成反应,生成的产物是
19.回答下列问题:
(1)现有下列6种有机物A.苯 B.乙烯 C.乙烷 D.乙醇 E.乙酸 F.油酸。
常温下能与溴水反应的有(填编号) 。
(2)下列各组物质:
A.金刚石与石墨; B.淀粉与纤维素; C.乙烯与聚乙烯; D.甲烷与戊烷;
E.CH3CH2CH(CH3)2与C(CH3)4 F. H2O与D2O G.葡萄糖与果糖
H.蔗糖与麦芽糖 I.甘氨酸与丙氨酸 J.乙醇与甘油
其中互为同分异构体的是 (填编号)。
(3)A.玻璃钢 B.明矾 C.隔热陶瓷瓦 D.氯丁橡胶
E.在合成树脂中加入碳纤维的材料 F.合成纤维
其中属于复合材料的是 (填编号)。
20.书写下列有机反应的方程式。
(1)与酯化成环 ;
(2)在氢氧化钠的乙醇溶液中加热 ;
(3)发生加聚反应 ;
(4)和缩聚 ;
(5)苯酚和乙醛的缩聚 ;
(6)与足量氢氧化钠溶液 。
21.按要求完成以下内容。
(1)肉桂醛是重要的医药原料,也是重要的香料,其结构简式如图一所示,以肉桂醛为原料合成的肉桂醛二乙缩醛的结构如图二所示:
肉桂醛是否存在顺反结构 (填写“是”或“否”),肉桂醛二乙缩醛的分子式为 。
(2)物质M结构如图, 具有的官能团除碳卤键外还有 (填名称)。
(3)正丙醇催化氧化的化学方程式为 。
(4)某高分子化合物的部分结构如图所示,合成此高聚物单体除CH2=CH-CH=CH2外,还有 、 。
(5)某烃A经红外光谱分析,含有-CH3、-CH2-和-CH-三种基团,质谱分析得出最大质荷比为86。则烃A的分子式为 ,符合题意的结构有 种。若烃A的核磁共振氢谱中吸收峰面积之比为6∶4∶3∶1,则烃A的系统名称为 ,它的一氯代物有 种。
22.完成下列填空:
I.下列 7 组物质或粒子:①淀粉和纤维素 ②16O 和18O ③氰酸铵(NH4CNO)与尿素[CO(NH2)2] ④C60和金刚石 ⑤CH3CH2CH3 和(CH3)2CHCH3 ⑥和⑦和
(1)互为同素异形体的是 (填编号,下同);
(2)互为同位素的是 ;
(3)互为同系物的是 ;
(4)互为同分异构体的是 。
II. 用系统命名法给下列有机物命名:
(1)
(2)(CH3)3COH
III.根据题目要求写出相应的化学方程式或结构简式。
(1)对苯二甲酸与乙二醇反应生成聚酯的方程式
(2)2-甲基-2-氯丙烷水解反应方程式
(3)某高聚物的结构简式如下:
则形成该高分子化合物的单体的结构简式分别为
23.工程塑料ABS树脂(结构简式如下),合成时用了三种单体(已知单体A中含有氰根,单体 S中含有苯环)
(1)书写三种单体的结构简式:A B S
(2)A、B和S三种单体,碳氢比(C:H)值最小的单体是 。
(3)经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比是 (用a、b、c表示)。
24.回答下列问题。
(1)将物质进行分类:①和②乙醇与二甲醚③D2O与H2O④和⑤和,用序号回答下列问题:
A互为同分异构体的是 ;B属于同一种化合物的是 ;C互为同系物的是 。
(2)分子中含有22个共价键的链状烷烃有多种同分异构体,写出其中含有三个甲基且等效氢有3种的结构简式:
(3)有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似。写出乙硅烷在空气中自燃的化学方程式: 。
(4)若、C2H4、C2H2、C6H6四种烃各为1g,在足量中燃烧,消耗最多的是: 。
(5)写出CH3—CH=CH—CH3发生加聚反应的化学方程式: 。
25.有机物具有广泛的用途。现有下列有机物:①乙烯 ②1,3-丁二烯 ③甲醛 ④油脂请将相应的序号填入空格内。
(1)能用于制备肥皂的是 ;
(2)能用于制备聚乙烯塑料的是 ;
(3)能用于制备顺丁橡胶的是 ;
(4)能用于制备酚醛树脂的是 ;
(5)为室内主要污染物的有毒的是 。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B B C C C D B B D C
题号 11 12 13 14 15
答案 B D C B D
1.B
【详解】
A.酚醛树脂是苯酚和甲醛通过缩聚反应制得的。方程式如下:n+nHCHO+nH2O,故A错误;
B.线型结构的高分子之间通过分子间作用力结合,强度小,聚乙烯由线型结构转变为网状结构时作用力增强,材料的强度增大,故B正确;
C.聚异戊二烯由异戊二烯()加聚获得,结构简式为,故C错误;
D.从涤纶()聚合物结构简式可以看出涤纶是由对苯二甲酸和乙二醇通过缩聚反应制得,故D错误;
故答案选B。
2.B
【详解】A.聚乳酸含酯基,能水解,聚乳酸在自然界可生物降解,A正确;
B.果汁中的还原性物质被酸性高锰酸钾溶液氧化,B错误;
C.鸡蛋主要成分是蛋白质,帮食堂师傅煎鸡蛋准备午餐,加热使蛋白质变性,C正确;
D.水垢的主要成分有碳酸钙,用白醋清洗水壶中的水垢,醋酸与碳酸钙反应生成二氧化碳,醋酸的酸性比碳酸强,强酸能制弱酸,D正确;
答案选B。
3.C
【详解】
A.尿素和甲醛制备线型脲醛树脂时,两者按物质的量之比为1∶2反应,生成(n-1)个水,化学方程式为+(n-1)H2O,A错误;
B.水杨酸与过量的碳酸钠溶液反应的化学方程式为2+→+,B错误;
C.两分子醛在碱催化下发生羟醛缩合,,然后再转化为RCH=CR -CHO,化学方程式为RCH=CR -CHO+H2O,C正确;
D.草酸与酸性高锰酸钾溶液反应的化学方程式为,D错误;
故答案为:C。
4.C
【详解】A.推广使用太阳能、风能,可以减少化石燃料的燃烧,有助于实现碳达峰、碳中和,A正确;
B.聚甲基丙烯酸甲酯为合成有机高分子材料,B正确;
C.高温结构陶瓷性能优良,属于新型无机非金属材料,C错误;
D.高倍聚光与光电转换的全链路、全系统太空电站可将太阳能转化为电能,实现太阳能与电能的转化,D正确;
故选C。
5.C
【分析】
根据反应①前后两个物质的结构简式,结合质量守恒,可以推出反应①的反应方程式为:n +nN2↑,根据反应②前后两个物质的结构简式,可以推出反应②的反应方程式为:n +n/2→+n,据此作答;
【详解】
A.根据分析,反应①的反应方程式为:n +nN2↑,反应①中有氮气生成,A正确;
B.根据分析,反应②的反应方程式为n +n/2→+n,是取代反应,B正确;
C.聚合物P为,C错误;
D.反应②的副产物也是聚合物,是网状结构的高分子,D正确;
故选C。
6.D
【详解】A.该有机物的官能团有碳碳双键、羟基、羧基3种官能团,A正确;
B.该物质含有碳碳双键,可以发生加成反应,含有羧基、羟基可以发生取代反应,羟基可以发生催化氧化反应,该物质还可以发生燃烧的氧化反应或是被酸性高锰酸钾氧化, B正确;
C.该物质含有碳碳双键,可以发生加聚反应,C正确;
D.含有羟基、羧基,都可以与钠反应生成氢气,则1mol该物质与足量的钠反应可以生成1mol氢气,标准状况下氢气的体积为11.2L ,D不正确;
故选D。
7.B
【详解】A. 石墨呈层状结构,层间以范德华力结合,该作用力较小,层与层容易滑动,石墨可用作润滑剂,A正确;
B. 具有漂白性,可用作漂白剂,B错误;
C. 聚丙烯酸钠()中含有亲水基团-COO-,聚丙烯酸钠可用于制备高吸水性树脂,C正确;
D. 冠醚18-冠-6空腔直径()与直径()接近,可识别,使K+存在于其空腔中,进而能增大在有机溶剂中的溶解度,D正确;
故选B。
8.B
【详解】
A.手性碳原子是指与四个各不相同原子或基团相连的碳原子,M分子中含有2个手性碳原子,位置为,A正确;
B.M中含有酯基,在酸性条件下水解开环得到,碱性条件下水解会生成相应的羧酸盐,B错误;
C.PM中含有酯基、醚键和羟基三种官能团,C正确;
D.由PM的结构简式可知,理论上,合成1mol PM需要消耗n mol M和1mol苯甲醇,D正确;
故选B。
9.D
【详解】
A. 的主链含有6个碳原子,名称为3,3,4-三甲基己烷,故A错误;
B. 高聚物的单体是,故B错误;
C.二甲醚和乙醇互为同分异构体,相对分子质量相等,无法用质谱法鉴别,故C错误;
D. 有机物CH3CH=CH2的碳碳双键一端的碳原子上连接有2个相同的基团,不存在顺反异构现象,故D正确;
故选D。
10.C
【详解】A.该聚合物为聚碳酸酯,酯类可以水解,所以该聚合物具有可降解性,故A正确;
B.环氧化物、CO2或环状酸酐在催化剂作用下开环共聚可制备脂肪族聚碳酸酯或聚酯,所以合成该聚合物的一种单体是环状酸酐,故B正确;
C.该聚合物是环氧化物、CO2、环状酸酐在催化剂作用下开环共聚制备的,所以合成该聚合物的反应类型为加聚反应,故C错误;
D.环氧乙烷()属于环氧化物,由题干可知:环氧化物、CO2或环状酸酐在催化剂作用下开环共聚,即环氧乙烷()可与二氧化碳发生开环加聚反应,实现二氧化碳的固定,故D正确;
故答案为:C。
11.B
【详解】A.煤炭燃烧过程中添加“固硫”装置,不减少二氧化碳的排放,A错误;
B.血液是胶体,而胶体不会通过半透膜,血液透析就是利用了该原理,B正确;
C.芯片主要成分是硅单质,C错误;
D.聚氨酯材料属于人工合成的有机高分子材料,D错误;
故选B。
12.D
【详解】A.超导陶瓷是一种特殊的材料,当温度降低到某一临界温度以下时,其电阻会降为零,表现出超导性。这种特性使得超导陶瓷在电力、交通、医疗等领域具有广泛的应用潜力。特别是在磁悬浮技术中,超导陶瓷的零电阻特性使得电流可以无损耗地流动,从而提高了磁悬浮系统的效率和稳定性,A正确;
B.是一种具有磁性的物质,因此被广泛应用于货币防伪技术中。在人民币的印刷过程中,通过使用含有的油墨,可以在票面上印制特定的磁性编码。这些磁性编码无法通过肉眼直接观察到,但可以通过专门的磁码识读器进行辨识,B正确;
C.缓释指慢慢释放药物,使其在血液中分解并逐渐发挥作用。这种技术可让药物效果长时间持续,从而有效减少服用药物的次数,C正确;
D.2014年7月1日起,新规定开始使用 高分子聚合物为原料的 新塑料球,其主要成分属于有机高分子材料,D错误;
故选D。
13.C
【详解】A.分子中含有羟基,能发生酯化反应,酯化反应是取代反应,故A正确;
B.分子中含有羟基和醚键两种官能团,故B正确;
C.分子中有2个羟基,能与水分子形成分子间氢键,易溶于水,故C错误;
D.分子中有2个羟基,能与乙二酸发生缩聚反应,故D正确;
答案选C。
14.B
【详解】A.合金和纯金属都属于金属材料,钛合金属于金属材料,A正确;
B.桑蚕丝属于蛋白质为天然纤维,B错误;
C.聚乙烯属于有机合成高分子材料,C正确;
D.淀粉在人体内水解生成葡萄糖,可以为人体提供能量,D正确;
答案选B。
15.D
【详解】A. 根据氢键形成的原理可知,环己醇中羟基上的H与NiOOH中的O能形成氢键,A正确;
B. 根据环己醇制备环己酮、己二酸的原理可知,环己醇断裂H—O键和H—C键形成了C=O键,B正确;
C. 根据环己酮、己二酸的结构可知,环己酮和己二酸在核磁共振氢谱上都有3组峰,且峰面积之比均为1:2:2,C正确;
D. 己二酸中的羧基和己二胺中的氨基会发生脱水反应,因此己二酸和己二胺发生了缩聚反应合成尼龙-66,D错误。
答案为:D。
16. 104 加成聚合 缩合聚合 双键的烯类 两个(或两个以上)官能团
【解析】略
17.(1)C6H12O6
(2)2S+2CH4CH2=CH2+2H2S
(3) 橙色褪去 加成反应 1,2-二溴乙烷
(4)
(5)2
【详解】(1)纤维素在动物体内彻底水解,最终可得到葡萄糖,化学式为C6H12O6,故答案为:C6H12O6。
(2)硫与CH4在一定条件下生成乙烯,化学方程式为2S+2CH4CH2=CH2+2H2S,故答案为:2S+2CH4CH2=CH2+2H2S。
(3)乙烯通入溴的CCl4溶液中,橙色褪去,发生加成反应CH2=CH2+Br2→BrCH2CH2Br,生成1,2-二溴乙烷,故答案为:橙色褪去;加成反应;1,2-二溴乙烷。
(4)氯乙烯CH2=CHCl发生加聚反应生成聚氯乙烯,则聚氯乙烯的链节为,故答案为:。
(5)在银的催化作用下,乙烯与氧气反应生成环氧乙烷,其化学方程式为2 ,故答案为: 。
18.(1)①;②;③
(2)①饱和碳酸钠溶液(或水);②NaOH溶液
(3)②④⑥
(4)②④②③①
(5)2-甲基-1,3-戊二烯和乙烯
(6)① 4 ② 2 ③ 5
(7)或
【详解】试题分析:(1)①电子式是把最外层电子用黑点标注在元素符合周围的式子,则甲基的电子式为;
②把浓H2SO4,浓HNO3和甲苯混合加热制备TNT,是苯环上氢原子被硝基取代生成三硝基甲苯,然后依据原子守恒配平化学方程式为;
③含有碳碳双键的烯烃有顺反异构,反式2一丁烯的结构简式为。
(2)①乙酸乙酯难溶于水,而乙醇与水互溶,所以除杂用饱和碳酸钠溶液或水;
②甲苯与NaOH溶液不反应且不溶于水,溴与NaOH溶液反应生成NaBr、NaBrO和水,所以除杂用NaOH溶液。
(3)卤代烃发生消去反应的条件是:①卤代烃含有的碳原子数大于等于2;②与卤素原子相连碳原子的相邻碳上有氢原子。①⑤中与卤素原子相连碳原子上的邻位碳上无氢原子,③中只有一个碳原子,没有邻位碳,②④⑥符合要求,答案选②④⑥。
(4)实验室用纯溴和苯反应制取的溴苯中含有溴、溴苯、HBr和水,先水洗除去溶于水的HBr,然后再用10%NaOH溶液洗除去Br2,再用水洗除去NaOH溶液,用干燥剂干燥除去水,最后蒸馏除去苯,正确的操作顺序是②④②③①。
(5)该高聚物的链接主链上有6个碳,说明是烯烃发生加聚反应生成的,主链碳上含有碳碳双键,截取双键两侧的2个碳原子,得到的单体为CH2=C(CH3)CH=CHCH3和CH2=CH2,对于有机物分子CH2=C(CH3)CH= CHCH3,选取含最多碳原子的链为主碳链,主链上有五个碳原子,从离碳碳双键最近的一端起编号,写出名称为2-甲基-1,3-戊二烯,同理另一种分子叫乙烯。
(6)有机物的结构简式为,含有两个碳碳双键和一个苯环。
①该物质苯环上有4种氢原子,其一氯代物有4种。
②该物质含有两个碳碳双键,则1mol该物质和溴水混合,消耗Br2的物质的量为2mol。
③该物质含有一个苯环和2个碳碳双键,则1mol该物质和H2加成需5mol氢气。
(7)属于共轭二烯烃,与等物质的量的Br2能发生1,2或1,4加成反应,生成的产物是或。
考点:考查电子式的书写,化学方程式的书写,物质的命名方法,消去反应的条件,有机物的提纯等知识。
19.(1)BF
(2)EGH
(3)ACE
【解析】(1)
乙烯和油酸结构中含有碳碳双键,能与溴水发生加成反应,故选BF;
(2)
分子式相同,结构不同的有机物互称同分异构体,其中E的分子式都为C5H12,互为同分异构体;葡萄糖和果糖分子式都为C6H12O6,结构不同,属于同分异构体;蔗糖和麦芽糖的分子式都为C12H22O11,结构不同,属于同分异构体,故选EGH;
(3)
玻璃钢是玻璃纤维与合成材料复合而成的一种特殊材料,属于复合材料,隔热陶瓷瓦是由纤维和陶瓷复合而成的复合材料,在合成树脂中加入碳纤维的材料形成复合材料,故选ACE。
20.(1)++2H2O
(2)+3NaOH+NaCl+3H2O
(3)n
(4)n+nHO-[-OC-CONHCH2CH2N2-]n-H+(2n-1)H2O
(5)n +nCH3CHO +nH2O
(6)+2nNaOH+n+nCH3OH
【详解】(1)
与 发生酯化反应得到,化学方程式为:++2H2O。
(2)
在氢氧化钠的乙醇溶液中加热发生消去和中和反应生成,化学方程式为:+3NaOH+NaCl+3H2O。
(3)
发生加聚反应生成,化学方程式为:n。
(4)
和发生缩聚反应生成HO-[-OC-CONHCH2CH2N2-]n-H,化学方程式为:n+nHO-[-OC-CONHCH2CH2N2-]n-H+(2n-1)H2O。
(5)
苯酚和乙醛的缩聚方程式为:n +nCH3CHO +nH2O。
(6)
与足量氢氧化钠溶液发生水解反应,方程式为:+2nNaOH+n+nCH3OH。
21.(1) 是 C13H18O2
(2)氨基、酮羰基
(3)2CH3CH2CH2OH+O22CH3CH2CHO+2H2O
(4) CH2=CHCN CH2=CH-CH3
(5) C6H14 2 3-甲基戊烷 4
【详解】(1)肉桂醛含碳碳双键,当相同的-H基团在同侧时为顺式结构,在异侧时为反式结构,根据肉桂醛二乙缩醛的分子式为C13H18O2;
(2)物质M结构如图,c具有的官能团除碳卤键外还有氨基、酮羰基;
(3)正丙醇催化氧化生成正丙醛,反应的化学方程式为2CH3CH2CH2OH+O22CH3CH2CHO+2H2O;
(4)主链只有C,应为加聚反应产物,添键断键法可知单体为CH2=CH-CH=CH2外,还有CH2=CHCN、CH2=CH-CH3;
(5)
烃A符合通式CnH2n+2,最大质荷比为86即相对分子质量为86,则12n+2n+2=86,解得n=6,则烃A的分子式为C6H14,含有-CH3、-CH2-和-CH-三种基团,结构有、共2种;核磁共振氢谱中吸收峰面积之比为6∶4∶3∶1,则烃A的系统名称为3-甲基戊烷,有4种氢,它的一氯代物有4种。
22. ④ ② ⑤ ③ 2,4-二甲基-3-乙基-3-己烯 2-甲基-2-丙醇 C(CH3)3Cl+NaOHC(CH3)3OH+NaCl CH2=CH—CH=CH2、 、NCCH=CH2
【详解】I(1)同种元素的不同单质互为同素异形体,C60和金刚石互为同素异形体,故答案为:④;
(2)同一原子的不同核素互为同位素,16O 和18O互为同位素,答案为:②;
(3)结构相似,相差n个—CH2的物质互为同系物,CH3CH2CH3 和(CH3)2CHCH3互为同系物,答案为:⑤;
(4)分子式相同,结构不同的物质互为同分异构体,氰酸铵(NH4CNO)与尿素[CO(NH2)2] 互为同分异构体,答案为:③;
II (1)选支链最多的最长碳链为主链,双键碳距两端等近时,从右边编号离甲基最近,故该物质命名为:2,4-二甲基-3-乙基-3-己烯;
(2)最长碳链是 3 个碳,官能团和取代基位置从哪端编号都一样,命名为:2-甲基-2-丙醇;
III(1)对苯二甲酸与乙二醇反应生成聚酯的方程式为:;
(2)卤代烃在氢氧化钠的水溶液中加热可发生水解反应,故2-甲基-2-氯丙烷水解反应方程式为:C(CH3)3Cl+NaOHC(CH3)3OH+NaCl;
(3) 从虚线处断开,把主链上的碳碳单键变成双键, 碳碳双键变成单键,就得到单体;故形成该高分子化合物的单体的结构简式分别为:CH2=CH—CH=CH2、 、NCCH=CH2。
23.(1) CH2=CHCN
(2)1,3-丁二烯
(3)
【详解】(1)该高聚物的形成过程属于加聚反应,加聚反应是由不饱和单体(如碳碳双键,碳碳三键以及碳氧双键等)聚合高分子的反应,其产物只有一种高分子化合物,凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换,直接合成该高聚物的物质为:CH2=CHCN、、;
(2)A、B和S三种单体,碳氢比(C:H)值分别是、、,所以最小的单体是,即1,3-丁二烯;
(3)若高聚物组成为CaHbNc,而三种单体中只有A的分子中含有一个氮原子,则高聚物中N原子个数必须等于单体A的个数,则根据高聚物CaHbNc可知CH2=CHCN为c个,因A、S中C和H的比值为1:1,碳氢个数的不同则是由单体B造成的,B分子中碳、氢原子的个数之差为2,因而高聚物中碳氢原子个数之差除以2,即是B分子的个数,因此可知A和B的物质的量之比为=。
24.(1) ①② ③⑤ ④
(2)
(3)
(4)
(5)
【详解】(1)①和分子式相同,结构不同,互为同分异构体;②乙醇与二甲醚分子式相同,结构不同,互为同分异构体;③D2O与H2O同种元素组成的相同的物质;④和结构相似,组成上相差1个CH2原子团,互为同系物;⑤和分子式相同,结构相同,属于同种物质;
(2)烷烃通式:,含共价键数目:,分子中含有22个共价键的链状烷烃碳原子个数:,分子式:,含有三个甲基且等效氢有3种说明结构对称,符合要求结构简式:;
(3)类比甲烷,乙硅烷燃烧化学方程式:;
(4)等质量的不同烃分别在氧气中完全燃烧,消耗氧气的量与烃的含碳量有关,烃的含碳量越小,消耗氧气的量越多,则消耗最多的是;
(5)
CH3—CH=CH—CH3发生加聚反应的化学方程式:。
25.(1)④
(2)①
(3)②
(4)③
(5)③
【详解】(1)肥皂的主要成分为高级脂肪酸盐,则油脂在碱性溶液中水解可制备肥皂,故答案为:④;
(2)乙烯中含双键,可发生加聚反应可制备聚乙烯塑料,故答案为:①;
(3)1,3-丁二烯中含双键,可发生加聚反应制备顺丁橡胶,故答案为:②;
(4)酚醛树脂为缩聚产物,苯酚与甲醛发生缩聚反应制备酚醛树脂,故答案为:③;
(5)为室内主要污染物的有毒的是甲醛,故答案为:③。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
