2.1元素与物质分类同步练习 2024-2025学年高一上学期化学鲁科版(2019)必修第一册(含答案)
文档属性
| 名称 | 2.1元素与物质分类同步练习 2024-2025学年高一上学期化学鲁科版(2019)必修第一册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 855.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-13 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2.1元素与物质分类
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质分类组合正确的是
选项 混合物 化合物 单质 盐
A 碱石灰 金刚石 O3 纯碱(Na2CO3)
B 盐酸 冰水混合物 液氮 CuSO4·5H2O
C 空气 澄清石灰水 铁 石灰石
D 食醋 CaCl2 水银 CaO
A.A B.B C.C D.D
2.朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…”则月光穿过薄雾形成美景的本质原因是
A.雾是一种胶体
B.光是一种胶体
C.发生了丁达尔效应
D.空气中的小水滴颗粒直径大小约为10﹣9m~10﹣7m
3.物质的世界每时每刻都在发生着变化,下列变化属于化学变化的是
①干冰升华 ②粮食酿酒 ③塑料老化 ④电灯通电发光 ⑤石油分馏 ⑥海水制镁 ⑦石块粉碎成石子 ⑧煤制成焦炭
A.②③⑥⑧ B.②⑤⑥⑧ C.①③④⑧ D.①④⑥⑦
4.牙膏是常见的日用品。某种牙膏中的摩擦剂为碳酸钙(CaCO3),它属于
A.氧化物 B.盐 C.碱 D.酸
5.做心电图检查时,为了保证电极探头与皮肤的良好接触,医生需要在皮肤上擦一种电解质溶液。下列溶液中适合使用的是
A.溶液 B.医用酒精 C.蔗糖溶液 D.溶液
6.下列有关溶液、胶体和浊液的说法中,正确的是( )
A.用过滤的方法可以除去胶体中的
B.胶体和浊液中粒子的大小相同
C.向氢氧化铁胶体中继续滴加NaCl溶液,可看到红褐色沉淀
D.将饱和溶液中滴入NaOH浓溶液中,制备胶体
7.下列叙述正确的是
A.分散质微粒直径的大小关系:溶液胶体浊液
B.胶体微粒不能透过滤纸
C.向沸水中加入可制得胶体
D.利用丁达尔效应可以区分溶液与胶体
8.中国科学家屠呦呦因成功提取青蒿素挽救了数百万人的生命而获得诺贝尔奖。青蒿素的化学式为,以下关于青蒿素的说法不正确的是
A.1个青蒿素分子由15个碳原子、22个氢原子和5个氧原子构成
B.青蒿素的相对分子质量为282
C.青蒿素不属于有机高分子化合物
D.青蒿素中,碳、氢、氧元素的质量比为45∶11∶40
9.按物质的组成分,SO2属于
A.酸 B.非金属氧化物 C.金属氧化物 D.单质
10.下列有关物质分类正确的是
选项 碱 酸 碱性氧化物 酸性氧化物 纯净物
A 烧碱 HNO3 CuO SO2 液氯
B 纯碱 HCl Na2O CO2 胆矾
C Ba(OH)2 H2SO4 MgO Mn2O7 盐酸
D 氨水 Na2O2 SO3 空气
A.A B.B C.C D.D
11.把少量下列物质分别放入水中,充分搅拌,可以得到蓝色溶液的是
A.植物油 B.氢氧化钠 C.蔗糖 D.硫酸铜
12.下列有关材料的说法,不正确的是
A.中国深海载人潜水器“蛟龙号”的发动机使用的氮化硅陶瓷属于新型无机非金属材料
B.华为首款 5G手机搭载了智能 7nm制程SOC“麒麟980”手机芯片的主要成分是二氧化硅
C.光伏电池是以硅为基底的硅太阳能电池
D.2022年北京冬奥会展示的智能服饰含有石墨烯,石墨烯与金刚石互为同素异形体
13.在给定条件下,下列选项所示的物质间转化均能实现的是
A.CO2COH2CO3
B.H2O2H2 H2O
C.Fe丝Fe3O4 Fe
D.KClO3O2P2O5
14.下列分散系中分散质直径最小的是
A.氯化银悬浊液 B.氢氧化铁胶体 C.雾 D.葡萄糖溶液
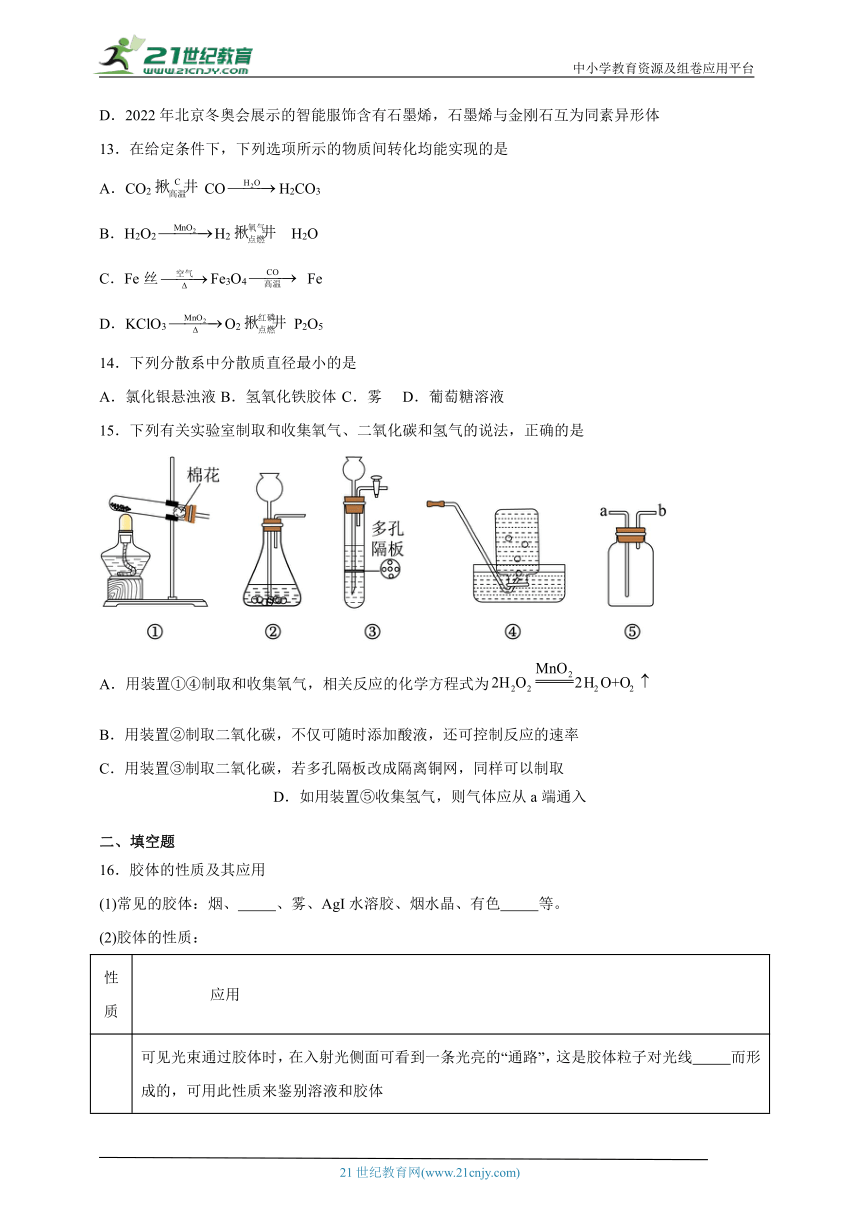
15.下列有关实验室制取和收集氧气、二氧化碳和氢气的说法,正确的是
A.用装置①④制取和收集氧气,相关反应的化学方程式为
B.用装置②制取二氧化碳,不仅可随时添加酸液,还可控制反应的速率
C.用装置③制取二氧化碳,若多孔隔板改成隔离铜网,同样可以制取
D.如用装置⑤收集氢气,则气体应从a端通入
二、填空题
16.胶体的性质及其应用
(1)常见的胶体:烟、 、雾、AgI水溶胶、烟水晶、有色 等。
(2)胶体的性质:
性质 应用
可见光束通过胶体时,在入射光侧面可看到一条光亮的“通路”,这是胶体粒子对光线 而形成的,可用此性质来鉴别溶液和胶体
胶体的稳定性介于溶液和浊液之间,属于介稳体系,同种胶体粒子的 相同,互相排斥,是胶体较稳定的主要原因
由于胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂中做定向移动的现象,此性质可用于工业上的
、 、加入与胶粒带相反电荷的胶体使胶体凝聚形成沉淀析出的现象,三角洲的形成;明矾、铁盐溶液净水;盐卤制豆腐等都属于聚沉
17.许多科学家在化学的发展方面起了重大作用。其中,研究空气成分,得出“空气是由氧气和氮气组成”结论的科学家是 ,提出分子概念的科学家是 ,提出近代原子学说的科学家是 ,最早发现电子的科学家是 。
18.I.某化学兴趣小组对下列三组物质进行研究:
A.HCl、H2SO4 、H2CO3 、HNO3
B.NaCl溶液、水、泥沙悬浊液、AgI胶体
C.Na2CO3 、NaNO3 、AgNO3 、Ba(NO3)2
请你帮他们完善下列空白:
A B C
分类标准 含氧酸 分散系 (3)
不属于该类别的物质 (1) (2) Na2CO3
II.“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线): 。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有 个,其中能“吃掉”盐酸的盐是 ,写出该反应的离子方程式 。
19.写出实验室制备CO2的化学方程式:
20.某同学对一组物质进行了如图所示分类:
(1)类别1为
(2)类别2的三种物质中,有一种物质与另外两种物质均能发生反应,其中属于复分解反应的是
21.现有Ca(OH)2、Na2CO3、BaCl2、NaOH、盐酸、稀硫酸六种溶液,它们存在如图所示的相互反应关系,图中每条线两端的物质可以发生化学反应,试将它们的化学式填入图中相应的六个方框中。
22.2021年在四川广汉三星堆新发现大量青铜器,如青铜面具、青铜神树等等。如图中的文物是三星堆出土的青铜面具之一,由于时间久远,表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、O2、CO2作用产生的,其化学式为Cu2(OH)2CO3,请用学过的方法对其展开探究。
(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有 、 (选取其中两点)。
(2)从不同的物质分类标准的角度分析,“铜绿”不属于 。
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐
(3)“铜绿”热稳定性差,受热易分解,请写出“铜绿”受热分解的化学方程式 。
(4)以“铜绿”为反应物可以实现以下物质转化:
经观察反应①固体物质溶解,有气泡产生,请写出该反应的化学方程式 。反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式 。
23.2016年9月15日,中秋夜的22时04分09秒,搭载着“天宫二号”空间实验室的“长征二号FT2”运载火箭在酒泉卫星发射中心点火发射,并取得了圆满成功。
(1)在对太空的探索过程中,科学家发现月球表面石坑中存在Hg、CH4、固态H2O等物质,其中属于氧化物的是 (填化学式)。
(2)运送“天宫二号”的火箭主要燃料是偏二甲肼(C2H8N2),偏二甲肼的摩尔质量为 ,它与氧气反应的生成物对大气均无污染(已知氮氧化合物多为污染物),请写出偏二甲肼与氧气反应的化学方程式 。
(3)在太空中,如果想在未来中国空间站进行以下化学实验,你认为最难完成的是_______。
A.将金粉和铜粉混合 B.将牛奶加入水中混合
C.蒸发食盐水制取食盐固体 D.用漏斗、滤纸过滤除去水中的泥沙
(4)载人航天飞行器的模拟座中,空气更新过程如下图所示:
①装置Ⅰ、Ⅱ、Ⅲ中发生化学变化的是 (填序号)。
②从装置Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,若产生12mol的氧气,消耗标准状下的二氧化碳224L,则同时消耗水 g。
24.下列物质属于氧化物的是 (填序号,下同),属于碱的是 ,属于酸的是 ,属于盐的是 。其中⑥属于 (填“纯净物”或“混合物”)。
①H2O;②NaCl;③H2SO4; ④Ca(OH)2;⑤ Fe3O4;⑥ CuSO4 5H2O;⑦HNO3;⑧AgNO3;⑨NaHCO3
25.化学与生产、生活密切相关。从化学视角回答下列问题:
(1)城市射灯在夜空形成五颜六色的光柱,属于 效应。
(2)除去固体中混有的少量杂质,应采取的最佳方法是 ,除杂过程中发生反应的化学方程式为 。
(3)电子工业常用30%的溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出溶液与铜发生反应的离子方程式: 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(4)空气质量报告的各项指标可以反映出各地空气的质量,下列气体已纳入我国空气质量报告的是___________(填字母,下同)。
A. B. C. D.
(5)当食盐不慎洒落在天然气的火焰上,观察到的现象是 。
(6)洁厕灵(主要成分HCl)和84消毒液不能混合使用,用离子方程式表示其理由: 。
(7)明矾可做净水剂的理由是 。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B D A B D C D D B A
题号 11 12 13 14 15
答案 D B D D C
1.B
【详解】A.金刚石是碳元素组成的单质,故A错误;
B.盐酸是氯化氢气体的水溶液,属于混合物;冰水混合物中只含水分子,属于化合物;液氮是氮元素组成的单质;CuSO4·5H2O属于盐,故B正确;
C.澄清石灰水是氢氧化钙的水溶液,属于混合物,故C错误;
D.CaO属于氧化物,故D错误;
选B。
2.D
【详解】月光穿过薄雾形成美景的本质原因是空气中的小水滴颗粒直径大小约为10﹣9m~10﹣7m,区别溶液和胶体的现象是丁达尔效应,故D符合题意。
综上所述,答案为D。
3.A
【详解】①干冰升华,没有生成新物质,属于物理变化;
②粮食酿酒,有新物质乙醇生成,属于化学变化;
③塑料老化是塑料被氧气氧化,属于化学变化;
④电灯通电发光,没有新物质生成,不属于化学变化;
⑤石油分馏,没有生成新物质,属于物理变化;
⑥海水制镁,氯化镁生成金属镁,有新物质生成,属于化学变化;
⑦石块粉碎成石子,没有生成新物质,属于物理变化;
⑧煤干馏制成焦炭,有新物质生成,属于化学变化;
属于化学变化的是②③⑥⑧,选A。
4.B
【详解】A.CaCO3中含有Ca、C、O三种元素,因此不属于氧化物,A错误;
B.CaCO3是由Ca2+与通过离子键结合形成的化合物,因此属于盐,B正确;
C.CaCO3是由金属阳离子和酸根阴离子构成的化合物,不能电离产生OH-,因此CaCO3属于盐,而不属于碱,C错误;
D.CaCO3电离产生的阳离子是金属阳离子Ca2+,而不能电离产生H+,因此CaCO3不属于酸,D错误;
故合理选项是B。
5.D
【详解】A.NaOH是电解质,NaOH稀溶液能导电,但具有腐蚀性,对人体有害、对设备造成损坏,A不符合题意;
B.医用酒精不是电解质、不导电,B不符合题意;
C.蔗糖不是电解质,蔗糖溶液不导电,不符合题意;
D.NaCl是电解质,医院里医生给病人做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液为氯化钠溶液,D符合题意;
故选D。
6.C
【详解】A.胶体和溶液都能透过滤纸,用渗析方法分离,故A错误;
B.在1nm-100nm之间的分散系称为胶体,而分散质粒子直径大于100nm的分散系叫做浊液,粒子的大小不同,故B错误;
C.向氧氧化铁胶体中继续滴加NaCl溶液,会引起胶体聚沉,生成红褐色氢氧化铁沉淀,故 C正确;
D.饱和FeCl3溶液中滴加NaOH溶液,反应生成沉淀,应把饱和氯化铁溶液滴加到沸水中制备胶体,故D错误;
故选:C。
7.D
【详解】A.分散系中分散质微粒直径小于1nm形成的分散系为溶液,大于100nm的分散系为浊液,1nm-100nm分散质形成的分散系为胶体,分散质微粒直径的大小关系:溶液<胶体<浊液,A错误;
B.胶体可以透过滤纸,即胶粒可以透过滤纸,但不能透过半透膜,B错误;
C.氢氧化铁胶体的制备是通过向沸水中滴加饱和氯化铁溶液制得,将氢氧化铁放入沸水中得到的是浊液,C错误;
D.丁达尔效应是胶体所特有的性质,而溶液没有,故可以用丁达尔效应来鉴别溶液和胶体,D正确;
故选D。
8.D
【详解】A.青蒿素的化学式为,1个青蒿素分子是由15个碳原子、22个氢原子和5个氧原子构成的,A正确;
B.青蒿素的相对分子质量为12×15+1×22+16×5=282,B正确;
C.青蒿素属于有机物,且相对分子质量比较小,不属于有机高分子化合物,C正确;
D.青蒿素中碳、氢、氧元素的质量比为(12×15):(1×22):(16×5)=90:11:40,D错误;
故选D。
9.B
【详解】SO2是由非金属元素硫元素和氧元素两种元素组成,属于氧化物,其中的硫元素为非金属元素,因此二氧化硫为非金属氧化物,故合理选项是B。
10.A
【详解】A.分类正确,A正确;
B.纯碱属于盐,B错误;
C.盐酸是氯化氢气体溶于水形成的混合物,C错误;
D.氨水是混合物,过氧化钠是过氧化物,不是碱性氧化物,空气是混合物,D错误;
答案选A。
11.D
【详解】A.植物油难溶于水,不能形成溶液,A错误;
B.氢氧化钠溶于水,形成的溶液是无色的,B错误;
C.蔗糖溶于水,形成无色溶液,C错误;
D.硫酸铜溶于水,形成蓝色溶液,D正确;
故选D;
12.B
【详解】A.氮化硅陶瓷是一种耐高温结构陶瓷,属于新型无机非金属材料,故A项正确;
B.芯片的主要成分是晶体硅,而不是二氧化硅,故B项错误;
C.光伏电池是以硅为基底的硅太阳能电池,能够将光能直接转化为电能,故C项正确;
D.石墨烯与金刚石都是由碳元素形成的两种不同单质,故互为同素异形体,故D项正确;
故答案为:B。
13.D
【详解】A.一氧化碳与水不反应,不会生成碳酸,故A错误;
B.双氧水在催化剂作用下分解为氧气和水,不会生成氢气,故B错误;
C.铁丝在空气中加热生成三氧化二铁,不会生成四氧化三铁,故C错误;
D.KClO3在催化剂作用下加热分解制取氧气,氧气与红磷在点燃条件下生成五氧化二磷,故D正确;
故选D。
14.D
【详解】葡萄糖溶液分散质微粒直径小于;雾、氢氧化铁胶体都属于胶体,分散质微粒直径在之间;氯化银悬浊液属于浊液,分散质微粒直径大于;葡萄糖溶液的分散质直径最小,答案选D。
15.C
【详解】A.用装置①④制取和收集氧气时,是加热高锰酸钾制取氧气,不是用过氧化氢制取氧气,故A错误;
B.用装置②制取二氧化碳,可随时添加酸液,但不能控制反应的速率,故B错误;
C.用装置③制取二氧化碳,若多孔隔板改成隔离铜网,Cu不和盐酸反应,同样可以制取,故C正确;
D.如用装置⑤收集氢气,氢气密度比空气小,则气体应从b端通入,故D错误;
故选C。
16.(1) 云 玻璃
(2) 丁达尔效应 散射 介稳定性 电性 电泳 静电除尘 聚沉 加热 加入电解质
【详解】(1)胶体是一种混合物,其中由微观分散的不溶性颗粒组成的一种物质悬浮在另一种物质中;常见的胶体:烟、云、雾、有色玻璃等;
故答案为:云;玻璃;
(2)当一束光线透过胶体,从垂直入射光方向可以观察到胶体里出现的一条光亮的“通路”,称为丁达尔效,可用此性质来鉴别溶液和胶体;胶体的稳定性介于溶液和浊液之间,属于介稳体系,同种胶体粒子电性相同,互相排斥;电泳是胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂中做定向移动的现象;加热、加入电解质加入与胶粒带相反电荷的胶体使胶体凝聚形成沉淀析出的现象,属于聚沉现象;
故答案为:丁达尔效应;散射;介稳定性;电性;电泳;静电除尘;聚沉;加热;加入电解质。
17. 拉瓦锡 阿伏加德罗 道尔顿 汤姆逊
【详解】试题分析:得出“空气是由氧气和氮气组成”结论的科学家是拉瓦锡;提出分子概念的科学
家是阿伏加德罗;提出近代原子学说的科学家是道尔顿;最早发现电子的科学家是汤姆生。
考点:考查化学史的有关判断
点评:本题是常识性知识的考查,主要是通过对化学史的了解,激发学生学习化学的积极性,树立科学的学习态度,有利于调动学生献身科学研究的热情,增强学生的学习自信心。
18. HCl 水 硝酸盐 ③⑥⑩⑦ 2 Na2CO3 Na2CO3+2HCl===2NaCl+H2O+CO2
【分析】I.按照物质的共性进行分类,不同性质进行区分;
II.根据盐酸的性质,能够与碱性气体、碱、碳酸盐等物质反应,而与酸性气体、不成盐气体、中性气体、酸和部分盐不反应。
【详解】I.A组中HCl不属于含氧酸;B组中水为纯净物,不属于分散系;C组,Na2CO3为碳酸盐,NaNO3、AgNO3、Ba(NO3)2为硝酸盐,所以分类标准为硝酸盐。
II.(1)盐酸不能和③O2、⑥NaCl、⑩CO、⑦Cu、 H2SO4、 Ag反应。
(2)中和反应是指酸与碱的反应,根据图中碱的种类确定中和反应的个数,碱有NaOH、Ca(OH)2两种,则中和反应有2个;能吃掉盐酸的盐是Na2CO3,碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,反应的化学方程式为:Na2CO3+2HCl==2NaCl+H2O+CO2。
19.
【详解】在实验室中,通常用大理石或石灰石(主要成分是碳酸钙)与稀盐酸反应来制取二氧化碳,反应同时生成氯化钙、水,。
20. 混合物 CuCl2 CuCl2+2NaOH=Cu(OH)2↓+2NaCl
【分析】(1)根据“分类标准1”分类后的两类物质含有的微粒特点判断分类标准1;
根据“分类标准2”分类后的两类物质含有的元素种类特点判断分类标准2,并根据盐的定义对该组物质进行判断;
(2)根据类别2中三种物质的性质分析判断,并用方程式表示该反应。
【详解】(1)“分类标准1”是按组成物质种类的多少分类的,“类别1”属于混合物,“分类标准2”是按组成纯净物元素种类的多少分类的,“类别2”属于化合物,其中CO2属于氧化物,NaOH属于碱,CuCl2属于盐。
(2)NaOH与CO2、CuCl2均能发生反应,其中属于复分解反应的是CuCl2+2NaOH=Cu(OH)2↓+2NaCl。
【点睛】本题考查物质分类方法及化学用语。明确物质的分类依据是分析图中的分类符合哪种分类依据的关键。掌握常见物质的性质和质量守恒定律是书写方程式的基础。
21.
【详解】
由物质的性质可知,稀硫酸除不能与盐酸反应外,能与其他四种溶液反应;碳酸钠溶液除不能与氢氧化钠溶液反应外,能与其他四种溶液反应;氢氧化钙溶液只能与碳酸钠溶液、盐酸和稀硫酸反应,盐酸只能与氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液反应,氯化钡溶液只能与碳酸钠溶液、稀硫酸反应,则符合题意的六种溶液位置关系如下:,故答案为:。
22.(1) 绿色 固体
(2)D
(3)(写成Cu2(OH)2CO3也可,下同)
(4)
【详解】(1)青铜面具由于时间久远,表面有一层“绿锈”,则可知Cu2(OH)2CO3的物理性质有:绿色、固体;
(2)铜绿是碱式碳酸铜的俗称,Cu2(OH)2CO3含有铜元素、碳酸根离子、氢氧根离子,故属于铜盐、碳酸盐、碱式盐、含氧酸盐,不属于碱,故选D;
(3)“铜绿”为碱式碳酸铜,受热分解的化学方程式(写成Cu2(OH)2CO3也可,下同)。
(4)铜绿加入盐酸生成氯化铜,然后加入强碱生成氢氧化铜,氢氧化铜受热分解生成氧化铜,氧化铜还原生成Cu,反应①的化学方程式。反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊,则该气体为CO,反应④的化学方程式。
23.(1)H2O
(2) 60g/mol C2H8N2+4O22CO2+4H2O+N2;
(3)D
(4) Ⅱ、Ⅲ 72g
【详解】(1)由两种元素组成,其中一种元素是氧,即为氧化物,则其中属于氧化物的是:H2O;
(2)以g/mol为单位时,摩尔质量在数值等于其分子量,则偏二甲肼的摩尔质量为:60g/mol;与氧气反应的产物没有污染,则,方程式为:C2H8N2+4O22CO2+4H2O+N2;
(3)通过人工手段可以使金粉和铜粉混合,也可以将牛奶加入水中混合,也可以蒸发食盐水得到氯化钠固体,因为在宇宙飞船的太空实验室中没有重量,所以混合容易完成而分离不易完成,特别是过滤操作需要利用重力将固体和液体分离,故选D;
(4)①在装置Ⅰ中无新物质生成,属于物理变化;装置Ⅱ中二氧化碳和氢气在一定条件下反应生成碳和水,有新物质生成,属于化学变化;装置Ⅲ中水在一定条件下反应生成氢气和氧气,有新物质生成,属于化学变化,故发生化学变化的是Ⅱ、Ⅲ;
②耗标准状下的二氧化碳224L产生氧气的物质的量为:,则消耗水产生氧气的物质的量为:12mol-10mol=2mol,则消耗水的质量为2mol×2×18g/mol=72g。
24. ①⑤ ④ ③⑦ ②⑥⑧⑨ 纯净物
【分析】根据混合物、纯净物、氧化物、酸、碱、盐的定义分析判断。
【详解】由氧合另外一种元素组成的物质是氧化物。
在上述物质中,①H2O;⑤Fe3O4仅有两种元素,其中一种是O元素,属于氧化物,故合理选项是①⑤;
电离产生的阴离子全部是OH-离子的化合物属于碱,在上述物质中, Ca(OH)2电离产生Ca2+、OH-,阴离子全部是OH-离子,属于碱所以合理选项是④;
酸是电离产生的阳离子全部是H+的化合物,在上述物质中, H2SO4电离产生H+、SO42-,⑦HNO3电离产生H+、NO3-,二者都属于酸,故合理选项是③⑦;
盐是由金属阳离子和酸根离子组成的化合物,在上述物质中,②NaCl;⑥CuSO4 5H2O;⑧AgNO3;⑨NaHCO3都是由金属阳离子和酸根离子组成,都属于盐,故合理选项是②⑥⑧⑨;
其中⑥CuSO4 5H2O是带有结晶水的盐,属于纯净物。
【点睛】本题考查物质的分类的知识。掌握物质的概念是进行正确分类的基础。
25.(1)丁达尔
(2) 加热 2NaHCO3Na2CO3+H2O+CO2↑
(3) Cu+2Fe3+=2Fe2++Cu2+ B
(4)C
(5)产生黄色火焰
(6)Cl-+ClO-+2H+=Cl2+H2O
(7)明矾溶于水后,与水反应生成的Al(OH)3胶体吸附水中悬浮物而沉降
【详解】(1)城市射灯在夜空形成五颜六色的光柱,是气溶胶,属于丁达尔效应;
(2)NaHCO3不稳定,可加热除杂,反应方程式为2NaHCO3Na2CO3+H2O+CO2↑;
(3)FeCl3溶液与金属铜发生反应的离子方程式为:Cu+2Fe3+=2Fe2++Cu2+;
A.Fe的还原性大于Cu,同时加入铁粉和铜粉,Fe先参加反应,当Fe完全反应后、Cu部分反应,则烧杯中可以有Cu无Fe,故A不选;
B.Fe的还原性大于Cu,同时加入铁粉和铜粉,Fe先参加反应,若有Fe剩余,则Cu不参与反应,所以不可能出现有Fe而无Cu现象,故B选;
C.如果铁有剩余,则Cu不参与反应,所以烧杯中铁、铜都有,故C不选;
D.如果铁离子过量,加入的Fe、Cu可完全反应,则烧杯中Cu、Fe都不存在,故D不选;
故答案为:B;
(4)空气质量报告的各项指标可以反映出各地空气的质量,二氧化碳、氮气、氧气为空气组成,二氧化氮为污染气体,纳入我国空气质量报告,故选C;
(5)食盐成分是NaCl,不慎洒落在天然气的火焰上,观察到的现象是产生黄色火焰;
(6)常用的“84消毒液”的主要成分是NaClO,而洁厕灵的主要成分是HCl,两者不能混合使用,用离子方程式表示原因为ClO-+Cl-+2H+=Cl2↑+H2O;
(7)明矾化学式为KAl(SO4)2 12H2O,明矾溶于水后,与水反应生成的Al(OH)3胶体吸附水中悬浮物而沉降。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2.1元素与物质分类
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质分类组合正确的是
选项 混合物 化合物 单质 盐
A 碱石灰 金刚石 O3 纯碱(Na2CO3)
B 盐酸 冰水混合物 液氮 CuSO4·5H2O
C 空气 澄清石灰水 铁 石灰石
D 食醋 CaCl2 水银 CaO
A.A B.B C.C D.D
2.朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…”则月光穿过薄雾形成美景的本质原因是
A.雾是一种胶体
B.光是一种胶体
C.发生了丁达尔效应
D.空气中的小水滴颗粒直径大小约为10﹣9m~10﹣7m
3.物质的世界每时每刻都在发生着变化,下列变化属于化学变化的是
①干冰升华 ②粮食酿酒 ③塑料老化 ④电灯通电发光 ⑤石油分馏 ⑥海水制镁 ⑦石块粉碎成石子 ⑧煤制成焦炭
A.②③⑥⑧ B.②⑤⑥⑧ C.①③④⑧ D.①④⑥⑦
4.牙膏是常见的日用品。某种牙膏中的摩擦剂为碳酸钙(CaCO3),它属于
A.氧化物 B.盐 C.碱 D.酸
5.做心电图检查时,为了保证电极探头与皮肤的良好接触,医生需要在皮肤上擦一种电解质溶液。下列溶液中适合使用的是
A.溶液 B.医用酒精 C.蔗糖溶液 D.溶液
6.下列有关溶液、胶体和浊液的说法中,正确的是( )
A.用过滤的方法可以除去胶体中的
B.胶体和浊液中粒子的大小相同
C.向氢氧化铁胶体中继续滴加NaCl溶液,可看到红褐色沉淀
D.将饱和溶液中滴入NaOH浓溶液中,制备胶体
7.下列叙述正确的是
A.分散质微粒直径的大小关系:溶液胶体浊液
B.胶体微粒不能透过滤纸
C.向沸水中加入可制得胶体
D.利用丁达尔效应可以区分溶液与胶体
8.中国科学家屠呦呦因成功提取青蒿素挽救了数百万人的生命而获得诺贝尔奖。青蒿素的化学式为,以下关于青蒿素的说法不正确的是
A.1个青蒿素分子由15个碳原子、22个氢原子和5个氧原子构成
B.青蒿素的相对分子质量为282
C.青蒿素不属于有机高分子化合物
D.青蒿素中,碳、氢、氧元素的质量比为45∶11∶40
9.按物质的组成分,SO2属于
A.酸 B.非金属氧化物 C.金属氧化物 D.单质
10.下列有关物质分类正确的是
选项 碱 酸 碱性氧化物 酸性氧化物 纯净物
A 烧碱 HNO3 CuO SO2 液氯
B 纯碱 HCl Na2O CO2 胆矾
C Ba(OH)2 H2SO4 MgO Mn2O7 盐酸
D 氨水 Na2O2 SO3 空气
A.A B.B C.C D.D
11.把少量下列物质分别放入水中,充分搅拌,可以得到蓝色溶液的是
A.植物油 B.氢氧化钠 C.蔗糖 D.硫酸铜
12.下列有关材料的说法,不正确的是
A.中国深海载人潜水器“蛟龙号”的发动机使用的氮化硅陶瓷属于新型无机非金属材料
B.华为首款 5G手机搭载了智能 7nm制程SOC“麒麟980”手机芯片的主要成分是二氧化硅
C.光伏电池是以硅为基底的硅太阳能电池
D.2022年北京冬奥会展示的智能服饰含有石墨烯,石墨烯与金刚石互为同素异形体
13.在给定条件下,下列选项所示的物质间转化均能实现的是
A.CO2COH2CO3
B.H2O2H2 H2O
C.Fe丝Fe3O4 Fe
D.KClO3O2P2O5
14.下列分散系中分散质直径最小的是
A.氯化银悬浊液 B.氢氧化铁胶体 C.雾 D.葡萄糖溶液
15.下列有关实验室制取和收集氧气、二氧化碳和氢气的说法,正确的是
A.用装置①④制取和收集氧气,相关反应的化学方程式为
B.用装置②制取二氧化碳,不仅可随时添加酸液,还可控制反应的速率
C.用装置③制取二氧化碳,若多孔隔板改成隔离铜网,同样可以制取
D.如用装置⑤收集氢气,则气体应从a端通入
二、填空题
16.胶体的性质及其应用
(1)常见的胶体:烟、 、雾、AgI水溶胶、烟水晶、有色 等。
(2)胶体的性质:
性质 应用
可见光束通过胶体时,在入射光侧面可看到一条光亮的“通路”,这是胶体粒子对光线 而形成的,可用此性质来鉴别溶液和胶体
胶体的稳定性介于溶液和浊液之间,属于介稳体系,同种胶体粒子的 相同,互相排斥,是胶体较稳定的主要原因
由于胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂中做定向移动的现象,此性质可用于工业上的
、 、加入与胶粒带相反电荷的胶体使胶体凝聚形成沉淀析出的现象,三角洲的形成;明矾、铁盐溶液净水;盐卤制豆腐等都属于聚沉
17.许多科学家在化学的发展方面起了重大作用。其中,研究空气成分,得出“空气是由氧气和氮气组成”结论的科学家是 ,提出分子概念的科学家是 ,提出近代原子学说的科学家是 ,最早发现电子的科学家是 。
18.I.某化学兴趣小组对下列三组物质进行研究:
A.HCl、H2SO4 、H2CO3 、HNO3
B.NaCl溶液、水、泥沙悬浊液、AgI胶体
C.Na2CO3 、NaNO3 、AgNO3 、Ba(NO3)2
请你帮他们完善下列空白:
A B C
分类标准 含氧酸 分散系 (3)
不属于该类别的物质 (1) (2) Na2CO3
II.“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线): 。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有 个,其中能“吃掉”盐酸的盐是 ,写出该反应的离子方程式 。
19.写出实验室制备CO2的化学方程式:
20.某同学对一组物质进行了如图所示分类:
(1)类别1为
(2)类别2的三种物质中,有一种物质与另外两种物质均能发生反应,其中属于复分解反应的是
21.现有Ca(OH)2、Na2CO3、BaCl2、NaOH、盐酸、稀硫酸六种溶液,它们存在如图所示的相互反应关系,图中每条线两端的物质可以发生化学反应,试将它们的化学式填入图中相应的六个方框中。
22.2021年在四川广汉三星堆新发现大量青铜器,如青铜面具、青铜神树等等。如图中的文物是三星堆出土的青铜面具之一,由于时间久远,表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、O2、CO2作用产生的,其化学式为Cu2(OH)2CO3,请用学过的方法对其展开探究。
(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有 、 (选取其中两点)。
(2)从不同的物质分类标准的角度分析,“铜绿”不属于 。
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐
(3)“铜绿”热稳定性差,受热易分解,请写出“铜绿”受热分解的化学方程式 。
(4)以“铜绿”为反应物可以实现以下物质转化:
经观察反应①固体物质溶解,有气泡产生,请写出该反应的化学方程式 。反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式 。
23.2016年9月15日,中秋夜的22时04分09秒,搭载着“天宫二号”空间实验室的“长征二号FT2”运载火箭在酒泉卫星发射中心点火发射,并取得了圆满成功。
(1)在对太空的探索过程中,科学家发现月球表面石坑中存在Hg、CH4、固态H2O等物质,其中属于氧化物的是 (填化学式)。
(2)运送“天宫二号”的火箭主要燃料是偏二甲肼(C2H8N2),偏二甲肼的摩尔质量为 ,它与氧气反应的生成物对大气均无污染(已知氮氧化合物多为污染物),请写出偏二甲肼与氧气反应的化学方程式 。
(3)在太空中,如果想在未来中国空间站进行以下化学实验,你认为最难完成的是_______。
A.将金粉和铜粉混合 B.将牛奶加入水中混合
C.蒸发食盐水制取食盐固体 D.用漏斗、滤纸过滤除去水中的泥沙
(4)载人航天飞行器的模拟座中,空气更新过程如下图所示:
①装置Ⅰ、Ⅱ、Ⅲ中发生化学变化的是 (填序号)。
②从装置Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,若产生12mol的氧气,消耗标准状下的二氧化碳224L,则同时消耗水 g。
24.下列物质属于氧化物的是 (填序号,下同),属于碱的是 ,属于酸的是 ,属于盐的是 。其中⑥属于 (填“纯净物”或“混合物”)。
①H2O;②NaCl;③H2SO4; ④Ca(OH)2;⑤ Fe3O4;⑥ CuSO4 5H2O;⑦HNO3;⑧AgNO3;⑨NaHCO3
25.化学与生产、生活密切相关。从化学视角回答下列问题:
(1)城市射灯在夜空形成五颜六色的光柱,属于 效应。
(2)除去固体中混有的少量杂质,应采取的最佳方法是 ,除杂过程中发生反应的化学方程式为 。
(3)电子工业常用30%的溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出溶液与铜发生反应的离子方程式: 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(4)空气质量报告的各项指标可以反映出各地空气的质量,下列气体已纳入我国空气质量报告的是___________(填字母,下同)。
A. B. C. D.
(5)当食盐不慎洒落在天然气的火焰上,观察到的现象是 。
(6)洁厕灵(主要成分HCl)和84消毒液不能混合使用,用离子方程式表示其理由: 。
(7)明矾可做净水剂的理由是 。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B D A B D C D D B A
题号 11 12 13 14 15
答案 D B D D C
1.B
【详解】A.金刚石是碳元素组成的单质,故A错误;
B.盐酸是氯化氢气体的水溶液,属于混合物;冰水混合物中只含水分子,属于化合物;液氮是氮元素组成的单质;CuSO4·5H2O属于盐,故B正确;
C.澄清石灰水是氢氧化钙的水溶液,属于混合物,故C错误;
D.CaO属于氧化物,故D错误;
选B。
2.D
【详解】月光穿过薄雾形成美景的本质原因是空气中的小水滴颗粒直径大小约为10﹣9m~10﹣7m,区别溶液和胶体的现象是丁达尔效应,故D符合题意。
综上所述,答案为D。
3.A
【详解】①干冰升华,没有生成新物质,属于物理变化;
②粮食酿酒,有新物质乙醇生成,属于化学变化;
③塑料老化是塑料被氧气氧化,属于化学变化;
④电灯通电发光,没有新物质生成,不属于化学变化;
⑤石油分馏,没有生成新物质,属于物理变化;
⑥海水制镁,氯化镁生成金属镁,有新物质生成,属于化学变化;
⑦石块粉碎成石子,没有生成新物质,属于物理变化;
⑧煤干馏制成焦炭,有新物质生成,属于化学变化;
属于化学变化的是②③⑥⑧,选A。
4.B
【详解】A.CaCO3中含有Ca、C、O三种元素,因此不属于氧化物,A错误;
B.CaCO3是由Ca2+与通过离子键结合形成的化合物,因此属于盐,B正确;
C.CaCO3是由金属阳离子和酸根阴离子构成的化合物,不能电离产生OH-,因此CaCO3属于盐,而不属于碱,C错误;
D.CaCO3电离产生的阳离子是金属阳离子Ca2+,而不能电离产生H+,因此CaCO3不属于酸,D错误;
故合理选项是B。
5.D
【详解】A.NaOH是电解质,NaOH稀溶液能导电,但具有腐蚀性,对人体有害、对设备造成损坏,A不符合题意;
B.医用酒精不是电解质、不导电,B不符合题意;
C.蔗糖不是电解质,蔗糖溶液不导电,不符合题意;
D.NaCl是电解质,医院里医生给病人做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液为氯化钠溶液,D符合题意;
故选D。
6.C
【详解】A.胶体和溶液都能透过滤纸,用渗析方法分离,故A错误;
B.在1nm-100nm之间的分散系称为胶体,而分散质粒子直径大于100nm的分散系叫做浊液,粒子的大小不同,故B错误;
C.向氧氧化铁胶体中继续滴加NaCl溶液,会引起胶体聚沉,生成红褐色氢氧化铁沉淀,故 C正确;
D.饱和FeCl3溶液中滴加NaOH溶液,反应生成沉淀,应把饱和氯化铁溶液滴加到沸水中制备胶体,故D错误;
故选:C。
7.D
【详解】A.分散系中分散质微粒直径小于1nm形成的分散系为溶液,大于100nm的分散系为浊液,1nm-100nm分散质形成的分散系为胶体,分散质微粒直径的大小关系:溶液<胶体<浊液,A错误;
B.胶体可以透过滤纸,即胶粒可以透过滤纸,但不能透过半透膜,B错误;
C.氢氧化铁胶体的制备是通过向沸水中滴加饱和氯化铁溶液制得,将氢氧化铁放入沸水中得到的是浊液,C错误;
D.丁达尔效应是胶体所特有的性质,而溶液没有,故可以用丁达尔效应来鉴别溶液和胶体,D正确;
故选D。
8.D
【详解】A.青蒿素的化学式为,1个青蒿素分子是由15个碳原子、22个氢原子和5个氧原子构成的,A正确;
B.青蒿素的相对分子质量为12×15+1×22+16×5=282,B正确;
C.青蒿素属于有机物,且相对分子质量比较小,不属于有机高分子化合物,C正确;
D.青蒿素中碳、氢、氧元素的质量比为(12×15):(1×22):(16×5)=90:11:40,D错误;
故选D。
9.B
【详解】SO2是由非金属元素硫元素和氧元素两种元素组成,属于氧化物,其中的硫元素为非金属元素,因此二氧化硫为非金属氧化物,故合理选项是B。
10.A
【详解】A.分类正确,A正确;
B.纯碱属于盐,B错误;
C.盐酸是氯化氢气体溶于水形成的混合物,C错误;
D.氨水是混合物,过氧化钠是过氧化物,不是碱性氧化物,空气是混合物,D错误;
答案选A。
11.D
【详解】A.植物油难溶于水,不能形成溶液,A错误;
B.氢氧化钠溶于水,形成的溶液是无色的,B错误;
C.蔗糖溶于水,形成无色溶液,C错误;
D.硫酸铜溶于水,形成蓝色溶液,D正确;
故选D;
12.B
【详解】A.氮化硅陶瓷是一种耐高温结构陶瓷,属于新型无机非金属材料,故A项正确;
B.芯片的主要成分是晶体硅,而不是二氧化硅,故B项错误;
C.光伏电池是以硅为基底的硅太阳能电池,能够将光能直接转化为电能,故C项正确;
D.石墨烯与金刚石都是由碳元素形成的两种不同单质,故互为同素异形体,故D项正确;
故答案为:B。
13.D
【详解】A.一氧化碳与水不反应,不会生成碳酸,故A错误;
B.双氧水在催化剂作用下分解为氧气和水,不会生成氢气,故B错误;
C.铁丝在空气中加热生成三氧化二铁,不会生成四氧化三铁,故C错误;
D.KClO3在催化剂作用下加热分解制取氧气,氧气与红磷在点燃条件下生成五氧化二磷,故D正确;
故选D。
14.D
【详解】葡萄糖溶液分散质微粒直径小于;雾、氢氧化铁胶体都属于胶体,分散质微粒直径在之间;氯化银悬浊液属于浊液,分散质微粒直径大于;葡萄糖溶液的分散质直径最小,答案选D。
15.C
【详解】A.用装置①④制取和收集氧气时,是加热高锰酸钾制取氧气,不是用过氧化氢制取氧气,故A错误;
B.用装置②制取二氧化碳,可随时添加酸液,但不能控制反应的速率,故B错误;
C.用装置③制取二氧化碳,若多孔隔板改成隔离铜网,Cu不和盐酸反应,同样可以制取,故C正确;
D.如用装置⑤收集氢气,氢气密度比空气小,则气体应从b端通入,故D错误;
故选C。
16.(1) 云 玻璃
(2) 丁达尔效应 散射 介稳定性 电性 电泳 静电除尘 聚沉 加热 加入电解质
【详解】(1)胶体是一种混合物,其中由微观分散的不溶性颗粒组成的一种物质悬浮在另一种物质中;常见的胶体:烟、云、雾、有色玻璃等;
故答案为:云;玻璃;
(2)当一束光线透过胶体,从垂直入射光方向可以观察到胶体里出现的一条光亮的“通路”,称为丁达尔效,可用此性质来鉴别溶液和胶体;胶体的稳定性介于溶液和浊液之间,属于介稳体系,同种胶体粒子电性相同,互相排斥;电泳是胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂中做定向移动的现象;加热、加入电解质加入与胶粒带相反电荷的胶体使胶体凝聚形成沉淀析出的现象,属于聚沉现象;
故答案为:丁达尔效应;散射;介稳定性;电性;电泳;静电除尘;聚沉;加热;加入电解质。
17. 拉瓦锡 阿伏加德罗 道尔顿 汤姆逊
【详解】试题分析:得出“空气是由氧气和氮气组成”结论的科学家是拉瓦锡;提出分子概念的科学
家是阿伏加德罗;提出近代原子学说的科学家是道尔顿;最早发现电子的科学家是汤姆生。
考点:考查化学史的有关判断
点评:本题是常识性知识的考查,主要是通过对化学史的了解,激发学生学习化学的积极性,树立科学的学习态度,有利于调动学生献身科学研究的热情,增强学生的学习自信心。
18. HCl 水 硝酸盐 ③⑥⑩⑦ 2 Na2CO3 Na2CO3+2HCl===2NaCl+H2O+CO2
【分析】I.按照物质的共性进行分类,不同性质进行区分;
II.根据盐酸的性质,能够与碱性气体、碱、碳酸盐等物质反应,而与酸性气体、不成盐气体、中性气体、酸和部分盐不反应。
【详解】I.A组中HCl不属于含氧酸;B组中水为纯净物,不属于分散系;C组,Na2CO3为碳酸盐,NaNO3、AgNO3、Ba(NO3)2为硝酸盐,所以分类标准为硝酸盐。
II.(1)盐酸不能和③O2、⑥NaCl、⑩CO、⑦Cu、 H2SO4、 Ag反应。
(2)中和反应是指酸与碱的反应,根据图中碱的种类确定中和反应的个数,碱有NaOH、Ca(OH)2两种,则中和反应有2个;能吃掉盐酸的盐是Na2CO3,碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,反应的化学方程式为:Na2CO3+2HCl==2NaCl+H2O+CO2。
19.
【详解】在实验室中,通常用大理石或石灰石(主要成分是碳酸钙)与稀盐酸反应来制取二氧化碳,反应同时生成氯化钙、水,。
20. 混合物 CuCl2 CuCl2+2NaOH=Cu(OH)2↓+2NaCl
【分析】(1)根据“分类标准1”分类后的两类物质含有的微粒特点判断分类标准1;
根据“分类标准2”分类后的两类物质含有的元素种类特点判断分类标准2,并根据盐的定义对该组物质进行判断;
(2)根据类别2中三种物质的性质分析判断,并用方程式表示该反应。
【详解】(1)“分类标准1”是按组成物质种类的多少分类的,“类别1”属于混合物,“分类标准2”是按组成纯净物元素种类的多少分类的,“类别2”属于化合物,其中CO2属于氧化物,NaOH属于碱,CuCl2属于盐。
(2)NaOH与CO2、CuCl2均能发生反应,其中属于复分解反应的是CuCl2+2NaOH=Cu(OH)2↓+2NaCl。
【点睛】本题考查物质分类方法及化学用语。明确物质的分类依据是分析图中的分类符合哪种分类依据的关键。掌握常见物质的性质和质量守恒定律是书写方程式的基础。
21.
【详解】
由物质的性质可知,稀硫酸除不能与盐酸反应外,能与其他四种溶液反应;碳酸钠溶液除不能与氢氧化钠溶液反应外,能与其他四种溶液反应;氢氧化钙溶液只能与碳酸钠溶液、盐酸和稀硫酸反应,盐酸只能与氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液反应,氯化钡溶液只能与碳酸钠溶液、稀硫酸反应,则符合题意的六种溶液位置关系如下:,故答案为:。
22.(1) 绿色 固体
(2)D
(3)(写成Cu2(OH)2CO3也可,下同)
(4)
【详解】(1)青铜面具由于时间久远,表面有一层“绿锈”,则可知Cu2(OH)2CO3的物理性质有:绿色、固体;
(2)铜绿是碱式碳酸铜的俗称,Cu2(OH)2CO3含有铜元素、碳酸根离子、氢氧根离子,故属于铜盐、碳酸盐、碱式盐、含氧酸盐,不属于碱,故选D;
(3)“铜绿”为碱式碳酸铜,受热分解的化学方程式(写成Cu2(OH)2CO3也可,下同)。
(4)铜绿加入盐酸生成氯化铜,然后加入强碱生成氢氧化铜,氢氧化铜受热分解生成氧化铜,氧化铜还原生成Cu,反应①的化学方程式。反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊,则该气体为CO,反应④的化学方程式。
23.(1)H2O
(2) 60g/mol C2H8N2+4O22CO2+4H2O+N2;
(3)D
(4) Ⅱ、Ⅲ 72g
【详解】(1)由两种元素组成,其中一种元素是氧,即为氧化物,则其中属于氧化物的是:H2O;
(2)以g/mol为单位时,摩尔质量在数值等于其分子量,则偏二甲肼的摩尔质量为:60g/mol;与氧气反应的产物没有污染,则,方程式为:C2H8N2+4O22CO2+4H2O+N2;
(3)通过人工手段可以使金粉和铜粉混合,也可以将牛奶加入水中混合,也可以蒸发食盐水得到氯化钠固体,因为在宇宙飞船的太空实验室中没有重量,所以混合容易完成而分离不易完成,特别是过滤操作需要利用重力将固体和液体分离,故选D;
(4)①在装置Ⅰ中无新物质生成,属于物理变化;装置Ⅱ中二氧化碳和氢气在一定条件下反应生成碳和水,有新物质生成,属于化学变化;装置Ⅲ中水在一定条件下反应生成氢气和氧气,有新物质生成,属于化学变化,故发生化学变化的是Ⅱ、Ⅲ;
②耗标准状下的二氧化碳224L产生氧气的物质的量为:,则消耗水产生氧气的物质的量为:12mol-10mol=2mol,则消耗水的质量为2mol×2×18g/mol=72g。
24. ①⑤ ④ ③⑦ ②⑥⑧⑨ 纯净物
【分析】根据混合物、纯净物、氧化物、酸、碱、盐的定义分析判断。
【详解】由氧合另外一种元素组成的物质是氧化物。
在上述物质中,①H2O;⑤Fe3O4仅有两种元素,其中一种是O元素,属于氧化物,故合理选项是①⑤;
电离产生的阴离子全部是OH-离子的化合物属于碱,在上述物质中, Ca(OH)2电离产生Ca2+、OH-,阴离子全部是OH-离子,属于碱所以合理选项是④;
酸是电离产生的阳离子全部是H+的化合物,在上述物质中, H2SO4电离产生H+、SO42-,⑦HNO3电离产生H+、NO3-,二者都属于酸,故合理选项是③⑦;
盐是由金属阳离子和酸根离子组成的化合物,在上述物质中,②NaCl;⑥CuSO4 5H2O;⑧AgNO3;⑨NaHCO3都是由金属阳离子和酸根离子组成,都属于盐,故合理选项是②⑥⑧⑨;
其中⑥CuSO4 5H2O是带有结晶水的盐,属于纯净物。
【点睛】本题考查物质的分类的知识。掌握物质的概念是进行正确分类的基础。
25.(1)丁达尔
(2) 加热 2NaHCO3Na2CO3+H2O+CO2↑
(3) Cu+2Fe3+=2Fe2++Cu2+ B
(4)C
(5)产生黄色火焰
(6)Cl-+ClO-+2H+=Cl2+H2O
(7)明矾溶于水后,与水反应生成的Al(OH)3胶体吸附水中悬浮物而沉降
【详解】(1)城市射灯在夜空形成五颜六色的光柱,是气溶胶,属于丁达尔效应;
(2)NaHCO3不稳定,可加热除杂,反应方程式为2NaHCO3Na2CO3+H2O+CO2↑;
(3)FeCl3溶液与金属铜发生反应的离子方程式为:Cu+2Fe3+=2Fe2++Cu2+;
A.Fe的还原性大于Cu,同时加入铁粉和铜粉,Fe先参加反应,当Fe完全反应后、Cu部分反应,则烧杯中可以有Cu无Fe,故A不选;
B.Fe的还原性大于Cu,同时加入铁粉和铜粉,Fe先参加反应,若有Fe剩余,则Cu不参与反应,所以不可能出现有Fe而无Cu现象,故B选;
C.如果铁有剩余,则Cu不参与反应,所以烧杯中铁、铜都有,故C不选;
D.如果铁离子过量,加入的Fe、Cu可完全反应,则烧杯中Cu、Fe都不存在,故D不选;
故答案为:B;
(4)空气质量报告的各项指标可以反映出各地空气的质量,二氧化碳、氮气、氧气为空气组成,二氧化氮为污染气体,纳入我国空气质量报告,故选C;
(5)食盐成分是NaCl,不慎洒落在天然气的火焰上,观察到的现象是产生黄色火焰;
(6)常用的“84消毒液”的主要成分是NaClO,而洁厕灵的主要成分是HCl,两者不能混合使用,用离子方程式表示原因为ClO-+Cl-+2H+=Cl2↑+H2O;
(7)明矾化学式为KAl(SO4)2 12H2O,明矾溶于水后,与水反应生成的Al(OH)3胶体吸附水中悬浮物而沉降。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
